| Bộ Y TẾ
|
CỘNG HÒA XÃ HỘI CHỦ NGHĨA VIỆT NAM
Độc lập – Tự do – Hạnh phúc
|
| Số:2674,QĐ-BYT
|
Hà Nội, ngày 27 tháng 04 năm 2018
|
QUYẾT ĐỊNH
Ban hành Hướng dẫn quốc gia xét nghiệm HIV
Căn cứ Nghị định số 75/2017/NĐ-CP ngày 20 tháng 6 năm 2017 của Chính phủ quy định chức năng, nhiệm vụ, quyền hạn và cơ cấu tổ chức của Bộ Y tế;
Căn cứ Luật “Phòng, chống nhiễm vi rút gây ra Hội chứng suy giảm miễn dịch mắc phải ở người (HIV/AIDS);
Căn cử Nghị định số 75/2016/NĐ-CP ngày 01 tháng 7 năm 2016 của Chính phủ quy định điều kiện thực hiện xét nghiệm HIV;
Xét đề nghị của Cục trưởng Cục Phòng, chống HIV/AIDS,
QƯYỂT ĐỊNH:
Điều 1. Ban hành kèm theo Quyết định này “Hướng dẫn quốc gia xét nghiệm HIV”.
Điều 2. Quyết định này có hiệu lực kề từ ngày ký, ban hành.
Điều 3. Quyết định này thay thế các Quyết định số 1098/QĐ-BYT ngày 04/4/2013 của Bộ Y tế về việc ban hành hướng dẫn quốc gia về xét nghiệm huyết thanh học HIV; Quyết định số 1053/QĐ-BYT ngày 02/4/2010 của Bộ Y tế về việc ban hành hướng dẫn xét nghiệm phát hiện nhiễm HIV cho trẻ dưới 18 tháng tuổi; Quyết định số 868/2005/QĐ-BYT ngày 29/3/2005 của Bộ Y tế về việc ban hành 07 biểu mẫu báo cáo dành cho phòng xét nghiệm.
Điều 4. Các ông/bà: Chánh Văn phòng Bộ, Cục trưởng, Vụ trưởng, Tổng Cục trưởng các Vụ, Cục, Tổng cục, Thủ trưởng các đơn vị trực thuộc Bộ Y tế, Giám đốc Sở Y tế các tỉnh/thành phố trực thuộc Trung ương và Thủ trưởng các đơn vị liên quan chịu trách nhiệm thi hành Quyết định này./
| KT BỘ TRƯỞNG
THỨ TRƯỞNG NGUYỄN THANH LONG |
| Bộ Y TẾ
|
CỘNG HÒA XÃ HỘI CHỦ NGHĨA VIỆT NAM
Độc lập – Tự do – Hạnh phúc
|
HƯỚNG DẪN QUỐC GIA XÉT NGHIỆM HIV
(Ban hành kèm theo Quyết định số 2674/QĐ-BYT, ngày27 tháng 4 năm 2018
của Bộ trướng Bộ Y tế)
Phần I
QUY ĐỊNH CHUNG
- Quyết định này hướng dẫn các vấn đề sau
1.1. Các kỹ thuật thực hiện xét nghiệm HIV: Xét nghiệm HIV bằng kỹ thuật huyết thanh học, xét nghiệm HIV bằng kỹ thuật sinh học phân tử.
1.2. Thực hiện đảm bảo chất lượng xét nghiệm HIV.
- Mục đích xét nghiệm
2.1.Đảm bảo an toàn trong truyền máu, cấy ghép mô, bộ phận cơ thể người và thụ tinh nhân tạo.
2.2. Giám sát dịch tễ HIV/AIDS: xác định tỷ lệ nhiễm HIV trong một số nhóm quần thể nhất định theo thời gian và địa điểm để theo dõi sự phân bố, chiều hướng phát triển của dịch nhằm cung cấp thông tin cho việc lập kế hoạch, dự phòng, khống chế và đánh giá hiệu quả các biện pháp phòng, chống HIV/AIDS.
2.3. Chẩn đoán phát hiện nhiễm HIV: xác định tình trạng nhiễm HIV của người được làm xét nghiệm.
- Nguyên tắc xét nghiệm
3.1. Đảm bảo tính bí mật, tự nguyện.
3.2. Cung cấp thông tin trước và tư vấn sau xét nghiệm.
3.3. Tuân thủ chiến lược, phương cách, quy trình xét nghiệm.
3.4. Đảm bảo chất lượng xét nghiệm và an toàn sinh học.
3.5. Kết nối với các chương trình dự phòng và chăm sóc điều trị.
- Phân loại phưong pháp, kỹ thuật xét nghiệm HIV
Các xét nghiệm phát hiện nhiễm HIV được chia thành các phương pháp chính:
4.1. Phương pháp xét nghiệm huyết thanh học để phát hiện sự hiện diện của kháng thể kháng HIV và/hoặc kháng nguyên HIV trong máu hoặc các dịch tiết để xác định tình trạng nhiễm HIV ở người lớn và trẻ em trên 18 tháng tuổi. Bao gồm các kỹ thuật sau:
-Xét nghiệm HIV bằng kỹ thuật đơn giản;
-Xét nghiệm HIV bằng kỹ thuật miễn dịch đánh dấu.
4.2. Phương pháp dùng xét nghiệm sinh học phân tử để phát hiện sự hiện diện ADN/ARN của HIV trong máu hoặc các dịch tiết. Phương pháp và kỹ thuật xét nghiệm HIV được hướng dẫn cụ thể tại phụ lục V ban hành kèm theo Hướng dẫn này.
Phần II
HƯỚNG DẪN XÉT NGHIỆM HIV
Chương I
XÉT NGHIỆM HUYẾT THANH HỌC
Mục 1 Chiến lược, phương cách, sinh phẩm xét nghiệm
- Các chiến lược xét nghiệm
Xét nghiệm huyết thanh học HIV được tiến hành theo những chiến lược khác nhau tùy thuộc vào mục đích xét nghiệm, tỷ lệ hiện nhiễm HIV của quần thể xét nghiệm.
Sơ đồ thực hiện các chiến lược xét nghiệm áp dụng theo hướng dẫn quy định tại phụ lục 1 ban hành kèm theo hướng dẫn này.
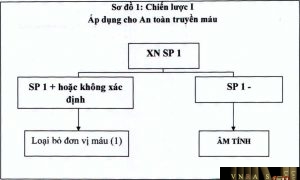
- Chiến lược I:
- Áp dụng cho sàng lọc nhiễm HIV trong an toàn truyền máu, người cho mô và bộ phận cơ thể, tinh trùng, noãn và phôi. Đối với an toàn truyền máu tuân thủ theo các quy định hiện hành về hoạt động truyền máu và sàng lọc đơn vị máu an toàn.
- Mẫu được coi là phản ứng với chiến lược 1 khi mẫu đó có phản ứng với một xét nghiệm bằng sinh phẩm có độ nhạy cao. Sinh phẩm dùng cho xét nghiệm sàng lọc máu theo quy định tại mục 3, chương I, Hướng dẫn này.
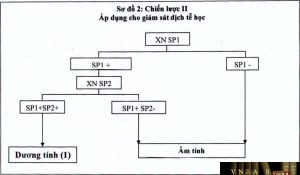
- Chiến lược II:
- Áp dụng cho giám sát dịch tễ học HIV.
- Mẫu được coi là dương tính với chiến lược II khi mẫu đó có phản ứng với cả hai loại sinh phẩm có nguyên lý hoặc chuẩn bị kháng nguyên khác nhau. Sinh phẩm dùng cho xét nghiệm giám sát dịch tễ học HIV theo quy định tại mục 3, chương I, Hướng dẫn này.
- Kết quả xét nghiệm này chỉ dùng cho mục đích giám sát dịch tễ không thông báo cho người được làm xét nghiệm.
- Chỉ được thông báo kết quả cho người được làm xét nghiệm khi tiếp tục thực hiện xét nghiệm bằng sinh phẩm thứ ba theo quy định của chiến lược III.
- Chiến lược III:
- Áp dụng cho chẩn đoán nhiễm HIV.
- mẫu được coi là dương tính với chiến lược III khi mẫu đó có phản ứng với cà ba loại sinh phẩm có nguyên lý hoặc chuẩn bị kháng nguyên khác nhau. Sinh phẩm dùng cho xét nghiệm chẩn đoán nhiễm HIV theo quy định tại mục 3, chương I, Hướng dẫn này.
- Phương cách xét nghiệm HIV
- Phương cách xét nghiệm là tổ hợp và thứ tự thực hiện xét nghiệm bằng các sinh phẩm cụ thể đã được lựa chọn theo từng chiến lược xét nghiệm.
- Thứ tự thực hiện xét nghiệm bằng các sinh phẩm được lựa chọn trong một phương cách xét nghiệm cần bảo đảm nguyên tắc: (i) sinh phẩm sàng lọc đầu tiên phải có độ nhạy cao nhất; (ii) các sinh phẩm bổ sung phải có độ đặc hiệu cao nhất; (iii) tránh lựa chọn các sinh phẩm có cùng nhược điểm như âm tính giả hoặc dương tính giả trong cùng một phương cách.
- Lựa chọn một phương cách xét nghiệm tùy thuộc vào: (i) mục đích xét nghiệm; (ii) số lượng mẫu; (iii) yêu cầu thời gian trả lời kết quả; (iv) điều kiện cụ thể và năng lực thực tế của cơ sở xét nghiệm.
- Lựa chọn sinh phẩm xét nghiệm nên theo khuyến cáo phương cách xét nghiệm HIV quốc gia và số lượng mẫu thực hiện xét nghiệm tại cơ sở xét nghiệm. Trong trường hợp số lượng mẫu > 40 mẫu/ngày nên sử dụng phương cách xét nghiệm sàng lọc bằng sinh phẩm miễn dịch đánh dấu, nếu số lượng mẫu < 40 mẫu/ngày nên xem xét sử dụng phương cách xét nghiệm sàng lọc bằng sinh phẩm nhanh.
- Sinh phẩm xét nghiệm HIV
- Các sinh phẩm xét nghiệm (viết tắt là SP) phải được Bộ Y tế cho phép sử dụng.
- Các sinh phẩm xét nghiệm đáp ứng các tiêu chuẩn sau:
- Các sinh phẩm sử dụng cho an toàn truyền máu phải tuân thủ theo các quy định về an toàn truyền máu.
- Các sinh phẩm dùng trong xét nghiệm HIV cho chiến lược II, III phải có đặc điểm sau:
| TT | Đặc điểm sinh phẩm thực hiện1 | Yêu cầu tối thiểu |
| 1 | Độ nhạy | |
| – | Sinh phẩm sàng lọc (SP1) | > 99,5% đối với SP nhanh 100% với SP miễn dịch đánh dấu |
| – | Sinh phẩm bổ sung (SP2, SP3) | > 99,5% đối với SP nhanh 100% với SP miễn dịch đánh dấu |
| 2 | Độ đặc hiệu | |
| – | Sinh phẩm sàng lọc (SP1) | > 98% đối với SP nhanh và SP miễn dịch đánh dấu |
| – | Sinh phẩm bổ sung (SP2, SP3) | > 99% đối với SP nhanh và SP miễn dịch đánh dấu |
1 Tham khảo Hướng dẫn xét nghiệm Hiv của Tổ chức Y tế thế giới 2015
– Độ nhạy, độ đặc hiệu của sinh phẩm xét nghiệm được lựa chọn dựa trên kết quả đánh giá chất lượng sinh phẩm của Quốc gia hoặc các tổ chức quốc tế như Tổ chức Y tế Thế giới, Trung tâm kiểm soát và phòng ngừa dịch bệnh Hoa kỹ, Phòng Thí nghiệm quốc gia úc (NRL) – là phòng thí nghiệm tham chiếu khu vực của WHO hoặc các tổ chức khác có uy tín.
- Các sinh phẩm xét nghiệm phải phát hiện được kháng thể kháng HIV týp 1 và 2 và/hoặc kháng nguyên HIV
- Bảo quản, sử dụng sinh phẩm xét nghiệm thực hiện theo đúng hướng dẫn của nhà sản xuất.
Mục 2
Thực hiện xét nghiệm
Việc thực hiện xét nghiệm sàng lọc HIV trong hướng dẫn này không áp dụng trong an toàn truyền máu.
- Xét nghiệm sàng lọc tại cộng đồng
Bao gồm các hình thức xét nghiệm sau:
- Tự xét nghiệm.
- Xét nghiệm do những nhân viên không làm trong phòng xét nghiệm HIV thực hiện.
- Xét nghiệm do nhân viên cơ sở xét nghiệm thực hiện.
- Tự xét nghiệm
- Khái niệm: Tự xét nghiệm HIV là quá trình người được xét nghiệm tự thực hiện tất cả các bước của việc xét nghiệm HIV bao gồm: tự lấy mẫu, tự làm xét nghiệm và tự đọc kết quả.
- Quy trình thực hiện:
- Thu thập mẫu bệnh phẩm
- Lấy dịch miệng
- Không ăn hoặc uống trước 15 phút, không sử dụng sản phẩm chăm sóc răng miệng trước 30 phút.
- Kiểm tra ngày hết hạn, tính nguyên vẹn của thanh xét nghiệm và các dung dịch đi kèm.
- Lấy thanh xét nghiệm ra khỏi túi bảo vệ. Khi lấy thanh ra khỏi túi tránh chạm tay vào phần bông thu thập mẫu.
- Kiểm tra túi giữ ẩm đi kèm trong túi đựng thanh xét nghiệm, nếu túi đựng thanh xét nghiệm không có túi giữ ẩm, loại bỏ thanh xét nghiệm và sử dụng thanh mới.
- Đặt phần bông vào vùng thấp của má và phần nướu răng (lợi) qúet nhẹ nhàng 1 vòng quanh nướu răng cả hàm trên và hàm dưới. Tránh quét xuống phía dưới vòm họng, bên trong má hoặc lưỡi. Cả hai mặt của phần bông thu thập mẫu đều có thể sử dụng để lấy mẫu.
- Lấy máu đầu ngón tay
- Chuẩn bị dụng cụ: Kim/lười chích dùng một lần có lẫy (lancet) chuyển dụng, ống mao quản có thể tích phù hợp, găng tay, bông thấm nước vô trùng, cồn 70 độ hoặc cồn I ốt, băng cá nhân, thùng đựng chất thải theo quy định.
- Chuẩn bị lấy máu
+ Điền đầy đủ các thông tin về người được làm xét nghiệm (họ tên hoặc mã số và năm sinh/tuổi) và ngày lấy mẫu trên phiếu xét nghiệm và trên thanh xét nghiệm (trong trường hợp cần thiết).
+ Rửa tay và đeo găng tay.
- Tiến hành lấy máu
+ Người được làm xét nghiệm làm ấm bàn tay bằng cách xoa hai tay với nhau hoặc rửa tay bằng nước ấm;
+ Xác định vị trí chích máu: Vị trí chích máu tốt nhất là mặt bên (trái hoặc phải của ngón tay thứ 3 (ngón giữa) hoặc thứ 4 (ngón áp út);
+ Người được làm xét nghiệm duỗi bàn tay xuống phía dưới;
+ Sát khuẩn vị trí lấy máu bằng cồn 70 độ và để khô trong vòng 30 giây;
+ Để kim/lười chích một cách vuông góc với mặt da đầu ngón tay ấn lẫy nhanh, mạnh dứt khoát. Đảm bảo giữ kim chích đúng góc và không làm nghiêng;
+ Lau bỏ giọt máu đầu tiên (vì giọt máu đầu tiên thường chứa dịch tổ chức có thể ảnh hưởng đến kết quả xét nghiệm, tế bảo kẽ không đủ lượng máu cho xét nghiệm);
+ Đợi cho đến khi máu chảy thành giọt lớn, dùng ống mao quản hút đù thể tích yêu cầu (không bóp nặn vùng chích máu để tiết ra dịch tổ chức mô xung quanh sê ảnh hưởng đén chất lượng mẫu);
+ Bỏ kim/lưỡi chích vào hộp đựng các vật sắc nhọn và ổng mao quản dùng đã hút mẫu máu vào hộp đựng rác thải y tế;
+ Sát trùng lại vị trí đã lấy máu bằng cồn 70 độ và băng lại;
+ mẫu sau khi lấy cần tiến hành xét nghiệm theo hướng dẫn của nhà sản xuất.
- Thực hiện xét nghiệm theo đúng hướng dẫn của nhà sản xuất.
- Biện luận kết quả
Kết quả xét nghiệm chỉ nhằm mục đích sàng lọc ban đầu, không được sử dụng để chẩn đoán nhiễm HIV, các trường hợp xét nghiệm có kết quả phản ứng cần được xét nghiệm khẳng định HI V theo quy định tại cơ sở y tế.
- Xét nghiệm do những nhân viên không làm trong phòng xét nghiệm HIV thực hiện.
- Khái niệm: Là hình thức xét nghiệm được thực hiện bởi nhân viên cộng đồng/y tế thôn bản/nhân viên y tế không được đào tạo chuyển ngành về xét nghiệm và không làm trong cơ sở xét nghiệm HIV đã được tập huấn về xét nghiệm HIV.
- Quy trình thực hiện:
Việc tư vấn, lấy mẫu xét nghiệm phải thực hiện tại khu vực sạch sẽ, thoải mái, đù ánh sáng và bảo đảm riêng tư cho khách hàng.
- Thu thập mẫu bệnh phẩm: thực hiện theo quy định tại điểm 1.2.1 khoản 1.2 mục 1, phần I của chương này.
- Thực hiện xét nghiệm, biện luận kết quả theo đúng hướng dẫn của nhà sản xuất.
- Trả kết quả
- Nếu kết quả xét nghiệm âm tính thì tư vấn và thông báo kết quả cho khách hàng.
- Nếu kết quả xét nghiệm có phản ứng cần tư vấn và giới thiệu khách hàng đến cơ sở y tế để xét nghiệm khẳng định HIV theo quy định.
- Xét nghiệm do nhân viên phòng xét nghiệm HIV thực hiện
- Khái niệm: Là hình thức xét nghiệm được thực hiện bởi nhân viên xét nghiệm thuộc các cơ sở xét nghiệm đã được tập huấn về xét nghiệm HIV.
- Quy trình thực hiện:
Việc tư vấn, lấy mẫu xét nghiệm phải thực hiện tại khu vực sạch sẽ, thoải mái, đủ ánh sáng và bảo đảm riêng tư cho khách hàng.
- Thu thập mẫu bệnh phẩm
- Việc lấy mẫu bệnh phẩm dịch miệng hoặc máu đầu ngón tay thực hiện theo quy định tại điểm 1.2.1 khoản 1.2 mục 1, phần I của chương này.
- Lấy máu tĩnh mạch, bệnh phẩm cần được thu thập như sau:
- Chuẩn bị dụng cụ: bơm kim tiêm vô trùng hoặc bộ dụng cụ lấy máu bằng ống hút chân không (vacutainer, kim, giá đỡ), pipet nhựa dùng 1 lần (ống bóp), ống nghiệm nhựa có nắp đậy, ống nghiệm có chất chống đông (khi cần thu thập mẫu huyết tương), găng tay, khẩu trang, dây ga rô, bông thấm nước vô trùng, cồn 70 độ, bút dạ (loại mực chịu nước), giá để ống nghiệm, thùng đựng các vật sắc nhọn và rác thải y tế.
- Chuẩn bị lấy máu
+ Điền đầy đủ các thông tin về người được làm xét nghiệm (họ tên/mã số và năm sinh/tuổi) và ngày lấy mẫu trên phiếu xét nghiệm và ống đựng mẫu.
+ Rửa tay và đeo găng tay.
- Tiến hành lấy máu
+ Xác định vị trí lấy máu (tĩnh mạch) và sát khuẩn bằng cồn 70 độ và để khô trong vòng 30 giây.
+ Đưa kim vào tĩnh mạch lấy 3- 4 ml máu cho vào ống đựng máu. Có thể dùng bơm kim tiêm loại 5ml (đầu kim cỡ 21G – 23G) để lấy máu hoặc dùng bộ dụng cụ lấy máu với ống hút chân không (vacutainer). Nếu dùng bơm kim tiêm để lấy máu thì tháo đầu kim ra, để bơm tiêm chếch với thành ống nghiệm và bơm từ từ cho máu chảy theo thành ống nghiệm tránh làm vỡ hồng cầu.
+ Tháo bỏ đầu kim vào hộp đựng các vật sắc nhọn và bơm tiêm hoặc giá đỡ ống lấy máu bẩn vào hộp đựng rác thải y tế;
+ Sát trùng lại vị trí lấy máu bằng cồn 70 độ và băng lại.
- Tách huyết thanh/huyết tương:
+ Sau khi lấy máu phải để ổn định 30 phút và không quá 2 giờ ở nhiệt độ phòng, tiến hành tách huyết thanh/huyết tương. Trường hợp không tách được huyết thanh/huyết tương trong vòng 2 giờ, để mẫu ổn định ở nhiệt độ phòng 30 phút sau đó bảo quản ở nhiệt độ 4°c -8°c và cần phải tách huyết thanh/huyết tương trong vòng 24 giờ.
+ Sử dụng máy ly tâm phải thăng bằng các ống nghiệm trước khi ly tâm. Tiến hành ly tâm tốc độ 2000 – 2500 vòng/phút trong vòng 10 phút. Sử dụng pi pét nhựa để tách phần huyết thanh/huyết tương vào một ống nghiệm nhựa rồi đóng chặt nắp.
+ Không có máy ly tâm: Để ống nghiệm trên giá trong vòng 30 phút sau đó để vào tử lạnh ở nhiệt độ 4°c -8°c, tối thiểu 2 giờ nhưng không quá 24 giờ phải tách huyết thanh/huyết tương cho vào một ống nghiệm nhựa rồi đóng chặt nắp.
+ Thể tích huyết thanh/huyết tương tối thiểu thu thập được là 1,5ml
- Thực hiện xét nghiệm, biện luận kết quả theo đúng hướng dẫn của nhà sản xuất.
- Trả kết quả
- Nếu kết quả xét nghiệm âm tính: tư vấn và thông báo kết quả âm tính cho khách hàng.
- Nếu kết quả xét nghiệm có phản ứng: lấy máu hoặc giới thiệu khách hàng chuyển đến cơ sở y tế để xét nghiệm khẳng định theo quy định, tư vấn hẹn trả kết quả.
- Bảo đảm chất lượng xét nghiệm
- Tuân thủ việc lấy mẫu, thực hiện xét nghiệm và đọc kết quả theo hướng dẫn của nhà sản xuất.
- Nơi thực hiện xét nghiệm cần sạch sẽ, đủ ánh sáng, bằng phẳng, dễ khử khuẩn.
- Bảo quản sinh phẩm xét nghiệm theo đúng hướng dẫn của nhà sản xuất. Trong trường hợp sinh phẩm bảo quản tại nhiệt độ phòng cần có nhiệt kế theo dõi nhiệt độ phòng tránh nhiệt độ bảo quản ngoài ngưỡng cho phép.
- Luôn sử dụng đồng hồ đảm ngược khi thực hiện xét nghiệm.
- Chi đọc kết quả xét nghiệm khi đủ thời gian theo quy định và vùng đọc kiểm chứng có xuất hiện vạch.
- An toàn sinh học:
- Hướng dẫn về an toàn sinh học cho toàn bộ nhân viên xét nghiệm.
- Nhân viên xét nghiệm sử dụng trang bị bảo hộ cá nhân phù hợp khi lấy mẫu và tiến hành xét nghiệm.
- Thực hiện rửa tay hoặc sát khuẩn tay ngay sau khi tháo găng tay, kết thúc quy trình xét nghiệm.
- Thực hiện khử nhiễm khu vực xét nghiệm bằng các chất khử nhiễm phù hợp.
- Phân loại, thu gom chất thải phát sinh trong quá trình thu thập mẫu, thực hiện xét nghiệm vào các vật dụng chưa phù hợp và vận chuyển đến cơ sở y tế để xử lý theo quy định.
- Xây dựng và tuân thủ quy định xử lý sự cố xảy ra trong quá trình thu thập mẫu và thực hiện xét nghiệm như sự cố vật sắc nhọn đâm vào tay, tràn đồ mẫu bệnh phẩm.
- Xét nghiệm sàng lọc HIV tại cơ sở y tế
Các yêu cầu về nhân sự, cơ sở vật chất, trang thiết bị và năng lực xét nghiệm cần đáp ứng theo Nghị định số 75/NĐ-CP ngày 01/7/2016 của Chính phủ quy định điều kiện thực hiện xét nghiệm HIV.
- Thu thập, vận chuyển, bảo quản, tiêu hủy bệnh phẩm xét nghiệm.
- Thu thập mẫu thực hiện theo các quy định tại điểm 3.2.1 khoản 3.2 mục 3 phần 1 chương này.
- Vận chuyển mẫu
- Đóng gói mẫu:
- Đóng gói 3 lớp
+ Lớp l(ống đựng mẫu): Đeo găng tay đóng chặt các nắp của ống mẫu và xếp tất cả các ống mẫu theo phương thẳng đứng vào trong giá đựng mẫu. Dùng băng dính cố định các ống mẫu trong giá đựng bệnh phẩm (nếu cần).
+ Lớp 2 (túi, hộp, gói bằng vật liệu bền không thấm nước, không dò rỉ, chịu được nhiệt độ 40-55°C): Cho đủ vật liệu thấm hút (bông thấm nước hoặc giấy thấm) vào giữa lớp thứ 1 và lớp thứ 2, để trong trường hợp đổ vỡ vật liệu thấm hút sẽ hấp thụ toàn bộ lượng mẫu.
+ Lớp ngoài cùng (hộp, thùng cứng, chịu được va đập, không dò rỉ). Giữa lớp thứ 2 và lớp ngoài cùng có các túi tích lạnh để đảm bảo mẫu được bảo quản
từ 4°c -8°c trong quá trình vận chuyển. Trong trường hợp mẫu vận chuyển ở nhiệt độ âm sâu cần sử dụng đá khô để vận chuyển, nếu dùng đá khô thì lớp ngoài cùng cần có lỗ thoát khí C02.
- Đóng nắp thùng đựng mẫu và chốt khoá lại. Trường hợp không có chốt khoá thì dùng băng dính dán xung quanh.
- Dán hoặc in ký hiệu nguy hiểm sinh học và số điện thoại liên hệ trong trường hợp khẩn cấp bên ngoài của hộp đựng mẫu bệnh phẩm.
- Lưu ỷ: Không để danh sách mẫu vào trong hộp vận chuyển mẫu.
- Vận chuyển mẫu
- Vận chuyển mẫu bệnh phẩm phải tuân thủ các quy định của quốc gia và chính quyền địa phương về vận chuyển các tác nhân có khả năng gây bệnh.
- Gọi điện báo trước cho phòng xét nghiệm biết thời gian bệnh phẩm sẽ tới đề phòng xét nghiệm bố trí cán bộ tiếp nhận.
- Bệnh phẩm gửi đi phải kèm theo phiếu yêu cầu xét nghiệm điền đầy đủ các thông tin.
- mẫu bệnh phẩm phải được bảo quản lạnh trong suốt quá trình vận chuyển.
- Trong quá trình vận chuyển mẫu phải buộc chặt hộp chứa mẫu bệnh phẩm vào giá chở hàng, đảm bảo gọn gàng, tránh đổ, võ.
- Tiếp nhận mẫu
- Kiểm tra nhiệt độ trong hộp vận chuyển, kiểm tra tình trạng mẫu, đối chiếu thông tin trên ống đựng máu, phiếu xét nghiệm. Trong trường hợp có sự sai lệch giữa thông tin trên phiếu và trên ống mẫu đơn vị gửi mẫu cần xác nhận thông tin đúng, hoặc kết quả sẽ trả theo thông tin trên ống đựng mẫu.
- Thông báo cho nơi gửi xét nghiệm lấy lạr mẫu trong các trường hợp: máu bị đông, huyết thanh đã bị tán huyết, mẫu được bảo quản và vận chuyển trong môi trường có nhiệt độ không đúng quy định, mẫu không đủ thể tích yêu cầu, mẫu được chuyển đến quá thời gian quy định.
- Thông báo cho nơi gửi mẫu xét nghiệm bổ sung thông tin trong trường hợp: thiếu thông tin về địa chỉ, ngày, thu thập mẫu trên phiếu xét nghiệm.
- Ký nhận vào phiếu gửi mẫu và ghi chép vào sổ nhận mẫu các thông tin về số lượng mẫu, người nhận, thời gian nhận.
- Bảo quản mẫu
- mẫu huyết thanh/huyết tương nếu xét nghiệm trong vòng 3-7 ngày phải bảo quản ở nhiệt độ 4°c -8°c (tùy thuộc vào hướng dẫn của nhà sản xuất). Nếu cần bảo quản lâu hơn phải lưu trữ ở nhiệt độ (- 20°C) hoặc lạnh hơn. Tuy nhiên mẫu không được tan đông quá 3 lần.
- Tiêu hủy mẫu
Tiêu hủy mẫu xét nghiệm tuân thủ theo quy định tại Thông tư liên tịch sô 58/2015/TTLT-BYT- BTNMT ngày 31/12/2015 của Bộ Y tế và Bộ Tài nguyên và môi trường quy định về quản lý chất thải y tế.
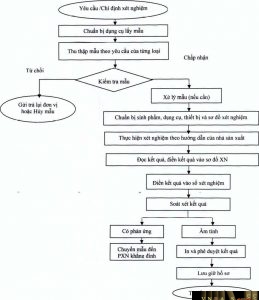
- Thực hiện xét nghiệm
- Sơ đồ thực hiện xét nghiệm
2.2 Thực hiện xét nghiệm bằng kỹ thuật đơn giản (sinh phắm xét nghiệm
nhanh).
– Mồi loại sinh phẩm sử dụng cần có quy trình cụ thể bằng tiếng Việt.
- Sinh phẩm, mẫu bệnh phẩm được bảo quản đúng nhiệt độ yêu cầu của nhà sản xuất.
- Đối với các sinh phẩm không có dụng cụ lấy mẫu đi kèm, phải sử dụng pipetman để hút mẫu.
- Lập sơ đồ xét nghiệm/phiếu làm việc cho mỗi lần thực hiện xét nghiệm. Sơ đồ xét nghiệm thể hiện các thông tin về sinh phẩm, sô lô, hạn sử dụng, ngày thực hiện, người thực hiện, kiểm soát mẫu chứng và kết quả của mẫu.
- Sử dụng trang bị bảo hộ cá nhân trong suốt thời gian làm việc tại phòng xét nghiệm.
- Thực hiện xét nghiệm theo đúng hướng dẫn của nhà sản xuất.
- Thực hiện xét nghiệm tại khu vực bàn xét nghiệm, dễ làm sạch bằng các chất khử khuẩn, đảm bảo đủ ánh sáng và tránh luồng gió. Sàn, tường và bàn xét nghiệm bằng phẳng, không thấm nước, chịu được nhiệt độ cao và các loại hóa chất ăn mòn, dễ cọ rửa vệ sinh.
- Thời gian chờ đọc kết quả sử dụng đồng hồ đếm ngược chuyển dụng cho xét nghiệm.
- Chỉ đọc và biện luận kết quả khi mẫu chứng đạt yêu cầu của nhà sản xuất. Trong trường hợp sử dụng mẫu nội kiểm thì ngoài chứng của nhà sản xuất đạt yêu cầu, chứng nội kiểm cùng đạt yêu cầu khi đó mới biện luận kết quả
- Các chất thải lây nhiễm phát sinh trong quá trình thực hiện xét nghiệm phải được xử lý trước khi chuyển vào nơi chứa chất thải chung theo quy định.
- Các mẫu sau khi thực hiện xét nghiệm nếu chuyển gửi đến các phòng xét nghiệm khẳng định cần lưu trữ trong tủ lạnh đảm bảo nhiệt độ 4°c – 8°c nếu vận chuyển trong vòng 3-7 ngày, trong trường hợp mẫu không vận chuyển được trong vòng 7 ngày, mẫu cần bảo quản ở nhiệt độ (-20 °C).
- Đọc kết quả vào sơ đồ xét nghiệm/phiếu làm việc.
- Điền kết quả vào sổ xét nghiệm và trả kết quả.
- Thực hiện xét nghiệm bằng kỹ thuật miễn dịch đánh dấu/hóa phát quang/điện hóa phát quang.
- Xây dựng quy trình sừ dụng của từng loại sinh phẩm cụ thể bằng tiếng việt.
- Sinh phẩm, mẫu bệnh phẩm được bảo quản trong tù lạnh đảm bảo nhiệt độ yêu cầu.
- Lập sơ đồ xét nghiệm trước mỗi lần thực hiện xét nghiệm. Sơ đồ xét nghiệm thể hiện các thông tin về sinh phẩm, số lô, hạn sử dụng, ngày thực hiện, người thực hiện,
- Sử dụng trang bị bảo hộ cá nhân trong suốt thời gian làm việc tại phòng xét nghiệm.
- Kiểm tra các mẫu trước khi thực hiện xét nghiệm trong trường hợp có hiện tượng có sợi tơ huyết, đông dây thì ống mẫu cần phải được ly tâm trước khi thực hiện xét nghiệm. Máy ly tâm phù hợp với ống nghiệm sử dụng và tốc độ ly tâm 3000-3500 vòng/phút trong 10 phút.
- Thực hiện xét nghiệm theo đúng quy trình, hướng dẫn của nhà sản xuất.
- Thực hiện xét nghiệm tại khu vực bàn xét nghiệm, dễ làm sạch bằng các chất khử khuẩn, đảm bảo đủ ánh sáng và tránh luồng gió. Sàn, tường và bàn xét nghiệm bằng phẳng, không thấm nước, chịu được nhiệt độ cao và các loại hóa chất ăn mòn, dễ cọ rửa vệ sinh.
- Thực hiện đầy đủ chứng theo yêu cầu của nhà sản xuất.
- Khi thực hiện xét nghiệm các dụng cụ khi rửa cần được rửa trong bồn rửa sâu tối thiểu 30cm, bằng chất liệu không thấm nước, chịu được các loại hóa chất ăn mòn;
- Hệ thống máy miễn dịch đánh dấu/hóa phát quang/điện hóa phát quang được bảo quản trong điều kiện khô bằng máy điều hòa nhiệt độ hoặc máy hút ẩm.
- Thời gian chờ đọc kết quả sử dụng đồng hồ đếm ngược chuyên dụng cho xét nghiệm.
- Chỉ đọc và biện luận kết quả khi mẫu chứng đạt yêu cầu của nhà sản xuất. Trong trường hợp sử dụng mẫu nội kiếm thì ngoài chứng của nhà sản xuất đạt yêu cầu, chứng nội kiểm cũng đạt yêu cầu khi đó mới biện luận kết quả.
- Các chất thải lây nhiễm phát sinh trong quá trình thực hiện xét nghiệm phải được xử lý trước khi chuyển vào nơi chứa chất thải chung theo quy định.
- Biện luận, trả kết quả
- Nếu kết quả xét nghiệm âm tính: tư vấn và trả kết quả âm tính cho khách hàng.
- Nếu kết quả xét nghiệm có phản ứng: tư vấn cho khách hàng, kết quả chưa xác định, mẫu cần làm thêm các xét nghiệm tại phòng xét nghiệm khẳng định để có kết quả cuối cùng. Tư vấn hẹn trả kết quả và chuyển mẫu bệnh phẩm hoặc giới thiệu khách hàng đến cơ sở xét nghiệm khẳng định theo quy định. Sau khi có kết quả khẳng định, tư vấn trả kết quả xét nghiệm HIV cho khách hàng theo quy định.
- Ghi chép biểu mẫu và quản lý số liệu
- Cơ sở thực hiện xét nghiệm sàng lọc HIV sau khi xét nghiệm có kết quả trên sơ đồ xét nghiệm/phiếu làm việc, kết quả được ghi chép vào sổ xét nghiệm.
- Thông tin trong sổ xét nghiệm cần có các thông tin tối thiểu sau: Thông tin hành chính (tên, tuổi, giới, địa chỉ, đối tượng), ngày thu thập mẫu, ngày xét nghiệm, kết quả của các sinh phẩm sử dụng và kết luận về tình trạng của mẫu, kết quả khẳng định của đơn vị khẳng định. Có thể tham khảo các biểu mẫu sổ sách tại phụ lục IV-A.
- Các kết quả xét nghiệm cần được lưu hồ sơ theo đúng quy định, không tẩy xóa.
- Cán bộ phụ trách phòng xét nghiệm chịu trách nhiệm kiểm tra toàn bộ thông tin xét nghiệm và hồ sơ xét nghiệm trước khi ký kết quả.
- Hồ sơ xét nghiệm phải lưu giữ 5 năm. Sau thời gian lưu nếu hủy cần có biên bản hủy.
- Đảm bảo chất lượng xét nghiệm
- Giai đoạn trước xét nghiệm
- Phòng xét nghiệm cần xây dựng các quy trình chuẩn phục vụ cho thu thập, đóng gói, bảo quản, vận chuyển mẫu bệnh phẩm cũng như các quy định về tiêu chuẩn chấp nhận, từ chối mẫu với các yêu cầu cơ bàn về thể tích mẫu, chất lượng mẫu, loại chất chống đông, nhiệt độ, thời gian bảo quản, thông tin trên ống đựng mẫu và phiếu yêu cầu xét nghiệm. Chỉ những mẫu đáp ứng yêu cầu mới được tiếp nhận. Các quy trình cần xây dựng ngắn gọn phù hợp với việc thực hiện tại đơn vị và với các quy định của Bộ Y tế, để ở nơi dễ tiếp cận.
- Có các quy định về an toàn phòng xét nghiệm, các quy định ra vào phòng xét nghiệm, xử lý sự cố tràn đổ, xử lý phơi nhiễm, phòng chống cháy, nô, phân loại rác thải.
- Các hướng dẫn thực hiện xét nghiệm của sinh phẩm sử dụng cần viết dưới dạng quy trình chuẩn.
- Giai đoạn trong xét nghiệm
- Sinh phẩm và vật tư tiêu hao.
- Chỉ sử dụng sinh phẩm còn hạn sử dụng, hạn ghi trên hộp và hạn sau khi mở hoặc pha các thuốc thử.
- Trong mỗi lần thực hiện xét nghiệm, chỉ sử dụng sinh phẩm trong cùng một hộp hoặc cùng lô. Luôn kiểm tra sinh phẩm, hóa chất và vật tư khi tiếp nhận, cần lưu ý đến tính toàn vẹn, nhiệt độ bảo quản, hạn sử dụng của các sinh phẩm, hóa chất và vật tư.
- Trước mỗi lần sử dụng, cần quan sát kỹ, nếu phát hiện có dấu hiệu bất thường cần ngưng sử dụng, tìm hiểu nguyên nhân và báo cho nhà cung cấp.
- Có số quản lý sinh phẩm, vật tư tránh hết hạn.
- Trang thiết bị.
- Trang thiết bị cần có hồ sơ quản lý bao gồm: Hồ sơ đánh giá sau lắp đặt, biên bản giao nhận, lý lịch máy, nhật ký sử dụng máy (đối với các thiết bị lạnh, nhật ký máy là phiếu theo dõi nhiệt độ hàng ngày). Có quy trình hướng dẫn sử dụng trang thiết bị bằng tiếng Việt và bản hướng dẫn sử dụng thiết bị dạng tóm tắt dán ở vị trí thuận tiện cho việc tra cứu trong quá trình sử dụng.
- Trang thiết bị được bảo dưỡng, bảo trì và hiệu chuẩn định kỹ theo quy định.
- Giai đoạn trong xét nghiệm
- Cơ sở vật chất
- Khu vực xét nghiệm phải gọn gàng, sạch sẽ đảm bảo đủ không gian để thực hiện xét nghiệm.
- Có biển báo nguy hiểm sinh học trên cửa ra vào của khu vực xét nghiệm
- Cần có hộp sơ cứu và dụng cụ rùa mất khẩn cấp, đảm bảo có nước sạch để khi cần có thể sử dụng ngay.
- Các trang thiết bị, máy móc của phòng xét nghiệm cần có bộ phận tiếp đất.
- Các thiết bị phòng, chống cháy nổ phải được kiểm tra định kỹ.
- Các chất thải cần được đựng trong các thiết bị, dụng cụ chứa chất thải y tế chuyên dụng và xử lý đúng quy định.
- Nhân sự
- Thường xuyên được đào tạo, cập nhật kiến thức và đánh giá năng lực nhân viên định kỹ hàng năm về kỹ thuật xét nghiệm tại đơn vị.
- Các cán bộ phòng xét nghiệm cần được giám sát sức khỏe định kỹ.
- Thực hiện xét nghiệm
- Có đầy đủ các quy trình xét nghiệm thực hiện tại đơn vị. Nên có bản hướng dẫn thực hiện xét nghiệm dạng rút gọn đặt ở vị trí thuận tiện cho việc theo dõi trong quá trình xét nghiệm. Các quy trình cần cập nhật ngay những thay đổi của nhà sản xuất và định kỹ hàng năm rà soát lại các quy trình.
- Tuân thủ đúng quy trình đã phê duyệt.
- Trong quá trình xét nghiệm luôn đối chiếu mẫu thử trên thanh xét nghiệm với phiếu sơ đồ.
- Tuân thủ đúng chiến lược và phương cách xét nghiệm.
- Giai đoạn sau xét nghiệm
- Các kết quả sau khi thực hiện xét nghiệm cần vào sổ xét nghiệm và có sự soát xét của người có thẩm quyền.
- Các hồ sơ xét nghiệm, kết quả của khách hàng cần được quản lý khoa học đảm bảo tính bảo mật và dễ dàng hồi cứu khi cần.
- Giám sát đảm bảo chất lượng
- Phòng xét nghiệm luôn thực hiện giám sát việc tuân thủ các quy trình chuẩn của nhân viên.
- Thực hiện đầy đủ mẫu chứng của nhà sản xuất và khuyến khích thực hiện mẫu nội kiểm chứng. Tần suất thực hiện mẫu nội kiểm chứng tùy thuộc vào cỡ mẫu của mỗi đơn vị.
- Có chứng nhận tham gia chương trình ngoại kiểm tra:
+ Tham gia đầy đù theo đúng quy định.
+ Thực hiện các mẫu ngoại kiểm tra như thường quy và trả kết quả cho nhà cung cấp mẫu đúng thời gian yêu cầu.
+ Khi nhận kết quả phản hồi cần xem xét kết quả ngoại kiểm. Trong trường hợp có kết quả không phù hợp cần tìm hiểu nguyên nhân và biện pháp khắc phục.
- Tổ chức giám sát hỗ trợ kỹ thuật:
+ Trung tâm phòng chống HIV/AIDS/cơ quan được giao chức năng, nhiệm vụ về công tác phòng chống HIV/AIDS của tỉnh kiểm tra giám sát hỗ trợ kỹ thuật định kỹ hoặc đột xuất hoạt động của các phòng xét nghiệm sàng lọc trên địa bàn tỉnh tối thiểu 1 lần/năm.
+ Các đơn vị thực hiện kiểm tra chéo hoặc kiểm tra nội bộ hàng năm.
- An toàn sinh học phòng xét nghiệm
- Cơ sở có phòng xét nghiệm cần phân công người chịu trách nhiệm về an toàn sinh học.
- Các cán bộ trực tiếp thực hiện xét nghiệm, người chịu trách nhiệm về an toàn sinh học phải được tập huấn về an toàn sinh học.
- Các cán bộ khác làm việc trong khu vực xét nghiệm phải được hướng dẫn về an toàn sinh học phù hợp với công việc.
- Có quy định ra vào khu vực xét nghiệm.
- Có kể hoạch đánh giá nguy cơ xảy ra sự cổ an toàn sinh học tại cơ sở xét nghiệm và xây dựng kế hoạch phòng ngừa, xừ lý xự cố an toàn sinh học.
- Không dùng pipét hút bằng miệng và không sử dụng bơm kim tiêm để thay thế pipét; bơm kim tiêm sau khi sử dụng phải được cho vào hộp đựng vật sắc nhọn chuyển biệt hoặc máy hủy tự động, không uốn cong, bẻ gãy, đậy lại nắp kim tiêm.
- Trước khi dời khỏi phòng xét nghiệm cần rửa sạch tay hoặc rửa tay ngay sau khi vùng da tiếp xúc với các hóa chất hóa học.
- Mặc áo bảo hộ, đi giày, dép kín mũi chân khi làm việc trong phòng xét nghiệm, không mặc quần áo bảo hộ ra khu vực công cộng.
- Sử dụng găng tay trong tất cả quá trình tiếp xúc trực tiếp hoặc có nguy cơ tiếp xúc với các chất lây nhiễm. Sau khi sử dụng, tháo bỏ găng tay đúng cách và phải rửa tay.
- Không để chung quần áo bảo hộ với quần áo thông thường.
- Không mang đồ dùng cá nhân, thực phẩm vào phòng xét nghiệm.
- Không sử dụng thiết bị phòng xét nghiệm để cất trữ hoặc chế biến thực phẩm.
- Không ăn uống, hút thuốc, cạo râu và sử dụng mỹ phẩm trong phòng xét nghiệm.
- Khử nhiễm bề mặt bàn làm việc ngay sau khi kết thúc xét nghiệm, vào cuối ngày làm việc hoặc khi có sự cố tràn, đổ mẫu bệnh phẩm chứa tác nhân gây bệnh.
- Phân loại, vận chuyển và xử lý chất thải theo quy định.
- Xét nghiệm chẩn đoán nhiễm HIV
Các yêu cầu về nhân sự, cơ sở vật chất, trang thiết bị và năng lực xét nghiệm cần đáp ứng theo Nghị định số 75/NĐ-CP ngày 01/7/2018 của Chính phủ quy định điều kiện thực hiện xét nghiệm HIV.
- Lấy mẫu, vận chuyển, bảo quản bệnh phấm xét nghiệm: Thu thập mẫu thực hiện theo các quy định tại mục 1 phần II chương này
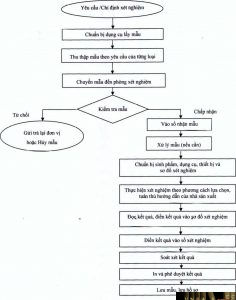
- Thực hiện xét nghiệm
2.1. Lưu đồ thực hiện xét nghiệm
1.2. Thực hiện xét nghiệm chẩn đoán nhiễm HIV bằng kỹ thuật xét nghiệm đom giàn áp dụng theo quy định tại khoản 2.2. mục 2 phần II chương này.
1.3. Thực hiện xét nghiệm chẩn đoán nhiễm HIV bằng kỹ thuật miễn dịch đánh dấu/hóa phát quang/điện hóa phát quang áp dụng theo quy định tại khoản 2.3. mục 2 phần II chương này.
1.4. Lưu giữ mẫu
– Các mẫu sau khi xét nghiệm có kết quả dương tính hoặc không xác định cần được lưu giữ tối thiểu 2 năm kể từ ngày có kết quả xét nghiệm khẳng định ờ nhiệt độ (-20° C) hoặc lạnh hơn. Hết thời gian lưu nếu đơn vị hủy mẫu cần có biên bản hủy mẫu, lưu giữ biên bản hủy theo quy định.
– Các ống nghiệm lưu mẫu ở nhiệt độ âm sâu phải là các ống nghiệm chuyên dụng có nắp xoáy chặt. Các ống nghiệm xếp trong hộp chuyên dụng. Phải ghi rõ thông tin về mẫu trên ống nghiệm bằng loại mực không xóa được, hoặc sử dụng nhãn chuyên dụng chịu được nhiệt độ âm sâu.
– Các mẫu khi lưu phải có mà số và ghi chép trong sổ lưu mẫu theo quy định.
- Biện luận, trả kết quả
– Phân tích và biện giải kết quả xét nghiệm theo sơ đồ chiến lược III tại phụ lục I.- Trả kết quả xét nghiệm cho cơ sở gửi mẫu hoặc bệnh nhân theo quy định.
– Kết quả xét nghiệm cần được trả sớm nhất cho đơn vị gửi mẫu trong thời gian tối đa là 01 ngày với kết quả âm tính và tối đa 03 ngày với kết quả HIV dương tính.
– Cơ sở y tế trả kết quả cho bệnh nhân trong vòng tối đa 72 giờ sau khi có kết quả khẳng định HIV chính thức.
- Ghi chép biểu mẫu và quản lý số liệu
– Cơ sở thực hiện xét nghiệm khẳng định HIV sau khi có kết quả xét nghiệm trên sơ đồ xét nghiệm/phiếu làm việc, bản đọc, các kết quả xét nghiệm này phải được ghi chép vào sổ xét nghiệm theo quy định tại phụ lục ỈY-A ban hành kèm theo Hướng dẫn này.
– Các kết quả xét nghiệm cần được lưu hồ sơ theo đúng quy định, không sử dụng bút xóa đc sừa các sai sót. Trong trường hợp có sự sai sót cần: gạch ngang, ghi lại thông tin đúng và ký xác nhận của người có thẩm quyền.
– Cán bộ phụ trách phòng xét nghiệm chịu trách nhiệm kiểm tra toàn bộ thông tin xét nghiệm và hồ sơ xét nghiệm trước khi ký kết quả trả cho khách hàng.
– Hồ sơ xét nghiệm phải lưu giữ 5 năm. Sau thời gian lưu nếu hủy cần có biên bản hủy.
- Đảm bảo chất lượng xét nghiệm
Thực hiện theo các quy định tại mục 5 phần II chương này và các quy định sau:
5.1. Nhân sự:
– Cán bộ phụ trách cần có khả năng phân tích biện luận kết quả xét nghiệm với các trường hợp chẩn đoán HIV âm tính, dương tính, dương tính yêu và không xác định.
– Các cán bộ phòng xét nghiệm HIV cần có kiến thức về kỹ thuật xét nghiệm Iirv, quản lý đảm bảo chất lượng xét nghiệm và các kiến thức pháp luật khác có liên quan.
5.2. Giám sát đảm bảo chất lượng:
– Các Viện Vệ sinh dịch tễ Trung ương, Viện Pasteur Thành phố Hồ Chí Minh. Viện Pasteur Nha Trang, Viện Vệ sinh dịch tễ Tây Nguyên kiểm tra giám sát hỗ trợ kỹ thuật định kỳ hoặc đột xuất hoạt động của các cơ sở xét nghiệm đã được cấp giấy chứng nhận đủ điều kiện khẳng định các trường hợp HIV dương tính thuộc khu vực phân công tối thiểu 1 lần/năm.
- An toàn sinh học phòng xét nghiệm
Thực hiện theo các quy định tại mục 6 phần II chương này
Chương II
XÉT NGHIỆM SINH HỌC PHÂN TỬ
- Thực hiện chẩn đoán sớm nhiễm HIV cho trẻ dưới 18 tháng tuổi.
- Đối tượng được chẩn đoán sớm nhiễm HIV
– Trẻ phơi nhiễm HIV dưới 18 tháng tuổi (trẻ sinh ra từ người mẹ nhiễm HIV).
– Trẻ dưới 18 tháng tuổi có dấu hiệu hoặc triệu chứng lâm sàng nghi ngờ nhiễm HIV và có kết quả xét nghiệm sàng lọc kháng thể kháng HIV dương tính.
- Năng lực thực hiện xét nghiệm chẩn đoán sớm nhiễm HIV cho trẻ dưới 18 tháng tuổi
Được Bộ Y tế hoặc cơ quan có thẩm quyền thẩm định cấp giấy chứng nhận đủ điều kiện khẳng định thực hiện xét nghiệm HIV bằng kỹ thuật sinh học phân tử cho trẻ dưới 18 tháng tuổi.
- Quy trình thực hiện
Chẩn đoán sớm HIV được thực hiện ngay khi trẻ đến cơ sở y tế lần đầu tiên quy trình tư vấn, chẩn đoán, chăm sóc, dự phòng và điều trị theo quy định tại hướng dẫn quốc gia về chẩn đoán và điều trị HIV/AIDS.
3.1. Tư vấn trước xét nghiệm, chỉ định xét nghiệm và điền các thông tin cần
thiết.
3.1.1. Tư vấn: Thực hiện tư vấn trước xét nghiệm theo các quy định tại hướng dẫn chẩn đoán và điều trị HIV/A1DS hiện hành. Đối với phần xét nghiệm cần chú ý
các nội dung sau:
– Lợi ích của chẩn đoán sớm nhiễm HIV và cách lấy mẫu xét nghiệm;
– Số lần xét nghiệm và thời gian trả kết quả xét nghiệm;
– Khẳng định về tính bảo mật của xét nghiệm.
3.1.2. Chỉ định xét nghiệm: Thực hiện theo hướng dẫn quốc gia về chẩn đoán và điều trị HI V/AIDS hiện hành
3.1.3. Điền các thông tin cần thiết:
Điền đủ thông tin vào “Phiếu xét nghiệm chẩn đoán sớm nhiễm HIV cho trẻ dưới 18 tháng tuổi” và “Phiếu gửi mẫu xét nghiệm chẩn đoán sớm nhiễm HIV cho trẻ dưới 18 tháng tuổi” theo quy định (mẫu số 1 và mẫu số 2, phụ lục 1V-C).
3.2. Lấy mẫu, vận chuyển, bảo quản
3.2.1. Lấy mẫu, vận chuyển:
– mẫu sử dụng để xét nghiệm sinh học phân tử có thể là mẫu giọt máu khô (DBS – Dried Blood Spot) trên giấy thấm, máu toàn phần chống đông bằng EDTA (Acid Ethylene Diamine Tetra Acetic).
– Lấỵ mẫu máu xét nghiệm bằng bộ dụng cụ lấy giọt máu khô (DBS) hoặc bộ dụng cụ lây máu toàn phân có chất chống dông bằng EDTA trong các điều kiện an toàn theo quy định.
– Điền đầy đù thông tin vào phiếu gửi mẫu và phiếu xét nghiệm theo Phụ lục IV-C, mẫul,2.
Quy trình lấy máu, đóng gói, vận chuyến, tiếp nhận mẫu giọt máu khô và/hoặc máu toàn phần chi tiết như phụ lục 11,111.
3.2.2. Tiếp nhận mẫu
Đơn vị thực hiện xét nghiệm khi tiếp nhận mẫu cần:
– Kiểm tra tình trạng mẫu, đối chiếu thông tin trên DBS/ống đựng máu, phiếu xét nghiệm. Trong trường hợp có sự sai lệch giữa thông tin trên phiếu và trên DBS/ống mẫu đơn vị gửi mẫu cần xác nhận thông tin đúng, hoặc kết quả sẽ trả theo thông tin trên DBS/ống đựng mẫu.
– Thông báo cho nơi gửi xét nghiệm lấy lại mẫu trong các trường hợp mẫu không đạt yêu cầu:
+ Máu toàn phần, huyết tương: tán huyết, không đủ thể tích, chống đông bằng Heparine, thời gian từ lúc lấy mẫu đến lúc chuyển phòng xét nghiệm trên 8 giờ, bảo quản, vận chuyển ở nhiệt độ không đúng quy định tại phụ lục III.
+ DBS: giọt máu quá nhỏ không đủ để thực hiện xét nghiệm, mẫu chưa khô, giấy bị ẩm, mẫu nhiễm nấm, lấy mẫu không đúng kỹ thuật tạo vẩy (tham khảo phụ lục II).
– Thông báo cho nơi gừi mẫu xét nghiệm bổ sung thông tin trong trường hợp: thiếu thông tin về địa chì, ngày, thu thập mẫu trên phiếu xét nghiệm.
3.2.3. Bào quản mẫu:
– Máu toàn phần trong trường hợp chưa nhỏ ngay lập tức vào giấy thấm giọt máu khô DBS cần được bảo quản trong tủ lạnh 2°c – 8°c và nhỏ vào giấy DBS hoặc xét nghiệm trong vòng 8 giờ kể từ lúc lấy mẫu.
– Huyết tương cần được bảo quản ở tủ đông sâu (-70°C) trở xuống cho đến khi thực hiện xét nghiệm.
– mẫu DBS sau khi tiếp nhận, nếu không thực hiện xét nghiệm ngay thì cần được bảo quản ở tủ đông sâu (-20°C) trở xuống cho đến khi thực hiện xét nghiệm
3.3. Thực hiện xét nghiệm:
– Thực hiện xét nghiệm chẩn đoán sớm nhiễm HIV bằng kỹ thuật PCR theo hướng dẫn của nhà sản xuất với thiết bị phù hợp theo yêu cầu của sinh phẩm sử dụng.
– Sinh phẩm sử dụng trong xét nghiệm chẩn đoán sớm phải có số lưu hành còn hiệu lực hoặc được Bộ Y tế cho phép sử dụng và đang còn hạn sử dụng. Sinh phẩm sử dụng phải được bảo quản theo đúng hướng dẫn của nhà sản xuất.
– Chuẩn bị mẫu và xữ lý mẫu phải thực hiện trong tủ an toàn sinh học cấp II.
– Mỗi khu vực xét nghiệm phải có các dụng cụ, thiết bị riêng để tránh nhiễm chéo trong quá trình thực hiện bao gồm: tủ lạnh, tủ đông sâu, bộ pi pét, máy ly tâm (lạnh) cho loại ống phù hợp với từng giai đoạn xét nghiệm, máy trộn – lắc, máy ủ.
– Sử dụng đồng hồ đếm ngược chuyên dụng trong các bước xét nghiệm cần đếm thời gian.
– Sử dụng trang phục bảo hộ cá nhân phù hợp trong suốt thời gian làm việc tại phòng xét nghiệm.
– Thực hiện việc bảo quản mẫu bệnh phẩm trong tủ đông sâu (-20°C) trở xuống theo quy định, thời gian lưu mẫu dương tính ít nhất là 2 năm, mẫu âm tính ít nhất 06 tháng sau khi đã làm xét nghiệm.
– Nhân dán trên mẫu bệnh phẩm cần sử dụng nhãn không thấm nước và không bị bong ở nhiệt độ âm sâu.
- Trả lời kết quả
4.1. Thời gian trả lời kết quả
– Kết quả xét nghiệm PCR cần được trả cho cơ sở chỉ định xét nghiệm trong vòng 02 tuần kể từ ngày phòng xét nghiệm nhận được mẫu.
-Trong trường hợp không trả được kết quả trong vòng 02 tuần, phòng xét nghiệm cần thông báo cho cơ sở chỉ định xét nghiệm lý do và thời hạn sẽ trả kết quả.
- 1. Theo dõi và xử lý sau khỉ có kết quả xét nghiệm
Khi có kết quả xét nghiệm, cơ sở chì định xét nghiệm PCR cần xử trí theo
hướng dẫn về chẩn đoán và điều trị HIV/AIDS của Bộ Y tế hiện hành.
- Ghi chép biểu mẫu và quản lý số liệu
– Cơ sở thực hiện xét nghiệm chẩn đoán sớm cho trẻ em dưới 18 tháng tuổi sau khi có kết quả xét nghiệm trên sơ đồ xét nghiệm/phiếu làm việc, bàn đọc, các kết quả xét nghiệm này phải được ghi chép vào sổ sách xét nghiệm theo quy định tại phụ lục IV-C ban hành kèm theo Hướng dẫn này.
– Các kết quả xét nghiệm cần được lưu hồ sơ theo đúng quy định, không sừ dụng bút xóa để sữa các sai sót. Trong trường hợp có sự sai sót cần, gạch ngang, ghi lại thông tin đúng và ký xác nhận của người có thẩm quyền.
– Cán bộ phụ trách phòng xét nghiệm chịu trách nhiệm kiểm tra toàn bộ thông tin xét nghiệm và hồ sơ xét nghiệm trước khi ký kết quả trả cho khách hàng.
– Hồ sơ xét nghiệm phải lưu giữ 5 năm. Sau thời gian lưu nếu hủy cần có biên bản hủy.
- Đảm bảo chất lượng xét nghiệm
Thực hiện như mục 5 phần II chương I và các quy định sau:
3.1. Sinh phẩm và vật tư tiêu hao: chỉ sử dụng dụng cụ chuyên dùng cho xét nghiệm sinh học phân tử: găng tay không bột, đầu típ có lọc. các loại ống không có men tiêu hủy axít nucleotit.
3.2. Thiết bị: phải phù hợp với kỹ thuật sử dụng tại đơn vị và đảm bảo mỗi khu vực phải có dụng cụ, thiết bị riêng để tránh nhiễm chéo.
3.3. Cơ sở vật chất
– Nếu đơn vị sừ dụng hệ thống thiết bị tự động – khép kín hoàn toàn thì cần bố trí vị trí lắp đặt theo đúng yêu cầu của nhà sản xuất và đảm bảo hạn chế được nguy cơ lây nhiễm chéo cho các hoạt động khác.
– Nếu đơn vị sử dụng hệ thống thiết bị không khép kín: cần bố trí tối thiểu 3 khu vực tách biệt hoàn toàn cho các giai đoạn: chuẩn bị hoá chất, chuân bị mẫu, khuếch đại và phân tích mẫu PCR
3.4. Nhân sự
– Phải được tập huấn và có kinh nghiệm thực hiện xét nghiệm sinh học phân tử, xét nghiệm HIV
– Cán bộ phụ trách cần có khả năng phân tích, biện giãi kết quả xét nghiệm
HIV.
- An toàn sinh học phòng xét nghiệm
– Thực hiện theo quy định tại mục 6 phần II chương I và các quy định về An toàn Sinh học cấp n.
- Đối với trẻ trên 18 tháng tuổi và người lớn.
- Đổi tượng xét nghiệm:
- Các trường hợp xét nghiệm huyết thanh học HIV không biện luận được kêt
quả.
- Trong trường hợp sàng lọc máu bằng kỹ thuật NAT thì thực hiện theo quy định hiện hành về hoạt động truyền máu và sàng lọc đơn vị máu an toàn.
- Năng lực thực hiện xét nghiệm
Thực hiện như phần I, mục 2, chưcmg II của Hướng dẫn này.
- Quy trình xét nghiệm
- 1. Lấy mẫu máu:
– Điền đủ thông tin vào “Phiếu xét nghiệm PCR định tính HIV cho trẻ >18 tháng tuổi và người lớn” theo quy định tại biểu mẫu số 4, phụ lục IV-C ban hành kèm theo hướng dẫn này.
– mẫu sử dụng để xét nghiệm sinh học phân tử có thể là DBS, máu toàn phần, huyết tương.
– Quy trình lấy máu, đóng gói, vận chuyển, tiếp nhận mẫu DBS theo quy định tại phụ lục II ban hành kèm theo hướng dẫn này.
– Quy trình lấy máu, đóng gói, vận chuyển, tiếp nhận máu toàn phần và huyết tương theo quy định tại phụ lục III ban hành kèm theo hướng dẫn này.
- 2. Tiến hành xét nghiệm và một số lưu ý
– Sinh phẩm sử dụng phải có số lưu hành còn hiệu lực hoặc được Bộ Y tế cho phép sử dụng và đang còn hạn sử dụng.
– Thực hiện xét nghiệm bằng kỹ thuật PCR theo hướng dẫn của nhà sản xuất.
– Thực hiện việc bảo quản mẫu bệnh phẩm trong tủ đông sâu (-70°C) trờ xuống theo quy định, thời gian lưu mẫu dương tính ít nhất là 2 năm.
– Nhãn dán trên mẫu bệnh phẩm sử dụng nhãn không thấm nước và không bị bong ở nhiệt độ âm sâu.
– Việc hủy mẫu phải tiến hành theo Thông tư liên tịch số 58/2015/TTLT- BYT-BTNMT ngày 31/12/2015 quy định về quản lý chất thải y tế và các qui định pháp luật có liên quan.
– Hủy mẫu lưu dương tính và nghi ngờ: sau khi hết thời gian lưu mẫu theo quy định, việc hủy mẫu cần phải lập biên bản ghi rò thời gian và danh sách các mẫu đã hùy. Biên bản này phải lưu trong thời gian 5 năm kể từ ngày hủy mẫu.
- 3. Trả lời kết quả
3.3.1. Thời gian trả lời kết quả
– Kết quả xét nghiệm PCR cần được trả cho cơ sở chỉ định xét nghiệm trong vòng 02 tuần kể lừ ngày phòng xét nghiệm nhận được mẫu.
– Trong trường hợp không trả được kết quả trong vòng 02 tuần, phòng xét nghiệm cần thông báo cho cơ sở chỉ định xét nghiệm lý do và thời hạn sẽ trả kêt quả.
3.3.2. Ghi chép kết quả
– Nếu kết quả xét nghiệm PCR âm tính, ghi bằng chữ “Âm tính” vào phần “Trà lời kết quả xét nghiệm”.
– Nếu kết quả xét nghiệm PCR dương tính, ghi bằng chừ “Dương tính” vào phần “Trà lời kết quả xét nghiệm”.
3.3.3. Trả lời kết quả
Kết quả xct nghiệm HIV theo quy định tại biểu mẫu số 4, phụ lục IV-C ban hành kèm theo hướng dẫn này, phải được ghi đầy đủ kết quả xét nghiệm, chừ ký và họ tên đầy đủ của cán bộ thực hiện xét nghiệm và trưởng khoa hoặc trường phòng xét nghiệm. Các phiếu này được khoa hoặc phòng xét nghiệm trả lại cho cơ sở chì định xét nghiệm.
3.3.4. Tư vấn và xử trí khi có kết quả xét nghiệm
Khi có kết quả xét nghiệm, cơ sở chì định xét nghiệm PCR cần tư vấn cho khách hàng theo hướng dẫn tư vân xét nghiệm HIV trong cơ sở y tê của Bộ Y tê hiện hành.
- Nếu kết quả dương tính
Cán bộ y tế của đơn vị lấy mẫu cần thực hiện các nội dung dưới đây ngay sau khi có kết quả PCR dương tính:
– Liên hệ đơn vị thực hiện xét nghiệm để xem xét việc lấy mẫu lần 2 (nếu
cần).
– Thông báo kết quả xét nghiệm và tư vấn theo quy định.
– Tiếp tục theo dõi tại Cơ sở chăm sóc và điều trị HĨV/AIDS.
- Nếu kết quả âm tính
Cán bộ y tế của đơn vị lấy mẫu cần thực hiện các nội dung dưới đây ngay sau khi có kết quả PCR âm tính:
– Thông báo kết quả xét nghiệm và tư vấn theo quy định.
– Giải thích ý nghĩa của kết quả xét nghiệm:
+ Đối với trường hợp phơi nhiễm trên 02 tuần có khả năng không nhiễm HIV, nhưng vẫn cần phải được tiếp tục theo dõi và làm xét nghiệm phát hiện kháng thể kháng HIV sau 3 tháng và 6 tháng kể từ khi phơi nhiễm.
+ Đối với trường hợp phơi nhiễm dưới 02 tuần vẫn có nguy cơ nhiễm HIV do đó cần xét nghiệm sinh học phân tử sau 02 tuần hoặc xét nghiệm phát hiện kháng thể kháng HIV sau 3 tháng và 6 tháng kể từ khi phơi nhiễm.
- Biểu mẫu ghi chép, quản lý số liệu
Thực hiện theo các quy định tại mục 5 phần I chương này.
- Quản lý đảm bảo chất lượng
Thực hiện theo các quy định tại mục 6 phần I chương này.
- An toàn sinh học
Thực hiện theo các quy định tại mục 7 phần I chương này.
Chương III
XÉT NGHIỆM LẠI HIV
- Xét nghiệm định kỳ HIV trong các trường hợp có hành vi nguy cơ cao tiếp diễn:
- Các trường hợp HIV âm tính trong nhóm có nguy cơ cao cần xét nghiệm định kỳ 06 tháng/lần:
– Nhóm quần thể hành vi nguy cơ cao
– Người có bạn tình nhiễm HIV
– Bệnh nhân nhiễm các bệnh lây truyền qua đường tình dục
– Người dự phòng sau phơi nhiễm (PEP) và trước phơi nhiễm (PrEP)
- Thực hiện xét nghiệm HIV theo đúng các quy định tại chương II hướng dẫn
này.
* Lưu ý: Các trường hợp nghi ngờ giai đoạn cửa sổ nên xét nghiệm lại trong vòng 3 tháng.
- Xét nghiệm HIV trong các trường hợp đã và đang điều trị ARV khi cần thiết.
- Nguyên tắc chung:
– Không khuyến cáo xét nghiệm lại HIV cho các bệnh nhân đã, đang điều trị ARV.
- Xác định tình trạng nhiễm HIV trong trường hợp cần thiết:
2.1. Những trường hợp đã có xét nghiệm đo tải lượng HIV trong quá trình theo dõi điều trị thuốc ARV:
– Nếu kết quả xét nghiệm tải lượng HIV trên ngưỡng phát hiện thì khẳng định tình trạng nhiễm HIV.
– Nếu kết quả xét nghiệm tải lượng HIV dưới ngưỡng phát hiện thì thực hiện xét nghiệm lại huyết thanh học phải xét nghiệm đủ 3 sinh phẩm theo phương cách quốc gia tại các cơ sở xét nghiệm được phép khẳng định HIV dương tính, cụ thể như sau:
+ Nếu kết quả dương tính theo chiến lược III thì trả kết quả theo quy định.
+ Nếu kết quả âm tính hoặc không xác định thì thực hiện việc lấy mẫu lại để thực hiện thêm các xét nghiệm sinh học phân tử theo quy trình thực hiện xét nghiệm tại điểm 2.3 mục này.
2.2. Những trường hợp chưa có kết quả xét nghiệm tải lượng HIV trong quá trình theo dõi điều trị thuốc ARV thì thực hiện theo quy trình thực hiện xét nghiệm tại mục 2.3.
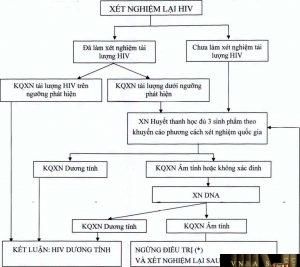
2.3. Quy trình thực hiện xét nghiệm lại:
QUY TRÌNH THỰC HIỆN XÉT NGHIỆM LẠI HIV
Ghi chú:
(*) Chỉ ngừng điều trị khi có kết quả xét nghiệm DNA
(**) Chỉ làm xét nghiệm lại 1 lần sau 3 tháng bằng xét nghiệm huyết thanh học:
– Nếu kết quả dương tính thì khẳng định nhiễm HIV và điều trị lại
– Nếu kết quả âm tính hoặc không xác định thì làm thêm xét nghiệm tải lượng HIV:
+ Nếu kết quả trên ngưỡng phát hiện thì khẳng định nhiễm HIV và điều trị lại + Nếu không phát hiện vật liệu di truyền thì kết luận âm tính.
III. Xét nghiệm HIV trong trường hợp điều trị dự phòng sau phơi nhiễm
HIV.
1. Cần tiến hành xét nghiệm HIV lại sau 3-6 tháng.
2. Việc thực hiện xét nghiệm HIV theo đúng các quy định tại chương II hướng dẫn này.
Phần III
TỔ CHỨC THỰC HIỆN
1. Trách nhiệm của cơ sở xét nghiệm sàng lọc HIV
1.1. Tiến hành việc lấy hoặc tiếp nhận mầu bệnh phẩm để thực hiện các kỹ thuật xét nghiệm phát hiện nhiễm HIV nhưng không được khắng định các trường họp HIV dương tính.
1.2. Tham gia chương trình ngoại kiểm tra xét nghiệm HIV do Bộ Y tế phê duyệt hoặc chỉ định.
1.3. Tổ chức thực hiện việc tư vấn xét nghiệm HIV, thông báo kết quả xét nghiệm HI V theo các quy định cùa Luật phòng, chống HIV/AIDS.
1.4. Thực hiện thống kê báo cáo số liệu theo quy định tại Thông tư số 09/2012/TT-BYT và ghi chép, lưu trữ biểu mẫu sổ sách xét nghiệm đầy đủ theo đúng quy định tại Quyết định này.
2. Trách nhiệm cùa cơ sở xét nghiệm khắng định HIV
Ngoài việc thực hiện các quy định tại mục 1, phần này, cơ sờ xét nghiệm khăng định HIV còn phái thực hiện các trách nhiệm sau:
1.1. Thực hiện các xét nghiệm chấn đoán HIV cho các mẫu bệnh phẩm thu thập trực tiếp.
1.2. Tiếp nhận các mầu bệnh phẩm nghi ngờ dương tính của các cơ sở xét nghiệm sàng lọc HIV trên địa bàn hoặc vùng lân cận để tiến hành xét nghiệm huyết thanh học khẳng định các trường hợp HIV dương tính. Lưu mầu dươne tính hoặc nghi ngờ 02 năm kể từ ngày làm xét nghiệm khẳng định tại cơ sở xét nghiệm.
1.3. Tham mưu hồ trợ cho Sờ Y tế trực thuộc tiến hành việc đào tạo, giám sát hồ trợ kỹ thuật và tham gia kiểm tra theo định kỳ 01 năm/lần hoạt động xét nghiệm tại các cơ sờ xét nghiệm sàng lọc HIV trên địa bàn phụ trách.
3. Trách nhiệm của phòng tham chiếu quốc gia về xét nghiệm HIV
3.1. Thực hiện các xét nghiệm chẩn đoán về huyết thanh học HIV và sinh học phân tử HIV.
3.2 Tiếp nhận các mẫu xét nghiệm nghi ngờ dương tính, các mầu khó biện luận do các cơ sở xét nghiệm được cấp Giấy chứng nhận đủ điều kiện xét nghiệm khẳng định các trường hợp HIV dương tính thuộc địa bàn phân công phụ trách gửi đến.
3.3. Nhận mầu và làm xét nghiệm tham chiếu khi kết quả xét nghiệm HIV giữa các tuyến không thống nhất.
3.4. Tổ chức triển khai và quản lý bảo đảm chất lượng cho hệ thống cơ sở xét nghiệm HIV.
3.5. tìánh giá năng lực thực hiện xét nghiệm của các cơ sở xét nghiệm nộp hồ sơ đề nghị cấp Giấy chứng nhận đủ điều kiện khẳng định các trường hợp HIV dương tính.
4. Trách nhiệm của Sở Y tế tỉnh
4.1. Chỉ đạo, kiểm tra công tác xét nghiệm HIV trên địa bàn tỉnh.
4.2. Chỉ định Trung tâm phòng, chống HIV/AIDS hoặc cơ quan được giao chức năng, nhiệm vụ về công tác phòng chống HIV/AIDS có cơ sở xét nghiệm khẳng định HIV hoặc phối hợp với đơn vị có cơ sở xét nghiệm khẳng định HIV xây dựng kế hoạch đào tạo, tổ chức đào tạo cấp chứng nhận cho cán bộ xét nghiệm HIV của các cơ sở xét nghiệm sàng lọc HIV tại địa bàn tỉnh/thành phố.
4.3. Kiến nghị sừa đồi, bổ sung nhằm khắc phục các bất cập liên quan đến thực hiện bảo đảm chất lượng xét nghiệm HIV trong quá trình thực hiện.
4.4. Phối hợp với-các sở, ban ngành có liên quan hồ trợ-và tổ chức giám sát việc triển khai xét nghiệm HIV.
4.5. Định kỳ hằng năm, báo cáo Bộ Y tế danh sách các cơ sở xét nghiệm khẳng định HIV, cơ sờ xét nghiệm sàng lọc HIV trên địa bàn.
5. Trách nhiệm của Viện Vệ sinh dịch tễ Trung ương, Viện Pasteur Thành phố Hồ Chí Minh, Viện Pasteur Nha Trang, Viện Vệ sinh dịch tễ Tây Nguyên
5.1. Đào tạo, hồ trợ kỹ thuật cho các cán bộ của các cơ sở xét nghiệm khẳng định HIV, cơ sở xét nghiệm sàng lọc H1V đối với các tinh không có cơ sờ xét nghiệm khẳng định HIV trên địa bàn được phân công phụ trách.
5.2. Kiểm tra giám sát các cơ sở xét nghiệm khẳng định HIV thuộc địa bàn được phân công định kỳ 1 lần/năm và báo cáo kết quả về Bộ Y tế (Cục phòng, chong HIV/AIDS).
6. Trách nhiệm của Cục Phòng, chống HIV/AIDS – Bộ Y tế
6.1. Chỉ đạo, kiểm tra, giám sát, đánh giá hoạt động và tổng hợp số liệu hoạt động xét nghiệm HIV trên phạm vi toàn quốc.
6.2. Chỉ đạo các cơ sở có phòng tham chiếu quốc gia về xét nghiệm H1V xây dựng tài liệu và tổ chức tập huấn về xét nghiệm HIV cho các đơn vị, địa phương.
6.3. Hằng năm, chủ trì, phổi họp tổ chức hội nghị đánh giá và triển khai công tác thực hiện bảo đảm chất lượng xét nghiệm HIV.
Phụ lục I
Sơ ĐỒ XÉT NGHIỆM HUYẾT THANH HỌC HIV
Ghi chú:
- Dấu (+): nghĩa là có phản ứng.
- Dấu (-): nghĩa là không phản ứng.
- (1) Kết quà phàn ứng này không được dùng cho mục đích chẩn đoán nhiễm HIV, vì vậy không thông báo kết quả cho người được xét nghiệm
Ghi chú:
– Dấu (+): nghĩa là có phản ứng.
– Dấu (-): nghĩa là không phản ứng.
– Các sinh phẩm xét nghiệm SP1, SP2 khác nhau về nguyên lý hoặc cách chuẩn bị kháng nguyên.
– (1) Kết quả này chỉ phục vụ cho mục đích giám sát dịch tễ học HIV/AIDS nên không thông báo cho người được xét nghiệm.
Ghi chú:
- – Dấu (+): nghĩa là có phản ứng.
- – Dấu (-): nghĩa là không phản ứng.
– Các sinh phẩm xét nghiệm SP1, SP2, SP3 khác nhau về nguyên lý hoặc cách chuẩn bị kháng nguyên.
– (1) Việc xét nghiệm lại bằng SP1, SP2 để kiểm tra loại trừ sai sót khi xét nghiệm bằng sinh phẩm SP1 hoặc SP2.
(2) Kết quả dương tính được dùng để kết luận các trường hợp nhiễm HIV khi xét nghiệm được thực hiện tại Phòng xét nghiệm đã được Bộ Y tế cho phép khẳng định các trường hợp nhiễm HIV.
(3) Trường hợp kết quả xét nghiệm không xác định, đề nghị lấy máu xét nghiệm lại lần thứ 2 sau 14 ngày và biện luận kết quả theo các tình huống sau:
– Nếu kết quả xét nghiệm lần 2 âm tính thì kết luận là âm tính.
– Nếu kết quả xét nghiệm lần 2 dương tính theo chiến lược 3 thì kết luận là dương
tính.
– Nếu kết quả lần 2 vẫn không xác định nhưng mức độ phản ứng với sinh phẩm của lần xét nghiệm thứ 2 không có sự thay đổi so với mức độ phản ứng với các sinh phẩm đã sử dụng trong xét nghiệm lần 1 và người được xét nghiệm không thuộc đối tượng có hành vi nguy cơ cao thì kết luận là âm tính.
– Sau 2 lần làm xét nghiệm mà không trả lời được kết quả các phòng xét nghiệm liên hệ phòng xét nghiệm tham chiếu tuyến trên và gửi mẫu nếu cần.
Phụ lục II
QUY TRÌNH LẤY MÁU GIỌT MAU KHÔ (DBS), ĐÓNG GÓI VÀ VẬN CHUYÊN CHO XÉT NGHIỆM SINH HỌC PHÂN TỦ HIV.
- LẤY MẪU MÁU
Cán bộ y tế đã được đào tạo tiến hành lấy mầu DBS theo một trong 2 cách dưới đây:
- Cách thứ nhất: Lấy giọt máu trực tiếp từ gót chân/ngón chân cái/ngón tay trên giấy thấm DBS
Bước 1: Điền đầy đù và chính xác các thông tin về tré được xét nghiệm trên tấm tấm DBS:
- – Họ lên đầy đủ
– Giới tính (Trai/Gái)
- – Ngày tháng năm sinh của trẻ (lịch dương)
- – Ngày lấy mẫu DBS
- – Tên cơ sở lấy mẫu, tên tỉnh/thành phố
Lưu ý: Không chạm, không để nước hoặc các dung dịch sát khuẩn dính vào các vòng tròn trên tấm DBS trước và sau khi lấy mẫu vì sẽ làm giảm chất lượng của mầu DBS.
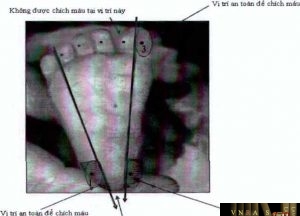
Bước 2: Xác định vị trí lấy
: Tùy thuộc vào cân nặng của trẻ, lựa chọn vị trí lấy máu cho phù hợp (xem hình
1).
- Trẻ nặng < 5kg (từ 1-4 tháng tuổi): chích vào gót chân (vị trí 1 hoặc 2 hình 1)
- Trẻ từ nặng 5kg-10kg (khoảng 4-10 tháng tuổi): chích vào ngón chân cái (vị trí số
- hình 1)
- Trẻ nặng >10kg (khoảng 10 tháng tuồi trở lên): chích vào ngón tay (chích vào cạnh bên của ngón tay áp út)
Lưu ý: Không chích vào phía sau gót chân, vào gần hay phía bên của ngón chân
Hình 1: Vị trí lấy máu ở gót chân hoặc ngón chân cái
Bước 3: Hướng dẫn bố mẹ/người giám hộ cách bế trẻ
Bế trẻ sao cho vị trí chích máu hướng xuống dưới. Người giữ trẻ ngồi cao hơn so với người lấy máu. Bế trẻ sao cho chân trẻ duỗi thẳng xuống, lưng của trẻ quay ra ngoài, toàn bộ thân trẻ ấp lên người giữ trẻ, đầu trẻ tựa lên vai người giữ trẻ. Một tay người giữ trẻ giữ phía vai và gáy, tay kia đỡ phía mông và đùi trẻ.
Nếu lấy máu ở ngón tay thì có thể đặt trẻ ngồi trong lòng mẹ, bàn tay duỗi thẳng xuống dưới.
Bước 4: Hướng dẫn bố mẹ/người giám hộ làm ấm vùng chích máu
Đặc biệt khi trẻ đang lạnh, cần làm ấm vùng lấy máu bằng khăn ấm hoặc bang tay bàng cách xoa nhiều lần vào vùng chích máu trong vòng 3 phút.
Xoa bóp nhẹ từ trên xuống dưới vùng lấy máu để máu dồn về nhiều hơn.
Bước 5: Rửa tay và đeo găng tay không bột
Rửa tay sạch và đeo găng tay không bột. Nếu mang găng tay có bột, phải rửa sạch bột bằng xà phòng và lau khô bằng khăn giấy trước khi lấy mẫu DBS.
Bước 6: Sát khuẩn vùng chích máu bằng dung dịch sát khuẩn và sử dụng bông cồn 70 độ và để khô trong 30 giây.
Bước 7: Chích máu
Chì được dùng kim chích (lancet) 2mm.
Tháo bỏ nắp đậy kim và ấn nhẹ vào da, khi thấy lancet đã tương đối áp sát vào da vùng định chích thì bấm lancet nhanh, mạnh và dứt khoát để chích máu.
Kim chích máu sau khi sứ dụng được thải bỏ vào hộp đựng các vật sắc nhọn, các chất thải không sắc nhọn khác cho vào thùng đựng rác thải y tế.
Bước 8: Bỏ giọt máu đầu ticn
Bỏ giọt máu đầu tiên bằng cách nhẹ nhàng lau sạch với một miếng gạc khô đã tiệt trùng (có trong bộ lấy DBS) hoặc bông sạch không có cồn.
Bước 9: Lấy giọt máu to tiếp theo
Khi máu chảy thành giọt to tiếp theo tại vị trí chích máu, để giọt máu nhỏ trực tiếp vào trung tâm của từng vòng tròn trên tấm DBS, không được ấn tấm DBS vào gót chân trẻ.
Liru ỷ:
- a) Trong quá trình đợi giọt máu chảy ra, nếu thấy lượng máu nhỏ chưa đủ, có thể bóp nhẹ vào vùng xa vị trí lấy máu để tạo áp lực cho máu chảy.
- b) Nếu giọt máu quá nhỏ không đủ để phủ kín hết vòng tròn trên tấm DBS thì không nhỏ giọt khác chồng lên. Chờ giọt máu tiếp theo lấy vào vòng tròn khác.
Bước 10: Sát trùng sau khi lấy máu
Lau sạch vị trí chích máu và ấn miếng bông/gạc đã tiệt trùng vào vị trí chích máu cho đến khi máu ngừng chảy và không cẩn băng. Trong trường hựp máu còn chảy thì cần bâng lại.
- Cách thử hai: Chuẩn bị mẫu DBS từ mẫu máu tĩnh mạch chống đông bằng EDTA
- – Lấy máu tĩnh mạch vào ống có chứa chất chống đông EDTA, đảo ngược ống 5-
6 lần;
- – Dùng pi pét hút 70|il máu từ ống máu nhỏ vào mỗi vòng tròn trên tấm DBS (sử dụne dầu côn có lọc).
Lưu ý: Trong trường hợp mẫu chưa được nhỏ vào tấm DBS ngay, có thể giữ ở nhiệt độ phòng trong 15 phút sau đó cất ờ tủ lạnh (4°c -8°C) trong 24 giờ đến khi nhỏ lên tấm DBS.
- Làm khô mẫu DBS
Sau khi đã nhỏ máu vào đủ 5 vòng tròn trên tấm DBS. đặt các tấm DBS này lên giá phơi khô, để mẫu máu khô tự nhiên ở nhiệt độ phòng (< 25°C) trong khoảng thời gian từ 4 giờ đến qua đêm tùy thuộc vào độ ẩm trong phòng (xem hình 2).
Lưu ý:
a) Không sử dụng máy sấy tóc hoặc để quạt điện hoặc máy điều hòa thổi trực tiếp vào các tấm mẫu DBS.
b) Tránh để tấm DBS tiếp xúc với ánh sáng mặt trời, chuột, côn trùng và bụi.
c) Không xếp các tấm DBS chồng lên nhau, không làm nóng hoặc để tấm mẫu DBS chạm vào các bề mặt khác trong suốt thời gian phơi khô
Lưu ý: các tấm mẫu DBS khi chưa khô hoàn toàn sẽ ảnh hưởng tới chất lượng của các giọt máu khô và kết quả xét nghiệm PCR.
II. ĐÓNG GÓI
1. Đóng gói mẫu DBS
a) Sau khi mẫu DBS đã khô hoàn toàn, xếp mỗi tấm DBS và các gói hút ẩm vào một túi nhựa chuyên dụng có khóa (xem hình 3,4).
b) Ép hết khí ra khỏi túi bằng cách đặt túi lên mặt bàn rồi vuốt ép lên bề mặt túi để dồn hết không khí ra khỏi miệng túi.
Sau đó miết chặt khóa để khóa kín túi, sát khuẩn mặt ngoài túi.
– Các gói chống ẩm có thể sử dụng lại bằng cách đặt vào lò sấy ở nhiệt độ 65°c qua đêm, sau đó lấy ra và bảo quản cho đến khi sừ dụng lại.
– Sử dụng trang bị bảo hộ cá nhân thích hợp khi thao tác với mẫu bệnh phẩm.
2. Bảo quản mẫu DBS
Bảo quản ở điều kiện nhiệt độ phòng (< 25°C) và chuyển tới phòng xét nghiệm trong vòng 1 tuần.
Lưu ỷ:
– Đảm bảo các túi chứa tấm DBS phải được cài chặt, kiểm tra tấm thẻ chì thị độ ẩm (nếu có)
– Tất cả các mẫu DBS cần phải được bảo quản theo điều kiện trên cho đến khi chuyển đến phòng xét nghiệm với đầy đủ phiếu xét nghiệm và phiếu gửi mẫu (theo phụ lục 2,3).
– Trong quá trình bảo quản tránh để các tấm DBS tiếp xúc trực tiếp với ánh sáng hoặc nguồn nhiệt cao.
III. VẬN CHUYẺN, TIÉP NHẬN MẢU MÁU
1. Vận chuyển mẫu
« » «k •
a) Kiểm tra lại các thông tin trên Phiếu gửi mẫu và tấm DBS
b) Đặt các túi mẫu DBS, phiếu chỉ định xét nghiệm và phiếu gửi mẫu xét nghiệm vào một phong bì tối màu. Đóng phong bì và chuyển phát nhanh đến phòng xét nghiệm bằng đường bưu điện càng sớm càng tốt (không cần giữ lạnh khi vận chuyển);
c) Cơ sở gửi mẫu cần thông báo cho Phòng xét nghiệm về việc gửi mẫu.
2. Tiếp nhận mẫu – tại phòng xét nghiệm
a) Kiểm tra chất lượng mẫu bệnh phẩm bao gồm quy cách đóng gói, chất lượng mẫu, đối chiếu với phiếu xét nghiệm và phiếu gửi mẫu xét nghiệm;
b) Ký nhận phiếu gửi mẫu xét nghiệm để xác nhận đã nhận được mẫu bệnh phẩm đạt chất lượng cho xét nghiệm;
c) Điền đủ thông tin vào sổ xét nghiệm:
d) Thông báo lịch trả kết quà cho cơ sờ gửi mẫu.
IV. TIÊU HỦY MẪU BỆNH PHẨM
1. Việc hủy mẫu phải tiến hành theo Thông tư liên tịch số 58/2015/TTLT-BYT- BTNMT ngày 31/12/2015 quy định về quản lý chất thải y tế và các qui định pháp luật có liên quan.
2. Hủy mẫu lưu dương tính và nghi ngờ: sau khi hết thời gian lưu mẫu theo quy định, việc hủy mẫu cần phải lập biên bản ghi rõ thời gian và danh sách các mẫu đã hủy. Biên bản này phải lưu trong thời gian 5 năm kc từ ngày hủy mẫu.
Phụ lục III
QUY TRÌNH LẨY MÁU, ĐÓNG GÓI VÀ VẬN CHUYỂN MÁU TRONG XÉT
NGHIỆM SINH HỌC PHÂN TỬ HIV
I. LẤY MẪU MÁU
1. Chuẩn bị dụng cụ:
– Bông thấm nước vô trùng; cồn 70 độ hoặc cồn I ốt; găng tay không bột; băng cá nhân; bom kim tiêm (đầu kim 21G – 23G) hoặc bộ dụng cụ lấy máu bằng ống hút chân không (vacutainer, kim. giá đờ); ống lấy máu có chứa chất chống đông EDTA: dây garô; giá để ống nghiệm: đầu côn có lọc (không có ADNase/ARNase); ống cyotube loại 1,8 – 2ml (không có ADNase/ARNase); hộp đựng các vật sắc nhọn và rác thải y tế.
Lưu ý: Không dùng chất chống đông bằng Heparin vì sẽ ức chế phản ứng của kỹ thuật sinh học phân tử. Sử dụng chất chống đông EDTA hoặc chất chống đông khác theo yêu cầu của kỹ thuật sử dụng (tốt nhất là dạng phun sương).
2. Chuẩn bị lấy mẫu:
a) Điền đầy đủ thông tin của người bệnh (Họ tên, mã số, tuổi) và giờ, ngày lấy mẫu trên ống đựng mẫu;
b) Kiểm tra đối chiếu tên người bệnh, mã số trên phiếu và trên ống nghiệm;
c) Rửa tay và đi găng tay không bột (trường hợp không có găng tay không bột có thể đi găng tay thường nhưng phải rửa sạch bột talc trước khi lấy máu cho bệnh nhân);
3. Tiến hành lấy máu:
a) Xác định vị trí lấy máu (tĩnh mạch) và ga rô cách vị trí lấy máu 5cm về phía
trên;
b) Sát trùng vị trí lấy máu bằng cồn 70 độ và để khô 30 giây.
c) Đưa kim vào tĩnh mạch lấy 6 ml máu cho vào ống có chứa chất chống đông. Có thể dùng bơm kim tiêm loại 10 ml (đầu kim cỡ 21G – 23G) để lấy máu hoặc dùng bộ dụng cụ lấy máu với ống hút chân không (vacutainer). Nếu dùng bơm kim tiêm để lấy máu thì tháo đầu kim ra (đảm bảo thao tác an toàn), để bơm tiêm chếch với thành ống nghiệm và bơm từ từ cho máu chảy theo thành ống nghiệm tránh làm vỡ hồng cầu.
d) Thải bỏ đầu kim vào hộp đựng các vật sắc nhọn, các chất thải không sắc nhọn khác cho vào thùng đựng rác thải y tế;
e) Sát trùng lại vị trí đã lấy máu bằng cồn 70 độ và băng lại;
f) Sau khi lấy máu vào ống có chất chống đông, trộn đều bằng cách nhẹ nhàng đảo ngược ống máu 8-10 lần hoặc để trên máy xoay tròn trong tối thiểu 2 phút. Để ống máu ờ nhiệt độ phòng tối thiểu 15 phút và bảo quản ờ 2°c -8°c cho đến khi chuyển đến phòng xét nghiệm;
g) Nếu trong vòng 6 giờ kể từ khi lấy mẫu máu mà không gửi được đến phòng xét nghiệm thì bắt buộc phải ly tâm tách huyết tương.
❖ Hướng dẫn tách huyết tương từ mẫu máu toàn phần:
+ Ly tâm ống máu với tốc độ 2500 – 3000 vòng/phút trong 20 phút ở nhiệt độ phòng (18-25°C) hoặc tốt nhất là ở 4°C;
+ Dùng ống hút nhựa (dùng một lần) hoặc pi pét với đầu côn có lọc (không có ADNase/ARNase) để hút toàn bộ huyết tương chuyển sang 02 ống cryotube loại 1.8 – 2ml (không có ADNase/ARNase) đã có dán mã số tương ứng.
+ Bảo quản các ống huyết tương ở 2°c -8°c cho đến khi mẫu được chuyển đến phòng xét nghiệm.
II. ĐÓNG GÓI MẢU BỆNH PHẤM
1. Đeo găng tay đóng chặt các nắp của ống mẫu và xếp tất cả các ống mẫu theo phương thẳng đứng vào trong giá đựng mẫu. Dùng băng dính cố định các ống mẫu trong giá đựng mẫu. Cho mẫu đã được cố định và vật liệu thấm hút (bông hoặc giấy thấm nước) để trong túi nylon dán kín.
2. Đặt túi nylon có chứa mẫu và cho đủ vật liệu thấm hút (bông hoặc giấy thấm nước) vào thùng vận chuyển mẫu.
3. Đặt các túi tích lạnh vào thùng đựng mẫu để đảm bảo mẫu được bảo quản từ 2-8°C trong quá trình vận chuyển.
4. Đóng nắp thùng đựng mẫu và chốt khoá lại. Trường hợp không có chốt khoá thì dùng băng dính dán xung quanh.
5. Dán hoặc in ký hiệu nguy hiểm sinh học và số điện thoại liên hệ trong trường hợp khẩn cấp bên ngoài của hộp đựng mẫu bệnh phẩm.
III. VẬN CHUYỂN, TIẾP NHẬN MẪU BỆNH PHẨM
1. Vận chuyển mẫu
a) Liên hệ gửi mẫu: nơi gửi mẫu cần gọi điện báo trước cho phòng xét nghiệm biết thời gian mẫu bệnh phẩm sẽ tới để phòng xét nghiệm bố trí cán bộ tiếp nhận. Khi vận chuyển mẫu phải kèm theo “Phiếu xét nghiệm sinh học phân tử HIV ” và “Phiếu chuyển gửi mẫu xét nghiệm sinh học phân tử HIV”.
b) Thời gian gửi mẫu:
– Đối với mẫu máu toàn phần: mẫu máu cần được chuyển đến phòng xét nghiệm trong vòng 6 giờ kể từ khi lấy máu.
– Đối với mẫu huyết tương: mẫu cần chuyển trong vòng 48 giờ kể từ khi tách huyết tương.
c) Phương tiện vận chuyển: tốt nhất là bằng xe ô-tô chuyên dụng. Trong trường hợp điều kiện không cho phép, có thể sử dụng xe gắn máy để vận chuyển nhưng phải buộc hộp chứa mẫu bệnh phẩm cẩn thận, gọn gàng vào giá chở hàng và tránh do, vỡ.
d) Người vận chuyển mẫu bệnh phẩm: phải là cán bộ của cơ sở y tế hoặc cộng tác viên đã qua tập huấn. Khi vận chuyển cần mang theo găng tay và các dụng cụ an toàn để xử lý khi gặp sự cố (chất tẩy trùng, khử khuẩn như cồn 70 độ, Cloramin B…); vật liệu thấm hút để lau chùi, giấy lau mềm; túi nylon dày chuyên dụng.
2. Tiếp nhận mẫu: thực hiện theo quy định tại mục 111, phụ lục II hướng dẫn này.
IV. TIÊU HỦY MẢU BỆNH PHẨM
Thực hiện theo quy định tại mục IV, phụ lục II hướng dẫn này
Phụ lục IV-A
ÁP DỤNG CHO CƠ SỞ THỰC HIỆN XÉT NGHIỆM SÀNG LỌC HIV
Mẫu số 1A
BỘ (SỞ) Y TẾ…………………….
Tên đơn vị………………………….
Kính gửi:
…………………………………………………………………………………………………………………..
PHIÊU LẤY MẪU XÉT NGHIỆM HIV
I
| STT | HỌ TÊN | NĂM SINH | ĐỊA CHỈ | ĐỐI
TƯỢNG |
NGÀY
LẤY MẪU |
KẾT QỦA XÉT NGHIỆM | CHẤT
LƯỢNG MẪU |
MÃ
SỐ PXN |
GHI
CHÚ |
|
| Nam | Nữ | SP
(ghi rõ tên sp) |
||||||||
| (1) | (2) | (3) | (4) | (5) | (6) | (7) | (8) | (9) | (10) | (11) |
Ghi chú: Phiếu này lập thành 02 bản, mỗi bên giữ 1 bản.
(Dùng cho đơn vị gửi mẫu xét nghiệm)
_____________________________________________________
Ngày… tháng………… năm …. Ngày……. tháng …. năm ….
NGƯỜI GIAO MẪU NGƯỜI NHẬN MẪU XÉT NGHIỆM
(Ký, ghi rõ họ tên) (Ký, ghi rõ họ tên)
Lưu ỷ:
(2) Họ tên: Ghi rõ họ và tên
(6) Đối tượng: Ghi rõ: Nghiện chích ma túy, mại dâm, nam quan hệ tình dục đồng giới, phụ nữ mang thai, đang điều trị ARV, hoặc khác nếu không thuộc các đối tượng đã liệt kê
(8) Kết quả xét nghiệm: ghi rõ (Dưomg tính) hoặc (âm tính) .
Chất lượng mẫu: Đạt, không đạt (ghi rõ: tán huyết, đóng cục, không đủ thể tích,….).
Đơn vị Khoa..
SỔ XÉT NGHIỆM SÀNG LỌC HIV
Bắt đầu từ đến
SỐ XÉT NGHIỆM SÀNG LỌC HIV
| STT | THÔNG TIN KHÁCH HÀNG | NGÀY LẤY MÁU | Ngày xét nghiệm | KẾT QUẢ XÉT NGHIỆM | KẾT LUẬN | KẾT QUẢ KHẲNG ĐỊNH | GHI CHÚ | |||||
| HỌ TÊN | MÃ SỐ | NĂM SINH | ĐỊA CHỈ | ĐỐI
TƯỢNG |
SP
(ghi rõ tên sinh phẩm) |
|||||||
| Nam | Nữ | |||||||||||
| 0) | (2) | (3) | (4) | (5) | (6) | (7) | (8) | (9) | (10) | (11) | (12) | (13) |
Lưu ỷ:
(2) Họ tên: Ghi rõ họ và tên
(4,5) Năm sinh, trường hợp trẻ dưới 2 tuôi thì ghi rỗ ngày tháng năm sinh.
(6) Địa chi của bệnh nhân: Ghi Xã/Phưòmg, quân/huyện, tinh/thènh phô?
(7) Đối tượng: Ghi rõ: Nghiện chích ma túy, mại dâm, nam quan hệ tình dục đông giới, phụ nữ mang thai
(8) Kết quả xét nghiệm: Ghi rõ âm tính, dương tính, nghi ngờ
Kết luận: Chỉ được phép kết luận âm tính, các trường hợp có kết quà dương tính, nghi ngờ với sinh phẩm sử dụng thì phải ghi chuyển tới cơ sở khẳng định và thực hiện chuyển mẫu.
Tên đơn vị……………..
Phòng xét nghiệm HIV:
Địa chì…………………..
Điện thoại………………
KẾT QUẢ XÉT NGHIỆM KHÁNG THÉ KHÁNG H1V (Áp dụng đế trà cho người được làm xét nghiệm)
Họ và tên:…………………………………………..
Giới tính:…………………………………………….
Năm sinh:……………………………………………
Địa chỉ:……………………………………………….
Số chứng minh thư nhân dân (nếu có):
Ngày xét nghiệm:………………………………..
Tên sinh phẩm xét nghiệm:…………………
Kết luận (Ghi rõ bằng chữ): Âm tính.
Ngày…… tháng……. năm ….
PHỤ TRÁCH PHÒNG XÉT NGHIỆM
(Kỷ, ghi rõ họ tên)
Lưu ỷ:
Trường hợp không có chứng minh nhân dân hoặc giấy tờ tùy thân để chứng minh người được làm xét nghiệm đúng với họ tên ghi trên giấy xét nghiệm thì ghi rõ: Không có giấy tờ tùy thân đối chiếu người được làm xét nghiệm xác thực với họ và tên ghi trên giấy xét nghiệm
Phụ lục IV-B
ÁP DỤNG CHO CƠ SỞ XÉT NGHIỆM KHẲNG ĐỊNH CÁC TRƯỜNG HỢP HIV DƯƠNG TÍNH
Mẫu số 1B
BỘ (SỞ) Y TẾ Tên đơn vị:
Kính gửi: …………………………………………………………………………………………………………..
Ngày…… tháng…….. năm
NGƯỜI LẬP PHIÊU (Ký, ghi rõ họ tên)
Ngày ………… tháng …… năm……
NGƯỜI NHẬN MẪU XÉT NGHIỆM (Ký, ghi rõ họ tên)
Ngày ……… tháng………… năm
NGƯỜI GIAO MẦU (Ký, ghi rõ họ tên)
PHIÉU GỦÌ MẢU XÉT NGHIỆM HIV
| STT | HỌ
TÊN |
NĂM
SINH |
ĐỊA CHỈ | ĐỐI TƯỢNG | NGÀY LẤY MẪU | KẾT QUẢ XÉT NGHIỆM | CHẤT LƯỢNG MẪU | MÃ SỐ PXN | GHI CHÚ | |||
| Nam | Nữ | SP1 (ghi rõ tên sp) | SP2 (ghi rõ tên sp) | SP3 (ghi rõ tên sp) | ||||||||
| (1) | (2) | (3) | (4) | (5) | ___ (6)__ | _ | (9) | (10) – | 01) | ____ (12}__ | (13) | ___ (14) |
Lưu ý:
1 .Đề nghị gửi kèm bản phô tô kết quả bản đọc của đơn vị gửi mẫu (trong trường hợp xét nghiệm ELISA ).
- Phiếu này lập thành 02 bàn, mỗi bên giữ 01 bàn.
- Cách ghi các cột:
– (2) Họ tên của bệnh nhân: Ghi rõ họ tên
– (3,4) Năm sinh, trường hợp tré dưới 2 tuồi thì ghi rõ ngày tháng năm sinh.
– (5) Địa chi cùa bệnh nhân: Ghi Xã/Phường, quân/huyện, tinh/thành phố.
– (6) Đối tượng: Ghi rồ: Nghiện chích ma túy, mại dâm. nam quan hệ tình dục đồng giới, phụ nữ mang thai..
– (9,10.11): Kết quà xét nghiệm: Ghi rõ âm tính, dương tính, nghi ngỏt Tên sinh phẩm (SP1, SP2, SP3): ghi rõ tèn sinh phẩm hiện đang sứ dụng.
(8) Chất lượng mẫu: Đạt, không đạt (ghi rõ: tán huyết, đóng cục, không đú thề tích,…).
(13) Mã số phòng xét nghiệm: Là mã số theo quy định cùa đơn vị thực hiện xét nghiệm.
Đơn vị Khoa..
SỔ NHẬN MẪU VÀ TRẢ KẾT QUẢ XÉT NGHIỆM HIV
Bắt đầu từ đến
SỔ NHẬN MẪU VÀ TRẢ KẾT QUẢ XÉT NGHIỆM HIV
| STT | ĐƠN VỊ GỬI MẪU | NGÀY NHẬN MẪU | SỐ LƯỢNG MẪU | NGƯỜI NHẬN MẪU (Ký, ghi rõ họ tên) | NGÀY LÀM XÉT NGHIỆM | NGÀY TRẢ KẾT QUẢ | XÁC NHẬN NHẬN KQ (Ký, ghi rõ họ tên) | GHI CHÚ |
| (1) | (2) | (3) | (4) | (5) | (6) | (7) | (8) | (9) |
Lưu ý:
(7) Xác nhận nhận kết quả: trong trường hợp gửi qua đường bưu điện thì người gửi ghi nhận lại ngày gừi. Các đơn vị tùy tình hình thực tế có thể thêm các cột thông tin khi cần thiết
Đơn vị Khoa..
SỔ XÉT NGHIỆM HIV
Bắt đầu từ đến
| STT | THÔNG TIN KHÁCH HÀNG (từ cơ sở gửi mẫu) | ĐƠN VỊ GỬI MẪU | KẺT QUẢ XÉT NGHIỆM | KẾT LUẬN | MÃ SỐ BN của PXN | GHI CHÚ | ||||||||||
| HỌ TÊN | MÃ SỐ | NĂM SINH | ĐỊA CHỈ | ĐỐI TƯỢNG | SP1
(ghi rõ tên sinh phẩm) |
SP2
(ghi rõ tên sinh phẩm) |
SP3
(ghi rõ tên sinh phẩm |
|||||||||
| Nam | Nữ | Ngày
XN |
Kết quả XN | Ngày
XN |
Kết quả XN | Ngày
XN |
Kết quả XN | |||||||||
| (1) | (2) | (3) | (4) | (5) | (6) | (7) | (8) | (9) | (10) | (11) | (12) | (13) | (14)___ | (16) | (17) | |
Lưu ý: Cách ghi các cột:
– (2,3) Họ tên và mã số của bệnh nhân.
– (4,5) Năm sinh, trường hợp trẻ dưới 2 tuổi thì ghi rõ ngày tháng năm sinh.
– (6) Địa chi cùa bệnh nhân: Ghi Xã/Phường. quân/huyện, tinh/thành phố.
– (7) Đối tượng: Ghi rõ: Nghiện chích ma túy, mại dâm, nam quan hệ tình dục đồng giới, phụ nừ mang thai
– (9,II, 13) Ngày xét nghiệm: Ngày xét nghiệm ghi ngày xét nghiệm chẩn đoán.
– (10, 12,14) Kết quả xét nghiệm: Ghi rõ âm tính, dương tính, nghi ngờ; Tên sinh phẩm (SP1, SP2, SP3): ghi rõ tên sinh phẩm hiện đang sử dụng.
– (15) Kết luận: Ghi rõ âm tính, dương tính hay không xác định.
– (16) Mã số BN cùa phòng xét nghiệm.
SỔ LƯU MẪU DƯƠNG TÍNII VÀ KHÔNG XÁC ĐỊNH
9
| STT | HỌ VÀ TÊN | MÃ SỐ BỆNH NHÂN CỦA PHÒNG XÉT NGHIỆM | NGÀY XÉT NGHIỆM | KẾT LUẬN | MÃ SỐ LƯU | VỊ TRÍ LƯU/SƠ ĐỒ LƯU MẪU | GHI CHÚ |
| (ỉ) | (2) | (3) | (4) | (5) | (6) | (7) | (8) |
BỘ (SỞ) Y TẾ…………………….. CỘNG HÒA XÃ HỘI CHỦ NGHĨA VIỆT NAM
Tên đơn vị………………………….. Độc lập – Tự do – Hạnh phúc
Ngày….tháng…năm 20…
Kính gửi:……………………………………………………………………………………………………
PHIẾU TRẢ LỜI KẾT QUẢ XÉT NGHIỆM HIV
(Dùng trả cho đơn vị gửi mẫu xét nghiệm)
Ngày nhận mẫu:… Ngày xét nghiệm :
| STT | HỌ TÊN | MẢ SỐ | NĂM SINH | ĐỊA CHỈ | ĐÓI
TƯỢNG |
KÉT QUẢ XÉT NGHIỆM | KÊT
LUẬN |
GHI
CHỦ |
||||
| Nam | Nữ | SP1
(ghi rõ tên SP) |
SP2
(ghi rõ tên SP) |
SP3
(ghi rõ tên SP) |
Kỹ thuật khác | |||||||
| (1) | (2) | (3) | (4) | (5) | (6) | (7) | (8) | (9) | (10) | (11) | (12) | (13) |
| ———- x:- | ||||||||||||
(Chú ý: Đi kèm phiêu nàv là trích lục từng két quà xét nghiệm cho bệnh nhân theo mâu sô 6, phụ lục này).
(Ký, ghi rõ họ tên)
Lưu v: Cách ghi các cột:
- (2,3) Họ tên và mã số cúa bệnh nhân.
(3,4) Năm sinh, trường hợp ưè dưới 2 tuối thì ghi rò ngày tháng năm sinh.
(5) Địa chi cùa bệnh nhân: Ghi Xã/Phường, quân/huyện, tinh/thành phố.
- (6) Đối tượng: Ghi rõ: Nghiện chích ma túy, mại dâm, nam quan hệ tình dục đồng giới, phụ nữ mang thai…………………………………………………
- (7.8.9,10) Kết quá xét nghiệm: Ghi rõ âm tính, dương tính, nghi ngờ; Tên sinh phẩm (SP1, SP2, SP3): ghi rõ tên sinh phẩm hiện đang sừ dụng. (11) Kết luận: Ghi rõ âm tinh, dương tính hay không xác dịnh.
Tên đơn vị……………
Phòng xét nghiệm HIV
Địa chỉ…………………
Điện thoại…………….
KẾT QUẢ XÉT NGHIỆM HIV
(Dùng để trà cho người được làm xét nghiệm)
Họ và tên:……………………………………………………….. Giới tính:…………………………..
Mã số người được xét nghiệm:……………………………………………………………………..
Năm sinh:……………………………………………………………………………………………………..
Địa chỉ:…………………………………………………………………………………………………………
Số chứng minh thư nhân dân (nếu có):
Ngày xét nghiệm:……….. (ghi ngày xét nghiệm kết luận cuối cùng)
Tcn các sinh phẩm xét nghiệm:…………………………………………………………………….
Kết luận (Ghi rõ bằng chữ):………………………………………………………………………….
XÁC NHÂN CỦA THỦ TRƯỞNG ĐƠN VỊ ……. ỉhảns – V năm •••■
PHỤ TRÁCH PHÒNG XN
(Ký, ghi rõ họ tên) . (Ký, ghi rõ họ tên)
(Trong trường hợp cần thiết và có yêu cầu đặc biệt)
Lưu ý:
– Phiếu trà lời kết quả đóng dấu ừeo của đơn vị hoặc dấu của dơn vị có phòng xét nghiệm tùy từng trường hợp có yêu cầu cụ thể
– Phần kết luận: ghi rõ bằng chữ Dương tính, Âm tính, Không xác định
MẪU THAM KHẢO SƠ ĐỒ XÉT NGHIỆM
BMXN- _________ Lần ban hành (version): 01__________
SƠ ĐỒ XÉT NGHIỆM CHO KỸ THUẬT XÉT NGHIỆM NHANH
Tên sinh phẩm…………………………………………………………….
số lô:…………………………………….
Hạn sử dụng:………………………………………………………………
* Mẫu xét nghiệm nhận từ ………. đẻn …………. (Xem Sổ nhận mẫu)
| STT | NgàyXN | Họ tên/Mâ số | Vùng kiềm chứng | Vùng kết quả | Kết quả | Nguời XN | Ghi chú |
Công văn 2674/QĐ-BYT ban hành hướng dẫn quốc gia về xét nghiệm HIV
DOWNLOAD VĂN BẢN GỐC TẠI ĐÂY 2674_QĐ_BYT_2018_VNRAS
COPY VUI LÒNG GHI NGUỒN VNRAS.COM