HƯỚNG DẪN THỰC HÀNH DƯỢC LÂM SÀNG CHO DƯỢC SĨ TRONG MỘT SỐ BỆNH KHÔNG LÂY NHIỄM
(Ban hành kèm theo Quyết định số 3809/QĐ-BYT ngày 27/08/2019)
Chủ biên: PGS.TS.BS. Lương Ngọc Khuê
CHỦ BIÊN
PGS.TS.BS. Lương Ngọc Khuê
BAN BIÊN SOẠN
TS.DS. Cao Hưng Thái
PGS.TS.DS. Đặng Nguyễn Đoan Trang
PGS.TS.DS. Phạm Thị Thúy Vân
ThS.DS. Nguyễn Thu Minh
PGS.TS.BS. Phạm Cẩm Phương
TS.DS. Bùi Thị Hương Quỳnh
BS CKI. Trần Minh Triết
ThS.DS. Dương Thanh Hải
ThS.DS. Nguyễn Kim Ngân
ThS.BS. Nguyễn Hoàng Hải
ThS.DS. Nguyễn Thị Thanh Minh
ThS.DS. Nguyễn Hoàng Phương Khanh
ThS.DS. Trần Ngọc Phương
DS CKII. Lê Ngọc Hiếu
ThS.DS. Châu Thị Ánh Minh
ThS.DS. Đào Thị Kiều Nhi
ThS.DS. Đỗ Vũ Thùy Giang
ThS.DS. Phạm Hồng Thắm
ThS.DS. Nguyễn Thị Anh Thư
ThS.DS. Hoàng Thị Minh Thu
DS. Nguyễn Thị Hà
DS. Bạch Văn Dương
DS. Võ Thái Nguyệt Cẩm
BAN THƯ KÝ BIÊN TẬP
ThS.BS. Nguyễn Đức Tiến
ThS.DS. Lê Kim Dung
ThS.DS. Phạm Hồng Thắm
HỘI ĐỒNG THẨM ĐỊNH
GS.TS.BS. Mai Trọng Khoa
PGS.TS.DS. Nguyễn Tuấn Dũng
PGS.TS.BS. Phạm Mạnh Hùng
PGS.TS.DS. Nguyễn Hoàng Anh
TS.BS. Phan Văn Báu
TS.DS. Nguyễn Quốc Bình
TS.BS. Nguyễn Anh Dũng
TS.BS. Phan Hướng Dương
TS.DS. Cẩn Tuyết Nga
CHUYÊN GIA PHẢN BIỆN
PGS.TS.DS. Nguyễn Thị Liên Hương
TS.DS. Phan Quỳnh Lan
ThS.DS. Đỗ Văn Dũng
ThS.DS. Nguyễn Thị Thu Ba
ThS.DS. Lê Thị Uyển
DS CKI. Võ Thị Kiều Quyên
| BỘ Y TẾ ——- |
CỘNG HÒA XÃ HỘI CHỦ NGHĨA VIỆT NAM Độc lập – Tự do – Hạnh phúc ————— |
| Số: 3809/QĐ-BYT | Hà Nội, ngày 27 tháng 8 năm 2019 |
QUYẾT ĐỊNH
VỀ VIỆC BAN HÀNH HƯỚNG DẪN THỰC HÀNH DƯỢC LÂM SÀNG CHO DƯỢC SĨ TRONG MỘT SỐ BỆNH KHÔNG LÂY NHIỄM
BỘ TRƯỞNG BỘ Y TẾ
Căn cứ Luật Dược năm 2016;
Căn cứ Nghị định số 75/2017/NĐ-CP ngày 20/6/2017 của Chính phủ quy định chức năng, nhiệm vụ, quyền hạn và cơ cấu tổ chức của Bộ Y tế;
Xét Biên bản họp ngày 19/4/2019 của Hội đồng chuyên môn thẩm định Hướng dẫn thực hành dược lâm sàng cho dược sĩ trong một số bệnh không lây nhiễm được thành lập theo Quyết định số 1149/QĐ-BYT ngày 29/3/2019 của Bộ trưởng Bộ Y tế;
Xét đề nghị của Cục trưởng Cục Quản lý Khám, chữa bệnh,
QUYẾT ĐỊNH:
Điều 1. Ban hành kèm theo Quyết định này “Hướng dẫn thực hành dược lâm sàng cho dược sĩ trong một số bệnh không lây nhiễm”.
Điều 2. “Hướng dẫn thực hành dược lâm sàng cho dược sĩ trong một số bệnh không lây nhiễm” được sử dụng để nâng cao năng lực thực hành dược lâm sàng cho các dược sĩ trong một số bệnh không lây nhiễm tại các cơ sở khám bệnh, chữa bệnh trong cả nước.
Điều 3. Quyết định này có hiệu lực kể từ ngày ký ban hành.
Điều 4. Các ông, bà: Chánh Văn phòng Bộ, Cục trưởng Cục Quản lý Khám, chữa bệnh, Chánh Thanh tra Bộ, Cục trưởng và Vụ trưởng các Cục/Vụ thuộc Bộ Y tế; Giám đốc các Bệnh viện/Viện có giường bệnh trực thuộc Bộ Y tế; Giám đốc Sở Y tế các tỉnh, thành phố trực thuộc Trung ương; Thủ trưởng y tế các Bộ, Ngành; Thủ trưởng các đơn vị có liên quan chịu trách nhiệm thi hành Quyết định này./.
| Nơi nhận: – Như Điều 4; – Bộ trưởng (để b/c); – Các Thứ trưởng BYT; – Cổng TTĐTBYT; – Website Cục QLKCB; – Lưu: VT, KCB |
KT. BỘ TRƯỞNG Nguyễn Viết Tiến |
LỜI GIỚI THIỆU
Bộ phận Dược lâm sàng (DLS) là một bộ phận của khoa Dược được quy định trong thông tư 22/2011/TT-BYT, hoạt động theo hướng dẫn của thông tư 31/2012/TT-BYT. Tuy nhiên, mức độ triển khai hoạt động DLS tại các bệnh viện còn rất khác nhau phụ thuộc trình độ nhân lực dược, cơ chế quản lý của bệnh viện, cơ quan quản lý, cơ cấu nguồn thu từ dịch vụ khám chữa bệnh của bệnh viện.
Tại nhiều nước trên thế giới, hiệu quả của công tác DLS đã được chứng minh qua rất nhiều báo cáo, nghiên cứu và vai trò của dược sĩ lâm sàng (DSLS) ngày càng được đề cao. Đặc biệt, đối với các bệnh mạn tính, không lây nhiễm như: ung thư, đái tháo đường (ĐTĐ), tim mạch … thì vai trò tư vấn, theo dõi, giám sát sử dụng thuốc của người DSLS càng quan trọng. Tại Thái Lan, sau rất nhiều năm với vai trò truyền thống là cấp phát thuốc, các dược sĩ đã bắt đầu công tác DLS với vai trò quản lý bệnh mạn tính trong cộng đồng. Tại Hoa Kỳ, Hội nghị Directions in Pharmacy 5th Annual CE Conference tại Plainsboro – New Jersey năm 2015 đã nhấn mạnh việc mở rộng vai trò của người DSLS sang quản lý các bệnh mạn tính bao gồm rà soát việc điều trị và các hướng dẫn điều trị trên các bệnh ĐTĐ típ 2, rối loạn lipid máu, viêm mũi dị ứng, hen suyễn và COPD. Nghiên cứu tổng quan hệ thống của Sarah Poushinho và cộng sự trên 36 nghiên cứu trên bệnh nhân ĐTĐ típ 2 cho thấy sự tư vấn, can thiệp của DSLS đã làm gia tăng tỷ lệ tuân thủ, cải thiện đường huyết, HbAlc, LDL cholesterol và triglycerid. Can thiệp DLS cũng được chứng minh làm cải thiện kiến thức về bệnh lý, sự tuân thủ, chất lượng sống của người bệnh cũng như chi phí – hiệu quả trong nhiều bệnh lý mạn tính.
Tại Việt Nam, hoạt động DLS nói chung cũng như các hoạt động DLS trong các bệnh không lây nhiễm hiện nay chưa được triển khai đồng bộ tại các cơ sở y tế. Đồng thời, hiện vẫn chưa có các hướng dẫn chuyên môn cụ thể về cách tiến hành và đánh giá hiệu quả của hoạt động DLS trên các bệnh lý mạn tính cũng như chưa có nhiều các nghiên cứu về hiệu quả kinh tế của các hoạt động DLS đã triển khai tại các cơ sở khám chữa bệnh. Điều này dẫn đến những khó khăn trong xây dựng chính sách và biên chế nhân sự cho hoạt động DLS.
Hướng dẫn hoạt động DLS của Bộ Y tế (BYT) là một hướng dẫn chuyên môn kỹ thuật rất có giá trị khoa học và thực tiễn sẽ giúp triển khai, đánh giá các hoạt động DLS tại các cơ sở khám chữa bệnh. Đồng thời, hướng dẫn này cũng sẽ giúp các cơ sở y tế xác định được mục tiêu, nội dung và cách triển khai hoạt động DLS phù hợp với điều kiện của cơ sở, góp phần chuẩn hoá và nâng cao chất lượng hoạt động DLS trên toàn quốc.
Nhân dịp này, Bộ Y tế cũng đánh giá cao và biểu dương các cơ sở khám bệnh, chữa bệnh, các giáo sư, bác sĩ, dược sĩ đã tích cực thực hiện công tác DLS, Cục Quản lý Khám, chữa bệnh đã hết sức nỗ lực cùng các nhà khoa học đã tâm huyết tham gia xây dựng hướng dẫn. Xin chân thành cảm ơn các cơ quan, tổ chức trong nước và quốc tế, đặc biệt là VPĐD Merck Export GmBH đã tham gia đồng hành, giúp đỡ trong quá trình biên soạn và triển khai thực hiện hướng dẫn này.
Bộ Y tế giao Cục Quản lý Khám, chữa bệnh tiếp tục tiếp thu, lắng nghe và tổng hợp các ý kiến góp ý của các nhà khoa học, chuyên môn cũng như thường xuyên, định kỳ bổ sung, cập nhật các thông tin, kiến thức mới để giúp bản Hướng dẫn ngày càng hoàn thiện.
GS.TS. NGUYỄN VIẾT TIẾN
Thứ trưởng thường trực Bộ Y tế
DANH MỤC CHỮ VIẾT TẮT TIẾNG VIỆT
| Từ viết tắt | Chú giải tiếng Việt |
| CB | Thuốc chẹn thụ thể beta |
| BHYT | Bảo hiểm y tế |
| BMK | Bệnh mắc kèm |
| BMV | Bệnh mạch vành |
| BN | Bệnh nhân |
| BTM | Bệnh thận mạn |
| BTMXV | Bệnh tim mạch do xơ vữa |
| BYT | Bộ Y tế |
| CAD | Bệnh động mạch vành |
| CKCa | Thuốc chẹn kênh canxi |
| CSDL | Cơ sở dữ liệu |
| CTTA | Thuốc chẹn thụ thể angiotensin II |
| DLS | Dược lâm sàng |
| DM | Dung môi |
| DS | Dược sĩ |
| DSLS | Dược sĩ lâm sàng |
| ĐTĐ | Đái tháo đường |
| ĐTN | Đau thắt ngực |
| HA | Huyết áp |
| HAPK | Huyết áp phòng khám |
| HATT | Huyết áp tâm thu |
| HATTr | Huyết áp tâm trương |
| KVK | Thuốc kháng đông kháng vitamin K |
| LT | Thuốc lợi tiểu |
| MLCT | Mức lọc cầu thận |
| NMCT | Nhồi máu cơ tim |
| NVYT | Nhân viên y tế |
| PNCT | Phụ nữ có thai |
| PNCCB | Phụ nữ cho con bú |
| RLLP | Rối loạn lipid |
| THA | Tăng huyết áp |
| TDKMM | Tác dụng không mong muốn |
| TMCB | Thiếu máu cục bộ |
| TNLS | Thử nghiệm lâm sàng |
| TTCQĐ | Tổn thương cơ quan đích |
| TTM | Truyền tĩnh mạch |
| TZD | Nhóm thiazolidinedion |
| ƯCMC | Nhóm thuốc ức chế men chuyển |
| XVĐM | Xơ vữa động mạch |
| YTNC | Yếu tố nguy cơ |
DANH MỤC CHỮ VIẾT TẮT TIẾNG ANH
| Từ viết tắt | Chú giải tiếng Anh | Chú giải tiếng Việt |
| ADA | American Diabetes Association | Hiệp hội Đái tháo đường Hoa Kỳ |
| ADR | Adverse Drug Reaction | Phản ứng có hại của thuốc |
| AFP | Alpha foeto protein | Alpha foeto protein |
| AJCC | American Joint Committee on Cancer | Hiệp hội Ung thư Hoa kỳ |
| AHA | American Heart Association | Hiệp hội Tim mạch Hoa Kỳ |
| ALK | Anaplastic Lymphoma kinase | Anaplastic Lymphoma kinase |
| ALP | Alkaline phosphatase | Alkaline phosphatase |
| ALT | Alanin transferase | Alanin transferase |
| AIDS | Acquired Immuno Deficiency Syndrome | Hội chứng suy giảm miễn dịch mắc phải |
| ASHP | American Society of Health – System Pharmacists | Hội Dược sĩ của Hệ thống Y tế Hoa Kỳ |
| AST | Aspartate amino transferase | Aspartate amino transferase |
| AUC | Area under the curve | Diện tích dưới đường cong |
| BMI | Body Mass Index | Chỉ số khối cơ thể |
| CAR-T | Chimeric Antigen Receptor T- cell | Tế bào lympho T chứa thụ thể kháng nguyên dạng khảm |
| CDC | The US Centers for Disease Control and Prevent | Trung tâm Kiểm soát và phòng ngừa dịch bệnh Hoa Kỳ |
| COPD | Chronic Obstructive Pulmonary Disease | Bệnh phổi tắc nghẽn mạn tính |
| Clcr | Clearance creatinine | Độ thanh thải creatinin |
| CT | Computed Tomography | Chụp cắt lớp vi tính |
| CTCs | Circulating tumor cell | Tế bào u lưu hành trong máu |
| CTLA-4 | Cytotoxic T lymphocyte- associated antigen 4 | Cytotoxic T lymphocyte- associated antigen 4 |
| CYP | Cytochrome | Cytochrome |
| DPP-4 | Dipeptidyl peptidase 4 | Dipeptidyl peptidase 4 |
| ECOG | Eastern Cooperative Oncology Group | Nhóm ung thư học hợp tác phương Đông |
| EF | Ejection fraction | Phân suất tống máu |
| ER | Extended release |
Phóng thích kéo dài |
| EGFR | Epidermal growth factor receptor |
Thụ thể yếu tố phát triển biểu mô |
| ESA | Erythropoiesis – stimulating agent | Tác nhân kích thích hồng cầu |
| ESC | European Socitey of Cardiology |
Hội Tim mạch châu Âu |
| ESRD | End Stage Renal Disease | Bệnh thận giai đoạn cuối |
| INR | International Normalized Ratio | Tỉ số bình thường hóa quốc tế |
| IARC | The International Agency for Research on Cancer |
Cơ quan nghiên cứu ung thư quốc tế |
| HbA1c | Hemoglobin A1c | Hemoglobin A1c |
| HEpEF | Heart failure with preserved ejection fraction | Suy tim phân suất tống máu bảo tồn |
| HFrEF | Heart failure with reduced ejection fraction |
Suy tim phân suất tống máu giảm |
| HDL | High Density Lipoprotein | Lipoprotein tỷ trọng cao |
| HIV | Human Immunodeficiency Virus |
Virus gây suy giảm miễn dịch ở người |
| IDF | International diabetes federation |
Liên đoàn Đái tháo đường thế giới |
| IGT | Impaired glucose tolerance | Rối loạn dung nạp glucose |
| LDL | Low Density Lipoprotein | Lipoprotein tỷ trọng thấp |
| LVEF | Left ventricular ejection fraction | Phân suất tống máu thất trái |
| MAP | Medication action plan | Kế hoạch hành động về thuốc |
| MRI | Magnetic Resonnance Imaging | Chụp ảnh cộng hưởng từ |
| NSAID | Non-steroidal antiinflammatory | Thuốc chống viêm không steroid |
| NYHA | New York Heart Asssociation | Hiệp hội Tim New York |
| PD-1 | Program death 1 | Program death 1 |
| PD-L1 | Programmed death-ligand 1 | Programmed death-ligand 1 |
| PET | Positron Emission Tomography | Ghi hình cắt lớp Positron |
| PIVKA-II | Prothrombin induced by vitamin K absence-II |
Yếu tố prothrombin do thiếu vitamin K – II |
| PO | Per Oral | Đường uống |
| PS | Performance Status | Chỉ số toàn trạng |
| PT | Prothrombin Time | Thời gian prothrombin |
| ROS-1 | ROS proto-oncogene 1 | ROS proto-oncogene 1 |
| SCr | Serum creatinin | Nồng độ creatinin trong huyết thanh |
| SGLT-2 | Sodium – glucose cotransporter 2 | Đồng vận chuyển natri – glucose 2 |
| SU | Sulfonylurea | Nhóm thuốc sulfonylurea |
| TACE | Transcatheter arterial chemoembolization | Nút động mạch bằng hóa chất qua ống thông |
| TDM | Therapeutic Drug Monitoring | Giám sát trị liệu bằng thuốc |
| TIA | Transient Ischemic Attack | Cơn thiếu máu não thoáng qua |
| TKI | Tyrosine kinase inhibitor | Thuốc ức chế tyrosine kinase |
| TMB | Tumor Mutation Burden | Lượng đột biến của tế bào bướu |
| TZD | Thiazolidinedione | Nhóm thiazolidinedion |
| WHO | World Health Organization | Tổ chức Y tế thế giới |
MỤC LỤC
Chương 1. Vai trò, nhiệm vụ dược sĩ, kỹ năng thực hành dược lâm sàng
1. Vai trò, nhiệm vụ của dược sĩ lâm sàng 1
2. Kỹ năng thực hành dược lâm sàng 5
Chương 2. Hướng dẫn thực hành dược lâm sàng trong bệnh đái tháo đường
2.1. Đại cương về bệnh và thuốc điều trị đái tháo đường
2.2. Hướng dẫn thực hành DLS trên người bệnh ĐTĐ
Phụ lục chương 2. Hướng dẫn cách sử dụng thuốc điều trị đái tháo đường
Phụ lục 2.1. Cách sử dụng thuốc điều trị đái tháo đường không phải insulin
Phụ lục 2.2. Đặc điểm của các loại insulin về thời gian khởi phát tác dụng, thời gian đạt tác dụng tối đa, thời gian tác dụng, thời điểm dùng thuốc và thời gian bảo quản sau khi mở nắp
Phụ lục 2.3. Hướng dẫn sử dụng insulin dạng lọ
Phụ lục 2.4. Hướng dẫn sử dụng insulin dạng bút tiêm
Phụ lục 2.5. Bảng kiểm tư vấn sử dụng insulin dạng bút tiêm cho người bệnh
Phụ lục 2.6. Bảng kiểm người bệnh ghi lại cách sử dụng insulin dạng bút tiêm
Chương 3. Hướng dẫn thực hành dược lâm sàng trong một số bệnh tim mạch
3.1. Hướng dẫn thực hành dược lâm sàng trong điều trị tăng huyết áp
3.2. Hướng dẫn thực hành dược lâm sàng trong điều trị suy tim
3.3. Hướng dẫn thực hành dược lâm sàng trong điều trị rung nhĩ không do van tim
3.4. Hướng dẫn thực hành dược lâm sàng trong điều trị bệnh mạch vành mạn
Phụ lục chương 3. Hướng dẫn thực hành dược lâm sàng trong một số bệnh tim mạch
Phụ lục 3.1. Đánh giá cận lâm sàng bệnh nhân tim mạch
Phụ lục 3.2. Chống chỉ định và thận trọng của thuốc tim mạch
Phụ lục 3.3. Liều dùng các thuốc tim mạch
Phụ lục 3.4. Tác dụng không mong muốn của các thuốc tim mạch
Phụ lục 3.5. Tương tác thuốc của các thuốc tim mạch
Phụ lục 3.6. Đánh giá nguy cơ tim mạch của bệnh nhân
Phụ lục 3.7. Thẩm định y lệnh các thuốc điều trị rung nhĩ
Phụ lục 3.8. Liều warfarin trên bệnh nhân rung nhĩ
Phụ lục 3.9. Phiếu thông tin dành cho bệnh nhân sử dụng thuốc kháng đông kháng vitamin K
Phụ lục 3.10. Chuyển đổi giữa các thuốc kháng đông
Chương 4. Thực hành dược lâm sàng trong chuyên ngành ung thư
Phụ lục chương 4. Hướng dẫn thực hành dược lâm sàng trong chuyên ngành ung thư
Phụ lục 4.1. Chỉ định, dược động học, độc tính thường gặp của các thuốc
điều trị năm bệnh ung thư phổ biến tại Việt Nam
Phụ lục 4.2. Hiệu chỉnh liều trên bệnh nhân suy thận, suy gan
Phụ lục 4.3. Bảng hướng dẫn sử dụng và độ ổn định sau khi pha
của một số thuốc độc tế bào thường gặp tại Việt nam
Phụ lục 4.4. Hướng dẫn bù nước và điện giải khi truyền cisplatin
Phụ lục 4.5. Bảng hướng dẫn thời điểm sử dụng thuốc đường uống
Phụ lục 4.6. Tương tác thuốc-thuốc trong điều trị cho bệnh nhân ung thư
Phụ lục 4.7. Thuốc chăm sóc giảm nhẹ không opioid và chế độ liều
Phụ lục 4.8. Thuốc chăm sóc giảm nhẹ opioid và cách chuyển đổi
các thuốc giảm đau opioid
Phụ lục 4.9. Bảng kiểm tra thông tin trước pha chế thuốc điều trị ung thư
Phụ lục 4.10. Độc tính và tác dụng không mong muốn thường gặp của thuốc điều trị ung thư
Phụ lục 4.11. Bảng kiểm giám sát tác dụng không mong muốn, độc tính của hóa trị
Phụ lục 4.12. Tác dụng phụ gây nôn, phân loại và phác đồ kiểm soát nôn trong hoá trị
Phụ lục 4.13. Tác dụng không mong muốn gây tiêu chảy của một số thuốc hoá trị và xử trí
Phụ lục 4.14. Tác dụng không mong muốn gây thoát mạch và quy trình xử trí thoát mạch của các thuốc điều trị ung thư
Phụ lục 4.15. Sốt và giảm bạch cầu trung tính trên bệnh nhân sử dụng hóa trị
Phụ lục 4.16. Thiếu máu và điều trị thiếu máu do hóa trị
Phụ lục 4.17. Tiêu chuẩn thực hành trong giai đoạn chuẩn bị thuốc
điều trị ung thư
Phụ lục 4.18. Tiêu chuẩn thực hành trong giai đoạn thực hiện thuốc
điều trị ung thư
Phụ lục 4.19. Một số nội dung tư vấn cho người bệnh mắc bệnh ung thư
DANH MỤC CÁC BẢNG
Bảng 1.1. Khuyến cáo thực hiện hoạt động chăm sóc dược theo phân tuyến chuyên môn
Bảng 1.2. Các thông tin DSLS cần thu thập
Bảng 1.3. Các vấn đề cơ bản liên quan đến dùng thuốc
Bảng 2.1. Mục tiêu cho người bệnh ĐTĐ ở người trưởng thành, không có thai
Bảng 2.2. Tóm tắt ưu, nhược điểm của các thuốc hạ đường huyết đường uống và thuốc đường tiêm không thuộc nhóm insulin
Bảng 2.3. Tác dụng không mong muốn của các thuốc hạ đường huyết đường uống và biện pháp xử trí
Bảng 2.4. Tóm tắt liều dùng và hướng dẫn hiệu chỉnh liều trên người bệnh suy thận của các thuốc hạ đường huyết đường uống và thuốc đường tiêm không thuộc nhóm insulinn
Bảng 2.5. Các thuốc làm tăng glucose huyết
Bảng 2.6. Các thuốc làm giảm glucose huyết
Bảng 2.7. Tương tác thuốc – thuốc thường gặp của các nhóm thuốc điều trị ĐTĐ
Bảng 2.8. Bảng kiểm phỏng vấn tiền sử dùng thuốc của người bệnh
Bảng 2.9. Lập kế hoạch điều trị
Bảng 2.10. Theo dõi điều trị
Bảng 1. Pl2.1. Các thuốc điều trị đái tháo đường không phải insulin
Chương 3. Hướng dẫn thực hành dược lâm sàng trong một số bệnh tim mạch
Bảng 3.1. Định nghĩa THA theo HA đo tại phòng khám, HA holter và HA đo tại nhà theo khuyến cáo về chẩn đoán và điều trị THA của Hội Tim mạch học Việt Nam 2018
Bảng 3.2. Phân loại THA theo mức HA đo tại phòng khám theo khuyến cáo về chẩn đoán và điều trị THA của Hội Tim mạch học Việt Nam 2018
Bảng 3.3. Các yếu tố ảnh hưởng nguy cơ tim mạch ở người bệnh THA
Bảng 3.4. Phân tầng nguy cơ tim mạch của người bệnh THA
Bảng 3.5. Ngưỡng điều trị dựa trên HA tại phòng khám theo khuyến cáo về chẩn đoán và điều trị THA của Hội Tim mạch học Việt Nam 2018
Bảng 3.6. HA mục tiêu trong các tình huống lâm sàng theo khuyến cáo về chẩn đoán và điều trị THA của Hội Tim mạch học Việt Nam 2018
Bảng 3.7. Phiếu khai thác tiền sử bệnh và dùng thuốc
Bảng 3.8. Lựa chọn thuốc điều trị THA trong một số tình huống lâm sàng
Bảng 3.9. Một số vấn đề liên quan đến sử dụng thuốc ở BN THA
Bảng 3.10. Lập kế hoạch điều trị THA
Bảng 3.11. Theo dõi điều trị tăng huyết áp
Bảng 3.12. Phân loại suy tim theo hội tim mạch new york (NYHA)
Bảng 3.13. Một số lưu ý khi lựa chọn thuốc cho bệnh nhân suy tim
có bệnh mắc kèm
Bảng 3.14. Phiếu khai thác tiền sử bệnh và dùng thuốc
Bảng 3.15. Một số vấn đề liên quan đến thuốc trong điều trị suy tim mạn tính
Bảng 3.16. Một số thuốc làm nặng thêm tình trạng suy tim
Bảng 3.17. Kế hoạch điều trị cho bệnh nhân suy tim
Bảng 3.18. Phân loại rung nhĩ
Bảng 3.19. Thang điểm CHAD2DS2-VASC
Bảng 3.20. Thang điểm HAS-BLED đánh giá nguy cơ chảy máu
Bảng 3.21. Phiếu khai thác tiền sử bệnh và dùng thuốc
Bảng 3.22. Một số vấn đề liên quan đến thuốc trong điều trị rung nhĩ
không do van tim
Bảng 3.23. Một số thuốc có nguy cơ gây rung nhĩ
Bảng 3.24. Kế hoạch điều trị cho bệnh nhân rung nhĩ
Bảng 3.25. Phiếu khai thác tiền sử bệnh và dùng thuốc bệnh mạch vành mạn
Bảng 3.26. Một số vấn đề thường gặp ở bệnh nhân BMV mạn
Bảng 3.27. Các thuốc gây thiếu máu cơ tim
Bảng 3.28. Kế hoạch điều trị cho bệnh nhân BMV
Bảng 4.1. Phân loại giai đoạn theo TNM bệnh ung thư gan
Bảng 4.2. Phân loại giai đoạn bệnh ung thư gan theo phân loại Barcelona
Bảng 4.3. Đánh giá chức năng gan theo hệ thống điểm CHILD-PUGH
Bảng 4.4. Phân loại giai đoạn bệnh theo TNM bệnh ung thư phổi
Bảng 4.5. Phân loại giai đoạn theo TNM và DUKES bệnh ung thư đại trực tràng
Bảng 4.6. Chẩn đoán giai đoạn theo TNM bệnh ung thư vú
Bảng 4.7. Xếp loại giai đoạn theo TNM lâm sàng (CTNM) bệnh ung thư dạ dày
Bảng 4.8. Xếp loại giai đoạn bệnh sau mổ theo TNM (pTNM) bệnh ung thư dạ dày
Bảng 4.9. Công việc cụ thể của dược sĩ lâm sàng trong điều trị ung thư
Bảng 1.PL4.2. Chỉnh liều của một số thuốc điều trị ung thư trên
bệnh nhân suy thận, suy gan
Bảng 1.PL4.6. Các tương tác thuốc của thuốc điều trị ung thư cần thận trọng và chống chỉ định
Bảng 2.PL4.6. So sánh phân loại mức độ nặng của tương tác trong MM VÀ SDI
Bảng 3.PL4.6. Phân loại mức độ y văn ghi nhận về tương tác trong MM và SDI
Bảng 4.PL4.6. Bảng phân loại mức độ của tương tác trong HH
Bảng 5.PL4.6. Phân loại mức độ chú ý khi sử dụng và mức độ tương tác thuốc
Bảng 6.PL4.6. So sánh ưu và nhược điểm các cơ sở dữ liệu
Bảng 1.PL4.7. Thuốc giảm đau không opioid
Bảng 2.PL4.7. Các thuốc hỗ trợ trong điều trị đau và cách sử dụng
Bảng 1.PL4.8. Các thuốc opioid và cách sử dụng
Bảng 2.PL4.8. Quy đổi đường tiêm sang đường uống
Bảng 3.PL4.8. Quy đổi liều các opioid khác sang morphin
Bảng 4.PL4.8. Quy đổi morphin đường tiêm sang fentanyl dán
Bảng 5.PL4.8. Opioid yếu dùng đường uống
Bảng 6.PL4.8. Opioid mạnh dùng đường uống và dưới da
Bảng 7.PL4.8. Opioid dùng ngoài da
Bảng 1.PL4.10. Tóm tắt độc tính chính của các thuốc trị ung thư
Bảng 2.PL4.10. Phân loại mức độ nghiêm trọng độc tính của hóa điều trị
Bảng 1.PL4.12. Mức độ gây nôn của các thuốc điều trị ung thư
Bảng 2.PL4.12. Phác đồ kiểm soát nôn trong hóa trị
Bảng 3.PL4.12. Chế độ liều của thuốc chống nôn trong kiểm soát tác dụng phụ gây nôn, buồn của thuốc điều trị ung thư
Bảng 1.PL4.13. Tần suất gặp tiêu chảy ở mức độ 3 và 4 của một số thuốc hóa trị
Bảng 2.PL4.13. Tần suất và mức độ tiêu chảy của một số tác nhân nhắm trúng đích
Bảng 1.PL4.14. Phân loại các tác nhân gây thoát mạch
Bảng 2.PL4.14. Các chất giải độc đặc hiệu đối với một số nhóm hóa điều trị
Bảng 1.PL4.15. Nguy cơ sốt do giảm bạch cầu theo phác đồ hóa trị
Bảng 2.PL4.15. Phân tầng nguy cơ nhiễm khuẩn ở bệnh nhân sốt có giảm bạch cầu trung tính
Bảng 3.PL4.15. Thang điểm mascc (multinational association for supportive care in cancer)
Bảng 4.PL4.15. Chỉ số tình trạng chức năng toàn thân
Bảng 1.PL4.16. Tỷ lệ thiếu máu liên quan đến tác nhân/phác đồ hóa trị
Bảng 2.PL4.16. Nguy cơ và lợi ích của điều trị thiếu máu và thiếu sắt
ở bệnh nhân ung thư
Bảng 3.PL4.16. Liều dùng và cách dùng một số tác nhân kích thích
hồng cầu và sắt
DANH MỤC CÁC HÌNH
Hình 1.1. Những kỹ năng và kiến thức của dược sĩ lâm sàng trong chăm
sóc người bệnh
Hình 3.1. Ngưỡng huyết áp ban đầu cần điều trị theo Khuyến cáo về chẩn đoán và điều trị THA của Hội Tim mạch học Việt Nam 2018
Hình 3.2. Sơ đồ khuyến cáo điều trị THA theo Khuyến cáo về chẩn đoán và điều trị THA của Hội Tim mạch học Việt Nam 2018
Hình 3.3. Chiến lược điều trị thuốc với tăng huyết áp không biến chứng theo Khuyến cáo về chẩn đoán và điều trị tăng huyết áp của Hội Tim mạch học Việt Nam 2018
Hình 3.4. Lưu đồ chẩn đoán suy tim của Hội Tim mạch học châu Âu 2016
Hình 3.5. Lưu đồ điều trị bệnh nhân suy tim phân suất tống máu giảm
Hình 3.6. Kiểm soát cấp tính tần số trong rung nhĩ
Hình 3.7. Kiểm soát nhịp tim trong điều trị rung nhĩ
Hình 3.8. Dự phòng huyết khối ở bệnh nhân rung nhĩ không do van tim
Hình 3.9. Lưu đồ điều trị đau thắt ngực ổn định
Hình 4.1. Kim chùm dùng đốt sóng cao tần
Hình 4.2. Minh họa hoạt động sinh nhiệt của kim đốt trong khối u
Hình 4.3. Hình ảnh nút mạch khối u gan
Hình 4.4. So sánh hai phương pháp xạ trị photon và xạ trị proton
Hình 4.5 Máy xạ phẫu gamma quay
Hình 4.6. Máy xạ trị áp sát
Hình 4.7. Hình ảnh cấy hạt phóng xạ điều trị ung thư tuyến tiền liệt
Chương 1. VAI TRÒ, NHIỆM VỤ DƯỢC SĨ, KỸ NĂNG
THỰC HÀNH DƯỢC LÂM SÀNG
1. VAI TRÒ, NHIỆM VỤ CỦA DƯỢC SĨ LÂM SÀNG
1.1. Một số định nghĩa
1.1.1. Dược lâm sàng
Theo Luật Dược 105/2016/QH13: Dược lâm sàng (DLS) là hoạt động nghiên cứu khoa học và thực hành dược về tư vấn sử dụng thuốc hợp lý, an toàn, hiệu quả nhằm tối
ưu hóa việc sử dụng thuốc.
1.1.2 Dược sĩ lâm sàng
Là những dược sĩ làm việc trong lĩnh vực DLS tại các cơ sở khám chữa bệnh, tại nhà thuốc, chăm sóc tại nhà, phòng khám hay bất cứ nơi nào có kê đơn và sử dụng thuốc; Thực hiện tư vấn về thuốc cho thầy thuốc trong chỉ định và điều trị, hướng dẫn sử dụng thuốc cho cán bộ y tế và người bệnh.
1.1.3 Thực hành dược lâm sàng
Thực hành dược lâm sàng là một cấu phần trong thực hành của đội ngũ chăm sóc sức khỏe với mục tiêu tối ưu hóa kết quả điều trị cho bệnh nhân bằng các can thiệp dược nhằm sử dụng thuốc an toàn, hợp lý và hiệu quả tại các cơ sở khám chữa bệnh.
Thực hành dược lâm sàng hướng tới người bệnh làm trung tâm, các hoạt động của DSLS gắn liền với quá trình sử dụng thuốc, không chỉ đơn thuần là xem xét đơn thuốc mà cần quan tâm hơn đến sử dụng thuốc trên người bệnh.
Thực hành dược lâm sàng bao gồm:
– Tham gia cùng đội ngũ chăm sóc sức khỏe (bác sĩ, điều dưỡng…) chăm sóc/điều trị từng bệnh nhân;
– Áp dụng bằng chứng tốt nhất hiện có trong thực hành dược lâm sàng hàng ngày;
– Đóng góp kiến thức và kỹ năng lâm sàng cho đội ngũ chăm sóc sức khỏe;
– Kiểm soát và giảm thiểu rủi ro liên quan đến sử dụng thuốc;
– Tham gia giáo dục/tư vấn bệnh nhân, người chăm sóc và các nhân viên y tế khác.
1.1.4 Chăm sóc dược
Chăm sóc dược là sự chăm sóc mà từng bệnh nhân yêu cầu và nhận được khi trị liệu bằng thuốc, giúp đảm bảo việc sử dụng thuốc an toàn và hợp lý. Khác với thực hành dược lâm sàng, chăm sóc dược chỉ tập trung vào bệnh nhân cụ thể, nói cách khác là tập trung vào thực hành dược lâm sàng trên từng người bệnh.
Hoạt động chăm sóc dược: là lĩnh vực thực hành lấy người bệnh làm trung tâm, trong đó chuyên gia y tế nhận trách nhiệm đáp ứng các nhu cầu liên quan đến thuốc của bệnh nhân và luôn luôn phải đảm bảo hoàn thành trách nhiệm đó.
Hoạt động chăm sóc dược gồm các nội dung sau:
– Thu thập và tổ chức thông tin của người bệnh
– Xác định những vấn đề liên quan đến điều trị bằng thuốc của người bệnh
– Xác định những nhu cầu của người bệnh
– Xác định mục tiêu điều trị bằng thuốc (cụ thể)
– Xây dựng kế hoạch điều trị bằng thuốc
– Xây dựng kế hoạch theo dõi
– Trao đổi kế hoạch điều trị, kế hoạch theo dõi với NVYT và người bệnh
– Thực hiện và theo dõi đáp ứng điều trị
– Thiết kế lại kế hoạch điều trị, kế hoạch theo dõi dựa trên đáp ứng lâm sàng của người bệnh.
1.2. Vai trò, nhiệm vụ dược sĩ lâm sàng
1.2.1. Nhiệm vụ theo quy định hiện hành
Theo Hướng dẫn của Thông tư số 31/2012/TT-BYT, dược sĩ lâm sàng thực hiện 14 nhiệm vụ chung như sau tại cơ sở khám chữa bệnh:
- Tham gia phân tích, đánh giá tình hình sử dụng thuốc;
2. Tham gia tư vấn trong quá trình xây dựng danh mục thuốc của đơn vị, đưa ra ý kiến hoặc cung cấp thông tin dựa trên bằng chứng về việc thuốc nào nên đưa vào hoặc bỏ ra khỏi danh mục thuốc để bảo đảm mục tiêu sử dụng thuốc an toàn, hợp lý và hiệu quả;
3. Tham gia xây dựng các quy trình chuyên môn liên quan đến sử dụng thuốc: quy trình pha chế thuốc (dùng cho chuyên khoa nhi, chuyên khoa ung bướu, dịch truyền nuôi dưỡng nhân tạo ngoài đường tiêu hóa), hướng dẫn điều trị, quy trình kỹ thuật của bệnh viện;
4. Tham gia xây dựng quy trình giám sát sử dụng đối với các thuốc trong danh mục (bao gồm các thuốc có khoảng điều trị hẹp, nhiều tác dụng phụ nghiêm trọng, kháng sinh, thuốc cần pha truyền đặc biệt (chuyên khoa nhi, ung bướu), thuốc cần điều kiện bảo quản đặc biệt) do Giám đốc bệnh viện ban hành trên cơ sở được tư vấn của Hội đồng Thuốc và Điều trị;
5. Hướng dẫn và giám sát việc sử dụng thuốc trong bệnh viện;
6. Thông tin thuốc cho người bệnh và cán bộ y tế: DSLS cập nhật thông tin sử dụng thuốc, thông tin về thuốc mới, thông tin cảnh giác được gửi đến cán bộ y tế và đến người bệnh bằng nhiều hình thức khác nhau như: trực tiếp, văn bản, bảng tin bệnh viện, thư điện tử, tranh ảnh, tờ hướng dẫn, trang thông tin điện tử;
7. Tập huấn, đào tạo về DLS: DSLS lập kế hoạch, chuẩn bị tài liệu, cập nhật kiến thức sử dụng thuốc cho bác sĩ, dược sĩ, điều dưỡng viên, kỹ thuật viên, hộ sinh viên của đơn vị mình. Kế hoạch và nội dung phải được Giám đốc bệnh viện phê duyệt;
8. Báo cáo định kỳ hằng tháng, hằng quý, hằng năm và báo cáo đột xuất theo yêu cầu của Ban Giám đốc, Hội đồng Thuốc và Điều trị: DSLS báo cáo công tác sử dụng thuốc trong buổi họp của Hội đồng Thuốc và Điều trị hoặc buổi giao ban của đơn vị, có ý kiến trong các trường hợp sử dụng thuốc chưa phù hợp;
9. Theo dõi, giám sát phản ứng có hại của thuốc (ADR) và là đầu mối báo cáo các phản ứng có hại của thuốc tại đơn vị theo quy định hiện hành;
10. Tham gia các hoạt động, công trình nghiên cứu khoa học, đặc biệt là các nghiên cứu liên quan đến vấn đề sử dụng thuốc an toàn – hợp lý, vấn đề cải tiến chất lượng và nâng cao hiệu quả công tác DLS, nghiên cứu sử dụng thuốc trên lâm sàng;
11. Tham gia hội chẩn chuyên môn về thuốc, đặc biệt trong các trường hợp bệnh nặng, bệnh cần dùng thuốc đặc biệt, người bệnh bị nhiễm vi sinh vật kháng thuốc;
12. Tham gia bình ca lâm sàng định kỳ tại khoa lâm sàng, tại bệnh viện;
13. Giám sát chặt chẽ việc tuân thủ quy trình sử dụng thuốc đã được Hội đồng Thuốc và Điều trị thông qua và Giám đốc bệnh viện phê duyệt;
14. Tham gia xây dựng và thực hiện quy trình giám sát điều trị thông qua theo dõi nồng độ thuốc trong máu (TDM) tại các bệnh viện có điều kiện triển khai TDM.
1.2.2 Nhiệm vụ của dược sĩ lâm sàng tại khoa lâm sàng
DSLS tham gia đi buồng bệnh và phân tích sử dụng thuốc của người bệnh. Tùy theo đặc thù của từng bệnh viện, mỗi bệnh viện sẽ lựa chọn khoa lâm sàng và đối tượng người bệnh cần ưu tiên để triển khai các hoạt động thực hành DLS. Đối với từng người bệnh, DSLS phải thực hiện năm nhóm nhiệm vụ sau:
1. Khai thác thông tin của người bệnh (bao gồm cả khai thác thông tin trên bệnh án và tiến hành phỏng vấn trực tiếp người bệnh) về:
a) Tiền sử sử dụng thuốc;
b) Tóm tắt các dữ liệu lâm sàng và các kết quả cận lâm sàng đã có.
2. Xem xét các thuốc được kê đơn cho người bệnh (trong quá trình đi buồng bệnh cùng với bác sĩ và xem xét y lệnh trong hồ sơ bệnh án, đơn thuốc) về:
a) Chỉ định;
b) Chống chỉ định;
c) Lựa chọn thuốc;
d) Dùng thuốc cho người bệnh: liều dùng, khoảng cách dùng, thời điểm dùng, đường dùng, dùng thuốc trên các đối tượng đặc biệt, thời gian dùng thuốc;
đ) Các tương tác thuốc cần chú ý;
e) Phản ứng có hại của thuốc.
Sau khi hoàn thành quá trình xem xét các thuốc được kê đơn cho người bệnh, nếu phát hiện có vấn đề liên quan đến sử dụng thuốc, DSLS trao đổi với bác sĩ điều trị để tối ưu hóa việc dùng thuốc.
3. Hướng dẫn sử dụng thuốc cho điều dưỡng.
4. Phối hợp với bác sĩ điều trị để cung cấp thông tin tư vấn cho người bệnh về những điều cần lưu ý trong quá trình sử dụng thuốc.
5. Giám sát và báo cáo sai sót thuốc.
1.2.3. Nhiệm vụ theo phân tuyến chuyên môn
Ở phạm vi hướng dẫn này, các hoạt động DLS được ưu tiên tập trung chủ yếu vào hoạt động DLS trên từng người bệnh hay cụ thể là thực hành chăm sóc dược trên từng người bệnh.
Tùy theo quy mô và nguồn lực của từng bệnh viện, hoạt động thực hành DLS được phân chia thành các cấp độ tương đương các tuyến chuyên môn kỹ thuật đối với hệ thống cơ sở khám chữa bệnh. Cách phân loại này tạo điều kiện thuận lợi hơn trong việc định hướng các hoạt động DLS của dược sĩ tại từng tuyến chuyên môn, chi tiết từng hoạt động xem thêm ở mục 1.2.
Bảng 1.1. Khuyến cáo thực hiện hoạt động chăm sóc dược theo phân tuyến chuyên môn
| Các tuyến chuyên môn kỹ thuật | Hoạt động lâm sàng ưu tiên theo tuyến | Diễn giải hoạt động |
| Tuyến 4 (tuyến xã, phường, thị trấn) | – Kiểm tra sự phù hợp giữa chẩn đoán và thuốc* | Cấp phát thuốc phù hợp với chẩn đoán |
| Tuyến 3 (tuyến huyện, quận, thị xã, thành phố trực thuộc tỉnh) | – Kiểm tra sự phù hợp giữa chẩn đoán và thuốc
– Kiểm tra tính hợp lý trong sử dụng thuốc – Kiểm tra tương tác thuốc* |
Cấp phát thuốc phù hợp theo chẩn đoán, phát hiện và can thiệp khi:
– Thuốc được sử dụng mà không có chỉ định – Chỉ định không phù hợp/tình trạng bệnh không được điều trị. – Thuốc không phù hợp về liều, dạng bào chế, đường dùng, thời gian dùng, cách dùng – Thuốc được kê trên bệnh nhân có chống chỉ định. – Thuốc được kê có tương tác chống chỉ định về thuốc – thuốc, thuốc – thực phẩm, thuốc – tình trạng bệnh, thuốc – khác. |
| Tuyến 2 (tuyến tỉnh, thành phố trực thuộc Trung ương) | Như tuyến 3 và bổ sung:
– Đánh giá người bệnh – Tư vấn phù hợp – Xây dựng và tiến hành các chương trình đào tạo, quản lý |
– Hoạt động của tuyến 3
– ADRs thực tế và tiềm ẩn; – Sự tuân thủ điều trị của bệnh nhân; – Sự hiểu biết của người bệnh về việc điều trị bằng thuốc; – Các sai sót, vấn đề liên quan đến sử dụng thuốc; – Quá trình điều trị (sự thay đổi về cận lâm sàng, thuốc sử dụng,…). – Tư vấn về chế độ dùng thuốc – Tư vấn về sự tuân thủ dùng thuốc – Quản lý phản ứng có hại của thuốc: Dị ứng thuốc, ADR thông thường / nghiêm trọng – Xem xét sai sót, vấn đề liên quan đến sử dụng thuốc. – Tập huấn ADR và tương tác cho nhân viên y tế |
| Tuyến 1 (tuyến
trung ương) |
Như tuyến 2 và bổ sung:
– Lập kế hoạch điều trị trên từng người bệnh – Đánh giá chi phí – hiệu quả điều trị* |
– Hoạt động của tuyến 2
– Lập kế hoạch chăm sóc dược – Theo dõi và đánh giá điều trị – Quản lý thuốc điều trị – Lựa chọn thuốc tối ưu – Sử dụng thuốc tối ưu |
* Khuyến khích hoạt động
2. KỸ NĂNG THỰC HÀNH DƯỢC LÂM SÀNG
2.1. Kỹ năng thực hành dƣợc lâm sàng
Hoạt động của DSLS bao gồm sử dụng thuốc trong điều trị cho cả bệnh nhân nội trú và ngoại trú đã được chẩn đoán bệnh và có liệu pháp điều trị. Hoạt động này không chỉ bắt đầu từ khi phân phối thuốc đến người bệnh mà phải ngay từ khâu lựa chọn thuốc cho kê đơn; hướng dẫn nhân viên y tế, người bệnh những vấn đề liên quan đến thuốc, theo dõi hiệu quả, độ an toàn, phát hiện nguyên nhân thất bại điều trị liên quan đến sử dụng thuốc (nếu có như: không tuân thủ điều trị, tương tác thuốc, sai thuốc, sai liều…).
Thực hành DLS được thực hiện trong từng giai đoạn của quá trình sử dụng thuốc từ những xem xét, đánh giá ban đầu đến thực hiện kế hoạch chăm sóc dược và đánh giá, theo dõi trị liệu.
Thực hành DLS cần được sự hỗ trợ của các cấp quản lý và được thực hiện bởi các dược sĩ được đào tạo chuyên sâu và đủ điều kiện theo quy định hiện hành, có thể được hỗ trợ bởi các nhân viên y tế khác có chuyên môn về dược (dược sĩ cao đẳng, điều dưỡng) được giám sát thích hợp, tạo điều kiện thuận lợi cho việc sử dụng thuốc hiệu quả và tiết kiệm nhất nhằm mục đích tối ưu hóa chăm sóc bệnh nhân, các hoạt động như sau:
2.1.1. Đánh giá sự phù hợp giữa chẩn đoán và thuốc
– Thuốc được kê đơn không phù hợp về chỉ định, phác đồ, thuốc được sử dụng mà không có chỉ định, có y lệnh nhưng không có thuốc;
– Kê đơn thuốc trên bệnh nhân có tiền sử dị ứng trước đó;
2.1.2. Đánh giá tính hợp lý trong sử dụng thuốc
– Liều dùng, dạng bào chế, đường dùng, thời gian dùng, cách dùng, thời điểm dùng;
– Kê đơn thuốc trên bệnh nhân có chống chỉ định;
– Sử dụng thuốc trên đối tượng đặc biệt: PNCT, PNCCB, trẻ em, người cao tuổi,người bệnh suy giảm chức năng thận, người bệnh suy giảm chức năng gan, người bệnh béo phì;
– Có tương tác thuốc thực tế hoặc tiềm ẩn: thuốc – thuốc, thuốc – bệnh, thuốc – thực phẩm, thuốc – khác.
2.1.3. Đánh giá người bệnh
– ADR thực tế và tiềm ẩn;
– Sự tuân thủ điều trị của người bệnh;
– Sự hiểu biết của người bệnh về việc điều trị bằng thuốc;
– Các sai sót, vấn đề liên quan đến sử dụng thuốc;
– Quá trình điều trị (sự thay đổi về cận lâm sàng, thuốc sử dụng,…).
2.1.4. Đánh giá chi phí – hiệu quả điều trị
– Lựa chọn thuốc tối ưu: các chi phí liên quan đến sử dụng thuốc hoặc liệu pháp điều trị với hiệu quả điều trị;
– Các vấn đề phát sinh liên quan đến chi phí điều trị bằng thuốc cho bệnh nhân, bao gồm những chi phí khác (chi phí trong dịch vụ chăm sóc, chi phí gián tiếp).
2.2. Các bước trong thực hành chăm sóc dược
Là những hoạt động lâm sàng cụ thể nhằm mục đích hỗ trợ và đánh giá các vấn đề liên quan về thuốc. Các bước cơ bản của cách tiếp cận và thực hành DLS cho từng người bệnh cụ thể như sau:
2.2.1. Thu thập, đánh giá và biện giải các dữ liệu liên quan đến người bệnh
Đánh giá các thông tin liên quan đến người bệnh cụ thể để hỗ trợ dược sĩ trong việc thiết lập các mục tiêu của kế hoạch điều trị và chăm sóc.
– Xác định những vấn đề về thuốc của người bệnh;
– Tìm hiểu về tiền sử dùng thuốc của người bệnh để đưa ra góp ý về quyết định điều trị;
– Khai thác những thông tin liên quan đến việc dùng thuốc;
– Đánh giá việc dùng thuốc của người bệnh thông qua bốn nội dung: tính phù hợp của thuốc với chỉ định; hiệu quả của thuốc cho chỉ định này; độ an toàn của thuốc; xem xét mức độ tuân thủ của người bệnh.
Bảng 1.2. Các thông tin DSLS cần thu thập
| Thông tin | Diễn giải hoạt động |
| Thông tin liên quan đến người bệnh | – Nhân khẩu học: tuổi, giới tính, chủng tộc, chiều cao, cân nặng
– Đặc điểm xã hội: nghề nghiệp, nhu cầu đặc biệt – Tiền sử gia đình: tiền sử bệnh của cha mẹ, anh chị em trong gia đình – Tiền sử điều trị |
| Thông tin liên quan đến bệnh lý | – Tiền sử bệnh
– Lý do nhập viện – Bệnh lý hiện tại, chẩn đoán quá trình tiến triển bệnh – Thông tin tổng quan về hiện trạng của người bệnh – Chẩn đoán bệnh chính, bệnh kèm, biến chứng, chẩn đoán phân biệt – Xét nghiệm cận lâm sàng – Kết quả chẩn đoán hình ảnh |
| Thông tin liên quan đến thuốc/Tiền sử dùng thuốc | – Dị ứng và tác dụng không mong muốn của thuốc
– Thuốc người bệnh hiện tại đang dùng – Lý do chỉ định – Người bệnh dùng thuốc này như thế nào – Hiệu quả và tác dụng phụ của thuốc đang điều trị – Thắc mắc của người bệnh liên quan đến dùng thuốc – Thuốc dùng đồng thời bao gồm: thuốc không kê đơn, thực phẩm chức năng, thuốc đông y, thuốc dùng ngoài… – Thuốc đã dùng trong vòng 3-6 tháng gần đây |
2.2.2. Xác định các vấn đề liên quan đến sử dụng thuốc
Thông qua đánh giá việc dùng thuốc của người bệnh, bao gồm các hoạt động sau:
- Đánh giá sự phù hợp của từng thuốc với chỉ định
- Tối ưu hóa điều trị: lựa chọn thuốc, chế độ liều
- Cá thể hóa trị cho từng người bệnh, giảm thiểu tối đa các tác dụng phụ
- Đánh giá các vấn đề khác bao gồm: chi phí, mức độ tuân thủ, thuận tiện cho người bệnh.
- Lựa chọn thuốc phù hợp (chỉ định, chống chỉ định)
- Tương tác thuốc-thuốc, thuốc-thức ăn, đồ uống
- Liều dùng
- Đường dùng và thời gian dùng
- Lựa chọn dạng dùng, nồng độ, tốc độ truyền, tương kỵ
- Đặc điểm của người bệnh (phụ nữ có thai, đang cho con bú, suy gan, suy thận, trẻ em, người cao tuổi.)
- Giám sát điều trị thông qua định lượng nồng độ thuốc trong máu nếu điều kiện cho phép.
Bảng 1.3. Các vấn đề cơ bản liên quan đến dùng thuốc
| Đánh giá | Vấn đề liên quan đến thuốc | Khả năng | Chi tiết/Nguyên nhân |
| Chỉ định | 1. Điều trị không cần thiết | Không có chỉ định điều trị | |
| Trùng lặp thuốc | Dùng nhiều thuốc trong cùng một nhóm dược lý trong khi một thuốc đã đủ tác dụng | ||
| Có chỉ định điều trị không dùng thuốc | |||
| Điều trị tác dụng phụ của thuốc trong khi có thể phòng ngừa được | |||
| 2. Cần bổ sung điều trị | Vấn đề chưa được điều trị | ||
| Dự phòng | Cần bổ sung thuốc dự phòng để giảm nguy cơ tiến triển bệnh | ||
| Thuốc có tác dụng hiệp đồng | |||
| Hiệu quả điều trị | 3. Cần thuốc khác | Có thuốc khác hiệu quả hơn | Người bệnh nhiễm vi khuẩn kháng với thuốc đang điều trị
Thuốc điều trị không phải là lựa chọn tối ưu Thuốc không hiệu quả trong điều trị bệnh này |
| Người bệnh không đáp ứng hoặc dung nạp thuốc | |||
| Liều thuốc không phù hợp | |||
| Thuốc đắt tiền và có thể thay bằng thuốc khác | |||
| 4. Liều thuốc quá thấp | Sai liều | ||
| Khoảng cách dùng quá xa | |||
| Thời gian dùng ngắn | |||
| Tương tác thuốc | Tương tác thuốc làm giảm tác dụng điều trị | ||
| Đánh giá | Vấn đề liên quan đến thuốc | Khả năng | Chi tiết/Nguyên nhân |
| Dùng thuốc không phù hợp (đường dùng, cách dùng, thời điểm dùng) | |||
| Sai sót thuốc | |||
| An toàn | 5. Tác dụng không mong muốn của thuốc | Tác dụng không mong muốn (TDKMM) | |
| Không an toàn cho người bệnh | Cần đổi sang thuốc an toàn hơn | ||
| Tương tác thuốc | |||
| Dị ứng thuốc | |||
| Chống chỉ định | |||
| Kỹ thuật đưa thuốc chưa hợp lý | |||
| 6. Liều thuốc quá cao | Sai liều | ||
| Khoảng cách dùng quá gần | |||
| Thời gian dùng thuốc kéo dài | |||
| Tương tác thuốc | Tương tác thuốc làm tăng TDKMM/độc tính | ||
| Dùng thuốc không phù hợp (đường dùng, cách dùng, thời điểm dùng) | Truyền nhanh thuốc so với khuyến cáo | ||
| Sai sót thuốc | |||
| Tuân thủ điều trị | Người bệnh không hiểu phương pháp điều trị | ||
| 7. Không tuân thủ | Người bệnh không muốn dùng thuốc | ||
| Người bệnh quên dùng thuốc | |||
| Giá thuốc cao | |||
| Người bệnh không thể nuốt hoặc tự dùng thuốc hoặc đường dùng không phù hợp | |||
| Thuốc không có sẵn | |||
2.2.3. Lập kế hoạch chăm sóc dược
– Xác định các mục tiêu điều trị: xác định mục đích chung của kế hoạch điều trị người bệnh (ví dụ như điều trị, kiểm soát triệu chứng, dự phòng) để có thể xây dựng kế hoạch chăm sóc dược phù hợp. Mục tiêu này cần được sự thống nhất của đội ngũ chăm sóc sức khoẻ và người bệnh.
– Đánh giá và chọn phương án điều trị: dựa vào tính hiệu quả, an toàn, khả năng sẵn có, chi phí, đặc điểm của từng người bệnh, lợi ích và nguy cơ, sự đồng thuận của người bệnh… để đạt được mục tiêu điều trị theo phương án phù hợp nhất. Trong một số trường hợp, lựa chọn phù hợp nhất có thể không bao gồm điều trị bằng thuốc (nói cách khác là biện pháp không dùng thuốc).
2.2.4. Theo dõi trị liệu
– So sánh thực trạng của người bệnh với mục tiêu điều trị ban đầu, nhận xét khách quan tác động tích cực hoặc tiêu cực của kế hoạch chăm sóc dược lên tình trạng của người bệnh. Xác định:
+ Vấn đề mới liên quan đến thuốc và có tác động phù hợp lên những vấn đề mới hoặc điều chỉnh, thay đổi hướng điều trị cũ nếu cần.
+ Tương tự như mục tiêu điều trị, kế hoạch theo dõi trị liệu cần cụ thể (tình trạng lâm sàng và cận lâm sàng) tần suất theo dõi, nhu cầu của người bệnh
| Tình trạng | Định nghĩa |
| Khỏi bệnh | Đã đạt được mục tiêu điều trị cho tình trạng cấp tính, ngừng điều trị |
| Ổn định | Đã đạt được mục tiêu điều trị, tiếp tục điều trị tương tự để kiểm soát bệnh mạn tính |
| Cải thiện | Tình trạng bệnh đang được cải thiện và hướng đến mục tiêu, tiếp tục điều trị vì cần nhiều thời gian để đạt được hiệu quả điều trị mong muốn |
| Cải thiện một phần | Tình trạng bệnh đang được cải thiện, tuy nhiên cần điều chỉnh một ít để đạt hiệu quả điều trị mong muốn |
| Không cải thiện | Tình trạng bệnh cải thiện một ít hoặc không cải thiện, cần thêm thời gian để đánh giá hiệu quả điều trị |
| Tình trạng nặng hơn | Tình trạng bệnh trở nên xấu hơn mặc dù đã dùng thuốc đủ thời gian, nên tăng liều, bổ sung thêm thuốc có tác dụng hiệp đồng |
| Thất bại | Mục tiêu điều trị không đạt mặc dù đã dùng đủ liều và thời gian Cân nhắc thay đổi thuốc điều trị |
| Tử vong | Người bệnh tử vong khi đang điều trị bằng thuốc, ghi lại những yếu tố liên quan và phân tích, đặc biệt nếu có liên quan đến thuốc |
2.3 Kỹ năng của dược sĩ lâm sàng
DSLS trong quá trình thực hành chăm sóc dược không những cần có những kiến thức chuyên môn về điều trị (điều trị bằng thuốc và điều trị không dùng thuốc); Hiểu biết tốt về sinh lý bệnh; kiến thức dược lý về thuốc; mà cần có kỹ năng giao tiếp; giám sát sử dụng thuốc, thông tin thuốc và kỹ năng lập kế hoạch điều trị; kỹ năng đánh giá và giải thích các kết quả liên quan (Hình 1.1). Trong chương này, chỉ tập trung vào một số kỹ năng cần thiết cho dược sĩ trong quá trình thực hành DLS.
2.3.1 Kỹ năng giao tiếp
Khả năng giao tiếp rõ ràng và hiệu quả với người bệnh, người nhà của người bệnh, bác sĩ, điều dưỡng, dược sĩ và các chuyên gia chăm sóc sức khỏe khác là một kỹ năng quan trọng. Giao tiếp kém giữa dược sĩ và người bệnh có thể dẫn đến tiền sử dùng thuốc cho người bệnh không chính xác và các quyết định điều trị không phù hợp; hoặc có thể làm cho người bệnh nhầm lẫn. Giao tiếp kém giữa dược sĩ – bác sĩ, dược sĩ – điều dưỡng, dược sĩ – dược sĩ có thể gây hại cho người bệnh nếu thông tin quan trọng không được trao đổi một cách thích hợp và kịp thời và kỹ năng giao tiếp có thể được học.
Kỹ năng giao tiếp gồm một số hình thức như sau:
– Kỹ năng giao tiếp bằng lời nói: bao gồm khả năng nghe, hiểu và trả lời câu hỏi của mọi người (lắng nghe tích cực); Khả năng diễn giải phi ngôn ngữ và phản hồi theo cách khuyến khích tiếp tục tương tác (đánh giá).
– Kỹ năng lắng nghe tích cực: Tập trung vào người bệnh, người nhà của người bệnh hoặc chuyên gia chăm sóc sức khỏe. Làm cho người nghe cảm thấy là trung tâm của sự chú ý. Truyền đạt với một thái độ cởi mở, thoải mái và không vội vã. Hạn chế các yếu tố gây gián đoạn (ví dụ: tiếng bíp, điện thoại di động, tham vấn).
– Kỹ năng quan sát và đánh giá: ngôn ngữ cơ thể và cử chỉ khi giao tiếp cũng cung cấp nhiều thông tin quan trọng cho dược sĩ và các nhân viên y tế khi giao tiếp với người bệnh.
– Kỹ năng giao tiếp bằng văn bản: Dược sĩ phải có khả năng ghi lại chính xác và hiệu quả những thông tin người bệnh trong hồ sơ bệnh án điều trị nội trú, trong hồ sơ sử dụng thuốc ngoại trú của nhà thuốc.
2.3.2 Kỹ năng khai thác tiền sử dùng thuốc
Tiền sử dùng thuốc là nền tảng để lập kế hoạch cho chế độ dùng thuốc đặc hiệu trên người bệnh. Tiền sử dùng thuốc là điểm khởi đầu để đưa ra các giả thuyết liên quan đến sự hiểu biết của bệnh nhân về vai trò của thuốc trong điều trị, tuân thủ dùng thuốc; hiệu quả của thuốc và liên quan tác dụng phụ, dị ứng và phản ứng có hại của thuốc.
Dược sĩ cần có sự kết hợp giữa kiến thức chuyên môn và kinh nghiệm liên quan đến thuốc; người bệnh tin tưởng và tôn trọng dược sĩ. Mặc dù các chuyên gia chăm sóc sức khỏe khác phỏng vấn người bệnh về việc sử dụng thuốc nhưng không có chuyên gia chăm sóc sức khỏe nào khác như dược sĩ có kiến thức chuyên sâu về thuốc. Do đó, điều quan trọng là dược sĩ khai thác được, ghi lại tiền sử thuốc của người bệnh và truyền đạt thông tin này cho nhân viên y tế khi cần thiết.
2.3.3 Kỹ năng lập kế hoạch điều trị
Lập kế hoạch điều trị hiệu quả tạo điều kiện thuận lợi cho việc lựa chọn các biện pháp điều trị (cả dùng thuốc và không dùng thuốc, bao gồm giáo dục bệnh nhân). Lập kế hoạch điều trị cần kết hợp các chế độ điều trị thay thế. Lập kế hoạch thành công đòi hỏi kiến thức chuyên môn về dược lý học, bệnh học, đánh giá thông số lâm sàng và các xét nghiệm chẩn đoán.
Lập kế hoạch kết hợp xem xét các yếu tố khác liên quan đến người bệnh có ảnh hưởng đến chế độ điều trị (tiền sử, không tuân thủ dùng thuốc, kinh nghiệm trước đó với thuốc kê đơn và không kê đơn, liệu pháp đồng thời, chế độ dùng thuốc khác), cũng như xem xét cách thức thuốc ảnh hưởng đến bệnh nhân (tác dụng phụ như buồn ngủ hoặc chóng mặt, chi phí điều trị).
2.3.4 Kỹ năng giám sát, theo dõi điều trị bằng thuốc
Chăm sóc tập trung vào người bệnh là một quá trình liên tục thu thập và đánh giá dữ liệu, xác định và ưu tiên vấn đề, lập kế hoạch điều trị và theo dõi bệnh nhân. Trong đó, giám sát, theo dõi điều trị bằng thuốc là một thành phần quan trọng của quy trình lập kế hoạch điều trị từ việc thu thập các thông tin chủ quan, thông tin khách quan; từ đó, đưa ra các đánh giá và xây dựng kế hoạch điều trị bao gồm xác định, đo lường và đánh giá các thông số kết quả cụ thể của người bệnh. Theo dõi kết quả người bệnh kịp thời, cung cấp cho bác sĩ lâm sàng thông tin cần thiết để xác định liệu các biện pháp can thiệp không dùng thuốc và dùng thuốc có đạt được mục tiêu điều trị hay liệu các biện pháp can thiệp có cần phải được thay đổi.
Giám sát trong sử dụng thuốc giúp cung cấp thông tin để chứng minh và giải thích lý do tại sao cần phải thay đổi điều trị (ví dụ: đáp ứng không đầy đủ, diễn tiến bệnh, than phiền của người bệnh, dị ứng thuốc, tương tác thuốc, phản ứng bất lợi không mong muốn hoặc có khả năng gây nguy hiểm).
TÀI LIỆU THAM KHẢO
Tiếng Việt
- Hoàng Kim Huyền, Brouwers J.R.B.J (2014), Những nguyên lý cơ bản và sử dụng thuốc trong điều trị, Tập 1, Nhà Xuất bản Y học, Hà Nội.
- Bộ Y tế (2012), Thông tư số 31/2012/TT-BYT Hướng dẫn hoạt động dược lâm sàng trong bệnh viện.
- Bộ Y tế (2013), Thông tư số 43/2013/ TT-BYT quy định chi tiết phân tuyến chuyên môn kỹ thuật đối với hệ thống cơ sở khám bệnh, chữa bệnh.
- Luật Dược số 105/2016/QH13, (2016).
Tiếng Anh
- American College of Clinical Pharmacy (2008). The definition of clinical pharmacy. Pharmacotherapy;28(6):817-8-8
- Karen J (2012), Clinical Skills for Pharmacist, Mosby, Elsevier Inc.
- Robert S., Carole L. (2008), Communication skills in pharmacy practice, Lippincott Williams.
- Philip Wiffen, Marc Mitchell (2017), Oxford Handbook of Clinical Pharmacy.
- American College of Clinical Pharmacy (2014). Standards of Practice for Clinical Pharmaci sts. Pharmacotherapy;34(8):794-797.
- SHPA Committe of Specialty Practice in Clinical Pharmacy (2005). SHPA Standards of Practice for Clinical Pharmacists. Pharmacotherapy; J Pharm Pract Res 35(2):122-7146.
Chương 2. HƯỚNG DẪN THỰC HÀNH DƯỢC LÂM SÀNG
TRONG BỆNH ĐÁI THÁO ĐƯỜNG
1. ĐẠI CƯƠNG VỀ BỆNH VÀ THUỐC ĐIỀU TRỊ ĐÁI THÁO ĐƯỜNG
1.1 Đại cương về bệnh
Bệnh ĐTĐ là bệnh rối loạn chuyển hóa phức tạp, có đặc điểm tăng glucose huyết do khiếm khuyết về tiết insulin, về tác động của insulin hoặc cả hai. Tăng glucose mạn tính trong thời gian dài gây nên những rối loạn chuyển hóa carbohydrat, protid, lipid, gây tổn thương ở nhiều cơ quan khác nhau, đặc biệt ở tim và mạch máu, thận, mắt, thần kinh.
Theo Liên đoàn ĐTĐ Thế giới (International Diabetes Federation – IDF), năm 2017 toàn thế giới có 425 triệu người bị bệnh ĐTĐ và con số này tiếp tục gia tăng, ước tính đến năm 2045 sẽ có 629 triệu người bị ĐTĐ. Bên cạnh đó, cùng với việc tăng sử dụng thực phẩm không thích hợp, ít hoặc không hoạt động thể lực ở người trẻ, bệnh ĐTĐ típ 2 đang có xu hướng tăng ở cả người trẻ, trở thành vấn đề sức khỏe cộng đồng nghiêm trọng. Bệnh ĐTĐ gây nên nhiều biến chứng nguy hiểm, là nguyên nhân hàng đầu gây bệnh tim mạch, mù lòa, suy thận và cắt cụt chi. Tuy nhiên, có đến 70% trường hợp ĐTĐ típ 2 có thể dự phòng hoặc làm chậm xuất hiện bệnh bằng cách tuân thủ lối sống lành mạnh, dinh dưỡng hợp lý và tăng cường luyện tập thể lực.
Ở Việt Nam, theo thống kê năm 1990, tỷ lệ bệnh ĐTĐ là 1,1% (Hà Nội), 2,25% (thành phố Hồ Chí Minh), 0,96% (Huế). Điều tra toàn quốc năm 2012 của Bệnh viện Nội tiết trung ương trên đối tượng 30 – 69 tuổi cho thấy tỷ lệ ĐTĐ toàn quốc là 5,4%, tỷ lệ rối loạn dung nạp glucose là 13,7% và tỷ lệ người mắc bệnh chưa được chẩn đoán tại cộng đồng là 63,6%.
1.1.1 Chẩn đoán
Chẩn đoán ĐTĐ
Tiêu chuẩn chẩn đoán ĐTĐ (theo Quyết định 3319/QĐ-BYT Ban hành ngày 19/7/2017 về việc ban hành tài liệu chuyên môn “Hướng dẫn chẩn đoán và điều trị ĐTĐ típ 2) dựa vào một trong bốn tiêu chí sau đây:
a) Glucose huyết tương lúc đói (fasting plasma glucose – FPG) > 126 mg/dL (hay 7 mmol/L). Người bệnh phải nhịn ăn (không uống nước ngọt, có thể uống nước lọc, nước đun sôi để nguội) ít nhất 8 giờ (thường phải nhịn đói qua đêm từ 8 – 14 giờ), hoặc:
b) Glucose huyết tương ở thời điểm sau 2 giờ làm nghiệm pháp dung nạp glucose đường uống 75 g (oral glucose tolerance test – OGTT) > 200 mg/dL (hay 11,1 mmol/L).
Nghiệm pháp dung nạp glucose đường uống phải được thực hiện theo hướng dẫn của Tổ chức Y tế Thế giới (World Health Organization – WHO): Người bệnh nhịn đói từ nửa đêm trước khi làm nghiệm pháp, dùng một lượng glucose tương đương với 75 g glucose, hòa tan trong 250 – 300 mL nước, uống trong 5 phút; trong 3 ngày trước đó người bệnh ăn khẩu phần có khoảng 150 – 200 g carbohydrat mỗi ngày.
c) HbA1c > 6,5% (48 mmol/mol). Xét nghiệm này phải được thực hiện ở phòng thí nghiệm được chuẩn hóa theo tiêu chuẩn quốc tế.
d) Ở người bệnh có triệu chứng kinh điển của tăng glucose huyết hoặc mức glucose huyết tương ở thời điểm bất kỳ > 200 mg/dL (hay 11,1 mmol/L).
Nếu không có triệu chứng kinh điển của tăng glucose huyết (bao gồm: tiểu nhiều, uống nhiều, ăn nhiều, sụt cân không rõ nguyên nhân), xét nghiệm chẩn đoán a, b, d ở trên cần được thực hiện lặp lại lần hai để xác định chẩn đoán. Thời gian thực hiện xét nghiệm lần hai sau lần thứ nhất có thể từ 1 đến 7 ngày.
Chẩn đoán tiền ĐTĐ
Chẩn đoán tiền ĐTĐ khi có một trong các rối loạn sau đây:
- Rối loạn glucose huyết đói (impaired fasting glucose – IFG): Glucose huyết tương lúc đói từ 100 (5,6mmol/L) đến 125 mg/dL (6,9 mmol/L), hoặc:
- Rối loạn dung nạp glucose (Impaired glucose tolerance – IGT): Glucose huyết tương ở thời điểm 2 giờ sau khi làm nghiệm pháp dung nạp glucose bằng đường uống 75 g từ 140 (7,8 mmol/L) đến 199 mg/dL (11 mmol/L), hoặc:
- HbA1c từ 5,7% (39 mmol/mol) đến 6,4% (47 mmol/mol).
Phân loại ĐTĐ
a) ĐTĐ típ 1 (do phá hủy tế bào beta tụy, dẫn đến thiếu insulin tuyệt đối).
b) ĐTĐ típ 2 (do giảm chức năng của tế bào beta tụy tiến triển trên nền tảng đề kháng insulin).
c) ĐTĐ thai kỳ (là ĐTĐ được chẩn đoán trong 3 tháng giữa hoặc 3 tháng cuối của thai kỳ và không có bằng chứng về ĐTĐ típ 1, típ 2 trước đó).
d) Thể bệnh chuyên biệt của ĐTĐ do các nguyên nhân khác, như ĐTĐ sơ sinh hoặc ĐTĐ do sử dụng thuốc và hóa chất như sử dụng glucocorticoid, điều trị HIV/AIDS hoặc sau cấy ghép mô, ĐTĐ người trẻ xuất hiện ở độ tuổi trưởng thành.
Tiêu chuẩn để làm xét nghiệm chẩn đoán ĐTĐ hoặc tiền ĐTĐ ở người không có triệu chứng ĐTĐ:
Người lớn có BMI > 23 kg/m2 hoặc cân nặng lớn hơn 120% cân nặng lý tưởng và có một hoặc nhiều hơn một trong các yếu tố nguy cơ sau:
- Ít vận động thể lực
- Gia đình có người bị ĐTĐ ở thế hệ cận kề (bố, mẹ, anh chị em ruột)
- Tăng HA (HATT > 140 mmHg và/hoặc HATTr > 90 mmHg hay đang điều trị thuốc hạ HA)
- Nồng độ HDL cholesterol < 35 mg/dL (0,9 mmol/L) và/hoặc nồng độ triglycerid > 250 mg/dL (2,82 mmol/L)
- Vòng bụng to: ở nam > 90 cm, ở nữ > 80 cm
- Phụ nữ bị buồng trứng đa nang
- Phụ nữ đã mắc ĐTĐ thai kỳ
- HbA1c > 5,7% (39 mmol/mol), rối loạn glucose huyết đói hay rối loạn dung nạp glucose ở lần xét nghiệm trước đó.
- Có các dấu hiệu đề kháng insulin trên lâm sàng (như: béo phì, dấu gai đen…).
- Tiền sử có bệnh tim mạch do xơ vữa (BTMXV) động mạch.
b) Ở người bệnh không có các dấu hiệu/triệu chứng trên, bắt đầu thực hiện xét nghiệm phát hiện sớm ĐTĐ ở người > 45 tuổi.
c) Nếu kết quả xét nghiệm bình thường, nên lặp lại xét nghiệm sau mỗi 1 – 3 năm. Có thể thực hiện xét nghiệm sớm hơn tùy thuộc vào kết quả xét nghiệm trước đó và yếu tố nguy cơ. Đối với người tiền ĐTĐ: thực hiện xét nghiệm hàng năm.
1.1.2 Điều trị
Mục tiêu điều trị cần đạt*
Bảng 2.1. Mục tiêu cho người bệnh ĐTĐ ở người trưởng thành, không có thai
| Mục tiêu | Chỉ số |
| HbA1c | < 7%* |
| Glucose huyết tương mao mạch lúc đói, trước ăn | 80 – 130 mg/dL (4,4 – 7,2 mmol/L)* |
| Đỉnh glucose huyết tương mao mạch sau ăn 1 – 2 giờ | < 180 mg/dL (10,0 mmol/L)* |
| Huyết áp | Có thể tham khảo các hướng dẫn sau đây:
• Hướng dẫn của BYT (2017): – Huyết áp tâm thu (HATT) < 140 mmHg, huyết áp tâm trương (HATTr) < 90 mmHg (hay HA < 140/90mmHg) – Nếu đã có biến chứng thận: HATT < 130 mmHg, HATTr < 85 – 80 mmHg (hay HA < 130/85 – 80mmHg) • Hướng dẫn của ADA (2019): – Người bệnh ĐTĐ, tăng HA với nguy cơ bệnh tim mạch cao (có BTMXV, hoặc có nguy cơ BTMXV năm > 5%): HA < 130/80 mmHg. – Người bệnh ĐTĐ, tăng HA với nguy cơ bệnh tim mạch thấp (nguy cơ BTMXV năm < 5%): HA < 140/90 mmHg (Đánh giá nguy cơ BTMXV có thể sử dụng công cụ ước tính của Hội Tim mạch Hoa Kỳ http://tools.acc.org/ASCVD-Risk-Estimator-Plus/) |
| Lipid huyết
|
Có thể tham khảo các hướng dẫn sau đây:
• Hướng dẫn của BYT (2017): – LDL cholesterol < 100 mg/dL ( 2,6 mmol L), nếu chưa có biến chứng tim mạch, LDL cholesterol < 70 mg/dL ( 1,8 mmol L) nếu đã có bệnh tim mạch – HDL cholesterol > 40 mg/dL ( 1,0 mmol/L) ở nam và > 50 mg/dL ( 1,3 mmol/L) ở nữ – Triglycerid < 150 mg/dL (1,7 mmol/L) • Hướng dẫn của ADA (2019): không có mục tiêu lipid huyết. Việc lựa chọn thuốc và liều thuốc dựa trên BTMXV, nguy cơ BTMXV năm, yếu tố nguy cơ BTMXV, tuổi, LDL-c ban đầu, khả năng dung nạp thuốc. |
* Mục tiêu điều trị ở người bệnh ĐTĐ có thể khác nhau, cần thiết phải cá thể hóa, phụ thuộc tình trạng sức khỏe, tuổi, biến chứng của bệnh, thời gian mắc bệnh …
- Mục tiêu điều trị có thể nghiêm ngặt hơn: HbA1c < 6,5% (48 mmol/mol) nếu có thể đạt được và không có dấu hiệu đáng kể của hạ đường huyết và những tác dụng không mong muốn của thuốc: Đối với người bị bệnh ĐTĐ trong thời gian ngắn, bệnh ĐTĐ típ 2 được điều trị bằng thay đổi lối sống hoặc chỉ dùng metformin, trẻ tuổi hoặc không có bệnh tim mạch quan trọng.
- Ngược lại, mục tiêu điều trị có thể ít nghiêm ngặt: HbA1c < 8% (64 mmol/mol) phù hợp với những người bệnh có tiền sử hạ đường huyết trầm trọng, lớn tuổi, có các biến chứng mạch máu nhỏ hoặc mạch máu lớn, có nhiều bệnh lý đi kèm hoặc bệnh ĐTĐ trong thời gian dài và khó đạt mục tiêu điều trị.
- Nếu đã đạt mục tiêu glucose huyết lúc đói nhưng HbA1c còn cao, cần xem lại mục tiêu glucose huyết sau ăn, đo vào lúc 1 – 2 giờ sau khi người bệnh bắt đầu ăn.
* Đánh giá về kiểm soát glucose huyết:
- Thực hiện xét nghiệm HbA1c ít nhất 2 lần trong 1 năm ở những người bệnh đáp ứng mục tiêu điều trị (và những người có glucose huyết được kiểm soát ổn định).
- Thực hiện xét nghiệm HbA1c hàng quý ở những người bệnh được thay đổi liệu pháp điều trị hoặc những người không đáp ứng mục tiêu về glucose huyết.
- Thực hiện xét nghiệm HbA1c tại thời điểm người bệnh đến khám, chữa bệnh để tạo cơ hội cho việc thay đổi điều trị kịp thời hơn.
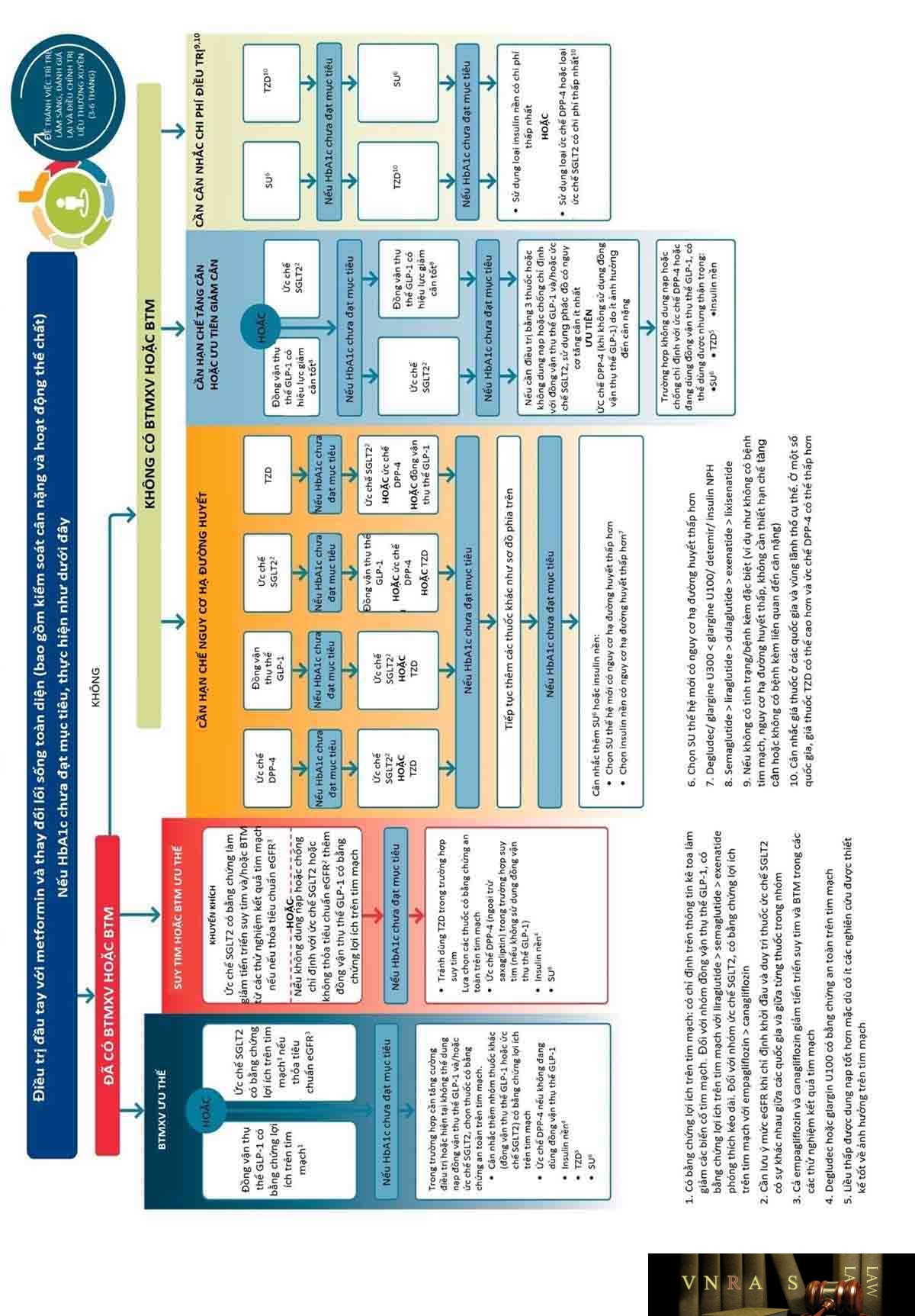
Điều trị cụ thể
(Tham khảo thêm Hướng dẫn chẩn đoán và điều trị bệnh đái tháo đường típ 2 của Bộ Y tế và của Hiệp hội Đái tháo đường Hoa Kỳ ADA 2019)
a) Thay đổi lối sống
- Điều trị nền tảng của bệnh ĐTĐ là thay đổi lối sống.
- Chế độ dinh dưỡng cần được cá thể hóa, phụ thuộc tình trạng bệnh, tuổi, thói quen ăn uống, phong tục tập quán và điều kiện kinh tế. Cần thiết có sự tư vấn của bác sĩ chuyên khoa dinh dưỡng.
- Chi tiết về dinh dưỡng sẽ được thiết lập cho từng người bệnh tùy tình trạng bệnh, loại hình hoạt động, các bệnh lý, biến chứng đi kèm.
- Loại hình luyện tập thông dụng và dễ áp dụng nhất: đi bộ tổng cộng 150 phút mỗi tuần (hoặc 30 phút mỗi ngày), không nên ngưng luyện tập 2 ngày liên tiếp. Mỗi tuần nên tập kháng lực 2 – 3 lần (kéo dây, nâng tạ). Mức độ và thời gian luyện tập thể lực thay đổi tùy theo tuổi, mức độ bệnh và các bệnh lý đi kèm.
- Nên theo chế độ ăn nhạt (theo khuyến cáo của WHO)
- Hạn chế bia, rượu.
- Ngưng hút thuốc lá.
b) Điều trị ĐTĐ bằng thuốc
- Metformin vẫn là lựa chọn hàng đầu trong điều trị ĐTĐ típ 2 trừ khi có chống chỉ định hoặc không dung nạp thuốc (dùng metformin đơn trị khi mới chẩn đoán ĐTĐ típ 2 nếu không có triệu chứng lâm sàng của tăng glucose huyết, mức glucose huyết không quá cao với HbA1c cao trên mức mục tiêu không quá 1,5%).
- Lựa chọn thuốc hàng thứ 2 kết hợp vào metformin sau khi metformin đơn trị không đạt mục tiêu HbA1c sau 3 tháng phụ thuộc vào các bệnh lý đi kèm:
+ BTMXV: BMV, bệnh mạch máu não, bệnh động mạch ngoại biên
+ Suy tim
+ Bệnh thận mạn (BTM)
- Đối với người bệnh ĐTĐ típ 2 có BTMXV, khuyến cáo ưu tiên sử dụng các thuốc ức chế SGLT-2 và đồng vận thụ thể GLP-1 có bằng chứng bảo vệ tim mạch (empagliflozin, canagliflozin, dapagliflozin, liraglutid, semaglutid).
- Đối với người bệnh ĐTĐ típ 2 có BTMVX và kèm theo suy tim, khuyến cáo nên ưu tiên sử dụng thuốc ức chế SGLT-2.
- Đối với người bệnh ĐTĐ típ 2 kèm BTM (có hoặc không có BTMXV kèm theo), cân nhắc sử dụng thuốc ức chế SGLT-2 có bằng chứng bảo vệ thận (empagliflozin, canagliflozin). Trong trường hợp chống chỉ định của thuốc ức chế SGLT-2, có thể sử dụng đồng vận thụ thể GLP-1 có tác dụng bảo vệ thận.
- Trong trường hợp người bệnh ĐTĐ típ 2 không có BTMXV hoặc BTM kèm theo, cân nhắc lựa chọn các nhóm thuốc sau metformin sẽ dựa trên các mục tiêu cụ thể cần đạt được: cân nặng, nguy cơ hạ đường huyết, chi phí điều trị.
+ Nhóm thuốc ức chế SGLT-2 và nhóm thuốc đồng vận thụ thể GLP-1 được khuyến cáo sử dụng trên những người bệnh ĐTĐ típ 2 cần giảm cân. Nhóm thuốc ức chế DPP-4 có thể sử dụng trong trường hợp cần hạn chế tăng cân.
+ Trong trường hợp cần hạn chế tối đa nguy cơ hạ đường huyết thì ưu tiên sử dụng các nhóm thuốc: ức chế DPP-4, đồng vận thụ thể GLP-1, ức chế SGLT-2 hoặc thiazolidinedion (TZD).
+ Các nhóm thuốc SU (ưu tiên sử dụng SU thế hệ mới với nguy cơ hạ đường huyết thấp hơn) hoặc TZD được ưu tiên lựa chọn khi cần tiết kiệm chi phí điều trị.
- Phối hợp thuốc từng bước được ưu tiên lựa chọn khi kiểm soát glucose huyết.
- Tuy nhiên, nếu khi chẩn đoán ĐTĐ típ 2 mà người bệnh có HbA1c > 1,5% so với mục tiêu điều trị: cần cân nhắc phối hợp thuốc sớm vì hầu hết các nhóm thuốc uống đều có hiệu quả giảm HbA1c ít hơn 1,0%.
- Viên phối hợp liều cố định giúp tăng tỷ lệ tuân thủ điều trị, dễ đạt mục tiêu điều trị hơn.
- Khi cần sử dụng thuốc đường tiêm để kiểm soát glucose huyết (HbA1C > 86 mmol/mol (10%) và/hoặc > 23mmol/mol (2%) so với mục tiêu điều trị), ưu tiên chọn lựa đồng vận thụ thể GLP-1 hơn so với insulin. Trong trường hợp không có sẵn đồng vận thụ thể GLP-1 hoặc không có điều kiện dùng đồng vận thụ thể GLP-1, có thể cân nhắc dùng insulin. Cân nhắc sử dụng insulin trước nếu HbA1c > 11% hoặc có triệu chứng của tăng glucose huyết (sụt cân, khát nhiều, tiểu nhiều) hoặc ĐTĐ típ 1.
- Sử dụng insulin khi điều trị bằng các thuốc hạ đường huyết khác mà không đạt mục tiêu điều trị, thường bắt đầu bằng thêm insulin nền.
- Người bệnh không đạt mục tiêu điều trị với insulin nền và thuốc uống, có thể phối hợp thêm đồng vận thụ thể GLP-1, ức chế SGLT2, hoặc các mũi insulin nhanh (insulin bữa ăn) hoặc chuyển sang insulin trộn sẵn 2 hoặc 3 lần/ngày (tuy nhiên cần lưu ý nguy cơ hạ đường huyết và tăng cân).
- Bên cạnh việc kiểm soát glucose huyết đạt mục tiêu, điều trị ĐTĐ cần kiểm soát toàn diện đa yếu tố: kiểm soát HA, lipid máu, cân nặng và các biến chứng cũng như các bệnh lý khác kèm theo.
1.2 Đại cương về thuốc
1.2.1 Các nhóm thuốc điều trị ĐTĐ
Các thuốc điều trị ĐTĐ bao gồm: metformin, nhóm thuốc SU, nhóm thuốc glinid, pioglitazon, nhóm thuốc ức chế enzym alpha glucosidase, nhóm thuốc đồng vận thụ thể GLP-1, nhóm thuốc ức chế DPP-4, nhóm thuốc ức chế kênh đồng vận chuyển natri – glucose (SGLT2), insulin.
Do bản chất đa dạng của cơ chế bệnh sinh ĐTĐ típ 2, việc phối hợp thuốc trong điều trị sẽ mang lại hiệu quả giảm glucose huyết tốt hơn, đồng thời giảm tác dụng phụ khi tăng liều một loại thuốc đến tối đa. Ngoài ra, viên thuốc phối hợp 2 nhóm thuốc sẽ giúp cho số viên thuốc cần sử dụng ít hơn, làm tăng tính tuân thủ dùng thuốc của người bệnh. Bất lợi của viên thuốc phối hợp là không thể chỉnh liều 1 loại thuốc.
Hiện nay, tại Việt Nam có các thuốc viên phối hợp như: glyburid/metformin, glimepirid/metformin, glibenclamid/metformin, sitagliptin/metformin, vildagliptin/metformin, saxagliptin/metformin dạng phóng thích chậm, pioglitazon/ metformin.
Bảng 2.2. Tóm tắt ưu, nhược điểm của các thuốc hạ đường huyết đường uống và thuốc đường tiêm không thuộc nhóm insulin
| Nhóm thuốc | Cơ chế tác dụng | Giảm HbA1c | Ưu điểm | Nhược điểm | Chi phí |
| SU
– Glipizid – Glyburid (glibenclamid) – Gliclazid – Glimepirid |
Kích thích tiết insulin | 1 – 1,5% | Được sử dụng từ lâu
↓ nguy cơ mạch máu nhỏ ↓ nguy cơ tim mạch và tử vong |
Hạ đường huyết (gliclazid ít gây hạ đường huyết hơn so với các SU khác)
↑ cân |
Thấp |
| Glinid
– Repaglinid – Nateglinid |
Kích thích tiết insulin | 1 – 1,5% | ↓ glucose huyết sau ăn
An toàn trên người bệnh có bệnh thận tiến triển với liều dùng thận trọng (đặc biệt với repaglinide) |
Hạ đường huyết (thấp hơn so với nhóm SU)
↑ cân Dùng một đến nhiều lần trong ngày tùy thuộc số lượng các bữa ăn |
Thấp |
| Biguanid
– Metformin |
Giảm sản xuất glucose ở gan
Gia tăng sự nhạy cảm insulin tại cơ Làm chậm hấp thu glucose tại ruột |
1 – 1,5% | Được sử dụng từ lâu
Dùng đơn độc không gây hạ đường huyết Không thay đổi cân nặng, có thể giảm cân ↓ LDL cholesterol, ↓ triglycerid Có thể giảm nguy cơ tim mạch và tử vong Giảm cholesterol toàn phần |
Chống chỉ định ở người bệnh suy thận (chống chỉ định tuyệt đối khi MLCT < 30 mL/phút)
↓ hấp thu vitamin B12 Rối loạn tiêu hóa: buồn nôn, đau bụng, tiêu chảy Nhiễm acid lactic |
Thấp |
| TZD
– Pioglitazon |
Hoạt hóa thụ thể PPARy
Tăng nhạy cảm với insulin |
0,5 – 1,4% | Dùng đơn độc không gây hạ đường huyết
↓ triglycerid, ↑ HDL cholesterol ↓ biến cố BTMXV |
↑ cân
Phù/ ↓ nguy cơ suy tim ↑ nguy cơ gãy xương (ở phụ nữ) ↑ nguy cơ ung thư bàng quang ↑ nguy cơ phù hoàng điểm |
Thấp |
| Ức chế enzym alpha glucosidase
– Acarbose – Miglitol |
Làm chậm hấp thu carbohydrate ở ruột | 0,5 – 0,8% | Dùng đơn độc không gây hạ đường huyết
Tác dụng tại chỗ ↓ glucose huyết sau ăn An toàn trên tim mạch |
Rối loạn tiêu hóa: đầy bụng, đầy hơi, đi ngoài phân lỏng Khả năng ↓ HbA1c thấp Dùng nhiều lần trong ngày | Thấp (miglitol: cao) |
| Ức chế DPP-4
– Sitagliptin – Saxagliptin – Vildagliptin – Linagliptin – Alogliptin |
Ức chế DPP-4
Tăng GLP-1 |
0,5 – 1% | Dùng đơn độc không gây hạ đường huyết
Không làm thay đổi cân nặng Dung nạp tốt |
Có thể gây dị ứng, mẩn ngứa, nổi mề đay, phù, viêm hầu họng, nhiễm trùng hô hấp trên, đau khớp
Nguy cơ viêm tụy cấp Chưa rõ tính an toàn lâu dài Khả năng ↓ HbA1c thấp ↑ nguy cơ nhập viện do suy tim (saxagliptin, alogliptin) |
Cao |
| Ức chế SGLT2
– Dapagliflozin – Empagliflozin – Canagliflozin – Ertugliflozin |
Ức chế tác dụng của kênh đồng vận chuyển SGLT tại ống lượn gần, tăng thải glucose qua đường tiểu | 0,5 – 1% | Dùng đơn độc ít gây hạ đường huyết
↑ cân ↓ huyết áp Lợi ích trên nhóm người bệnh có BTMXV, suy tim, bệnh thận mạn (empagliflozin, canagliflozin) |
Nhiễm nấm đường niệu dục, nhiễm trùng tiết niệu, nhiễm ceton acid
Hiệu quả ↓ HbA1c thấp ↑ LDL cholesterol Mất xương (canagliflozin) ↑ khả năng cắt cụt chi, gãy xương (canaglifozin) |
Cao |
| Đồng vận thụ thể GLP-1 Tác dụng kéo dài
– Liraglutid – Dulaglutid – Exenatid ER – Semaglutid Tác dụng ngắn – Exenatid – Lixisenatid |
Tăng tiết insulin khi glucose tăng cao trong máu, ức chế sự tiết glucagon, làm chậm nhu động dạ dày và giảm cảm giác thèm ăn | 0,6 – 1,5% | ↓ glucose huyết sau ăn, giảm cân
Dùng đơn độc ít gây hạ đường huyết ↓ tử vong liên quan đến bệnh tim mạch ở người bệnh ĐTĐ típ 2 có nguy cơ tim mạch cao (liraglutid > semaglutid > exenatid ER) |
Buồn nôn, nôn, tiêu chảy, có thể gặp viêm tụy cấp nhưng hiếm
Phản ứng tại vị trí tiêm Không dùng khi có tiền sử gia đình ung thư giáp dạng tủy, bệnh đa u tuyến nội tiết loại 2 ↑ nhịp tim |
Cao |
| Chất gắn acid mật
Colesevelam |
↓ sản xuất glucose tại gan | 0,3 – 0,5% | Không làm hạ đường huyết ↓ LDL cholesterol | Táo bón
↑ triglycerid Có thể giảm hấp thu các thuốc khác |
Cao |
| Chất chủ vận
dopamin D2 Bromocriptin |
Chưa rõ: điều hòa hoạt động của vùng dưới đồi làm tăng nhạy cảm insulin, giảm sản xuất glucose. | 0,1 – 0,6% | Không làm hạ đường huyết | Đau đầu, mệt mỏi, buồn nôn, viêm mũi dị ứng | Cao |
↑: tăng, ↓: giảm, ?: dữ liệu còn nhiều tranh cãi
1.2.2. Tác dụng không mong muốn của các thuốc hạ đường huyết đường uống và biện pháp xử trí
Bảng 2.3. Tác dụng không mong muốn của các thuốc hạ đường huyết đường uống và biện pháp
| Nhóm thuốc | ADR | Tần số | Biện pháp xử trí |
| SU
– Glipizid – Glyburid (glibenclamid) – Gliclazid – Glimepirid
|
Hạ đường huyết | Thường gặp | Gliclazid ít gây hạ đường huyết hơn so với các SU khác.
Hướng dẫn người bệnh tuân thủ chế độ ăn uống, không bỏ bữa và cách nhận biết các triệu chứng của hạ đường huyết và cách xử trí hạ đường huyết |
| Rối loạn tiêu hóa: đau bụng, buồn nôn, tiêu chảy | Thường gặp | Uống thuốc cùng bữa ăn hoặc ngay sau miếng ăn đầu tiên | |
| Tăng cân (có thể do làm tăng tiết insulin, như vậy, có thể làm tăng sức thèm ăn) | Chưa rõ tần suất | Chế độ ăn hợp lý. | |
| Glinid
– Repaglinid – Nateglinid |
Hạ đường huyết (5,88 % đến 31 %) | Rất thường gặp | Trên người bệnh suy gan hoặc suy thận nặng, thuốc có thể làm tăng nguy cơ hạ đường huyết, cần phải điều chỉnh liều
Hướng dẫn người bệnh tuân thủ chế độ ăn uống, không bỏ bữa, cách nhận biết các triệu chứng của hạ đường huyết và cách xử trí hạ đường huyết |
| Biguanid
– Metformin
|
Rối loạn tiêu hóa: buồn nôn, đau bụng, tiêu chảy | Thường gặp | Có thể hạn chế bằng cách dùng liều thấp sau đó tăng dần, uống sau bữa ăn hoặc dùng dạng phóng thích chậm |
| Nhiễm acid lactic (mức độ nghiêm trọng) | Rất hiếm | Thận trọng khi dùng metformin ở người bệnh > 80 tuổi, những người bệnh có nguy cơ nhiễm acid lactic như suy thận, nghiện rượu mạn. Ngưng metformin giờ trước khi chụp hình với thuốc cản quang, phẫu thuật, cho người bệnh uống đủ nước hay truyền dịch để phòng ngừa suy thận do thuốc cản quang Ngưng sử dụng metformin 24 giờ trước thời điểm thực hiện chiếu chụp có sử dụng thuốc cản quang có chứa iod ở những người bệnh có MLCT nằm trong khoảng 30 – 60 mL/phút/1,73 m2, những người bệnh có tiền sử suy gan, nghiện rượu, suy tim hoặc những người bệnh sẽ sử dụng thuốc cản quang chứa iod theo đường động mạch Đánh giá lại mức lọc cầu thận 48 giờ sau khi chiếu chụp và sử dụng lại metformin nếu chức năng thận ổn định
Tuân thủ giảm liều và chống chỉ định dựa trên MLCT (xem bảng 2.4) |
|
| TZD
– Pioglitazon
|
Phù | Thường gặp | Thận trọng ở những người bệnh bị phù hoặc có nguy cơ bị suy tim sung huyết, theo dõi trong quá trình sử dụng |
| Gan: Mức ALT/ AST tăng, suy gan | Ít gặp | Cần theo dõi chức năng gan trước khi điều trị và định kỳ sau đó.
Chống chỉ định: bệnh gan đang hoạt động, enzym gan ALT tăng gấp 2,5 giới hạn trên của trị số bình thường . |
|
| Tăng nguy cơ suy tim (mức độ nghiêm trọng) | Thường gặp (< 8%) | Chống chỉ định: suy tim độ III – IV theo Hiệp hội Tim New York (NYHA). | |
| Tăng nguy cơ gãy xương ở phụ nữ | Thường gặp | ||
| Tăng nguy cơ ung thư bàng quang | Hiếm gặp | Sử dụng kéo dài (hơn 12 tháng) và /hoặc các liều tích lũy cao, tăng nguy cơ ung thư bàng quang .
Khi sử dụng thuốc pioglitazon cần phải hỏi kỹ người bệnh về tiền sử ung thư, đặc biệt là ung thư bàng quang, kiểm tra nước tiểu tìm hồng cầu trong nước tiểu, nên dùng liều thấp và không nên dùng thuốc kéo dài. |
|
| Ức chế enzym alpha glucosidase
– Acarbose – Miglitol |
Rối loạn tiêu hóa: sình bụng, đầy hơi, đi ngoài phân lỏng | Rất thường gặp | Uống thuốc ngay trước ăn hoặc ngay sau miếng ăn đầu tiên |
| Ức chế DPP-4
– Sitagliptin – Saxagliptin – Vildagliptin – Linagliptin – Alogliptin
|
Có thể gây dị ứng, ngứa, nổi mề đay, phù | Báo cáo ca < 1% (Dựa trên báo cáo từ các thuốc lưu hành trên thị trường) | Ngưng dùng thuốc, đánh giá người bệnh, có thể xem xét chuyển thuốc khác thay thế |
| Viêm hầu họng, nhiễm khuẩn hô hấp trên | Thường gặp | Theo dõi các triệu chứng cảm lạnh, đau họng, ngạt mũi, chảy mũi | |
| Đau khớp (mức độ nghiêm trọng) | Báo cáo ca < 1% (Dựa trên báo cáo từ các thuốc lưu hành trên thị trường) | Đau khớp dữ dội và kéo dài đã được báo cáo với thuốc ức chế DPP-4 có thể khởi phát từ ngày đến nhiều năm sau khi bắt đầu sử dụng; có thể cần phải ngừng thuốc | |
| Nhiễm khuẩn tiết niệu (saxagliptin) | Thường gặp | Theo dõi các triệu chứng của nhiễm trùng tiết niệu như: có máu trong nước tiểu, cảm giác đau, nóng rát khi tiểu, đi tiểu nhiều lần, sốt, đau vùng dưới dạ dày hoặc vùng châu,… | |
| Viêm gan (vildagliptin) | Hiếm gặp | Xét nghiệm chức năng gan trước khi bắt đầu và định kỳ mỗi 3 tháng trong năm đầu tiên và định kỳ hàng năm sau đó | |
| Viêm tụy cấp (mức độ nghiêm trọng) | Báo cáo ca < 1% (Dựa trên báo cáo từ các thuốc lưu hành trên thị trường) | Hướng dẫn người bệnh nhận biết triệu chứng đặc trưng của viêm tụy cấp: đau bụng dữ dội và liên tục Nếu nghi ngờ viêm tụy, nên ngưng dùng thuốc (viêm tụy được ghi nhận hồi phục sau khi ngưng dùng thuốc) | |
| Ức chế SGLT2
– Dapagliflozin – Empagliflozin – Canagliflozin – Ertuglifozin
|
Nhiễm nấm đường tiết niệu – sinh dục | Thường gặp | Thường xảy ra hơn ở nữ và người bệnh có tiền sử bệnh
Hầu hết mức độ từ nhẹ đến trung bình, người bệnh đáp ứng với điều trị bằng phác đồ điều trị chuẩn và hiếm khi phải ngưng điều trị. |
| Nhiễm khuẩn tiết niệu | Thường gặp | Thường xảy ra hơn ở nữ và người bệnh có tiền sử bệnh
Hầu hết nhiễm khuẩn từ nhẹ đến trung bình, người bệnh đáp ứng với điều trị bằng phác đồ điều trị chuẩn và hiếm khi phải ngưng điều trị. |
|
| Nhiễm toan ceton (mức độ nghiêm trọng) | Báo cáo ca < 1% (Dựa trên báo cáo từ các thuốc lưu hành trên thị trường) | Khi người bệnh có những dấu hiệu buồn nôn, nôn ói, đau bụng, mệt mỏi và thở nhanh, nên được đánh giá về nhiễm toan ceton (ngay cả khi glucose huyết < 14 mmol l) Nếu nghi ngờ nhiễm toan ceton, nên xem xét tạm ngưng sử dụng thuốc và đánh giá người bệnh kịp thời Không sử dụng thuốc này ở ĐTĐ típ và thận trọng nếu nghi ngờ người bệnh ĐTĐ típ 2 thiếu hụt trầm trọng insulin. | |
| Buồn nôn, nôn, tiêu chảy | Thường gặp | Có thể giảm dần và tự hết theo thời gian điều trị, có thể điều chỉnh tăng liều dần | |
| Đồng vận thụ thể GLP-1
Tác dụng kéo dài – Liraglutid – Dulaglutid – Exenatid ER – Semaglutid Tác dụng ngắn – Exenatid – Lixisenatid
|
Viêm tụy cấp | Hiếm gặp | Viêm tụy cấp và mạn tính đã được báo cáo (bao gồm tử vong, không tử vong, viêm tuỵ xuất huyết hoặc hoại tử) Theo dõi các dấu hiệu và triệu chứng của viêm tụy (đau bụng dữ dội kéo dài, có thể lan ra phía sau, có thể kèm theo nôn mửa) Nếu nghi ngờ viêm tuỵ, cần ngừng thuốc Xác định nguyên nhân viêm tuỵ, không sử dụng lại thuốc trừ khi nguyên nhân khác được xác định |
| Ung thư giáp dạng tủy hoặc bệnh đa u tuyến nội tiết loại 2 | Hiếm gặp | Chống chỉ định ở người bệnh có tiền sử bản thân hoặc gia đình ung thư giáp dạng tủy hoặc bệnh đa u tuyến nội tiết loại 2 Tư vấn người bệnh nguy cơ tiềm ẩn ung thư giáp dạng tủy và các triệu chứng khối u tuyến giáp (có khối ở cổ, khó thở, khàn giọng kéo dài) | |
| Táo bón, khó tiêu, buồn nôn | Thường gặp | Không khuyến cáo dùng ở người bệnh liệt dạ dày, rối loạn nhu động tiêu hoá nặng, tiền sử phẫu thuật lớn đường tiêu hóa, nguy cơ tắc ruột | |
| Chất gắn acid mật
Colesevelam |
Buồn ngủ, mệt mỏi, chóng mặt, đau đầu | Rất thường gặp | Tránh làm việc cần sự tập trung như lái xe, vận hành máy móc. Cân nhắc giảm liều hoặc ngừng thuốc nếu xảy ra tác dụng phụ.
Nếu đau đầu dữ dội hoặc thay đổi thị giác (có thể xuất hiện khi bắt đầu dùng thuốc hoặc chậm hơn, thường tuần điều trị thứ 2), người bệnh cần được ngừng thuốc, đánh giá ngay lập tức HA, tính chất đau đầu, độc tính thần kinh trung ương. |
| Chất chủ vận dopamin D2
Bromocriptin
|
Buồn nôn | Rất thường gặp | Theo dõi người bệnh |
| Hạ HA, ngất | Thường gặp | Lưu ý theo dõi khi bắt đầu điều trị hoặc tăng liều |
Ghi chú: Tần số được định nghĩa như sau:
Rất thường gặp ≥ 1/10; thường gặp ≥ 1/100, < 1/10; ít gặp ≥ 1/1.000, < 1/100; hiếm ≥ 1/10.000, < 1/1.000; rất hiếm < 1/10.000.
1.2.3. Liều dùng và hướng dẫn hiệu chỉnh liều trên người bệnh suy thận của các thuốc hạ đường huyết đường uống và thuốc đường tiêm không thuộc nhóm insulin
Bảng 2.4. Tóm tắt liều dùng và hướng dẫn hiệu chỉnh liều trên người bệnh suy thận của các thuốc hạ đường huyết đường uống và thuốc đường tiêm không thuộc nhóm insulin
| Thuốc | Hàm lượng | Liều mỗi ngày trên người bệnh có chức năng thận bình thường | Thời gian tác dụng | Hiệu chỉnh liều trên người bệnh suy giảm chức năng thận |
| SU | ||||
| Glipizid | 5 – 10 mg
2,5 – 5 – 10 mg dạng phóng thích chậm |
Viên thường: liều từ 2,5 – 40 mg/ngày, uống 30 phút trước khi ăn . Liều uống tối đa mỗi ngày 1 lần được khuyến cáo là 15 mg. Khi liều hàng ngày vượt quá 15 – 20 mg, phải chia làm nhiều liều trước các bữa ăn có đủ calo.
Dạng phóng thích chậm 2,5 – 10 mg/ngày uống 1 lần . Liều tối đa 20 mg/ngày uống 1 lần |
6 – 12 giờ Dạng phóng thích chậm: 24 giờ | Người bệnh suy thận: Khởi đầu với liều 2,5 mg/ngày |
| Glibenclamid | 1,25 mg, 1,5 mg, 2,5 mg, 3mg, 5 mg, 6 mg (dạng vi hạt) |
Viên thông thường: khởi đầu 2,5 đến 5 mg/ngày. Nếu người bệnh có nguy cơ hạ đường huyết do thuốc, khởi đầu với liều 1,25 mg/ngày. Điều chỉnh liều: không tăng hơn 2,5 mg/ngày mỗi tuần . Liều duy trì: 1,25 đến 20 mg/ngày Viên dạng vi hạt: khởi đầu 1,5 đến 3mg/ngày . Nếu người bệnh có nguy cơ hạ đường huyết do thuốc, khởi đầu với liều 0,75 mg/ngày. Điều chỉnh liều: không tăng hơn 2,5 mg/ngày mỗi tuần. Liều duy trì: 0,75 đến 12 mg/ngày | < 24 giờ | Không cần điều chỉnh liều (theo nhà sản xuất), tuy nhiên glibenclamid không khuyến cáo dùng trên người bệnh suy thận mạn, nếu dùng SU nên lựa chọn thuốc khác. |
| Gliclazid | 80 mg
30 – 60 mg dạng phóng thích chậm |
Viên thường: 40 mg – 320 mg/ngày, chia uống 2 – 3 lần
Dạng phóng thích chậm: 30 – 120 mg, uống 1 lần/ngày |
12 giờ
24 giờ, dạng phóng thích chậm |
Người bệnh suy thận mức độ nhẹ – vừa: không cần hiệu chỉnh liều
Thuốc không được khuyến cáo ở người bệnh suy thận nặng |
| Glimepirid | 1,2 và 4 mg | Liều thông thường: 1 – 4 mg/ngày Liều tối đa: 8 mg/ngày | 24 giờ | Người bệnh suy thận: khởi đầu với liều 1 mg/ngày |
| Glinid | ||||
| Repaglinid | 0,5 – 1 – 2 mg | Người bệnh ĐTĐ típ 2 chưa từng dùng thuốc hoặc HbA1c dưới 8 %, nên khởi đầu với liều 0,5 mg/lần, 3 lần/ngày trước mỗi bữa ăn.
Người bệnh đã được điều trị bằng thuốc hạ đường huyết và có HbA1c lớn hơn hoặc bằng 8 %, thì liều khởi đầu là 1 mg hoặc 2 mg/lần, 3 lần/ngày trước mỗi bữa ăn . Điều chỉnh liều: Xác định mức liều điều chỉnh dựa trên cơ sở đáp ứng đường huyết khi dùng thuốc, thông thường cần xác định đường huyết lúc đói . Tăng liều lên gấp đôi đến mức liều tối đa là 4 mg/lần đến khi đạt được mục đích kiểm soát đường huyết . ít nhất sau 1 tuần điều chỉnh liều cần kiểm tra đáp ứng của bệnh nhân. Khoảng liều điều trị: 0,5 – 4 mg/lần. Repaglinide có thể được dùng 2, 3 hoặc 4 lần/ngày trước mỗi bữa ăn phụ thuộc vào đáp ứng và thay đổi phù hợp với chế độ ăn của bệnh nhân. Tổng liều trong ngày không quá 16 mg. |
3 giờ | MLCT từ 40 – 80 ml/phút (suy thận nhẹ đến trung bình): không cần phải điều chỉnh liều khởi đầu.
ClCr từ 20 – 40 ml/phút (suy thận nặng): liều khởi đầu 0,5 mg/lần trước bữa ăn, thận trọng khi điều chỉnh liều. MLCT < 20 ml/phút và chạy thận nhân tạo: chưa có nghiên cứu. |
| Nateglinid | 60 mg, 120 mg | 120 mg x 3 lần/ngày . Nếu người bệnh có HbA1c gần mục tiêu điều trị có thể bắt đầu với liều 60 mg x 3 lần/ngày | 4 giờ | Không cần hiệu chỉnh liều ở bệnh nhân suy thận nhẹ đến trung bình
MLCT < 30 mL/phút/1,73m2: khởi đầu với liều 60mg x 3 lần/ngày. Lưu ý nguy cơ tích luỹ chất chuyển hoá, có thể gây hạ đường huyết. |
| Biguanid | ||||
| Metformin | 500 – 850 – 1000 mg
Dạng phóng thích chậm: 500 – 750 mg – 1000 mg |
1 – 2,5 gam, uống 1 viên sau ăn, ngày 2 – 3 lần Liều tối đa 3 g/ngày, chia 3 lần
– Dạng phóng thích chậm: 500 – 2000 mg/ngày uống 1 lần. Liều tối đa 2 g/ngày, có thể chia 2 lần |
Dạng phóng thích chậm: kéo dài 24 giờ | MLCT < 30 mL/phút/1,73m2: chống chỉ định
MLcT 30 – 45 mL/phút /1,73m2: không khuyến cáo khởi đầu điều trị MLCT giảm xuống <45mL/phút/1,73m2 sau khi bắt đầu điều trị: đánh giá lợi ích và nguy cơ của việc tiếp tục điều trị MLCT giảm xuống < 30 mL/phút/1,73 m2 sau khi bắt đầu điều trị: ngừng điều trị MLCT: 45 – 59 mL/phút/1,73m2: Metformin có thể sử dụng nhưng chỉ trong trường hợp không có các yếu tố khác có thể làm tăng nguy cơ nhiễm toan lactic . Điều chỉnh liều như sau: khởi đầu 500 mg ngày 1 lần, tối đa 1000 mg/ngày, chia 2 lần |
| TZD | ||||
| Pioglitazon | 15 – 30 – 45mg/ngày | 15 – 45 mg/ngày | 24 giờ | Suy thận: không cần chỉnh liều |
| Ức chế enzym alpha glucosidase | ||||
| Acarbose | 50 – 100 mg | 25 – 1 00 mg/lần, uống 3 lần/ngày ngay trước bữa ăn hoặc ngay sau miếng ăn đầu tiên
Tối đa 50 mg/lần x 3 lần/ngày với người bệnh < 60 kg Tối đa 100 mg/lần x 3 lần/ngày với người bệnh > 60 kg |
4 giờ | MLCT < 30 mL/phút/1,73m2: không nên sử dụng |
| Miglitol | 25 mg, 50 mg, 100 mg | Khởi đầu: 25 mg x 3 lần/ngày, có thể tăng dần liều 2 5 mg/ngày đến 25 mg x3lần/ngày để giảm tác dụng phụ trên tiêu hóa Sau 4 – 8 tuần: tăng liều đến 50 mg x3lần/ngày, tiếp tục đến 3 tháng, nếu chưa đạt mục tiêu HbA1c, tăng đến liều tối đa 100 mg x3 lần/ngày.
Dựa theo dung nạp, nên duy trì liều thấp nhất có hiệu quả |
T1/2: 2giờ | ClCr > 25 mL/phút: không cần chỉnh liều
ClCr < 25 mL/phút: không nên sử dụng |
| Ức chế DPP-4 | ||||
| Sitagliptin | 50 – 100 mg | Liều thường dùng 100 mg/ngày | 2 4 giờ | ClCr 30 – 50mL/1 phút: 50 mg/ngày ClCr < 30mL/L phút: 25 mg/ngày
ESRD cần lọc máu hoặc thẩm phân phúc mạc: 25 mg, 1 lần/ngày không phụ thuộc vào thời gian lọc máu |
| Saxagliptin | 2,5 – 5 mg | 2,5 – 5 mg/ngày, uống 1 lần
Giảm liều đến 2,5 mg/ngày khi dùng cùng thuốc ức chế CYP3A4 mạnh, ví dụ ketoconazol |
24 giờ | Giảm liều đến 2,5 mg/ngày khi
ClCr < 50mL/1phút ESRD cần lọc máu: 2,5 mg/ngày, uống sau lọc máu. Thẩm phân phúc mạc không cần chỉnh liều |
| Vildagliptin | 50 mg | 50 mg/lần uống 1 – 2 lần/ngày. Chống chỉ định khi AsT/ALT tăng gấp 2,5 giới hạn trên của bình thường | 24 giờ | ClCr > 50mL/phút: không cần chỉnh liều
ClCr < 50mL/phút hoặc ESRD: 50 mg/ngày, uống 1 lần |
| Linagliptin
Alogliptin |
5 mg
6,25 mg, 12,5 mg, 25 mg |
5 mg uống 1 lần /ngày
25 mg 1 lần /ngày |
24 giờ
T1/2: 21giờ |
Không cần chỉnh liều khi độ lọc cầu thận > 15mL/phút
ClCr > 60 mL/phút: Không cần chỉnh liều ClCr > 30 – < 60 mL/phút: 12,5 mg 1 lần/ngày ClCr > 15 – < 30 mL/phút: 6,25 mg 1 lần/ngày ESrD (ClCr < 15 mL/phút hoặc lọc máu): 6,25 mg 1 lần/ngày; thời điểm dùng thuốc không phụ thuộc thời điểm lọc máu Thẩm phân phúc mạc: Không cần chỉnh liều |
| Đồng vận thụ thể GLP-1 | ||||
| Liraglutid | 0,6 mg | 0,6 mg – 1,2 mg/ngày, tiêm 1 lần/ngày tối đa 1,8 mg/ngày | 24 giờ | Thận trọng khi độ lọc cầu thận < 30 mL/phút |
| Dulaglutid | 0,75 mg/0,5 mL (0,5 mL); 1,5 mg/0,5 mL (0,5 mL) (có chứa polysorbat 80) | Tiêm dưới da: khởi đầu: 0,75 mg 1 lần/tuần, có thể tăng đến 1,5 mg/tuần. Liều tối đa 1,5 mg/tuần. | T1/2: 5 ngày | Không cần điều chỉnh, sử dụng thận trọng khi khởi đầu điều trị hoặc tăng liều |
| Exenatid | – Dạng phóng thích ngay: 5mcg/0,02 mL (1,2 mL), 10mcg/0,04mL (2,4 mL)
– Dạng phóng thích kéo dài (ER): 2 mg/0,85 mL (0,85 mL) |
– Dạng phóng thích tức thời: Ban đầu: 5 mcg 2 lần/ngày trong vòng 60 phút trước bữa ăn sáng và tối (hoặc trước hai bữa ăn chính trong ngày, cách nhau > 6 giờ); sau 1 tháng có thể tăng lên 10 mcg 2 lần/ ngày (dựa theo đáp ứng).
– Dạng phóng thích kéo dài: 2mg 1 lần/tuần vào bất kỳ thời điểm nào trong ngày Chuyển đổi từ dạng phóng thích tức thời sang dạng ER: Bắt đầu sử dụng exenatide ER hàng tuần vào ngày sau khi ngừng dạng phóng thích tức thời exenatide . Lưu ý: Có thể glucose huyết tăng trong ~ 2 đến 4 tuần sau khi chuyển đổi. Không cần thiết điều trị trước với exenatide phóng thích ngay lúc bắt đầu exenatide ER. |
Dạng phóng thích ngay:
T1/2: 2,4 giờ Dạng ER: T1/2 2 tuần |
ClCr > 50mL/phút: không cần điều chỉnh
ClCr: 30 – 50mL/phút: không cần điều chỉnh, sử dụng thận trọng đặc biệt khi khởi đầu và tăng liều ClCr < 30 mL/phút, ESRD: không khuyến cáo sử dụng |
| Semaglutid | 0,25 mg, 0,5 mg, 1 g/liều (2 mg/1,5 mL) | Tiêm dưới da: liều khởi đầu 0,25 mg 1 lần/tuần trong 4 tuần, sau đó tăng đến 0,5 mg 1 lần/tuần trong ít nhất 4 tuần, nếu chưa đạt mục tiêu có thể tăng đến liều tối đa 1 mg 1 lần/tuần
Lưu ý: 0,25 mg không hiệu quả trong kiểm soát glucose huyết, có thể dùng khởi đầu. Nếu thay đổi ngày dùng thuốc, cách ít nhất 48 giờ giữa 2 liều |
T1/2: 1 tuần | Không cần chỉnh liều |
| Lixisenatid | 10 – 20 mcg/0,02 mL (3 mL) | Tiêm dưới da: liều ban đầu 10mcg 1 lần/ngày trong 14 ngày, sau đó từ ngày 15 tăng đến 20 mcg 1 lần/ngày. Liều duy trì 20 mcg 1 lần/ngày. | T1/2: 3 giờ | Không cần hiệu chỉnh liều ở bệnh nhân suy thận nhẹ đến trung bình
MLCT< 15 mL/phút/1,73m2: không khuyến cáo |
| Ức chế SGLT2 | ||||
| Dapagliflozin | 5 – 10 mg | 10 mg/ngày, uống 1 lần, 5 mg khi có suy gan | 24 giờ | MLCT > 60 mL/phút/1,73m2: không cần chỉnh liều Không nên bắt đầu sử dụng ở người bệnh có eGRF < 60 mL/phút/1,73 m2 và ngừng sử dụng khi MLCT < 45 mL/phút/1,73 m2 dai dẳng |
| Empagliflozin | 10 mg, 25 mg | 10 mg/ngày, uống 1 lần. Liều tối đa 25 mg/ngày | T1/2:12,4 giờ | MLCT > 45 mL/phút/1,73m2: không cần chỉnh liều
MLcT 30 – < 45 mL/phút/1,73m2: không nên sử dụng mlcT < 30mL/phút/1,73m2, ESRD hoặc người bệnh lọc máu: chống chỉ định |
| Canagliflozin | 100 mg, 300 mg | Khởi đầu 100 mg 1 lần/ngày, có thể tăng đến 300 mg/ngày | 24 giờ | MLCT > 6 0 mL/phút/1,73m2: không cần chỉnh liều
MLcT 45 – < 60 mL/phút/1,73m2: liều tối đa 100 mg 1 lần/ngày MLcT 30 – < 45 mL/phút/1,73m2: không khuyến cáo MLcT < 30 mL/phút/1,73m2, ESRD, lọc máu: chống chỉ định |
| Ertugliflozin | 5 mg, 15 mg | Khởi trị 5 mg 1 lần/ngày, có thể tăng lên đến tối đa 15 mg 1 lần/ngày | T1/2: 16 giờ | MLcT > 60 mL/phút/1,73m2: không cần chỉnh liều
MLcT 30 – < 60 mL/phút/1,73m2: không khuyến cáo MLcT < 30 mL/phút/1,73m2, ESRD, lọc máu: chống chỉ định |
| Chất gắn acid mật | ||||
| Colesevelam | Gói 3,75 g
Viên nén 625 mg |
Gói: 3,75g 1 lần/ngày (6 viên)
Viên nén: 1,875 g (3 viên) 2 lần/ngày |
Giảm HbA1c: khởi phát tác dụng 4 – 6 tuần | Không cần chỉnh liều, không hấp thu từ đường tiêu hóa |
| Chất chủ vận dopamin 2 | ||||
| Bromocriptin | 0,8 mg, 2,5 mg, 5 mg | Khởi đầu 0,8 mg 1 lần/ngày, tăng mỗi tuần thêm 0,8 mg nếu dung nạp, liều thường dùng 1,6 mg đến 4,8 mg (liều tối đa) | T1/2: Khoảng 5 giờ | Không cần chỉnh liều |
1.2.4. Tương tác thuốc và hướng dẫn xử trí
Thông thường, người bệnh ĐTĐ phải sử dụng nhiều thuốc. Bên cạnh thuốc kiểm soát glucose huyết, người bệnh có thể được điều trị đồng thời các bệnh lý mắc kèm và phòng ngừa biến chứng tim mạch bằng các nhóm thuốc khác bao gồm: thuốc điều trị rối loạn lipid máu, thuốc điều trị tăng HA, thuốc kháng kết tập tiểu cầu, thuốc điều trị rối loạn tâm thần. Các thuốc này có thể ảnh hưởng đến glucose huyết hoặc tương tác với các thuốc kiểm soát glucose huyết mà người bệnh đang được sử dụng. Giảm thiểu các nguy cơ do tương tác thuốc cũng là một mục tiêu quan trọng trong chăm sóc thuốc cho người bệnh ĐTĐ. Đây là lĩnh vực mà người DSLS cần chú trọng.
Trong số các nhóm thuốc điều trị ĐTĐ, nhóm thuốc SU là nhóm có nguy cơ xảy ra nhiều tương tác do có đặc tính liên kết protein cao, là cơ chất của CYP2C9 và p – glycoprotein. Bảng 2.5, 2.6 và 2.7 liệt kê các thuốc ảnh hưởng đến glucose huyết và tương tác thuốc – thuốc thường gặp ở người bệnh ĐTĐ. Tuy nhiên, đây không phải là danh sách đầy đủ; do đó, DSLS luôn phải rà soát lại khi người bệnh được thêm hoặc bớt bất kỳ thuốc nào trong quá trình điều trị.
Các thuốc ảnh hưởng đến glucose huyết
– Các thuốc làm tăng glucose huyết
Bảng 2.5. Các thuốc làm tăng glucose huyết
| Thuốc | Cơ chế và lưu ý |
| Interferon alpha | Giảm nhạy cảm với insulin. |
| Thuốc an thần kinh không điển hình (olanzapin, sulpirid, quetiapin, risperidon) | Gây tăng cân và làm giảm nhạy cảm với insulin dẫn đến tăng glucose huyết. |
| Ức chế calcineurin (cyclosporin, tacrolimus) | Ức chế bài tiết insulin từ tế bào beta tụy. |
| Thuốc lợi tiểu thiazid | Tăng đề kháng insulin và/hoặc giảm bài tiết insulin, thay đổi nồng độ kali huyết. Có thể cần tăng liều thuốc điều trị ĐTĐ và theo dõi glucose huyết khi sử dụng đồng thời. |
| Glucocorticoid | Giảm hoạt tính của insulin. |
| Kháng sinh fluoroquinolon | Cơ chế chưa rõ. |
| Acid nicotinic | Giảm hoạt tính của insulin, tăng đề kháng insulin. |
| Pentamidin | Gây độc với tế bào beta tụy, ban đầu gây giải phóng insulin dự trữ, sau đó theo thời gian, người bệnh tăng thiếu hụt insulin do phá hủy tế bào tụy dẫn đến tăng glucose huyết. Sử dụng thuốc trong vòng vài tuần đến vài tháng có thể gây ra bệnh ĐTĐ . |
| Phenytoin | Giảm bài tiết insulin, đặc biệt với liều cao phenytoin. |
| Ức chế protease | Giảm nhạy cảm và tăng đề kháng insulin. Ngoài ra, ritonavir còn ức chế hoạt tính của chất vận chuyển glucose. |
| Chẹn beta giao cảm | Propranolol, metoprolol và atenolol có thể làm tăng glucose huyết lúc đói do giảm bài tiết insulin từ tế bào beta tụy. Không quan sát thấy với carvedilol, bisoprolol và nebivolol. |
| Cường giao cảm | Tăng phân giải glycogen và tăng tân tạo đường. |
– Các thuốc làm giảm glucose huyết
Bảng 2.6. Các thuốc làm giảm glucose huyết
| Thuốc | Cơ chế và lưu ý |
| Thuốc ƯCMC | Cơ chế giả thuyết: tăng nhạy cảm với insulin do tăng lượng kinin lưu hành trong máu dẫn đến giãn mạch máu ở các cơ và tăng bắt giữ glucose ở mô cơ |
| Kháng sinh fluoroquinolon | Gây hạ đường huyết do làm tăng giải phóng insulin ở tế bào beta tụy. Tác dụng này phụ thuộc liều |
| Salicylat | Tăng bài tiết insulin, tăng nhạy cảm với insulin, có thể đẩy SU ra khỏi liên kết protein huyết tương và ức chế thải trừ ở thận. |
| Cồn | Gây ức chế tổng hợp glucose
Cơ chế chưa rõ hoàn toàn; tuy nhiên, khi xảy ra hạ đường huyết, giảm glycogen dự trữ ở gan sẽ dẫn đến tân tạo đường từ các acid amin, quá trình này bị ức chế khi uống cồn Do đó, làm tăng thêm nguy cơ hạ đường huyết nghiêm trọng (đặc biệt khi dùng cùng nhóm SU) |
Tương tác thuốc – thuốc thường gặp của các nhóm thuốc điều trị ĐTĐ
Bảng 2.7. Tương tác thuốc – thuốc thường gặp của các nhóm thuốc điều trị ĐTĐ
| Thuốc/nhóm thuốc điều trị ĐTĐ | Thuốc tương tác | Mức độ – cơ chế – kiểm soát |
|
Metformin |
Cimetidin | Mức độ: nặng
Cơ chế: Cimetidin ức chế các OCT (organic cation transporter) (đặc biệt OCT2) gây giảm bài tiết metformin ở ống thận, từ đó tăng nồng độ metformin làm tăng nguy cơ hạ đường huyết. Kiểm soát: xem xét đổi sang thuốc kháng tiết acid khác. |
| Thuốc cản quang chứa iod | Mức độ: nặng
Cơ chế: Giảm chức năng thận do dùng thuốc cản quang chứa iod làm tăng nguy cơ độc tính trên thận và toan acid lactic. Kỉểm soát: Tránh dùng metformin trước và trong vòng 48 giờ sau khi dùng thuốc cản quang, kiểm tra chức năng thận trước khi dùng lại metformin. |
|
| Các thuốc SU (glipizid, glyburid, gliclazid, glimepirid)
|
Thuốc ức chế CYP2C9: fluconazol, ức chế thụ thể H2, fluoxetin… | Mức độ: trung bình – nặng, kiểm tra lại từng cặp tương tác.
Cơ chế: SU là cơ chất của CYP2C9. Các thuốc ức chế CYP2C9 mạnh có thể làm tăng nồng độ SU làm tăng nguy cơ hạ đường huyết nghiêm trọng. Kiểm soát: Cần giảm liều SU và theo dõi chặt chẽ glucose huyết khi dùng đồng thời. |
| Thuốc cảm ứng CYP2C9: rifampicin, carbamazepin, ritonavir… | Mức độ: trung bình – nặng, kiểm tra lại từng cặp tương tác.
Cơ chế: Các thuốc cảm ứng CYP2C9 có thể làm giảm nồng độ SU và nguy cơ tăng glucose huyết nghiêm trọng. Kiểm soát: Theo dõi glucose huyết và điều chỉnh liều SU nếu cần |
|
| Chất ức chế P – glycoprotein: verapamil, clarithromycin | Mức độ: trung bình
Cơ chế: Tăng nồng độ SU dẫn đến tăng nguy cơ hạ đường huyết. Kiểm soát: Theo dõi chặt chẽ glucose huyết và điều chỉnh liều SU nếu cần. |
|
| Bosentan | Mức độ: chống chỉ định
Cơ chế: chưa rõ, tăng nồng độ bosentan làm tăng độc tính trên gan. Kiểm soát: Tránh dùng đồng thời |
|
| Nhóm thuốc TZD | Rifampicin | Mức độ: trung bình
Cơ chế: Rifampicin cảm ứng CYP2C8 làm giảm nồng độ rosiglitazone và pioglitazone. Kiểm soát: Cần tăng cường theo dõi glucose huyết. |
| Gemfibrozil, trimethoprim | Mức độ: nặng (gemfibrozil), trung bình (trimethoprim)
Cơ chế: Gemfibrozil ức chế CYP2C8, làm tăng nồng độ rosiglitazon và pioglitazon. Trimethoprim ức chế CYP C làm tăng nồng độ rosiglitazon. Kiểm soát: Nếu phối hợp gemfibrozil: Liều tối đa pioglitazone 15 mg/ngày, cân nhắc giảm liều rosiglitazone. Cần tăng cường theo dõi glucose huyết. Nếu phối hợp trimethoprim: Cần tăng cường theo dõi glucose huyết. |
|
| Nhóm thuốc ức chế DPP-4 (sitagliptin, saxagliptin,
|
Digoxin | Mức độ: trung bình
Cơ chế: Sitagliptin là cơ chất của P – glycoprotein, có thể ảnh hưởng đến sự hấp thu digoxin Tuy nhiên, chưa có dữ liệu rõ ràng về tác động trên lâm sàng. Kiểm soát: theo dõi biểu hiện độc tính digoxin. |
| Các thuốc ức chế CYP3A4 mạnh: ketoconazol, itraconazol, clarithromycin, ritonavir… | Mức độ: nặng
Cơ chế: Saxagliptin là cơ chất của CYP 3A4. Việc sử dụng đồng thời các thuốc ức chế CYP3A4 mạnh có thể làm tăng nồng độ saxagliptin. Kiểm soát: Cần giảm liều saxagliptin còn 2,5 mg/ngày (theo thông tin trên nhãn sản phẩm thuốc tại Hoa Kỳ (US product labeling)). Tuy nhiên, thông tin trên nhãn sản phẩm thuốc tại Canada (Canadian product labeling) lại không khuyến cáo giảm liều saxagliptin. |
|
| Nhóm glinid (repaglinid, nateglinid) | Gemfibrozil, itraconazol, clarithromycin, trimethoprim, cyclosporin | Mức độ: tùy theo cặp tương tác Cơ chế: Ức chế enzym CYP3A4 và CYP C làm tăng nồng độ glinide. Kiểm soát: Tuỳ theo mức độ tương tác
– Gemfibrozil: chống chỉ định – Itraconazol, clarithromycin, trimethoprim, cyclosporin: cần theo dõi chặt chẽ glucose huyết, điều chỉnh liều repaglinid nếu cần. |
| Rifampicin | Mức độ: nặng
Cơ chế: Rifampicin làm giảm nồng độ glinide, chủ yếu do cảm ứng CYP3A4. Kiểm soát: Cân nhắc thay thế thuốc điều trị ĐTĐ Cần theo dõi chặt chẽ glucose huyết nếu dùng đồng thời. |
Ghi chú: Mức độ tương tác thuốc được xác định theo Lexicomp – Interact: tránh kết hợp (avoid combination), nặng (major), trung bình (moderate), nhẹ (minor).
2. HƯỚNG DẪN THỰC HÀNH DƯỢC LÂM SÀNG TRÊN NGƯỜI BỆNH ĐÁI THÁO ĐƯỜNG
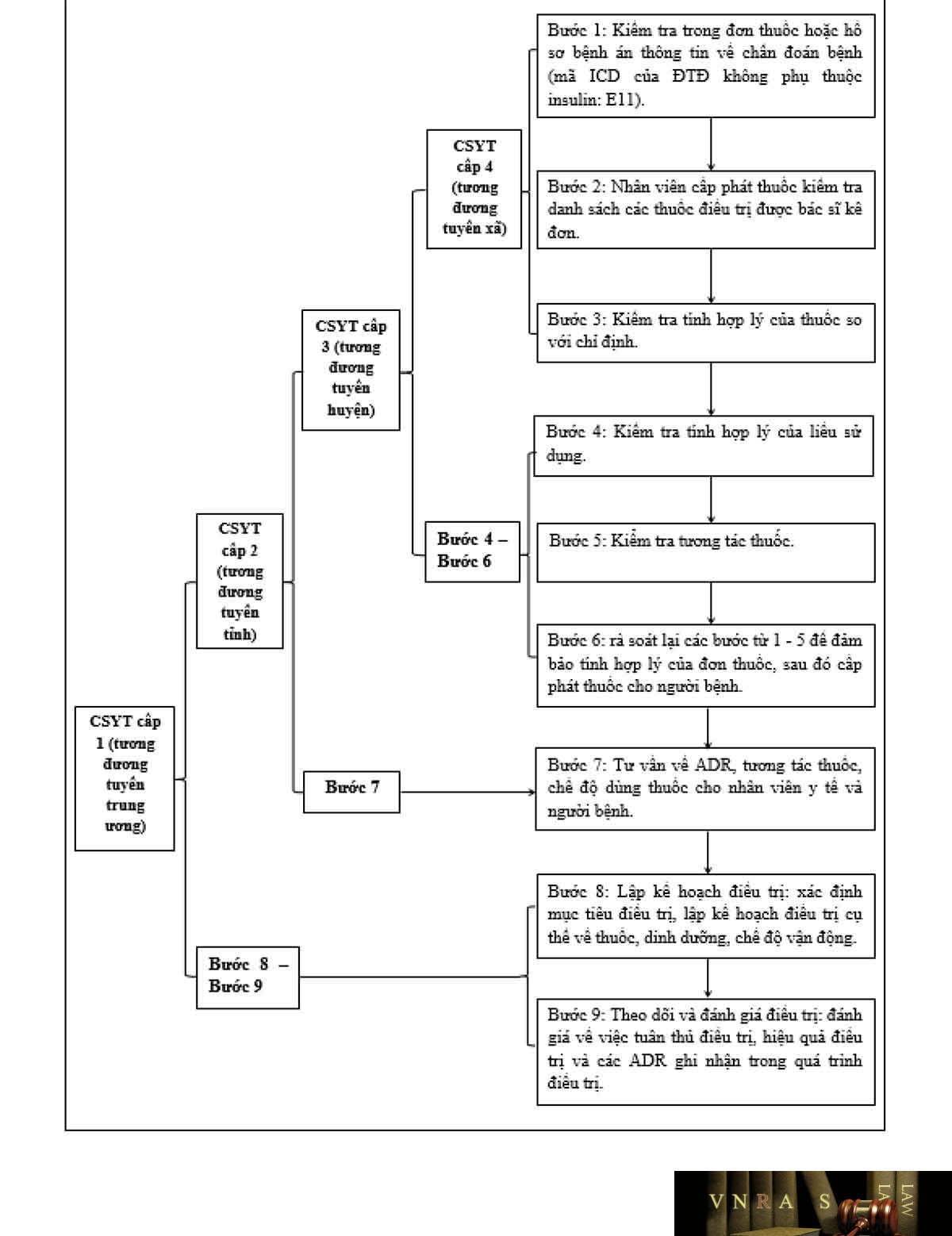
Trong nội dung này, các hoạt động thực hành dược lâm sàng được trình bày theo các bước của quy trình chăm sóc dược đầy đủ trên người bệnh. Tùy theo điều kiện của từng cơ sở y tế tại các tuyến khác nhau, có thể triển khai các hoạt động theo hướng dẫn chung được trình bày trong chương 1.
2.1 Hướng dẫn thực hành tại cơ sở y tế tuyến 4 (tương đương tuyến xã)
Yêu cầu cần đạt được
Cấp phát thuốc phù hợp với chẩn đoán.
Phạm vi thực hiện
Khuyến khích thực hiện, không quy định cụ thể về mức độ, quy mô thực hiện.
Các bước tiến hành
- Bước 1: Kiểm tra trong đơn thuốc hoặc hồ sơ bệnh án thông tin về chẩn đoán bệnh (mã ICD của ĐTĐ không phụ thuộc insulin E11).
- Bước 2: Nhân viên cấp phát thuốc kiểm tra danh sách các thuốc điều trị được bác sĩ kê đơn.
- Bước 3: Kiểm tra tính hợp lý của thuốc so với chỉ định (bảng 2.2)
+ Nếu người bệnh có chẩn đoán ĐTĐ nhưng thuốc được kê không phải thuốc điều trị ĐTĐ, nhân viên cấp phát thuốc thông báo lại cho bác sĩ để làm rõ tính chính xác của chỉ định hoặc bổ sung thuốc điều trị ĐTĐ.
+ Nếu không có chẩn đoán ĐTĐ nhưng người bệnh được kê thuốc điều trị ĐTĐ, nhân viên cấp phát thuốc thông báo lại cho bác sĩ để bỏ thuốc được kê hoặc bổ sung chỉ định (nếu có).
+ Nếu người bệnh có chẩn đoán ĐTĐ, thuốc được kê là thuốc điều trị ĐTĐ, nhân viên cấp phát thuốc cấp phát thuốc cho người bệnh.
2.2 Hướng dẫn thực hành tại cơ sở y tế tuyến 3 (tương đương tuyến huyện)
Yêu cầu cần đạt được
- Tương tự cơ sở y tế tuyến 4 (cấp phát thuốc phù hợp với chẩn đoán).
- Kiểm tra liều thuốc: rà soát liều thuốc không vượt quá giới hạn liều tối đa.
- Kiểm tra tương tác thuốc (khuyến khích thực hiện), chặn các tương tác thuốc chống chỉ định.
Phạm vi thực hiện
- Cấp phát thuốc phù hợp chẩn đoán: bắt buộc thực hiện với tất cả đơn thuốc.
- Kiểm tra liều thuốc: Khuyến khích thực hiện với tất cả đơn thuốc. Tuy nhiên, tùy thuộc điều kiện nhân lực của cơ sở và tình hình thực tế, yêu cầu kiểm tra một tỷ lệ đơn nhất định, tập trung một số đối tượng nhất định (ví dụ: các đơn có nhiều thuốc, đối tượng đặc biệt: phụ nữ có thai, cho con bú, trẻ em).
- Kiểm tra tương tác thuốc: khuyến khích thực hiện, không quy định cụ thể về mức độ, quy mô thực hiện.
Các bước tiến hành
- Bước 1 đến bước 3: tương tự hướng dẫn thực hành tại cơ sở y tế tuyến 4
- Bước 4: kiểm tra liều thuốc
+ Nếu thuốc được kê với liều vượt quá giới hạn liều tối đa theo hướng dẫn, dược sĩ thông báo lại cho bác sĩ để có điều chỉnh hợp lý.
+ Nếu thuốc điều trị ĐTĐ được kê trong khoảng liều đúng liều theo hướng dẫn, dược sĩ tiếp tục kiểm tra các tương tác thuốc.
- Bước 5: kiểm tra tương tác thuốc (tham khảo bảng 2.5, 2.6, 2.7, các phần mềm (Lexicomp, Micromedex) hoặc trang web (drugs.com, www.medscape.com) hoặc sách (Stockley drug interactions, Tương tác thuốc – BYT).
+ Nếu có tương tác thuốc ở mức độ chống chỉ định dùng chung, dược sĩ cần thông báo lại cho bác sĩ để thay đổi thuốc.
+ Nếu có tương tác thuốc cần hiệu chỉnh liều, dược sĩ thông báo lại cho bác sĩ để chỉnh liều thuốc (khuyến khích thực hiện).
+ Nếu có những tương tác thuốc khác (bảng 2.7), cần có tư vấn cho người bệnh sau khi phát thuốc (khuyến khích thực hiện).
- Bước 6: rà soát lại các bước từ 1 – 5 để đảm bảo tính hợp lý của đơn thuốc, sau đó cấp phát thuốc cho người bệnh.
2.3 Hướng dẫn thực hành tại cơ sở y tế tuyến 2 (tương đương tuyến tỉnh)
Yêu cầu cần đạt được
- Tương tự cơ sở y tế tuyến 3.
- Tư vấn chế độ dùng thuốc dựa trên tiền sử dùng thuốc của người bệnh, tư vấn về ADR và tương tác thuốc cho nhân viên y tế và người bệnh.
Phạm vi thực hiện
- Cấp phát thuốc phù hợp chẩn đoán: bắt buộc thực hiện với tất cả đơn thuốc.
- Kiểm tra liều thuốc: Khuyến khích thực hiện với tất cả đơn thuốc. Tuy nhiên, tùy thuộc điều kiện nhân lực của cơ sở và tình hình thực tế, yêu cầu kiểm tra một tỷ lệ đơn nhất định, tập trung trên một số đối tượng nhất định.
- Kiểm tra tương tác thuốc, tư vấn về ADR, chế độ dùng thuốc: yêu cầu kiểm tra và tư vấn trên một tỷ lệ nhất định đơn thuốc tùy điều kiện nhân lực của cơ sở, tập trung vào một số đối tượng nhất định (ví dụ: các đơn có nhiều thuốc, đối tượng đặc biệt: phụ nữ có thai, cho con bú, trẻ em).
Các bước tiến hành
- Bước 1 đến bước 6: tương tự hướng dẫn thực hành tại cơ sở y tế tuyến 3 (Mục 2.2).
- Bước 7: Tư vấn chế độ dùng thuốc dựa trên tiền sử dùng thuốc của người bệnh, tư vấn về ADR và tương tác thuốc cho nhân viên y tế và người bệnh.
+ Tư vấn về ADR: tham khảo bảng 3 hoặc các nguồn tài liệu khác (Dược thư quốc gia Việt Nam, Hướng dẫn sử dụng thuốc kèm sản phẩm).
+ Tư vấn về tương tác thuốc cho nhân viên y tế và người bệnh (tham khảo Bảng 2.5, Bảng 2.6, Bảng 2.7, các phần mềm (Lexicomp, Micromedex) hoặc trang web (www.drugs.com, www.medscape.com) hoặc sách (Stockley Drug Interactions, Sách “Tương tác thuốc và chú ý khi chỉ định – BYT). Đối với người bệnh, ưu tiên hướng dẫn cách sử dụng thuốc để hạn chế tương tác (ví dụ: tương tác do hấp thu).
+ Tư vấn chế độ dùng thuốc: cần căn cứ vào tiền sử dùng thuốc để có nội dung tư vấn phù hợp.
Khai thác tiền sử dùng thuốc
Các bước tiến hành phỏng vấn tiền sử dùng thuốc thông thường
Rà soát thông tin nền: nhằm mục đích xác định các vấn đề cần tập trung trong cuộc phỏng vấn. Thông tin nền gồm các yếu tố sau:
- Tuổi, giới tính, chiều cao, cân nặng.
- Chủng tộc/tôn giáo.
- Tình trạng sinh lý: mang thai, cho con bú.
- Khả năng giao tiếp (ví dụ: chức năng nhận thức, sự tỉnh táo, minh mẫn, trạng thái tâm lý và các yêu cầu trợ giúp về giao tiếp như: kính, máy trợ thính, phiên dịch).
- Tiền sử bệnh, chẩn đoán bệnh và các xét nghiệm liên quan (nếu có).
Sử dụng các nguồn phù hợp để thu thập thông tin:
- Các thuốc của người bệnh mang theo và/hoặc danh sách thuốc.
- Hồ sơ bệnh án của người bệnh (hồ sơ bệnh án cũ, đơn thuốc ra viện/ngoại trú).
- Các phương tiện hỗ trợ tuân thủ (nếu có).
Tiến hành phỏng vấn người bệnh/người chăm sóc về thuốc người bệnh đang sử dụng ngay trước khi nhập viện, thuốc người bệnh đã ngừng sử dụng nhưng vẫn có thể ảnh hưởng đến quá trình điều trị hiện tại, khả năng tuân thủ điều trị. Xem hướng dẫn phỏng vấn tiền sử dùng thuốc tại bảng 2.8.
Xác nhận tính chính xác của tiền sử dùng thuốc: để đảm bảo thông tin thu thập được chính xác, DSLS cần lưu ý xác nhận lại thông tin, đặc biệt trong các trường hợp: người bệnh tự sử dụng thuốc, có tiền sử dùng thuốc phức tạp, thuốc sử dụng có nguy cơ cao hoặc không thể thu thập được một tiền sử dùng thuốc đáng tin cậy từ người bệnh/người chăm sóc. DSLS có thể xác nhận tiền sử dùng thuốc của người bệnh dựa vào: người thân/người chăm sóc chịu trách nhiệm giám sát việc sử dụng thuốc của người bệnh, hồ sơ bệnh án của người bệnh (hồ sơ bệnh án cũ, đơn thuốc ra viện/ngoại trú) hoặc từ thông tin của cán bộ y tế khác (ví dụ bác sĩ kê đơn trước đó).
Một số thông tin khác cần khai thác khi tiến hành phỏng vấn tiền sử dùng thuốc ở người bệnh ĐTĐ:
- Người bệnh đã được chẩn đoán ĐTĐ bao lâu, gia đình có ai mắc bệnh hay không?
- Người bệnh có biết các nguy cơ nếu ĐTĐ không được kiểm soát?
- Người bệnh có tự theo dõi glucose huyết ở nhà hay không? Cách theo dõi và tần suất như thế nào? Nồng độ glucose huyết thông thường là bao nhiêu? Mục tiêu glucose huyết cần đạt mà bác sĩ đã hướng dẫn cho người bệnh? Các kết quả này có được ghi chép lại hay không?
- Khi glucose huyết cao, người bệnh đã xử trí như thế nào? Tương tự, khi glucose huyết thấp người bệnh đã được hướng dẫn xử trí thế nào?
- Tìm hiểu người bệnh có gặp các triệu chứng hạ đường huyết sau đây: nhìn mờ, hoa mắt, đau đầu, mệt mỏi, yếu cơ, lo lắng, nhịp nhanh, run, vã mồ hôi, choáng váng.
- Tìm hiểu người bệnh đã bao giờ bị các dấu hiệu/triệu chứng tăng glucose huyết sau đây: đi tiểu thường xuyên, cảm thấy khát hơn, ăn ngon miệng và nhanh đói. Đau bụng hoặc buồn nôn, mệt mỏi.
- Đáp ứng điều trị của người bệnh với phác đồ đang sử dụng (dựa vào các chỉ số glucose huyết, HbA1c). Các biến chứng nghiêm trọng (nếu có). Ví dụ: nhiễm toan ceton…
- Người bệnh có các công cụ hỗ trợ nào để giúp tăng tuân thủ điều trị?
Tư vấn chế độ dùng thuốc
Tư vấn về lý do chỉ định thuốc, cách sử dụng thuốc (phụ lục 2.1, phụ lục 2.2), việc tuân thủ, các vấn đề cần lưu ý trong sử dụng thuốc dựa trên tiền sử dùng thuốc của người bệnh (tham khảo thêm bảng 2.9).
Bảng kiểm phỏng vấn tiền sử dùng thuốc của người bệnh
Bảng 2.8. Bảng kiểm phỏng vấn tiền sử dùng thuốc của người bệnh
| 1
|
Mở đầu cuộc phỏng vấn | Đánh dấu |
| Giới thiệu và chào hỏi (Sử dụng khung AIDET):
Hỏi tên của người bệnh (Acknowledge) Giới thiệu (Introduce) tên và nghề nghiệp của bản thân Thời gian dự kiến (Duration), xác nhận thời gian thuận tiện để phỏng vấn Giải thích (Explain) mục đích của cuộc phỏng vấn Cảm ơn (Thank) người bệnh khi kết thúc cuộc phỏng vấn Xác định người chịu trách nhiệm quản lý việc dùng thuốc của người bệnh tại nhà |
||
| 2
|
Xác định tiền sử bệnh, dị ứng và ADR | |
| Tiền sử bệnh, thời gian mắc bệnh | ||
| Tiền sử sử dụng các chất kích thích như: rượu, thuốc lá… và tần suất sử dụng. | ||
| Xác nhận và ghi chép một cách chính xác và đầy đủ về tiền sử dị ứng và ADR:
+ Dị nguyên: thuốc, thức ăn, thời tiết + Mô tả phản ứng, thời gian xuất hiện phản ứng |
||
| 3
|
Rà soát tất cả thuốc, thực phẩm chức năng mà người bệnh đang sử dụng ngay trước khi nhập viện, thuốc người bệnh đã ngừng sử dụng nhưng vẫn có thể ảnh hưởng đến điều trị hiện tại, lưu ý đến thuốc/thực phẩm chức năng mà người bệnh sử dụng trong vòng 3 tháng trước đó | |
| Tên thuốc (hoạt chất và biệt dược), liều lượng, tần suất dùng và thời gian dùng thuốc | ||
| ADR/ phản ứng dị ứng liên quan tới các thuốc hiện dùng. | ||
| Các thuốc đã ngừng/thay đổi gần đây và lý do của sự thay đổi đó . | ||
| Biện pháp hỗ trợ tuân thủ điều trị (nếu có) (ví dụ: dụng cụ chia thuốc) | ||
| Cách bảo quản thuốc (ví dụ: insulin) | ||
|
4
|
Đánh giá tuân thủ | |
| Đánh giá hiểu biết và thái độ của người bệnh về liệu pháp điều trị thuốc hiện tại và trước đây bao gồm:
• Chỉ định • Nhận thức về hiệu quả • Nhận thức về các vấn đề do thuốc • Theo dõi hiện tại • Lý do thay đổi thuốc. |
||
| Đánh giá khả năng sử dụng các loại thuốc theo đơn
Tìm hiểu những yếu tố ngăn cản tuân thủ điều trị (ví dụ: thiếu kiến thức về thuốc, lú lẫn, vấn đề về chi phí, niềm tin cá nhân hay văn hóa, gặp khó khăn về thể chất hoặc sức khỏe, ví dụ thị lực kém, khó nuốt, sức khỏe yếu hoặc thiếu sự phối hợp các hành động) |
||
| Đánh giá sự tuân thủ của người bệnh | ||
| Tần suất, lý do quên thuốc | ||
| 5
|
Tóm tắt phỏng vấn | |
| – Cho phép người bệnh/người chăm sóc đặt các câu hỏi liên quan đến thuốc trong thời gian phỏng vấn và tại thời điểm kết thúc cuộc phỏng vấn.
– Tóm tắt những thông tin quan trọng và mô tả kế hoạch dự kiến cho việc quản lý sử dụng thuốc của người bệnh, ví dụ các vấn đề liên quan đến thuốc cần được giải quyết, các biệt dược khác nhau của thuốc được sử dụng. |
2.4. Hướng dẫn thực hành tại cơ sở y tế tuyến 1 (tương đương tuyến trung ương)
Yêu cầu cần đạt được
- Tương tự cơ sở y tế tuyến 2
- Lập kế hoạch điều trị
- Theo dõi và đánh giá điều trị
Phạm vi thực hiện
- Cấp phát thuốc phù hợp chẩn đoán: bắt buộc thực hiện với tất cả đơn thuốc.
- Kiểm tra liều thuốc: Khuyến khích thực hiện với tất cả đơn thuốc. Tuy nhiên, tùy thuộc điều kiện nhân lực của cơ sở và tình hình thực tế, yêu cầu kiểm tra một tỷ lệ đơn nhất định, tập trung trên một số đối tượng nhất định.
- Kiểm tra tương tác thuốc, tư vấn về ADR, chế độ dùng thuốc: yêu cầu kiểm tra và tư vấn trên một tỷ lệ nhất định đơn thuốc tùy điều kiện nhân lực của cơ sở, tập trung vào một số đối tượng nhất định (ví dụ: các đơn có nhiều thuốc, đối tượng đặc biệt: phụ nữ có thai, cho con bú, trẻ em)
- Lập kế hoạch điều trị, theo dõi và đánh giá điều trị: khuyến khích thực hiện khi có đủ điều kiện về nhân lực, tiến hành tại các cơ sở y tế có quy định cụ thể về dịch vụ chăm sóc dược trên các đối tượng có yêu cầu về dịch vụ này.
Các bước tiến hành
- Bước 1 đến bước 7: tương tự hướng dẫn thực hành tại cơ sở y tế tuyến 2 (Mục 2.2.3).
- Bước 8: Lập kế hoạch điều trị
Xác định mục tiêu điều trị, lập kế hoạch điều trị cụ thể về thuốc, dinh dưỡng, chế độ vận động (tham khảo bảng 2.9)
- Bước 9: Theo dõi và đánh giá điều trị
Đánh giá về việc tuân thủ điều trị, hiệu quả điều trị và các ADR ghi nhận trong quá trình điều trị (tham khảo bảng 2.10).
Bảng 2.9. Lập kế hoạch điều trị
| Hoạt động chính | Nội dung hoạt động | Hướng dẫn chi tiết | Kế hoạch chăm sóc của DSLS cho người bệnh | Thực hiện |
| Xác định mục tiêu điều trị
|
Kiểm soát ĐTĐ | HbA1c | < 7 % với đa số người bệnh . Tham khảo mục 1.1.2.1 với đối tượng đặc biệt | □ |
| Glucose huyết lúc đói, trước ăn | 80 – 130 mg/dL (4,4 – 7,2 mmol/L) | □ | ||
| Glucose huyết sau ăn 1 – 2 giờ | < 180 mg/dL (10,0 mmol/L) | □ | ||
| Kiểm soát yếu tố nguy cơ của biến chứng
|
Lipid máu | Có thể tham khảo các hướng dẫn sau đây:
– Hướng dẫn của BYT (2017): + LDL cholesterol < 100 mg/dL (2,6 mmol/L) nếu chưa có biến chứng tim mạch. + LDL cholesterol < 70 mg/dL (1,8 mmol/L) nếu đã có bệnh tim mạch. + Triglycerid < 150 mg/dL (1,7 mmol/L) + HDL cholesterol > 40 mg/dL ( 1,0 mmol/L) ở nam và > 50 mg/dL ( 1,3 mmol/L) ở nữ – Hướng dẫn của ADA (2019): không có mục tiêu lipid huyết. Việc lựa chọn thuốc và liều thuốc dựa trên BTMXV, nguy cơ BTMXV năm, yếu tố nguy cơ BTMXV, tuổi, LDL- c ban đầu, khả năng dung nạp thuốc. |
□ | |
| HA | Có thể tham khảo các hướng dẫn sau đây:
– Hướng dẫn của BYT (2017): HA < 140/90 mmHg. Nếu đã có biến chứng thận: Huyết áp < 130/85 – 80 mmHg – Hướng dẫn của ADA (2019): + Người bệnh ĐTĐ, tăng HA với nguy cơ bệnh tim mạch cao (có BTMXV, hoặc có nguy cơ BTMXV năm > 5%): HA < 130/80 mmHg. + Người bệnh ĐTĐ, tăng HA với nguy cơ bệnh tim mạch thấp (nguy cơ BTMXV năm < 5%): HA < 140/90 mmHg (Đánh giá nguy cơ BTMXV có thể sử dụng công cụ ước tính của Hội Tim mạch Hoa Kỳ http://tools.acc.org/ASCVD-Risk-Estimator-Plus/) |
□ | ||
| BMI mục tiêu | 18,5 – 22,9 kg/m2 | □ | ||
| Hút thuốc lá | Cai thuốc lá (ở người bệnh có hút thuốc lá) | □ | ||
|
Lập kế hoạch điều trị |
Thuốc điều trị | Thông tin chung về thuốc | □ | |
| Cách sử dụng thuốc | Phụ lục 2.1 | □ | ||
| Chế độ sinh hoạt | Chế độ dinh dưỡng
Luyện tập thể dục |
Dưới đây là chế độ dinh dưỡng tham khảo cho người bệnh:
– Người bệnh béo phì, thừa cân (BMI > 23 kg/m2), cần giảm cân ít nhất 3 – 7 % so với cân nặng nền – Carbohydrat: nên dùng loại hấp thu chậm có nhiều chất xơ như: gạo lứt, bánh mì đen, nui còn chứa nhiều chất xơ – Protid: nên dùng khoảng 1- 1,5 gam kg cân nặng ngày ở người không suy chức năng thận Nên ăn cá ít nhất 3 lần/tuần Nếu ăn chay trường, có thể bổ sung nguồn đạm từ các loại đậu (đậu phụ, đậu đen, đậu đỏ) – Lipid: nên dùng các loại lipid có chứa acid béo không no một nối đôi hoặc nhiều nối đôi như dầu ô liu, dầu mè, dầu lạc, mỡ cá Cần tránh các loại mỡ trans, phát sinh khi ăn thức ăn rán, chiên ngập dầu mỡ – Muối: Ăn càng nhạt càng tốt, giảm muối trong bữa ăn (còn khoảng 2.300 mg natri mỗi ngày) – Chất xơ ít nhất 15 gam mỗi ngày – Yếu tố vi lượng (bổ sung nếu thiếu): Sắt ở bệnh nhân ăn chay trường; vitamin B12 ở người bệnh dùng metformin lâu ngày nếu bệnh nhân có thiếu máu hoặc triệu chứng bệnh lý thần kinh ngoại vi – Rượu: giảm uống rượu, ít hơn một lon bia (33 mL) ngày, rượu vang đỏ khoảng 150 – 200 mL/ngày – Thuốc lá: Cai thuốc lá (ở người bệnh hút thuốc lá) – Chất tạo vị ngọt: như: đường bắp, aspartame, saccharin cần hạn chế đến mức tối thiểu
|
□
□ |
|
| Phòng ngừa biến chứng và chăm sóc bàn chân |
Các thăm khám giúp tầm soát biến chứng |
+ Bệnh nhân ĐTĐ típ 2 cần được khám mắt toàn diện, đo thị lực tại thời điểm được chẩn đoán bệnh ĐTĐ. + Nếu không có bằng chứng về bệnh võng mạc ở một hoặc nhiều lần khám mắt hàng năm và đường huyết được kiểm soát tốt, có thể xem xét khám mắt 2 năm một lần. + Nếu có bệnh võng mạc do ĐTĐ, khám võng mạc ít nhất hàng năm. Nếu bệnh võng mạc đang tiến triển hoặc đe dọa đến thị lực, phải khám mắt thường xuyên hơn.
+ Tất cả bệnh nhân cần được đánh giá về bệnh thần kinh ngoại biên tại thời điểm bắt đầu được chẩn đoán ĐTĐ típ 2 sau đó ít nhất mỗi năm một lần. Bàn chân ĐTĐ: + Thực hiện đánh giá bàn chân toàn diện ít nhất mỗi năm một lần để xác định các yếu tố nguy cơ của loét và cắt cụt chi. + Tất cả các bệnh nhân ĐTĐ phải được kiểm tra bàn chân vào mỗi lần khám bệnh. |
□ | |
| Chăm sóc bàn chân | Hướng dẫn người bệnh cách chăm sóc bàn chân như sau:(www.diabetes.co.uk, www.diabetes.org)
□ Rửa bàn chân hàng ngày với nước ấm và xà phòng □ Lau thật khô bàn chân bằng khăn mềm, đặc biệt kẽ giữa các ngón chân □ Bôi kem dưỡng da cho bàn chân, nhưng không bôi giữa các ngón chân □ Kiểm tra bàn chân hàng ngày xem các dấu hiệu bị đứt, xước, sưng, mụn nước hoặc tổn thương khác □ Không cắt móng chân quá sát và nên cắt, dũa thẳng □ Không bao giờ đi chân trần □ Mang giày, vớ vừa vặn với chân. Chọn giầy đế lót mềm và kiểm tra trước khi mang để không có vật thể cứng (đá, sỏi, …) ở trong giày □ Kiểm tra độ nóng/lạnh của nước trước khi ngâm chân vào để tránh bị bỏng hoặc tổn thương □ Thể dục xoay vận động bàn chân để máu lưu thông Không ngồi bắt chéo chân lâu. |
□
□ |
||
| Giáo dục, tư vấn cho người bệnh
|
Về bệnh và mục tiêu điều trị | Giải thích về bệnh | Tư vấn cho người bệnh hiểu về bệnh ĐTĐ: là bệnh lý mạn tính, suốt đời . Để kiểm soát được bệnh, cần có sự điều chỉnh về lối sống và nhất định phải tuân thủ đúng việc sử dụng thuốc được kê. Nếu không được kiểm soát tốt, bệnh sẽ làm ảnh hưởng tới chất lượng cuộc sống của người bệnh. | □ |
| Giải thích mục tiêu điều trị | Cung cấp cho người bệnh các thông số mục tiêu của HbA1c, glucose huyết đói, glucose huyết sau ăn giờ. Cần đạt được mục tiêu điều trị sau 3 tháng bắt đầu điều trị hoặc thay đổi điều trị bằng thuốc. | □ | ||
| Về kế hoạch điều trị
|
Thuốc – liều dùng | Với mỗi thuốc điều trị ĐTĐ được kê, người bệnh được tư vấn về: công dụng, liều dùng và cách nhận biết ADR. | □ | |
| Cách dùng thuốc uống | Với mỗi loại thuốc uống điều trị ĐTĐ được kê toa, người bệnh được tư vấn về: thời điểm uống thuốc, cách uống thuốc và khoảng cách giữa các lần dùng thuốc. | □ | ||
| Cách dùng bơm tiêm hoặc bút tiêm insulin | Phụ lục 2.3 (bơm tiêm)
Phụ lục 2.4 (bút tiêm) |
□ | ||
| Cách bảo quản thuốc insulin | Phụ lục 2.2 | □ | ||
| Chế độ ăn | Tư vấn cho người bệnh về chế độ ăn uống | □ | ||
| Tập thể dục | Tư vấn cho người bệnh về chế độ thể dục | □ | ||
| Phòng và điều trị biến chứng | Tư vấn cho người bệnh thăm khám định kỳ giúp tầm soát sớm biến chứng của ĐTĐ . | □ | ||
| Chăm sóc bàn chân | Tư vấn cho người bệnh về cách chăm sóc bàn chân | □ | ||
| Cai thuốc lá | Tư vấn cho người bệnh về các biện pháp cai nghiện thuốc lá | □ | ||
| Tư vấn về điều trị RLLP máu tăng HA | Tư vấn cho người bệnh về tác dụng của việc kiểm soát toàn diện các bệnh lý mắc kèm như tăng HA/ RLLP huyết Tư vấn về tác dụng, cách sử dụng và những lưu ý đặc biệt của các thuốc điều trị RLLP huyết và tăng HA (nếu có) | □ | ||
| Về theo dõi điều trị |
Sử dụng máy đo glucose huyết tại nhà | Tư vấn cho người bệnh về cách sử dụng máy đo glucose huyết tại nhà như sau:
Thử glucose huyết lúc đói (khi đã nhịn đói được 8 giờ trở đi. Tốt nhất là vào buổi sáng vừa ngủ dậy, chưa ăn sáng) và sau các bữa ăn 1,5 – 2 giờ tính từ khi bắt đầu ăn
Chuẩn bị: hộp đựng que lấy máu, hộp kim, bút bắn kim, máy đo, hộp đựng bông tẩm cồn
Chú ý khi đọc kết quả: 1 mmol/L = 18 mg/dL. Nếu kết quả thấy lớn hơn 7 0 thì máy đang hiện theo đơn vị mg/dL. Sau khi lấy máu, dùng một miếng bông tẩm cồn lau sạch chỗ lấy máu. |
□ | |
| ADR thường gặp của thuốc | Tham khảo bảng 2.3 | □ | ||
| Theo dõi tuân thủ điều trị |
Thuốc | Tuân thủ thuốc điều trị |
Hỏi người bệnh bộ câu hỏi tuân thủ điều trị MMAS – 8 mỗi lần người bệnh tái khám
Người bệnh có tuân thủ điều trị (MMAS – 8 = 8) Người bệnh không tuân thủ điều trị (MMAS – 8 < 8). Cần nhắc nhở người bệnh về tầm quan trọng của tuân thủ điều trị và tăng tuân thủ điều trị |
|
| Tập luyện | Tuân thủ chế độ tập luyện thể dục | Hỏi người bệnh về chế độ tập luyện thể dục, đánh dấu vào những điểm người bệnh thực hiện được.
– Loại hình luyện tập: + Tương đương đi bộ 30 phút mỗi ngày, 1 50 phút/tuần . Nếu người bệnh còn trẻ tuổi, tập 60 phút mỗi ngày + Không ngưng tập luyện 2 ngày liên tiếp + Tập kháng lực (kéo dây, nâng tạ) từ 2 – 3 lần/tuần – Nếu người bệnh cao tuổi, mắc bệnh đau khớp + Đi bộ sau 3 bữa ăn, mỗi lần 10 – 15 phút |
□ | |
| Chế độ ăn | Tuân thủ chế độ ăn | Hỏi người bệnh về chế độ ăn hàng ngày, thuyết phục người bệnh thực hiện đúng chế độ ăn hợp lý cho người ĐTĐ. | □ | |
| Hạn chế rượu | Hỏi người bệnh về lượng rượu trung bình người bệnh uống mỗi ngày . Nhắc lại cho người bệnh hạn chế rượu ít hơn một lon bia (330 mL)/ngày, rượu vang đỏ khoảng 150 – 200 mL/ngày | □ | ||
| Cai thuốc lá | Hỏi người bệnh về thói quen hút thuốc lá. Nếu còn, thuyết phục người bệnh cai thuốc lá | □ | ||
| Kế hoạch phòng và điều trị biến chứng | Tuân thủ thăm khám tầm soát biến chứng | Hỏi người bệnh về việc tầm soát biến chứng:
□ Biến chứng thận (khám mỗi năm) □ Biến chứng võng mạc (khám mỗi năm, nếu kiểm soát glucose huyết tốt – khám 2 năm một lần) □ Bệnh thần kinh do ĐTĐ (khám mỗi năm) □ Bàn chân ĐTĐ (kiểm tra bàn chân mỗi lần tái khám, khám toàn diện mỗi năm) |
□ | |
| Tuân thủ chăm sóc bàn chân | Hỏi người bệnh về cách người bệnh chăm sóc bàn chân hàng ngày
□ Đúng □ Cần nhắc nhở lại cách chăm sóc bàn chân cho người bệnh |
□ | ||
| Theo dõi kết quả điều trị
|
Kiểm soát glucose huyết
|
HbA1c | Dược sĩ lâm sàng đọc xét nghiệm HbA1 c:
□ Đạt mục tiêu □ Không đạt mục tiêu |
□ |
| Glucose đói, trước ăn | Dược sĩ lâm sàng đọc xét nghiệm glucose đói, trước ăn:
□ Đạt mục tiêu □ Không đạt mục tiêu |
□ | ||
| Glucose sau ăn 2 giờ | Dược sĩ lâm sàng đọc xét nghiệm glucose sau ăn 2 giờ:
□ Đạt mục tiêu □ Không đạt mục tiêu |
□ | ||
| Kiểm soát yếu tố nguy cơ biến chứng | 1. Lipid huyết | Dược sĩ lâm sàng đọc các xét nghiệm:
LDL cholesterol: □ Đạt mục tiêu □ Không đạt mục tiêu Triglyceride: □ Đạt mục tiêu □ Không đạt mục tiêu HDL cholesterol: □ Đạt mục tiêu □ Không đạt mục tiêu |
□ | |
| Huyết áp | Dược sĩ lâm sàng đọc chỉ số huyết áp:
□ Đạt mục tiêu □ Không đạt mục tiêu |
□ | ||
| Chức năng thận | Dược sĩ lâm sàng đọc chỉ số creatinin huyết thanh và tính MLCT:
□ Không suy giảm so với giá trị lần khám trước đó □ Giảm từ 25% so với giá trị lần khám trước đó Phối hợp với bác sĩ tìm hiểu nguyên nhân |
□ | ||
| BMI | Tính BMI cho người bệnh . Nếu là người bệnh béo phì từ lần khám trước (BMI > 23 kg/m2) . Người bệnh đạt mục tiêu BMI nếu đã giảm 3 – % so với cân nặng nền
□ Đạt mục tiêu □ Không đạt mục tiêu |
□ | ||
| Hút thuốc lá | □ Đã cai thuốc lá
□ Chưa cai được thuốc lá |
□ | ||
| Biểu hiện của biến chứng
|
2. Biến chứng tim mạch | Dược sĩ cung cấp thông tin về các biểu hiện của biến chứng tim mạch: ví dụ – đau thắt ngực, nhồi máu cơ tim | □ | |
| 3. Biến chứng thần kinh | Dược sĩ cung cấp thông tin về triệu chứng thần kinh ngoại biên: ví dụ – mất cảm giác ở bàn chân, tê bì | □ | ||
| 4. Biến chứng thận | Dược sĩ cung cấp thông tin về triệu chứng thận: ví dụ – tăng cân nhanh chóng do phù hoặc bí tiểu | □ | ||
| 5. Biến chứng trên mắt | Dược sĩ cung cấp thông tin về triệu chứng trên mắt: ví dụ – mắt nhìn mờ hoặc đau nhức | □ | ||
| 6. Biến chứng bàn chân | Dược sĩ cung cấp thông tin về triệu chứng bàn chân: ví dụ – bàn chân trầy xước, có vết phù nề hoặc dấu hiệu sưng, nóng, đỏ, đau | □ | ||
| Theo dõi ADR | Các biểu hiện ADR | Hạ đường huyết quá mức | □ Có (Nếu có, ghi rõ số lần …)
□ Không |
□ |
| Rối loạn tiêu hóa | □ Có
□ Không |
□ | ||
| Viêm đường hô hấp trên | □ Có
□ Không |
□ | ||
| Nhiễm khuẩn đường tiết niệu, sinh dục | □ Có
□ Không |
□ | ||
| Loạn dưỡng mô mỡ | □ Có
□ Không |
□ |
TÀI LIỆU THAM KHẢO
Tiếng Việt
- Bộ Y tế. (2017). Hướng dẫn chẩn đoán và điều trị ĐTĐ típ 2, ban hành ngày 19 tháng 07 năm 2017.
Tiếng Anh
- Alldredge BK. Koda Kimble and Young’s Applied therapeutics, The Clinical Use of Drugs, 10th Lippincott Williams & Wilkins.
- American Diabetes Association (ADA), (2019), Standards of Medical Care in Diabetes.
- Davies MJ et al. (2018). Management of hyperglycaemia in type 2 diabetes. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD).
- DiPiro JT et al. (2017). Pharmacotherapy – A Pathophysiologic approach, 10th McGraw-Hill education.
- Hurren KM, Pinelli NR. (2012). Drug – drug interactions with glucagon – like peptide – 1 receptor agonists. Ann Pharmacother, 46(5):710 – 7
- International Diabetes Federation (IDF). (2017). Diabetes Atlas, 8th
- Lexicomp Drug Interation software. (2019).
- Nguyen T. et al. (2015). Translation and cross – cultural adaptation of the brief illness perception questionnaire, the beliefs about medicines questionnaire and the Morisky Medication Adherence Scale into Vietnamese. Pharmacoepidemiology and Drug Safety, 24: 159 – 160.
- Philip Wiffen, Marc Mitchell (2017), Oxford Handbook of Clinical Pharmacy
- Rehman A, Setter SM, Vue MH. (2011). Drug – Induced Glucose Alterations Part 2: Drug – Induced Hyperglycemia. Diabetes Spectrum, 24(4): 234 – 238.
- Scheen AJ. (2007). Drug – drug and food – drug pharmacokinetic interactions with new insulinotropic agents repaglinide and nateglinide. Clin Pharmacokinet, 46(2): 93 – 108.
- Scheen AJ. (2007). Pharmacokinetic interactions with thiazolidinediones. Clinical Pharmacokinetics, 46(1):1 – 12.
- Scheen AJ. (2010). Dipeptidyl peptidase – 4 inhibitors (gliptins): focus on drug – drug interactions. Clin Pharmacokinet, 49(9): 573 – 88.
- Scheen AJ. (2014). Drug-Drug Interactions with Sodium – Glucose Cotransporters Type 2 (SGLT-2) Inhibitors, New Oral Glucose – Lowering Agents for the Management of Type 2 Diabetes Mellitus. Clin Pharmacokinet, 53(4):295 – 304.
- Vue MH, Setter SM (2011). Drug – Induced Glucose Alterations Part 1: Drug – Induced Hypoglycemia. Diabetes Spectrum, 24(3): 171 – 177.
- www. diabetes.org.uk (Truy cập ngày 8/12/2018).
PHỤ LỤC CHƯƠNG 2. HƯỚNG DẪN CÁCH SỬ DỤNG THUỐC ĐIỀU TRỊ ĐÁI THÁO ĐƯỜNG
Phụ lục 2.1. Cách sử dụng thuốc điều trị ĐTĐ không phải insulin
Phụ lục 2.2. Đặc điểm của các loại insulin về thời gian khởi phát tác dụng, thời gian đạt tác dụng tối đa, thời gian tác dụng, thời điểm dùng thuốc và thời gian bảo quản sau khi mở nắp
Phụ lục 2.3. Hướng dẫn sử dụng insulin dạng lọ
Phụ lục 2.4. Hướng dẫn sử dụng insulin dạng bút tiêm
Phụ lục 2.5. Bảng kiểm tư vấn sử dụng insulin dạng bút tiêm cho người bệnh
Phụ lục 2.6. Bảng kiểm người bệnh ghi lại cách sử dụng insulin dạng bút tiêm
Phụ lục 2.1. Cách sử dụng thuốc điều trị đái tháo đường không phải insulin
Bảng 1.PL2.1. Các thuốc điều trị đái tháo đường không phải insulin
| STT | Nhóm thuốc | Hoạt chất | Hàm lượng | Cách dùng |
| 1. | Biguanid | Metformin | • 500 mg (IR)
• 850 mg (IR) • 1.000 mg (IR) • 500 mg (XR) • 750 mg (XR) • 1.000 mg (XR) |
Đường uống:
• Dùng cùng bữa ăn (trong bữa ăn hoặc ngay sau ăn) (để giảm kích ứng đường tiêu hóa). • Dạng XR: nuốt nguyên viên, không được bẻ, nhai hoặc nghiền. Dùng 1 lần/ ngày cùng bữa ăn tối. |
| 2. | Sulfonylurea | Glipizid | • 5mg; 10 mg (IR)
• 5mg; 10mg (XL) |
Đường uống:
• Viên giải phóng chậm: nuốt nguyên viên, không được bẻ, nhai hoặc nghiền. Thường uống 1 lần/ngày vào bữa sáng. • Viên dạng thông thường: uống khoảng 30 phút trước một bữa ăn để giảm tối đa nồng độ glucose trong máu sau ăn |
| Glyburid (glibenclamid) | • 5 mg
• 6 mg (dạng vi hạt) |
Đường uống:
• Dùng cùng bữa ăn tại cùng thời điểm mỗi ngày (nên dùng liều 2 lần/ ngày nếu glyburide dạng truyền thống > 10 mg hoặc glyburide dạng vi hạt > 6 mg). |
||
| Glimepirid | • 4 mg
|
Đường uống:
Dùng 1 lần/ngày cùng bữa ăn sáng hoặc bữa ăn chính đầu tiên trong ngày. |
||
| Gliclazid | • 80 mg
• 30 mg (MR): không có lactose • 60 mg (MR) có lactose |
Đường uống:
• Dùng cùng bữa ăn (dạng MR nên được dùng trong bữa sáng). Có thể bẻ đôi viên thuốc 60 mg (MR), viên thuốc 30 mg (MR) phải nuốt nguyên viên. Các dạng MR không được nhai hoặc nghiền. |
||
| 3. | Meglitinid (Glinid) | Repaglinid | • 1 mg
• 2 mg |
Đường uống:
• Dùng trong vòng 30 phút trước bữa ăn, có thể được dùng trước bữa ăn 2, 3, hoặc 4 lần ngày để phù hợp với những chế độ ăn thay đổi trong mỗi bữa ăn Nếu một bữa ăn bị bỏ lỡ, không dùng liều được chỉ định tiếp theo, nếu hạ đường huyết xảy ra, cần giảm liều. |
| Nateglinid | • 120 mg | Đường uống:
• Dùng trong vòng 30 phút-1 giờ trước bữa ăn Nếu một bữa ăn bị bỏ lỡ, không dùng liều được chỉ định tiếp theo để tránh hạ đường huyết. |
||
| 4. | Thiazolidinedion | Pioglitazon | • 15 mg, 30 mg, 45 mg | Đường uống:
• Thời điểm dùng không liên quan đến bữa ăn |
| 5. | Ức chế enzym alpha glucosidase | Acarbose | • 50 mg
• 100 mg |
Đường uống:
• Dùng ngay lúc bắt đầu bữa ăn của các bữa ăn chính |
| Miglitol | • 100 mg | Đường uống:
• Dùng ngay lúc bắt đầu bữa ăn của các bữa ăn chính |
||
| 6.
|
Ức chế DPP-4
|
Sitagliptin | • 25 mg
• 50 mg • 100 mg |
Đường uống:
• Thời điểm dùng không liên quan đến bữa ăn |
| Saxagliptin | • 2,5 mg
• 5 mg |
Đường uống:
• Thời điểm dùng không liên quan đến bữa ăn Không được chia nhỏ hoặc cắt viên thuốc. |
||
| Linagliptin | • 5 mg | Đường uống:
• Thời điểm dùng không liên quan đến bữa ăn |
||
| Alogliptin | • 25 mg | Đường uống:
• Thời điểm dùng không liên quan đến bữa ăn |
||
| Vildagliptin | • 50 mg | Đường uống:
Thời điểm dùng không liên quan đến bữa ăn |
||
| 7 | Ức chế SGLT2 | Canagliflozin | • 300 mg | Đường uống:
• Thời điểm dùng không liên quan đến bữa ăn • Người bệnh nên dùng trước bữa ăn đầu tiên trong ngày (có thể làm giảm việc tăng đường huyết sau ăn do làm chậm việc hấp thu glucose ở ruột). |
| Dapagliflozin | • 5mg
• 10 mg |
Đường uống:
• Dùng thuốc vào buổi sáng và không liên quan đến bữa ăn |
||
| Empagliflozin | • 10 mg
• 25 mg |
Đường uống:
• Dùng thuốc 1 lần/ngày vào buổi sáng và không liên quan đến bữa ăn |
||
| Ertugliflozin | • 5 mg
• 15 mg |
Đường uống:
Dùng thuốc 1 lần/ngày vào buổi sáng và không liên quan đến bữa ăn |
||
| 8 | Đồng vận thụ thể GLP-1 | Liraglutid | • 18 mg/3 mL: bút tiêm | Tiêm dưới da:
• Tiêm dưới da ở phần trên của cánh tay, đùi hoặc bụng Không tiêm tĩnh mạch hoặc tiêm bắp. Thời điểm dùng không liên quan đến bữa ăn hoặc thời gian trong ngày. Thay kim mỗi lần dùng. Chỉ dùng thuốc nếu thuốc trong, không màu, không có hạt lạ. Không dùng chung bút giữa các người bệnh ngay cả khi kim được thay đổi. Nếu dùng đồng thời với insulin, không trộn, có thể tiêm trên cùng vị trí cơ thể như insulin nhưng không tiếp giáp với nhau. • Bảo quản: Trước khi sử dụng bảo quản ở 2 °C đến 8°C. Sau lần sử dụng đầu tiên, có thể được bảo quản ở 2°C đến 8°C hoặc ở 15°C đến 30°C. Không để thuốc đông lại (loại bỏ nếu thuốc bị đông) Tránh tiếp xúc nhiệt và ánh sáng Bút nên được bỏ đi sau 30 ngày kể từ ngày đầu sử dụng.
|
| Dulaglutid | • 0,75 mg/0,5 mL bút tiêm • 1,5 mg/0,5 mL bút tiêm |
Tiêm dưới da: • Tiêm dưới da ở phần trên của cánh tay, đùi hoặc bụng Không tiêm tĩnh mạch hoặc tiêm bắp. Thời điểm dùng không liên quan đến bữa ăn hoặc thời gian trong ngày. • Bảo quản: Trước khi sử dụng bảo quản ở 2 °C đến 8°C. Sau lần sử dụng đầu tiên, bảo quản được tối đa 14 ngày ở nhiệt độ dưới 30°C. |
||
| Exenatid ER | 2 mg bột pha tiêm; kèm 0,65 mL dung dịch pha |
Tiêm dưới da: Tiêm dưới da ở phần trên của cánh tay, đùi hoặc bụng. Tiêm ngay sau khi hoàn nguyên. Nếu dùng đồng thời với insulin, phải tiêm 2 lần riêng biệt. Bảo quản: Trước khi sử dụng bảo quản ở 2 °C đến 8°C, có thể bảo quản trong vòng 4 tuần ở nhiệt độ dưới 30°C. Thuốc phải được sử dụng ngay sau khi hoàn nguyên. |
||
| Semaglutid | 2mg/1,5 mL bút tiêm |
Tiêm dưới da: Tiêm dưới da ở phần trên của cánh tay, đùi hoặc bụng. Nếu dùng đồng thời với insulin, phải tiêm 2 lần riêng biệt.Bảo quản: Trước khi sử dụng bảo quản ở 2 °C đến 8°C. Sau lần sử dụng đầu tiên, bảo quản dưới 25°C |
||
| Exenatid | • 5mcg/20 mcL bút tiêm
• 10mcg/40 mcL bút tiêm |
Tiêm dưới da:
Tiêm dưới da ở phần trên của cánh tay, đùi hoặc bụng. Nếu dùng đồng thời với insulin, phải tiêm 2 lần riêng biệt. Bảo quản: Trước khi sử dụng, bảo quản ở 2°C đến 8°C. Sau lần sử dụng đầu tiên, bảo quản dưới 25°C |
||
| Lixisenatid | 10mcg/0,2 mL bút tiêm 3mL
20mcg/0,2 mL bút tiêm 3 mL |
Tiêm dưới da:
Tiêm dưới da ở phần trên của cánh tay, đùi hoặc bụng. Tiêm trong vòng 1 giờ trước bữa ăn Bảo quản: Trước khi sử dụng bảo quản ở 2°C đến 8°C. Sau lần sử dụng đầu tiên, bảo quản dưới 30°C. |
||
| 9. | Chất gắn acid mật | Colesevelam | • 625 mg: viên nén
• 1,875 g: hỗn dịch |
Đường uống:
• Viên nén: Dùng cùng với bữa ăn và nước uống Do kích thước viên thuốc lớn nên người bệnh gặp khó khăn khi nuốt viên nên sử dụng dạng hỗn dịch. • Dạng hỗn dịch: Dùng cùng bữa ăn Bột không được dùng ở dạng khô (để tránh gây rối loạn tiêu hóa). • Cách pha: Cho 1 gói vào ly, thêm 1/2-1 cốc (120- 240 mL) nước hoặc nước ép trái cây và khuấy đều. |
| 10. | Chủ vận dopamine D2 | Bromocriptin | • 0,8 mg | Đường uống:
• Dùng cùng bữa ăn (để giảm kích ứng đường tiêu hóa). • Biệt dược Cycloset: Dùng trong vòng 2 giờ sau khi thức dậy vào buổi sáng. |
Chú thích:
|
||||
Phụ lục 2.2. Đặc điểm của các loại insulin về thời gian khởi phát tác dụng, thời gian đạt tác dụng tối đa, thời gian tác dụng, thời điểm dùng thuốc và thời gian bảo quản sau khi mở nắp
1. Một số lưu ý chung
a) Một số lưu ý về cách ghi chỉ định insulin
– Insulin phải được chỉ định bằng tên biệt dược.
– Từ “đơn vị” nên được đánh máy trong bảng chỉ định insulin, không được viết tay hoặc không được viết tắt “IU” hoặc “U”.
– Xây dựng quy trình kiểm soát đường huyết nội viện để thống nhất cách ghi chỉ định insulin.
Ví dụ: Cách ghi chỉ định insulin tiêm dưới da đối với người bệnh nội trú (liều thực tế dựa trên quy trình nội bộ kiểm soát đường huyết nội viện)
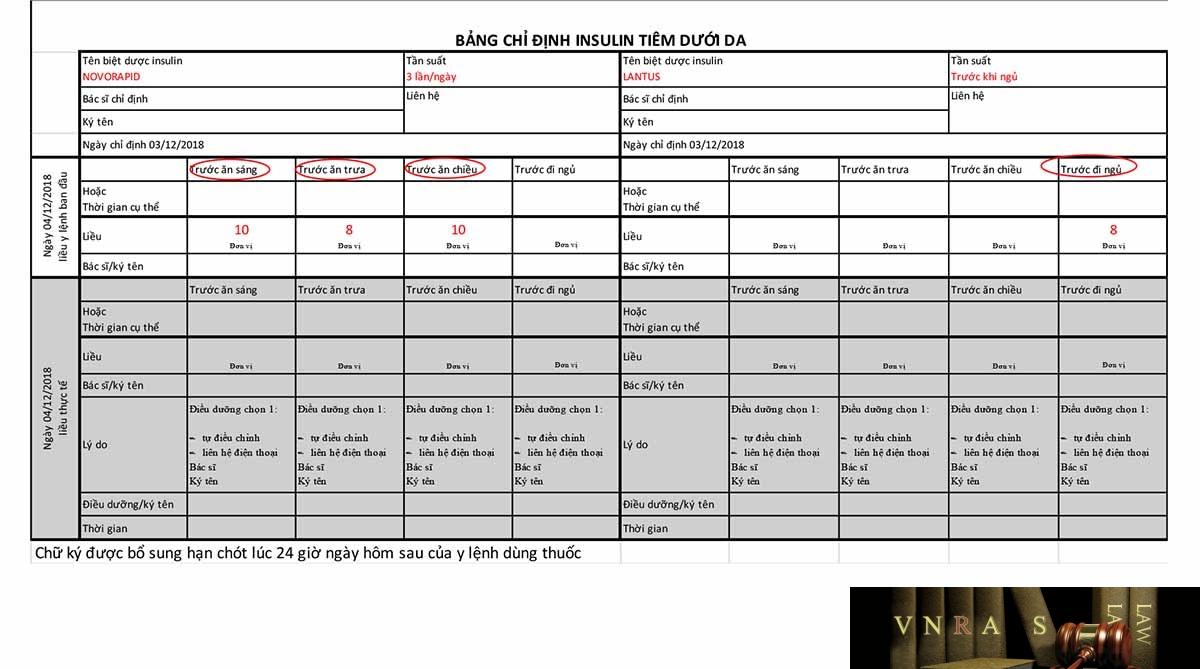
|
BẢNG THEO DÕI ĐƯỜNG HUYẾT |
||||||||
| Tần suất theo dõi đường huyết
□ Trước ăn □ Sau ăn 2 giờ □ Lúc 22:00 giờ □ Lúc 2:00-3:00 giờ □ Khác Cụ thể: |
||||||||
| Ngày: | 2:00-3:00 giờ | Buổi sáng | Buổi trưa | Buổi tối | Trước khi ngủ 22:00 giở | |||
| Trước ăn | Sau ăn 2 giờ | Trước ăn | Sau ăn 2 giờ | Trước ăn | Sau ăn 2 giờ | |||
| Thời gian đo | ||||||||
| Đường huyết (mg/dl) | ||||||||
| Thành phần bữa ân | ||||||||
| Điều dưỡng/ký tên | ||||||||
| BẢNG ĐIỀU CHỈNH LIỀU INSULIN | ||||||||
| THEO QUY TRÌNH KIỂM SOÁT ĐƯỜNG HUYẾT NỘI VIỆN | ||||||||
b) Bảo quản insulin
– Khi chưa mở lọ/bút tiêm
+ Bảo quản trong ngăn mát tủ lạnh (2-8 oC) + Có thể bảo quản cho đến hết hạn sử dụng
+ Lưu ý không để insulin trong hay gần ngăn đá
– Khi đã mở lọ/bút tiêm (đã sử dụng)
+ Có thể bảo quản ở nhiệt độ phòng < 30 0C từ 4-6 tuần (xem HDSD)
Đặc điểm của các loại insulin về thời gian khởi phát tác dụng, thời gian đạt tác dụng tối đa, thời gian tác dụng, thời điểm dùng thuốc và thời gian bảo quản sau khi mở nắp
| Loại insulin | Hoạt chất | Biệt dược | Hàm lượng và dạng bào chế | Thời gian khởi phát tác dụng | Thời gian đạt tác dụng tối đa | Thời gian tác dụng | Thời điểm dùng thuốc- tiêm dưới da | Thời gian bảo quản sau khi mở nắp |
| Tác dụng nhanh (analog) | Lispro | Humalog | Lọ U-100 | 0,25 – 0,5 giờ | 0,5 – 2,5 giờ | ≤ 5 giờ | Dùng trong vòng 15 phút trước hoặc ngay sau bữa ăn | 28 ngày |
| Humalog Junior Kwikpen Humalog Kwikpen | Bút tiêm U-100
Bút tiêm U-200 |
|||||||
| Aspart | Novolog | Lọ U-100 | ~0,2 – 0,3 giờ | 1 – 3 giờ | 3 – 5 giờ | Dùng ngay (trong vòng 5 -10 phút) trước bữa ăn | 28 ngày | |
| Novolog
Flexpen Novorapid |
Bút tiêm U-100 | |||||||
| Glulisin | Apidra | Lọ U-100 | 0,2 – 0,5 giờ | 1,6 – 2,8 giờ | 3 – 4 giờ | Dùng trong vòng 15 phút trước hoặc trong vòng 20 phút sau bữa ăn | 28 ngày | |
| Apidra Solostar | Bút tiêm U-100 | |||||||
| Tác dụng ngắn | Human Regular | Humulin R Actrapid | Lọ U-100 | 0,25 – 0,5 giờ | 2,5 – 5 giờ | 4 – 12
giờ |
Dùng khoảng 30 phút trước bữa ăn | 31 ngày |
| Tác dụng trung bình | Human NPH | Humulin N Insulatard | Lọ U-100 | 1 – 2 giờ | 4 – 12 giờ | 14 – 24 giờ | Dùng 1-2 lần/ngày | 31 ngày |
| Humulin N Kwikpen | Bút tiêm U-100 | 14 ngày theo Lexicomp, kiểm tra tờ HDSD biệt dược tại VN | ||||||
| Concentrated Human Regular insulin | U-500 Human Regular insulin | Humulin R U-500 | Lọ U-500 | 0,25 – 0,5 giờ | 4 – 8 giờ | 13 – 24 giờ | Dùng khoảng 30 phút trước bữa ăn | 40 ngày |
| Humulin R U-500
Kwikpen |
Bút tiêm U-500 | 28 ngày | ||||||
| Insulin nền (analog)
|
Glargine | Lantus | Lọ U-100 | 3 – 4 giờ | Gần như không có đỉnh tác dụng | ~24 giờ (Lantus: 10,8 – >24 giờ (đến ~30 giờ trong một số nghiên cứu) | Dùng 1 lần/ngày, dùng cùng thời điểm mỗi ngày | 28 ngày |
| Lantus Solostar | Bút tiêm U-100 | |||||||
| Toujeo Max Solostar Toujeo Solostar | Bút tiêm U-300 | 6 giờ | Tác dụng giảm đường huyết tối đa có thể mất 5 ngày với liều lặp lại, ở trạng thái ổn định, tác dụng giảm đường huyết 24 giờ thấp hơn 27% so với Lantus ở liều tương đương | >24 giờ | Dùng 1 lần/ngày, dùng cùng thời điểm mỗi ngày | 42 ngày | ||
| Glargine biosimilar | Basaglar Kwikpen | Bút tiêm U-100 | 3 – 4 giờ | Gần như không có đỉnh | ~24 giờ | Dùng 1 lần/ngày, dùng cùng thời điểm mỗi ngày | 28 ngày | |
| Detemir | Levemir | Lọ U-100 | 3 – 4 giờ | 3 – 9 giờ | Phụ thuộc liều: 6 – 23 giờ | 2 lần /ngày hoặc 1 lần /ngày với bữa ăn tối hoặc trước khi đi ngủ | 42 ngày | |
| Levemir Flex-Uch | Bút tiêm U-100 | |||||||
| Degludec | Tresiba
Flex-Uch |
Bút tiêm U-100
Bút tiêm U-200 |
~1 giờ | 9 giờ | > 42 giờ | Dùng 1 lần/ngày vào bất kỳ thời điểm nào trong ngày | 56 ngày | |
| Insulin
premixed
|
NPH/Regular 70/30 (70%
NPH/30% regular) |
Humulin 70/30
Mixtard |
Lọ U-100 | 0,5 giờ | 2-12 giờ | 18-24 giờ | Dùng 1-2 lần/ngày
Dùng khoảng 30 – 45 phút trước bữa ăn |
31 ngày |
| Humulin 70/30
Kwikpen |
Bút tiêm U-100 | 10 ngày theo Lexicomp, kiểm tra tờ HDSD biệt dược tại VN | ||||||
| LisproMix 50/50 (50% lispro protamin /50% lispro ) | Humalog Mix 50/50 | Lọ U-100 | 0,25-0,5 giờ | 0,8-4,8 giờ | 14-24 giờ | Dùng 1-2 lần/ngày
Dùng trong vòng 15 phút trước bữa ăn |
28 ngày | |
| Humalog Mix 50/50 Kwikpen | Bút tiêm U-100 | 10 ngày theo Lexicomp, kiểm tra tờ HDSD biệt dược tại VN | ||||||
| LisproMix 75/25 (75% lispro protamin /25% lispro) | Humalog Mix 75/25 | Lọ U- 100 | 0,25- 0,5 giờ | 1-6,5 giờ | 14-24 giờ | Dùng 1-2 lần/ngày
Dùng trong vòng 15 phút trước bữa ăn |
28 ngày | |
| Humalog Mix 75/25 Kwikpen | Bút tiêm U-100 | 10 ngày theo Lexicomp, kiểm tra tờ HDSD biệt dược tại VN | ||||||
| Aspart Biphasic Aspart 70/30 (70% aspart protamin/30% aspart) | Novolog Mix 70/30 | Lọ U-100 | 10 – 20 phút | 1 – 4 giờ | Novolog Mix 70/30: 18 – 24 giờ | Thường dùng 2 lần/ngày
Dùng trong vòng 15 phút trước bữa ăn (đái tháo đường típ 1) hoặc trong vòng 15 phút trước hoặc ngay sau bữa ăn (đái tháo đường típ 2) |
28 ngày | |
| Novolog
Mix 70/30 Flexpen Novomix |
Bút tiêm U-100 | 14 ngày theo Lexicomp, kiểm tra tờ HDSD biệt dược tại VN |
Phụ lục 2.3. Hướng dẫn sử dụng insulin dạng lọ
Căn cứ theo thông tin kê toa thuốc
Ví dụ: HUMULIN R – dung dịch tiêm insulin human, cập nhật tháng 11/2018, truy cập 03/12/2018
| Bước | Nội dung | Hình ảnh | Chú ý chung cho các loại insulin |
| 1. | Kiểm tra insulin Dung dịch trong suốt và không màu. KHÔNG sử dụng dung dịch bị đục, nhày, có màu hoặc có vật lạ. | Trong kỹ thuật tiêm thuốc chung, cần kiểm tra:
• 5 đúng • Hạn sử dụng • Chất lượng thuốc: màu sắc, độ đồng nhất Insulin có thành phần protamin sẽ có dạng hỗn dịch đục Hỗn dịch bắt buộc phải làm đồng nhất để đảm bảo đúng liều lượng – Bước 1: Xoay tròn ít nhất 10 lần trong lòng bàn tay – Bước : Đảo ngược ít nhất 10 lần Hỗn dịch phải có màu trắng đục. KHÔNG sử dụng nếu lọ thuốc trong và có hạt lạ
|
|
| 2. | Nếu dùng lọ thuốc lần đầu, chưa mở nắp, hãy lật nắp bảo vệ bằng nhựa, nhưng KHÔNG tháo miếng đệm cao su. | 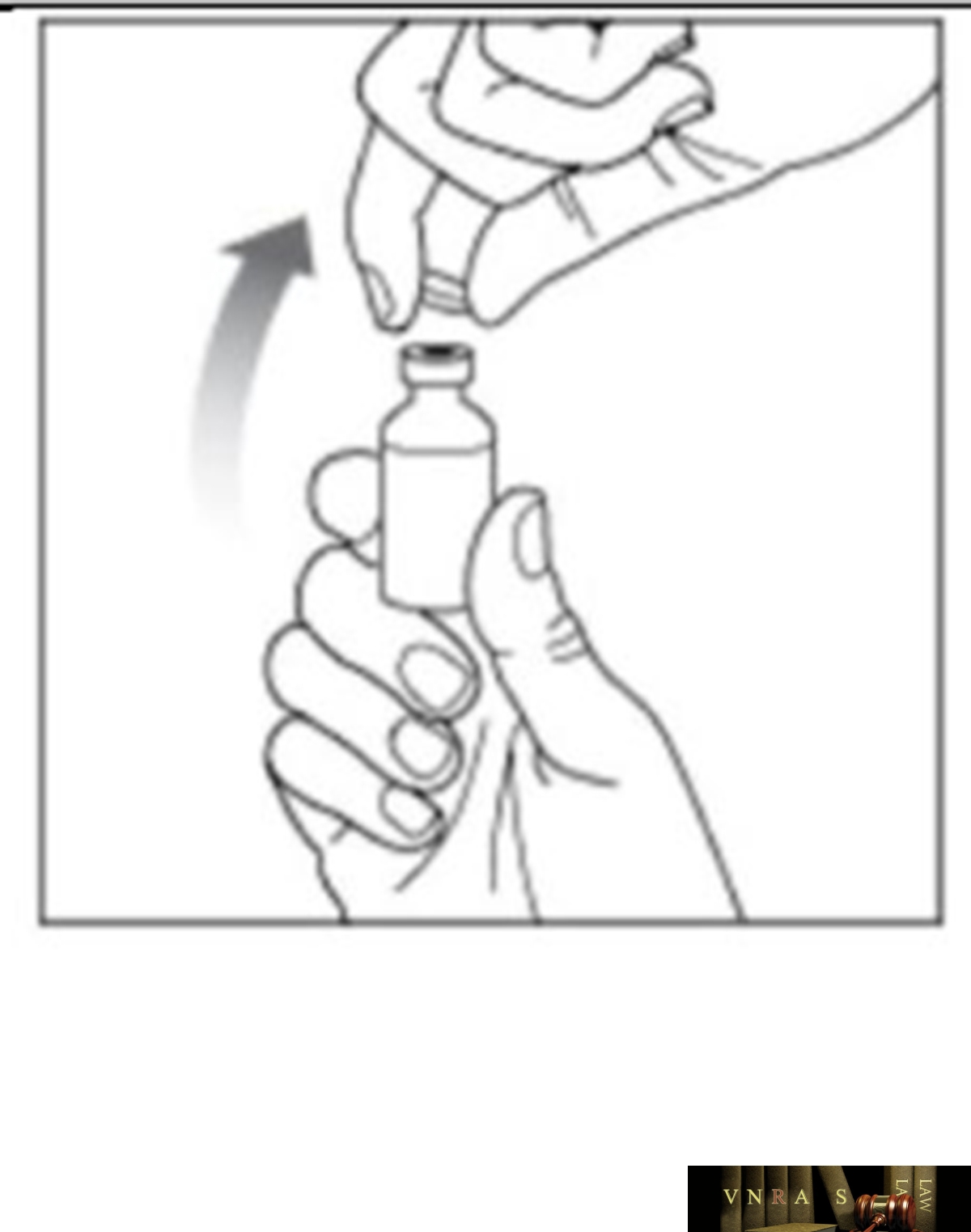 |
|
| 3. | Lau miếng đệm cao su bằng bông alcohol | 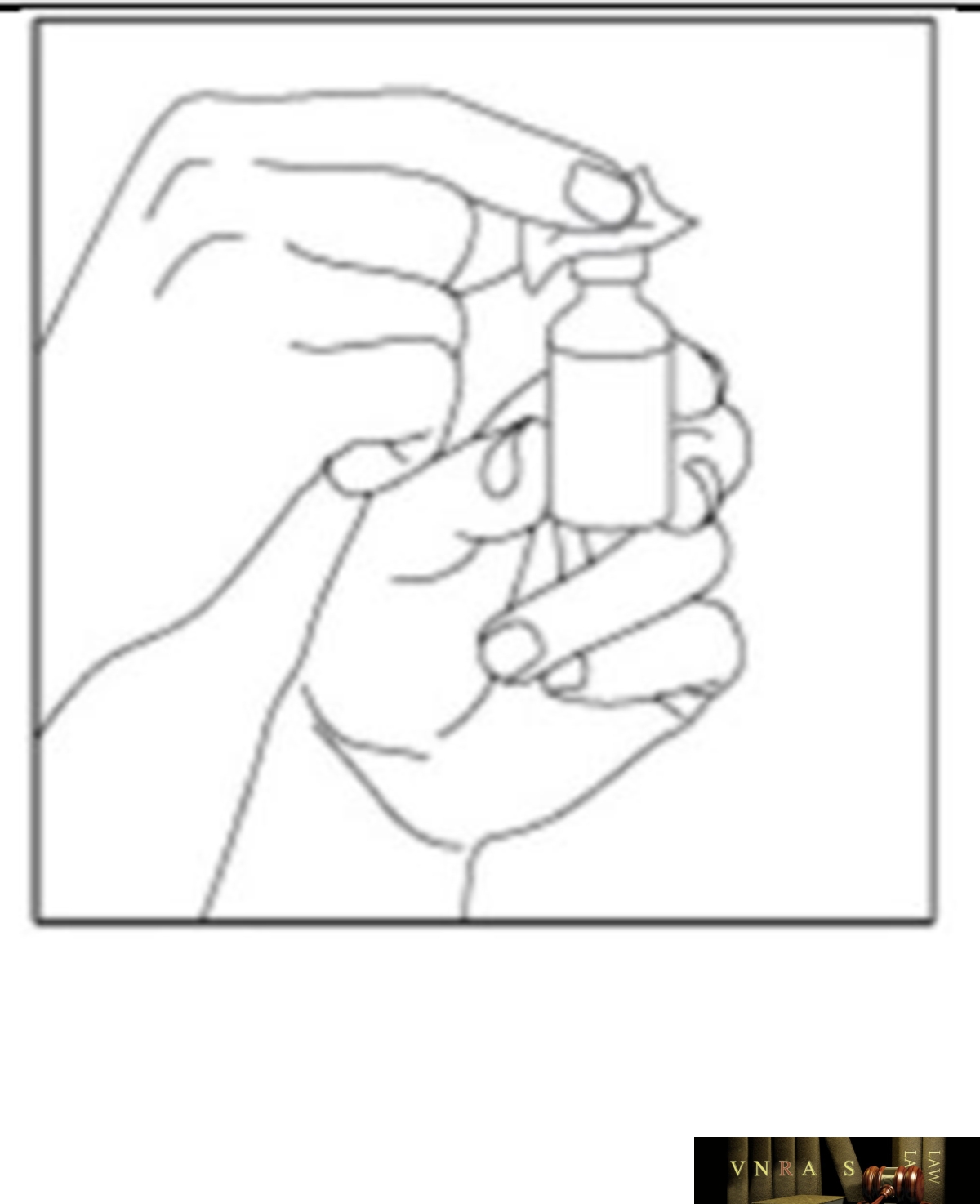 |
|
| 4. | Chọn đúng loại bơm tiêm (1ml = 40 đơn vị 1 ml = 100 đơn vị) Giữ bơm tiêm theo chiều kim tiêm hướng lên. Kéo pít-tông xuống cho đến khi đầu pít-tông đạt đến vạch số đơn vị liều lượng được chỉ định Ví dụ: liều đơn vị như hình bên |
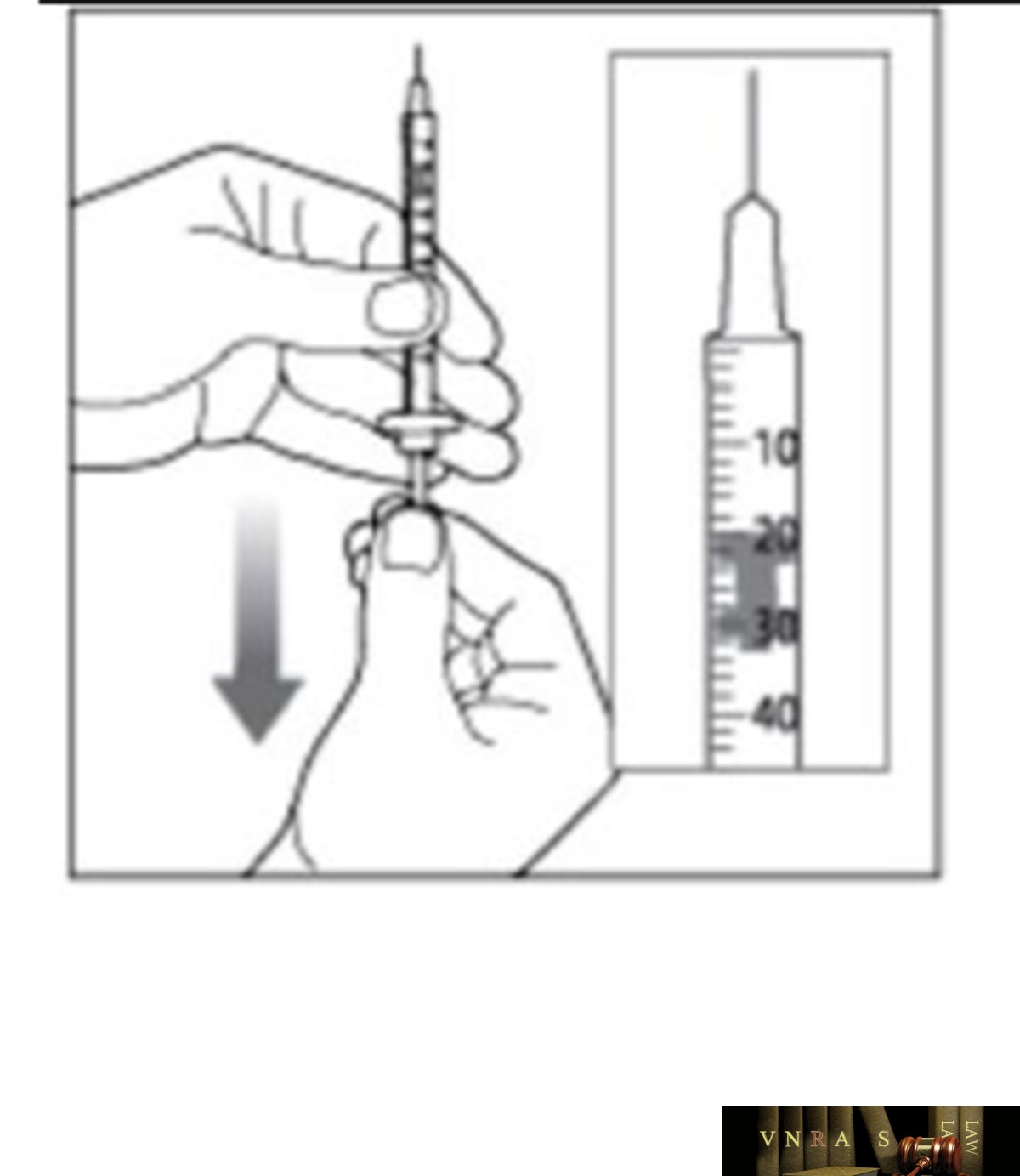 |
|
| 5. | Đâm kim tiêm xuyên qua nút cao su | 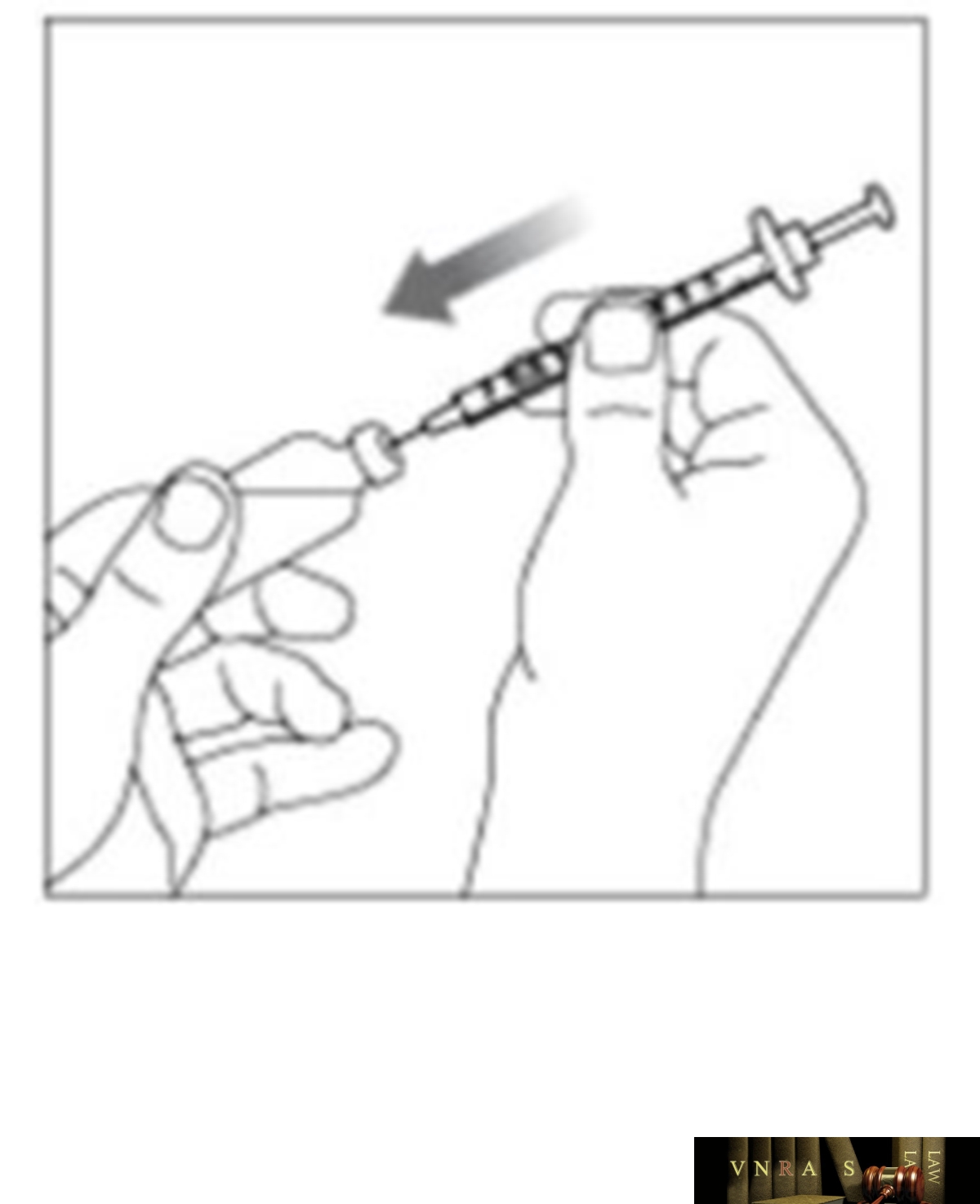 |
|
| 6. | Đẩy pít-tông hoàn toàn vào trong, đưa không khí vào trong lọ thuốc |
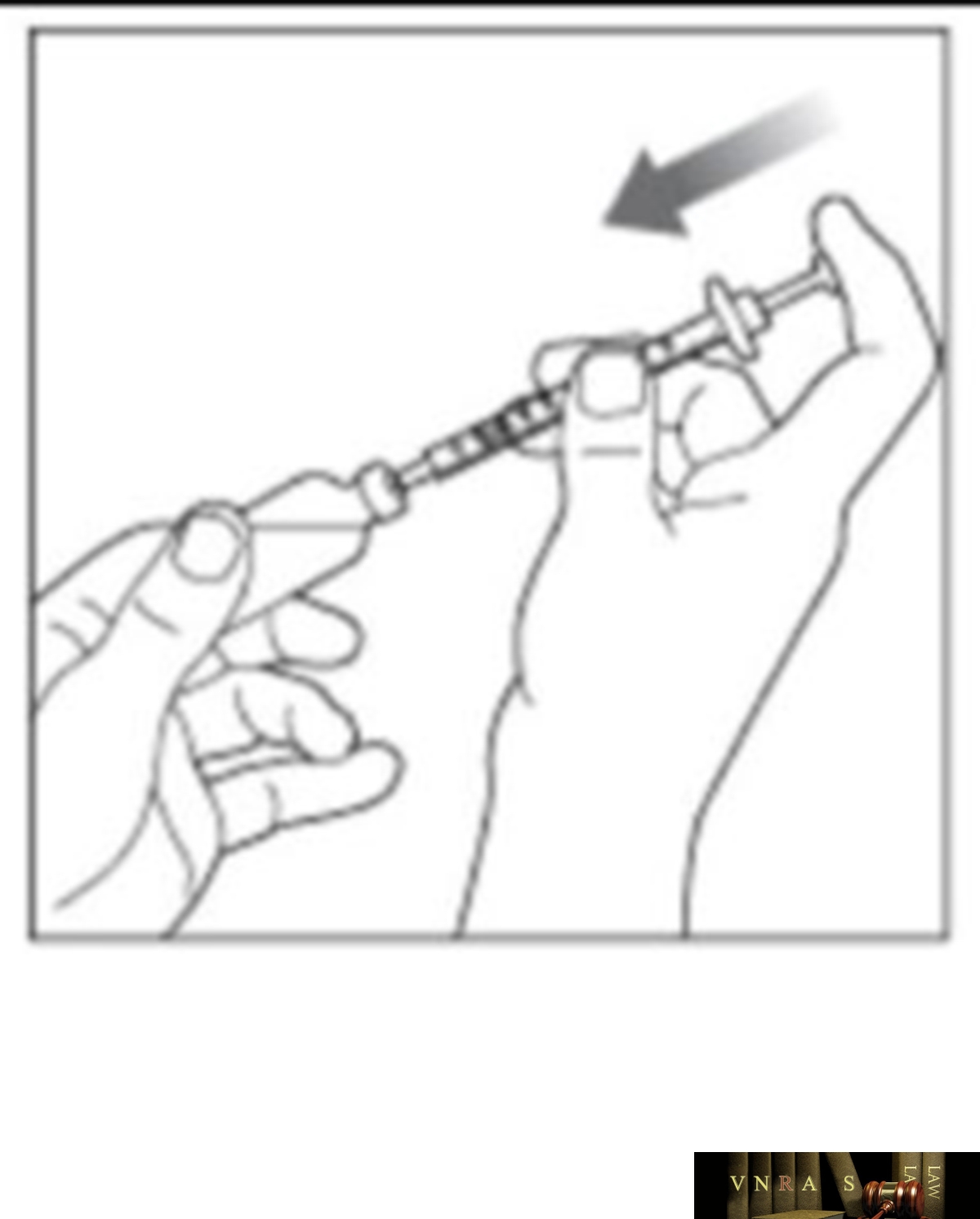 |
|
| 7. | Xoay ngược lọ thuốc và bơm tiêm, từ từ kéo pít-tông xuống cho đến khi đầu pít-tông vượt qua 3-4 đơn vị liều lượng được chỉ định Ví dụ: liều chỉ định là 20 đơn vị, kéo pít- tông đến khi đầu pít- tông đạt vạch 24 đơn vị Nếu có bọt khí trong ống tiêm, hãy vỗ nhẹ vào ống tiêm một vài lần để đẩy bọt khí lên đầu xi lanh |
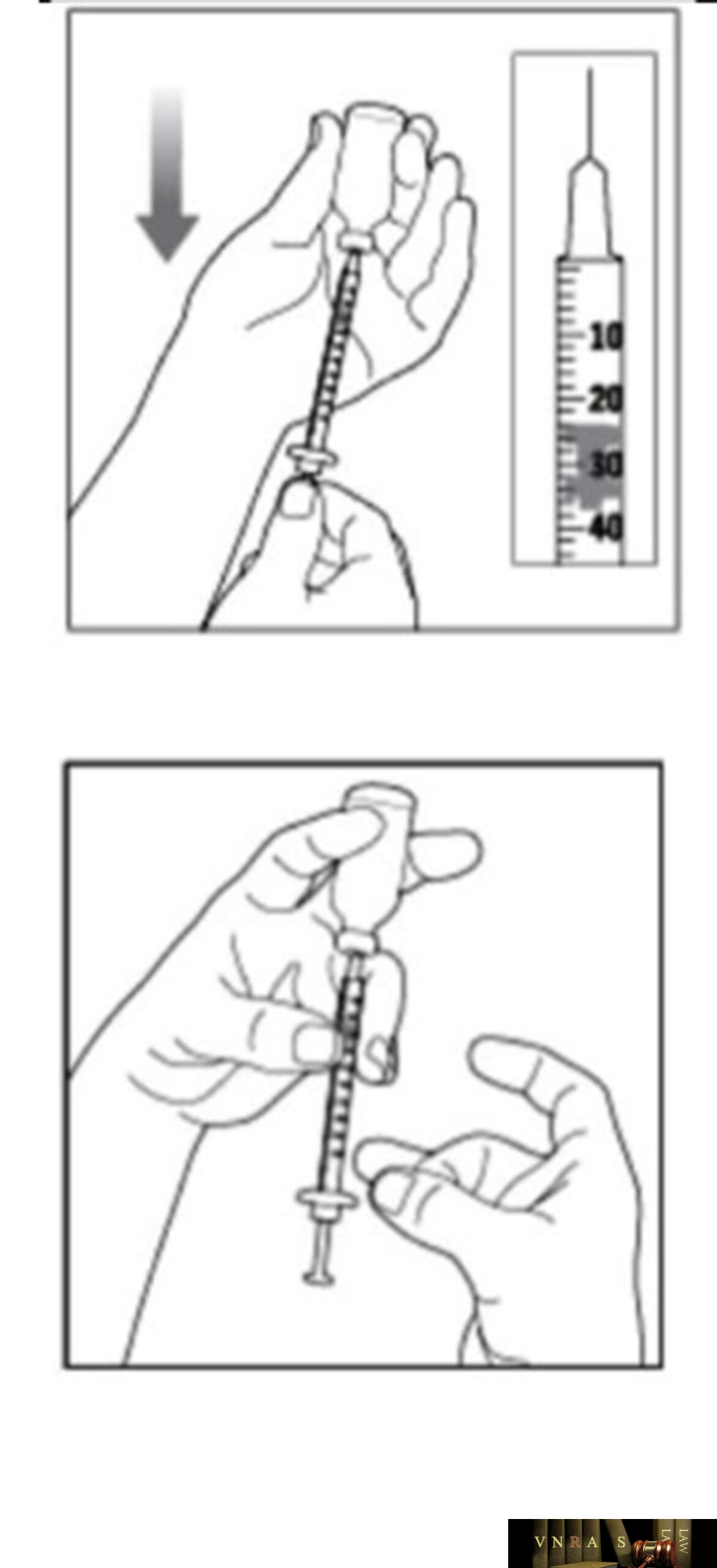 |
|
| 8. | Từ từ đẩy pít-tông lên cho đến khi đầu pít-tông đạt đến vạch số đơn vị liều lượng được chỉ định Ví dụ: 20 đơn vị |
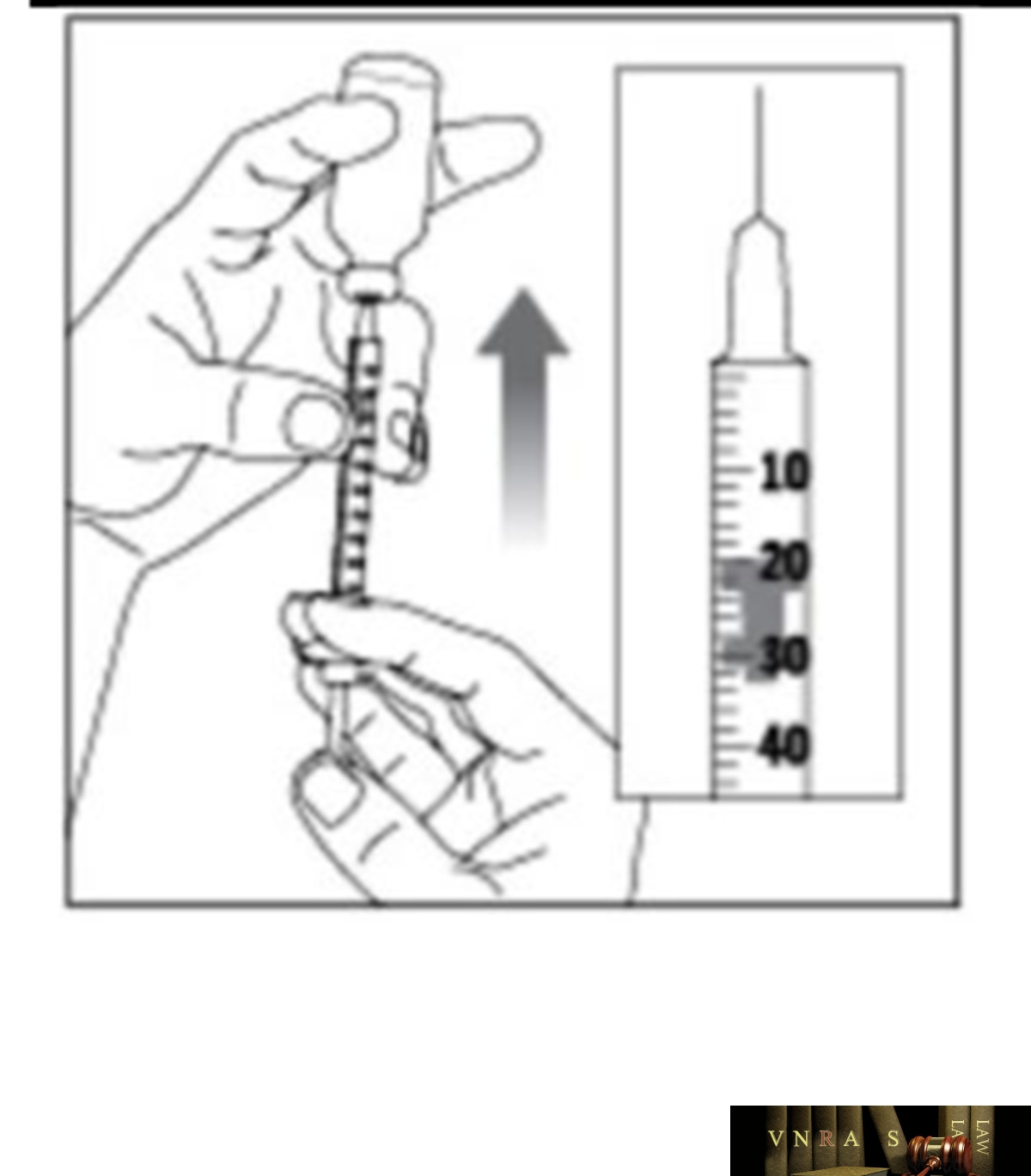 |
|
| 9. | Rút bơm tiêm khỏi lọ thuốc Lưu ý Phải hỏi bác sĩ nếu phải trộn các loại insulin Thay đổi vị trí tiêm mỗi lần tiêm |
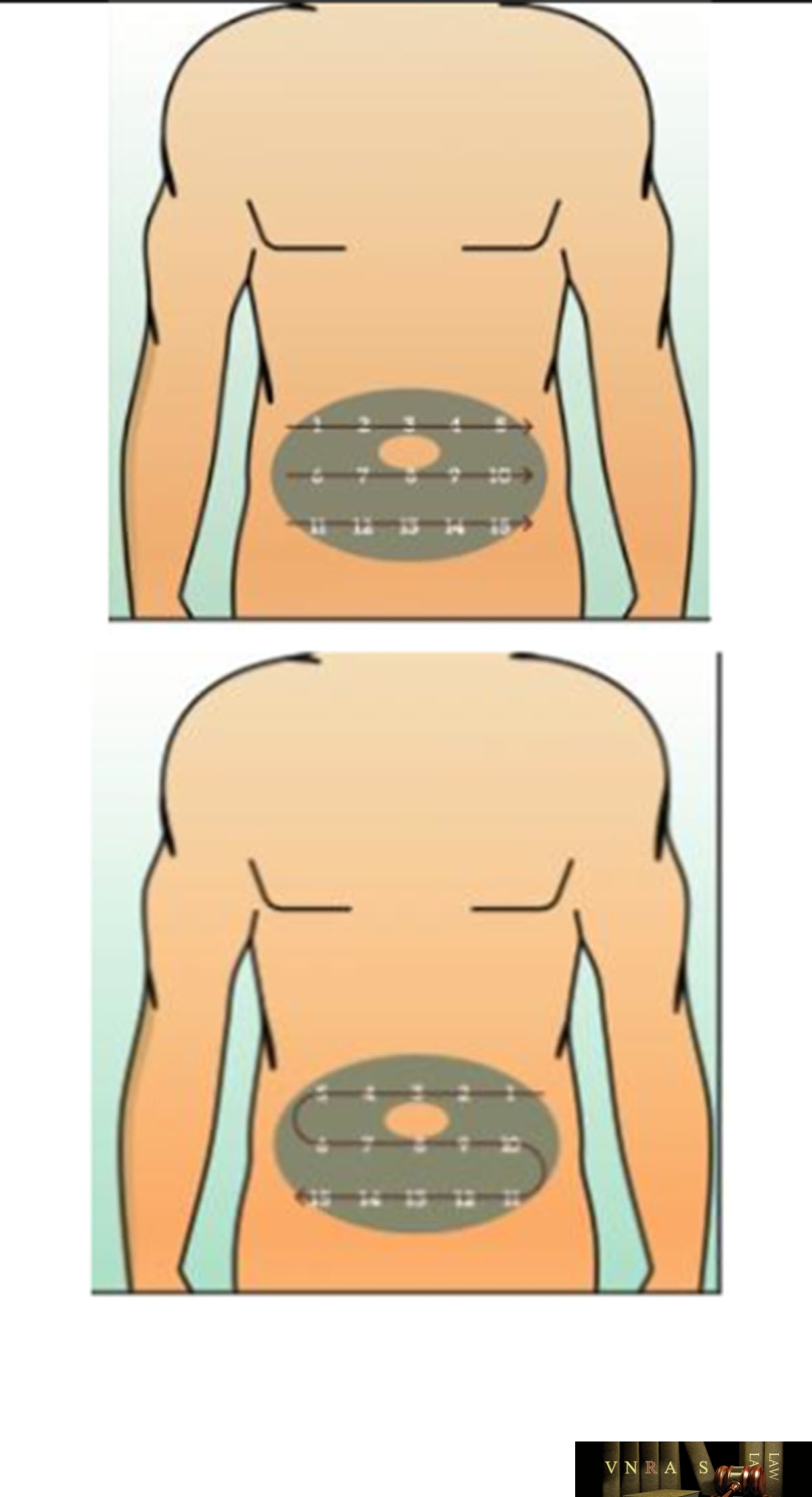
Ví dụ các cách thay đổi vị trí tiêm mỗi lần tiêm |
|
| 10. | Chọn vị trí tiêm Có thể tiêm dưới da vùng bụng mông, đùi hoặc cánh tay trên. Lau sạch da bằng bông alcohol. Hãy để chỗ tiêm khô trước khi tiêm thuốc |
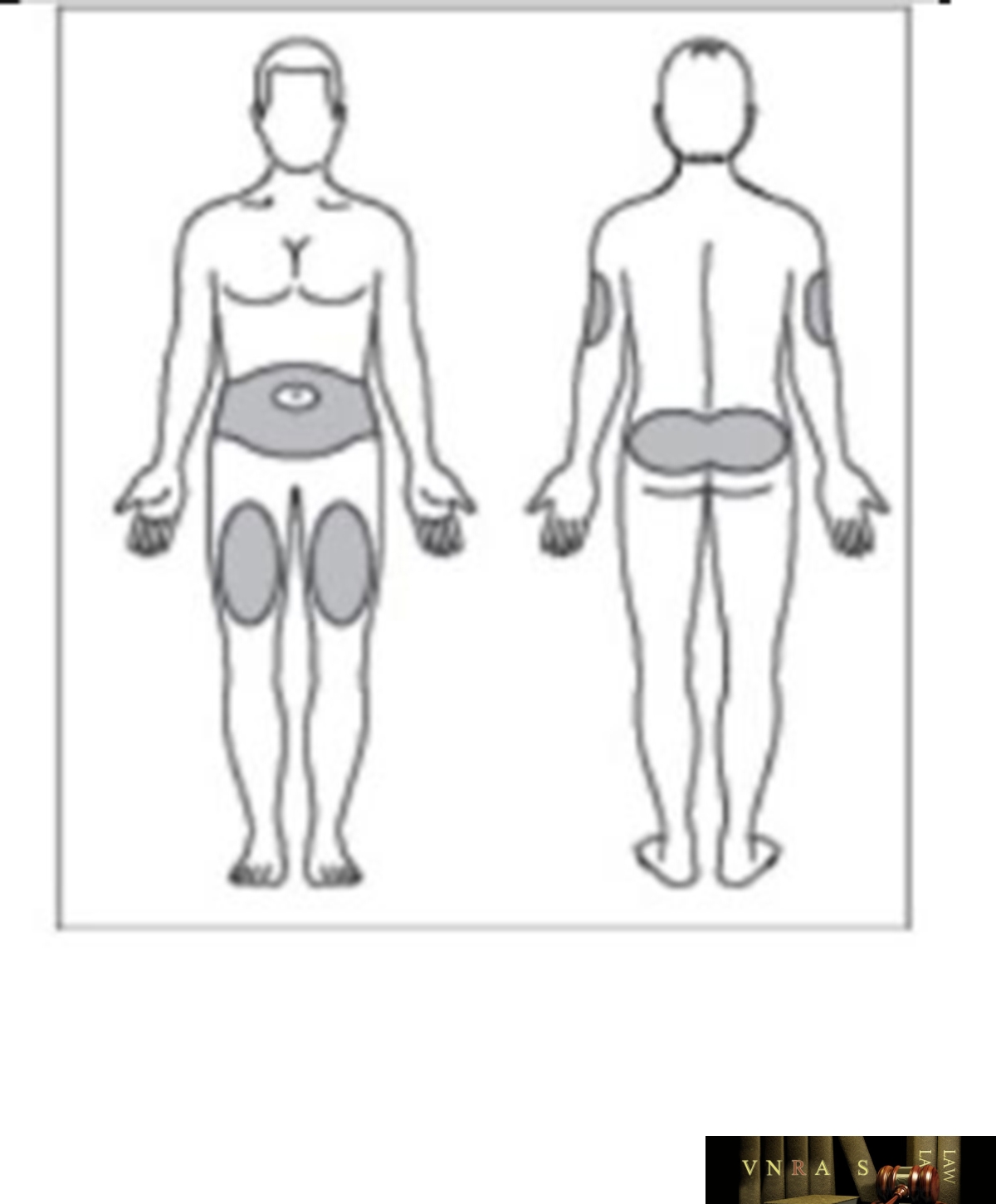 |
|
| 11. | Đưa kim tiêm vào da (tiêm dưới da) | 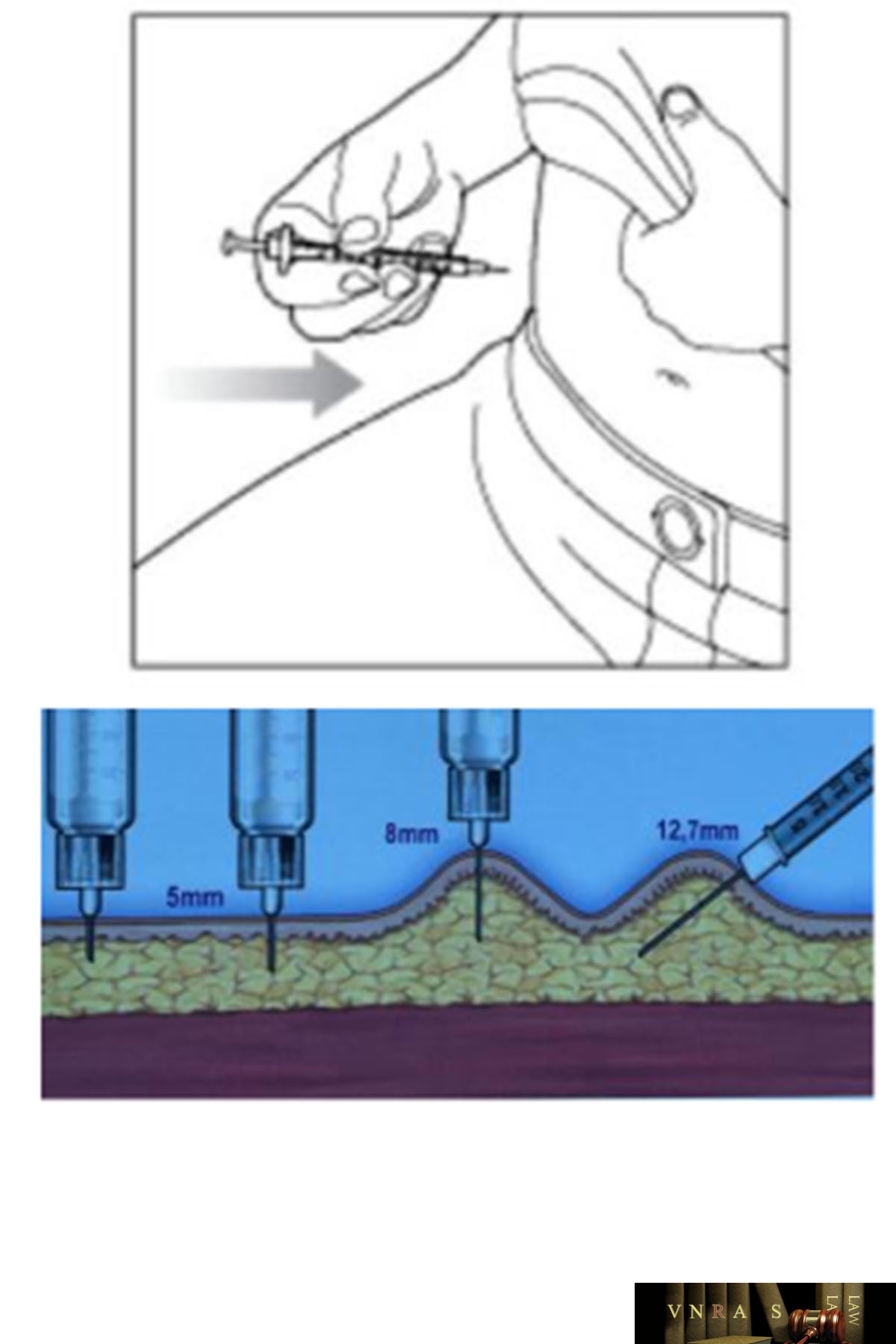 |
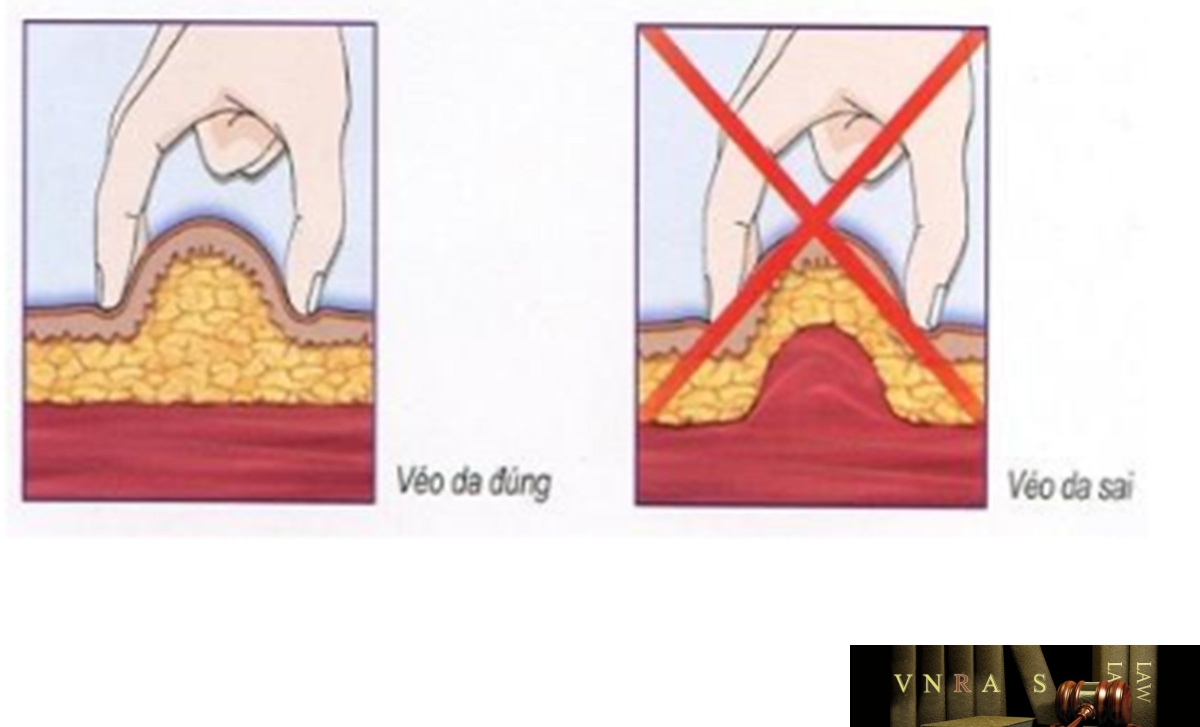
Nên véo da để đảm bảo |
| 12. | Đẩy pít-tông xuống Giữ kim tiêm trong da trong ít nhất 5 giây để chắc chắn rằng đã tiêm đủ liều insulin |
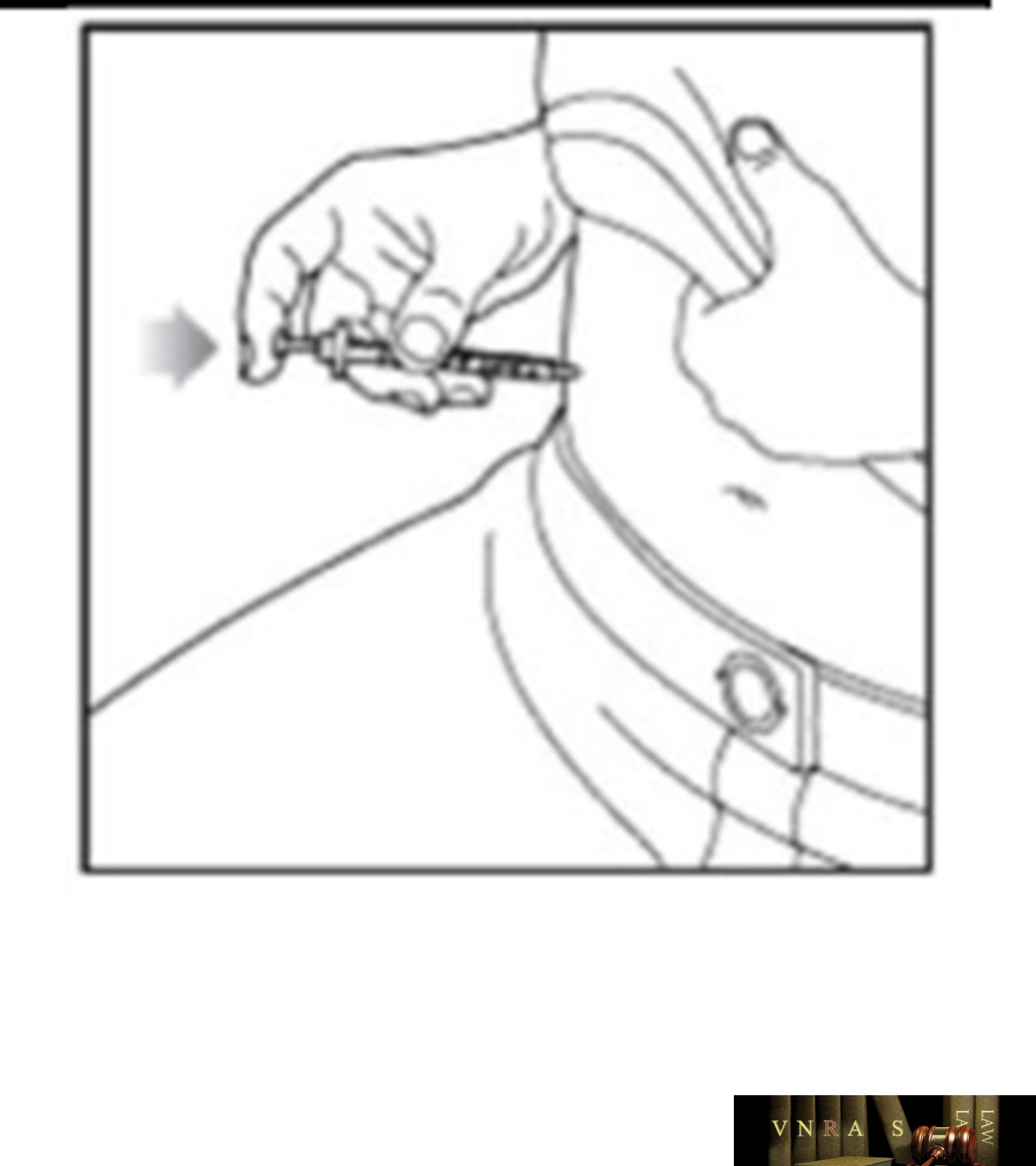 |
|
| 13. | Rút kim tiêm ra khỏi da Có thể thấy một giọt insulin ở đầu kim. Điều này là bình thường và không ảnh hưởng đến liều nhận được. Nếu thấy máu sau khi lấy kim ra khỏi da, hãy ấn chỗ tiêm bằng bông alcohol. KHÔNG chà xát, xoa bóp quanh chỗ tiêm Huỷ kim an toàn |
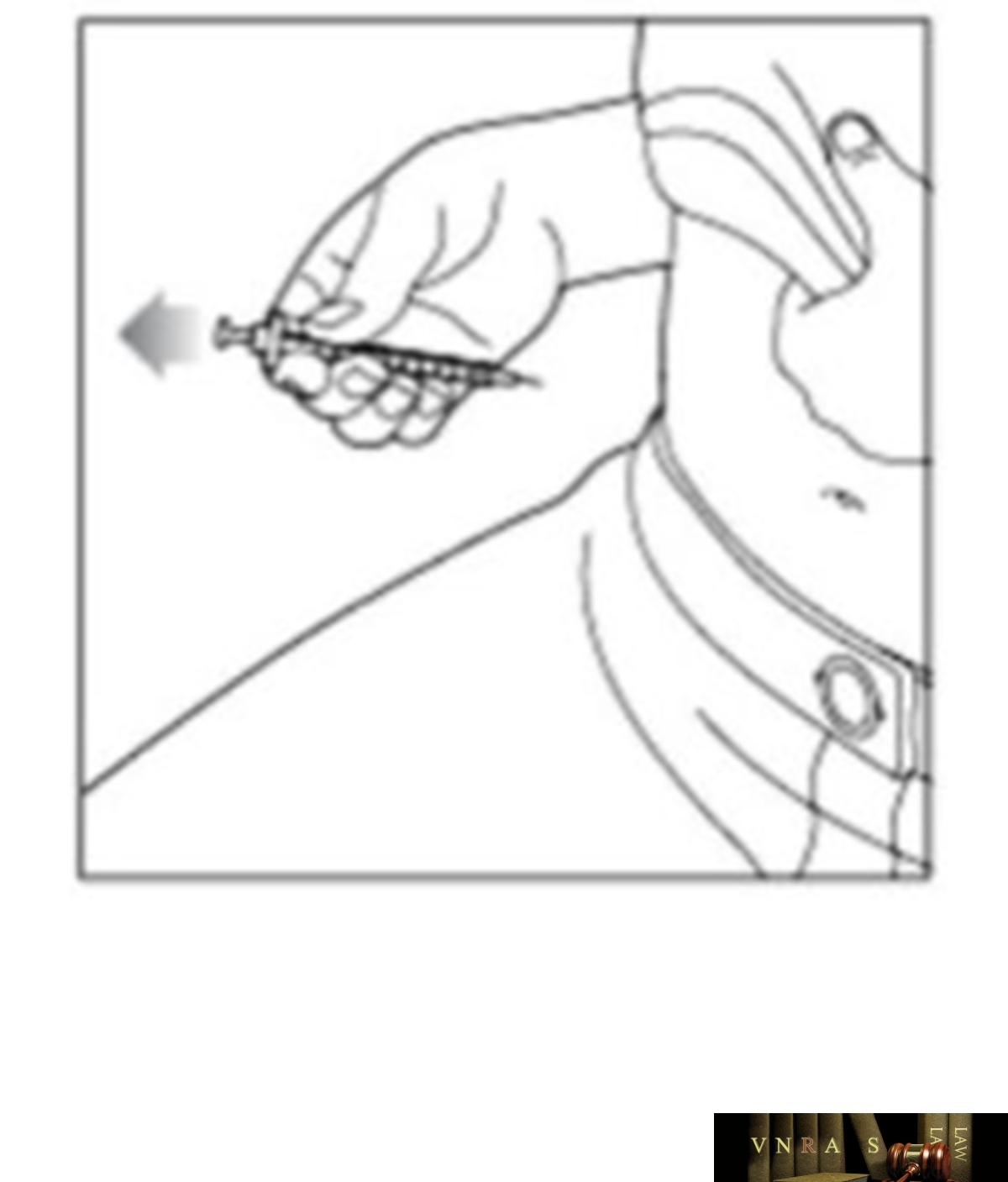 |
Phụ lục 2.4. Hướng dẫn sử dụng insulin dạng bút tiêm
Căn cứ theo thông tin kê toa thuốc (bút Novolet, Kwikpen, Solostar, Flexpen,
Flextouch)
Ví dụ: Tresiba® (insulin degludecflextouch) cập nhật tháng 09/2015, truy cập
03/12/2018
| Bước |
Nội dung | Hình ảnh | Chú ý chung cho các loại insulin |
Cấu tạo bút tiêm flextouch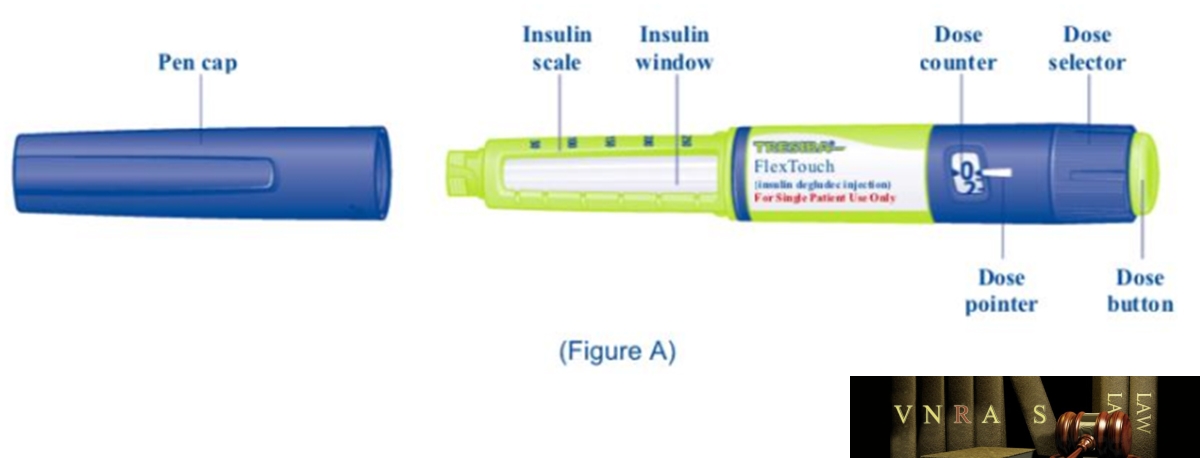 |
|||
| 1. | Kéo thẳng nắp bút Dung dịch trong suốt và không màu. KHÔNG sử dụng dung dịch bị đục, nhày, có màu hoặc có vật lạ. | 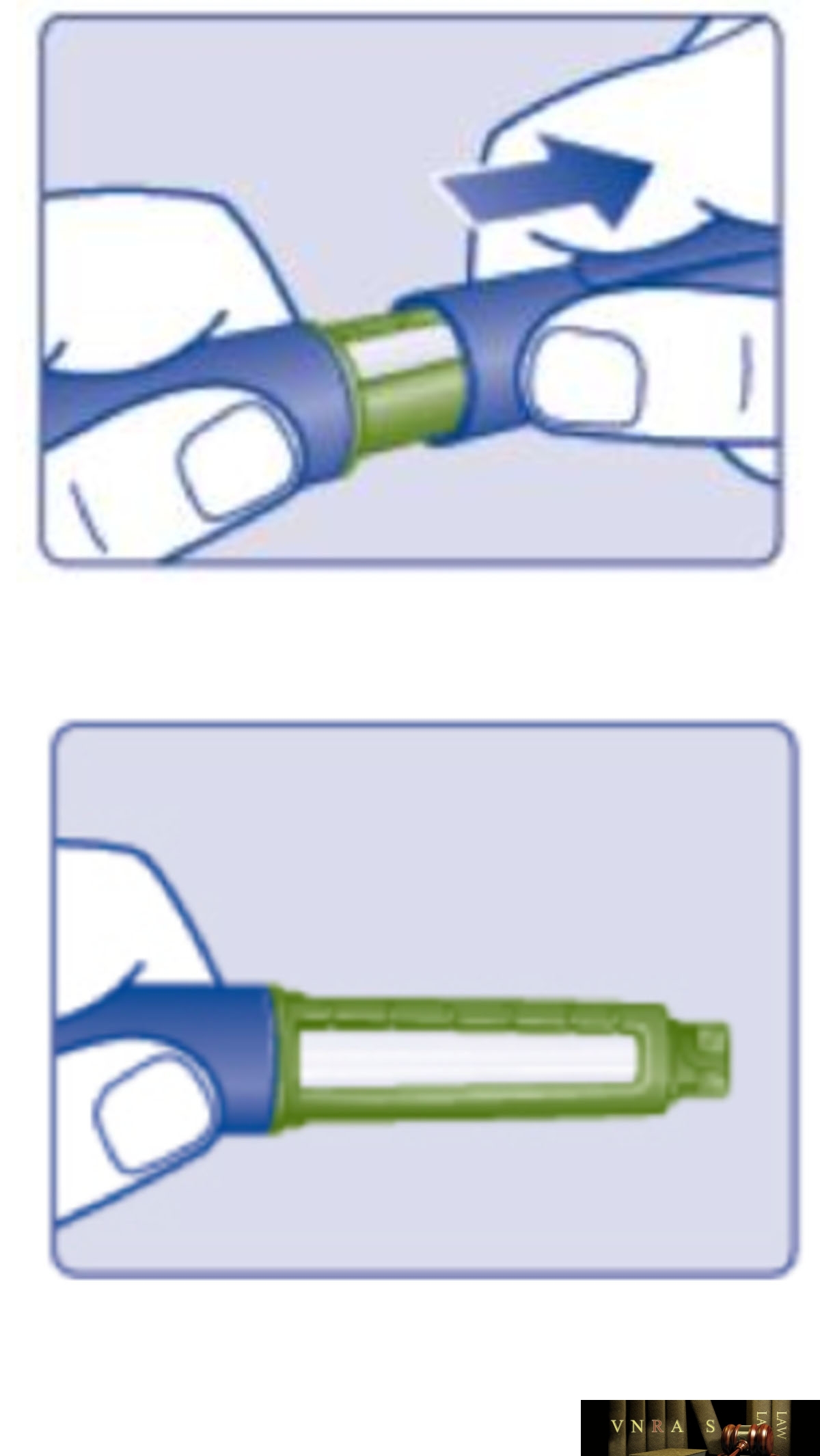 |
Insulin có thành phần protamin sẽ có dạng hỗn dịch đục Hỗn dịch bắt buộc phải làm đồng nhất để đảm bảo đúng liều lượng – Bước 1: Xoay tròn ít nhất 10 lần trong lòng bàn tay – Bước 2: Di chuyển bút lên xuống ít nhất 10 lần Hỗn dịch phải có màu trắng đục. KHÔNG sử dụng nếu lọ thuốc trong và có hạt lạ 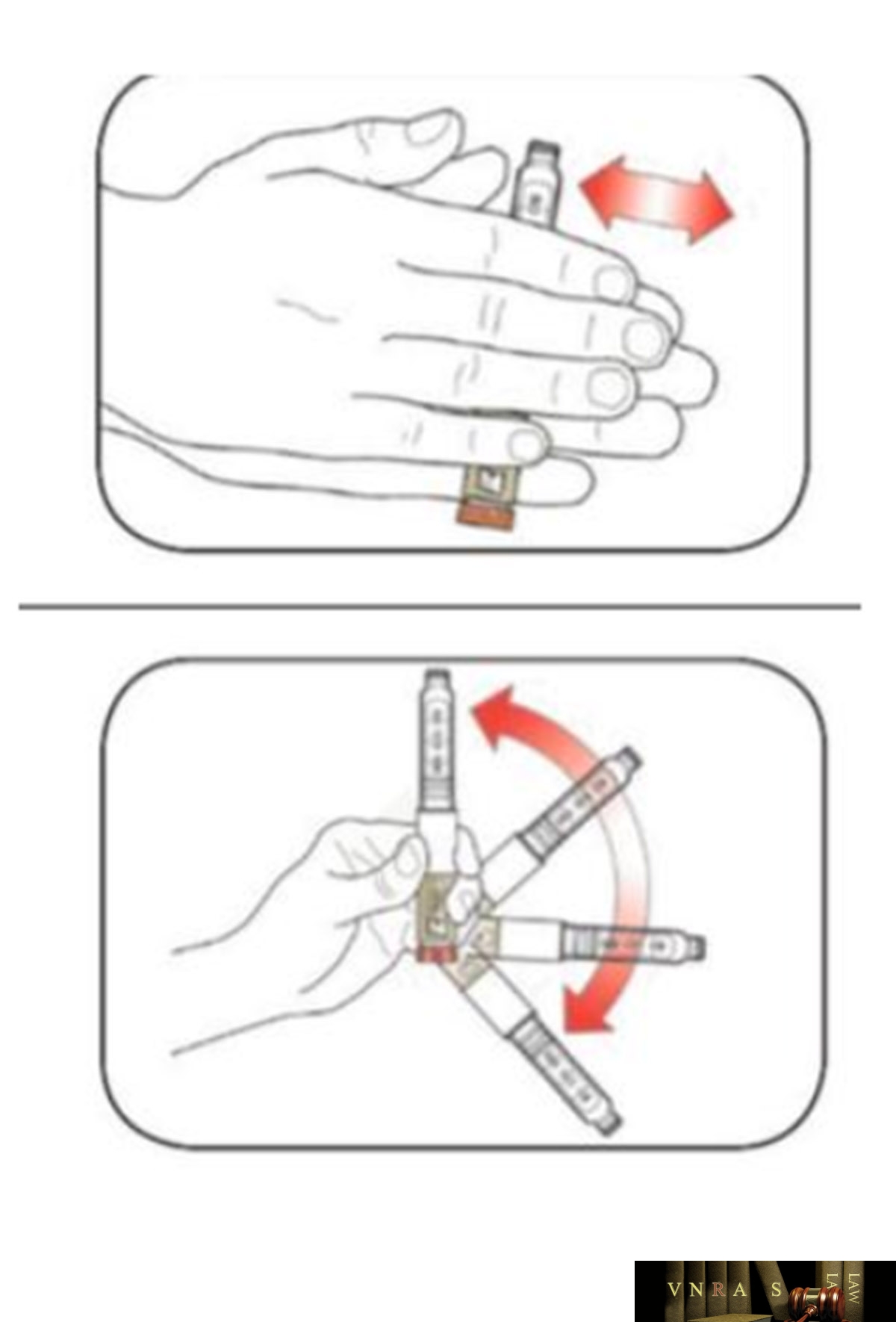 |
| 3. | Chọn một cây kim mới Kéo miếng bảo vệ ra khỏi nắp kim ngoài |
 |
|
| 4. | Đưa kim tiêm vào thẳng bút và vặn chặt kim | 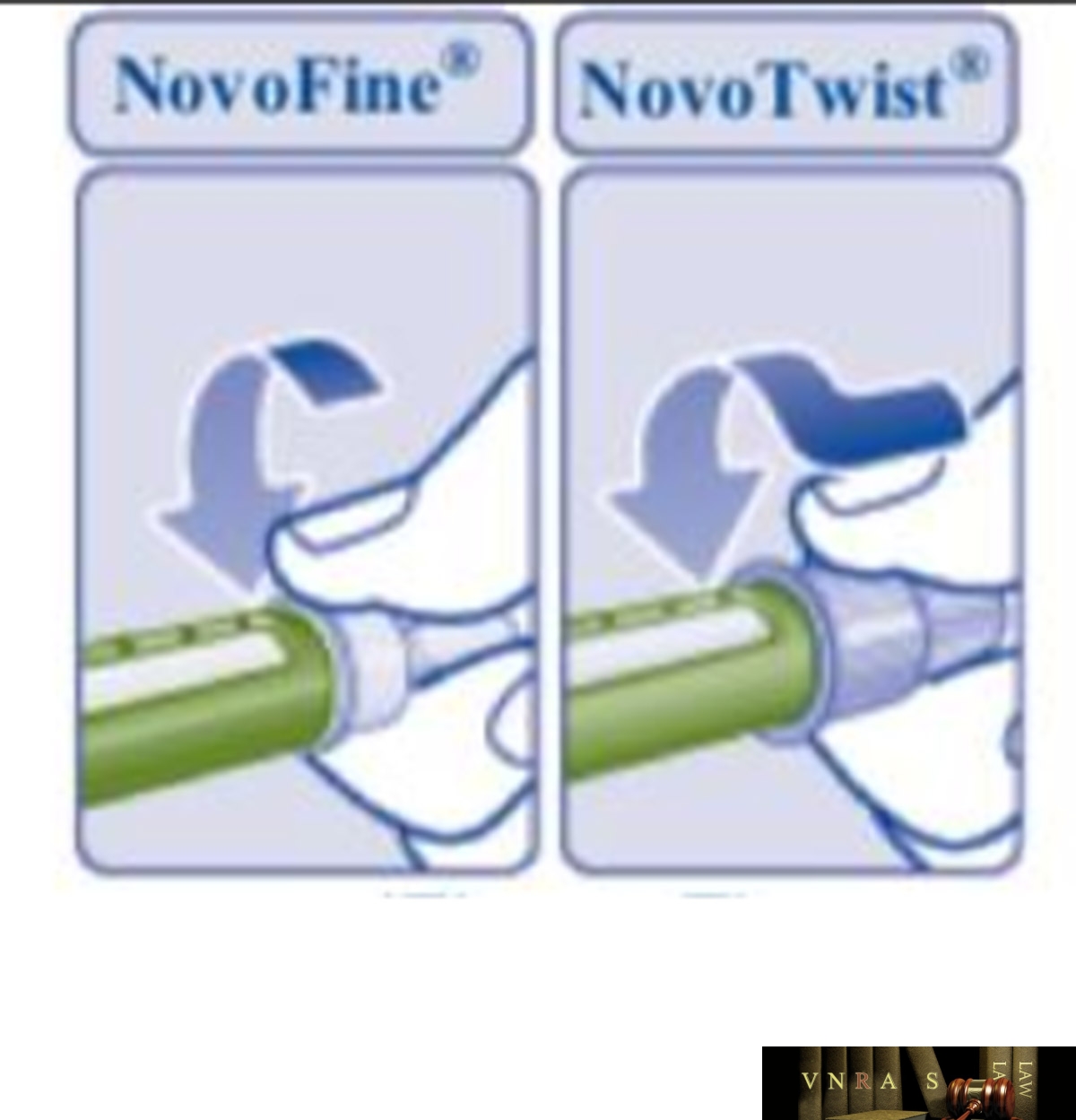 |
|
| 5. | Kéo nắp kim ngoài ra. KHÔNG vứt bỏ | 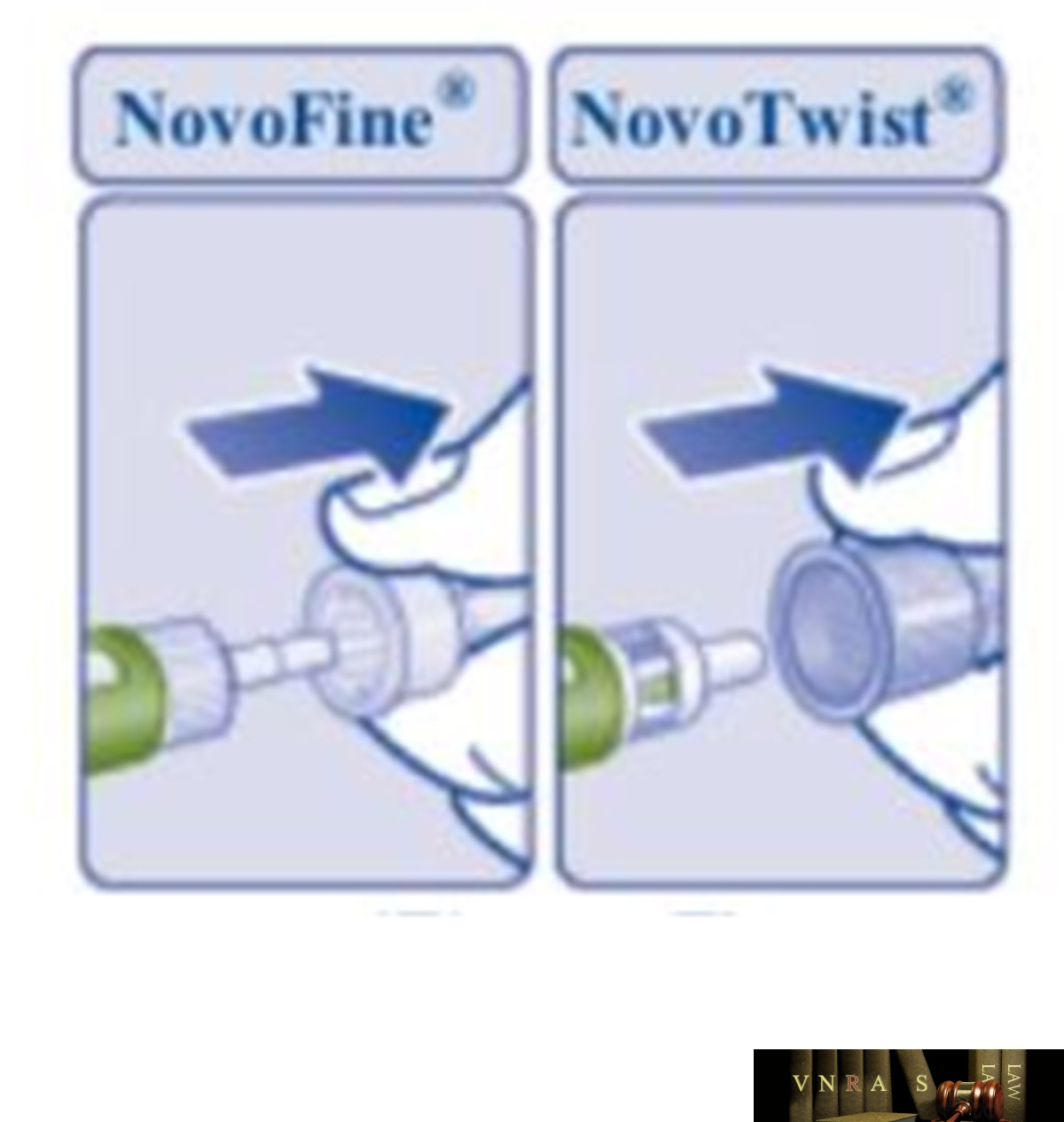 |
|
| 6. | Kéo nắp kim trong ra và vứt đi |
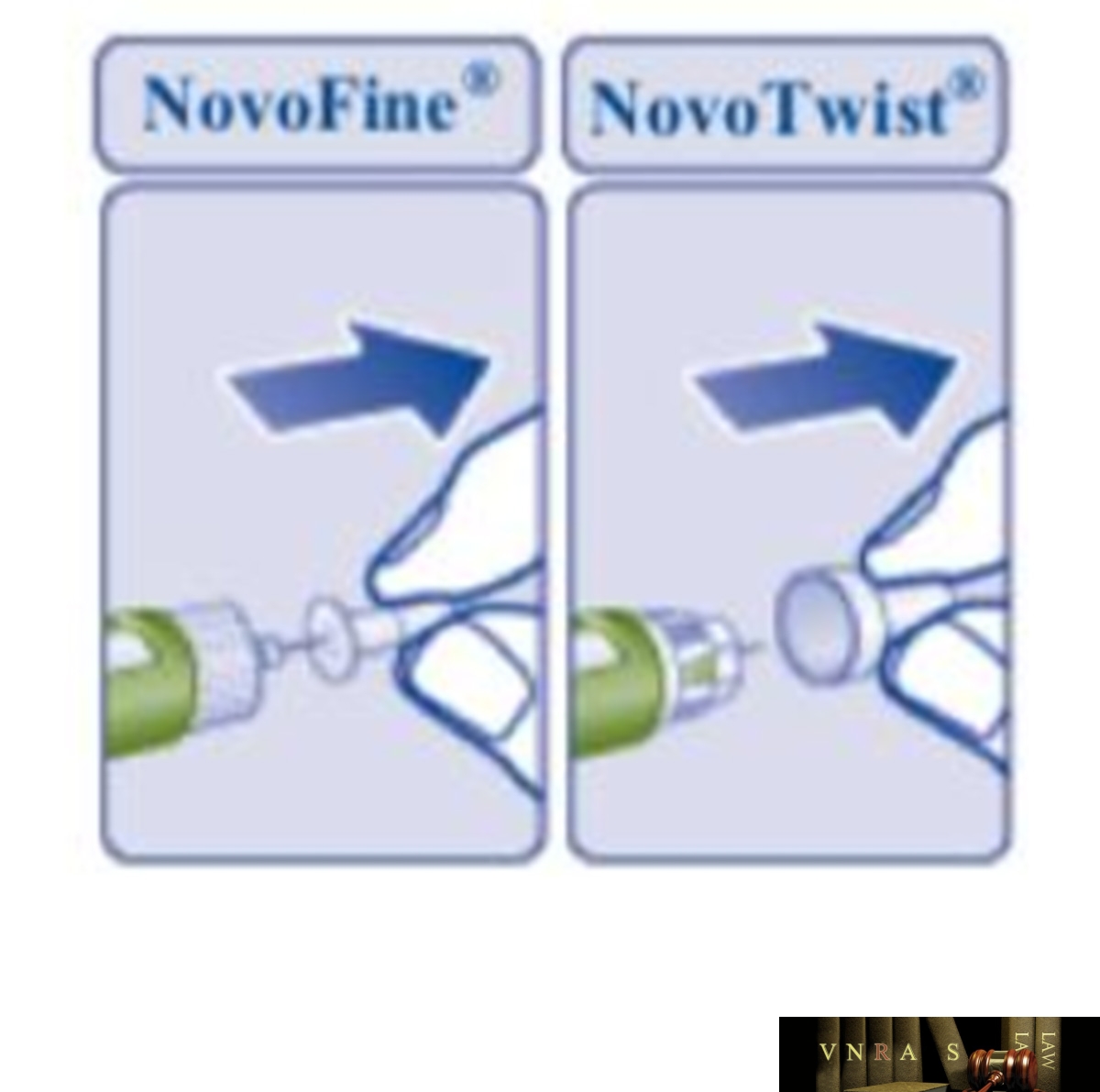 |
|
| 7. | Xoay nút chọn liều tiêm để chọn 2 đơn vị |
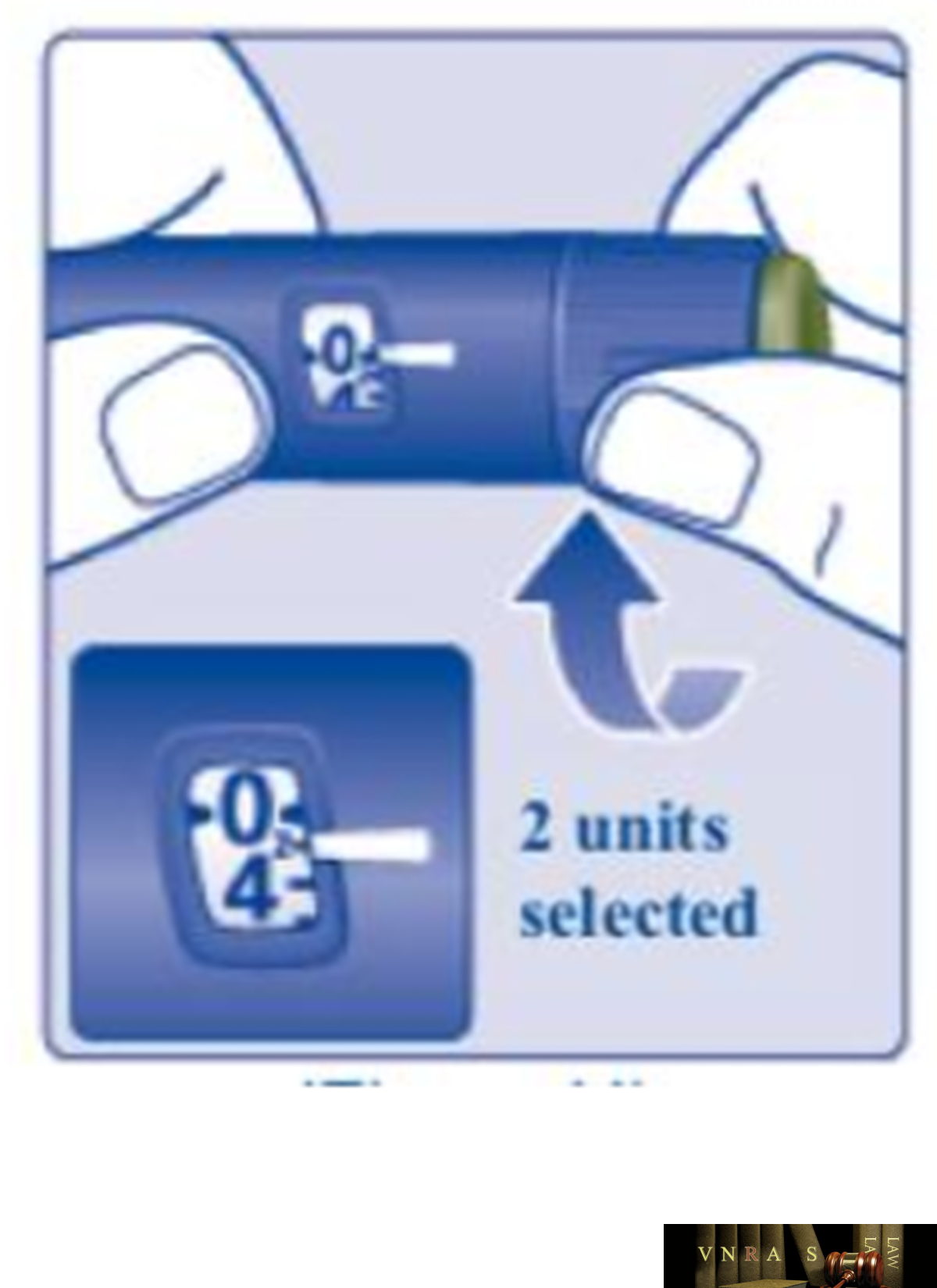 |
|
| 8. | Giữ bút cho kim hướng lên trên, gõ nhẹ ống thuốc vài lần để bọt khí di chuyển lên đỉnh ống thuốc. | 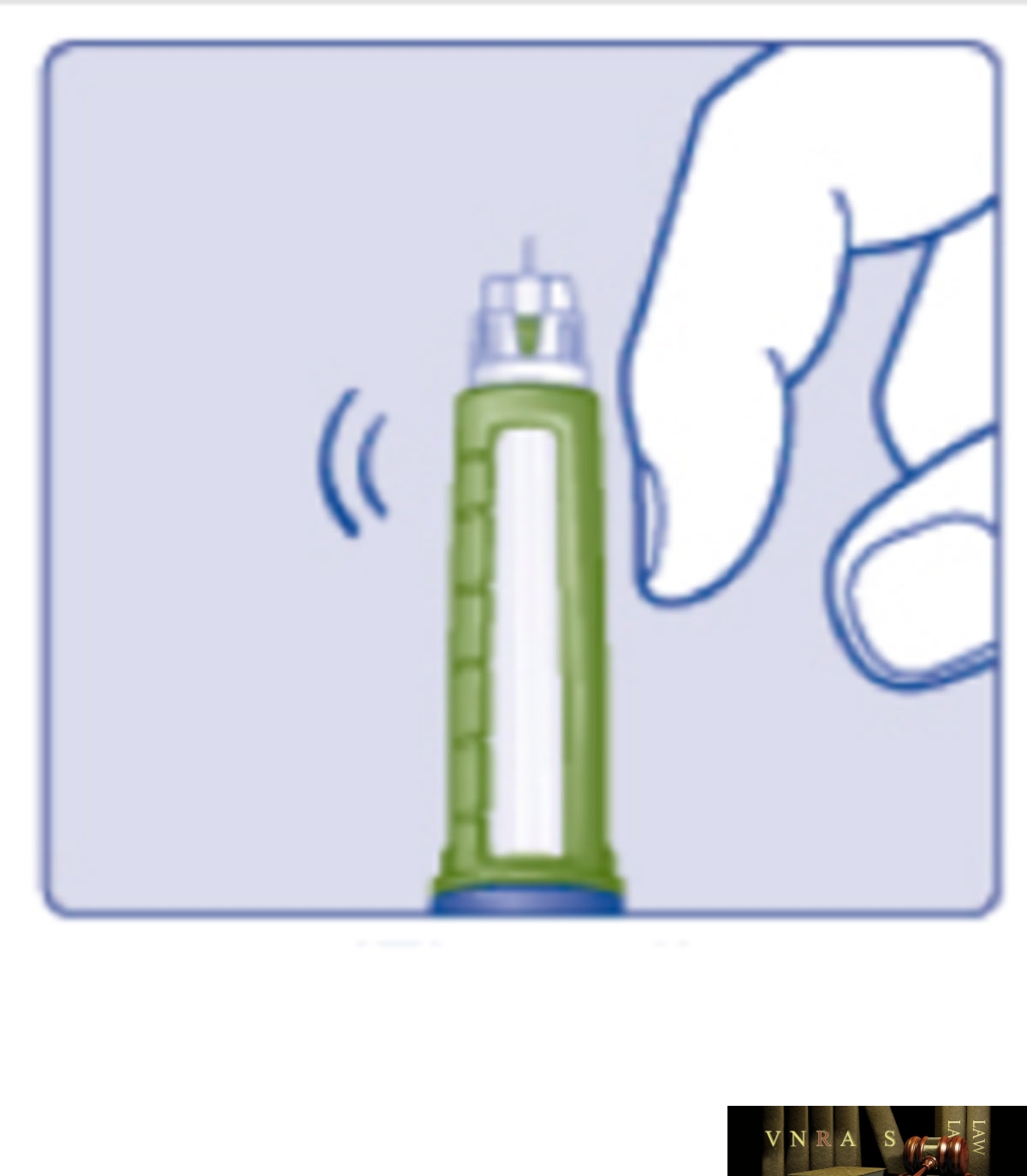 |
|
| 9. | – Giữ bút cho kim hướng lên trên. Nhấn và giữ nút liều xuống hết cỡ, nút chọn liều tiêm trở về 0 – Sẽ có một giọt insulin ở đầu kim + Nếu không thấy một giọt insulin, hãy lặp lại các bước từ đến 9, không quá 6 lần. + Nếu vẫn không thấy một giọt insulin, hãy thay kim và lặp lại các bước từ đến 9. |
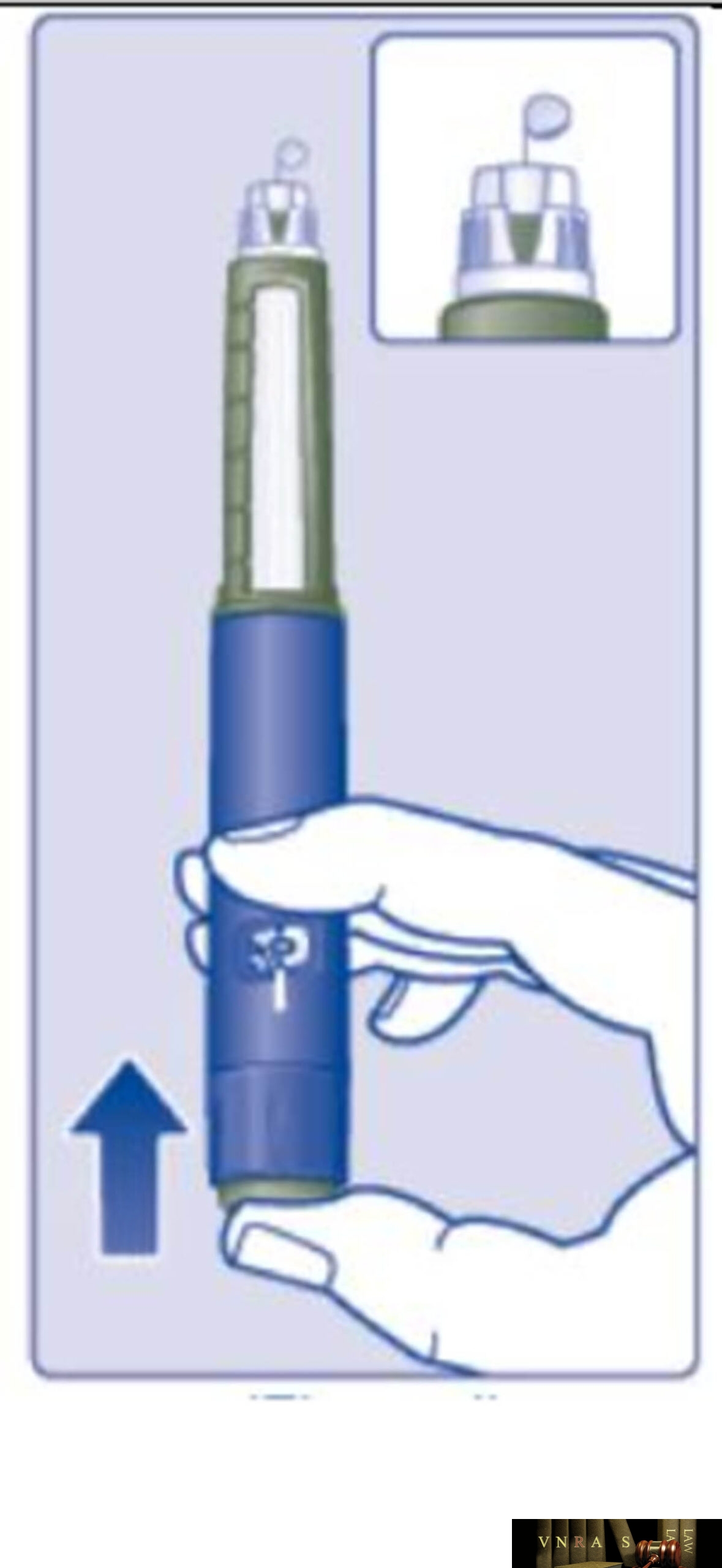 |
|
| 10. | Chọn liều: Kiểm tra bộ chọn liều được đặt ở 0. Xoay bộ chọn liều để chọn số lượng đơn vị bạn cần tiêm. Các con trỏ liều ngang với liều được chọn + Nếu chọn liều lượng sai, có thể xoay tới hoặc xoay ngược về liều đúng + Các số chẵn được in trên mặt số + Các số l được hiển thị dưới dạng gạch dòng – Bút có hiển thị số đơn vị còn lại như hình bên |
 |
|
| 11. | Chọn vị trí tiêm Có thể tiêm dưới da vùng bụng mông, đùi hoặc cánh tay trên. Lau sạch da bằng bông alcohol. Hãy để chỗ tiêm khô trước khi tiêm thuốc | 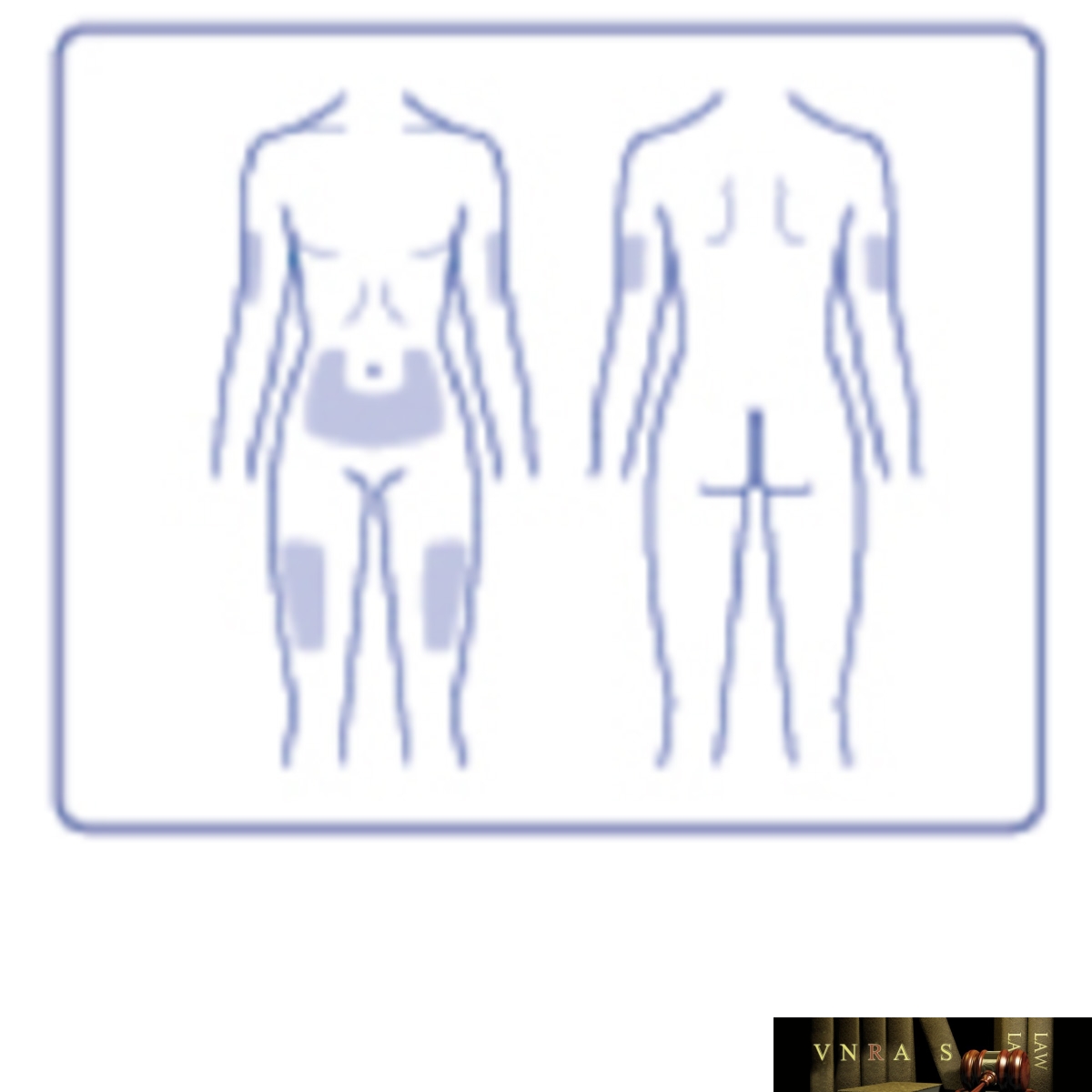 |
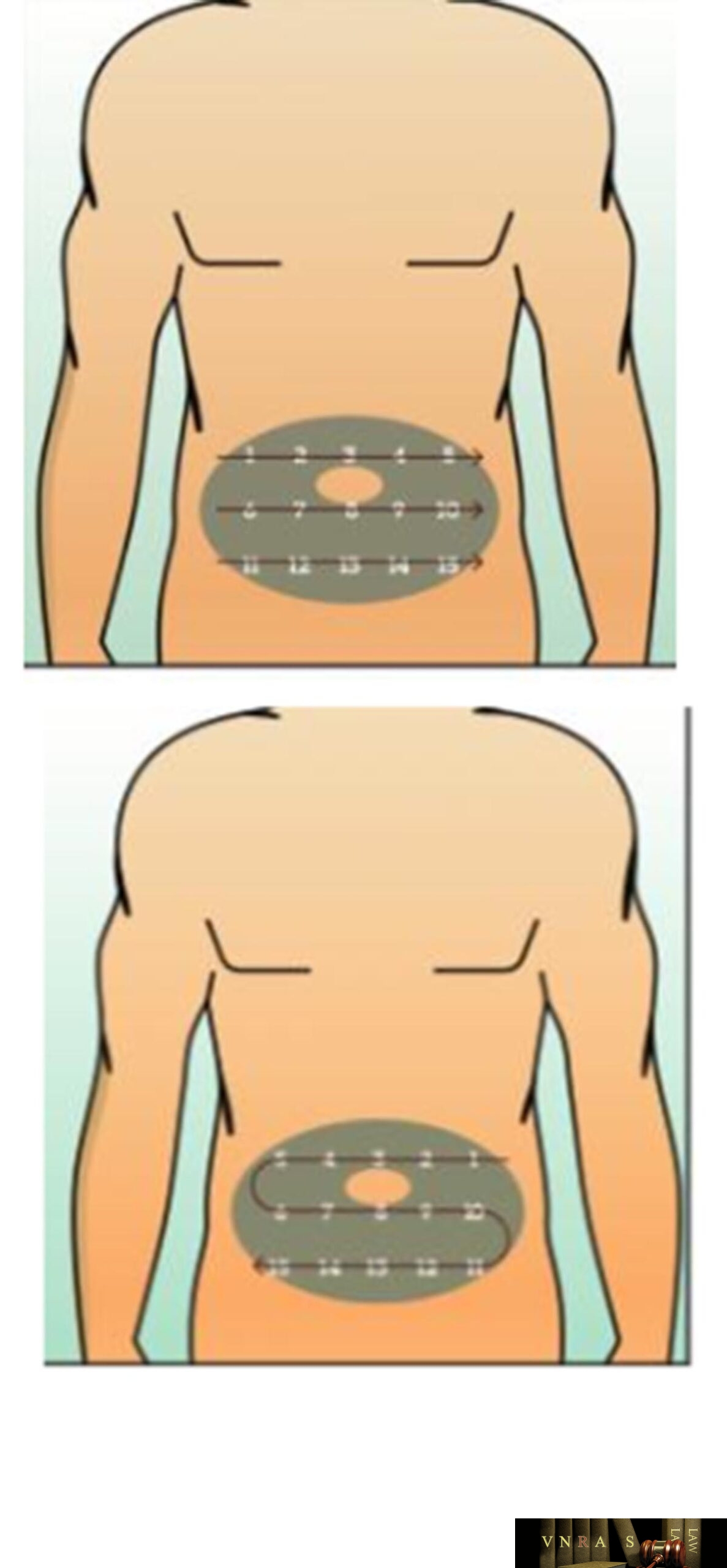
Ví dụ các cách thay đổi vị trí tiêm mỗi lần tiêm |
| 12. | Đưa kim vào da Đảm bảo có thể thấy bộ đếm liều. Không che bằng ngón tay vì có thể ngăn chặn quá trình tiêm | 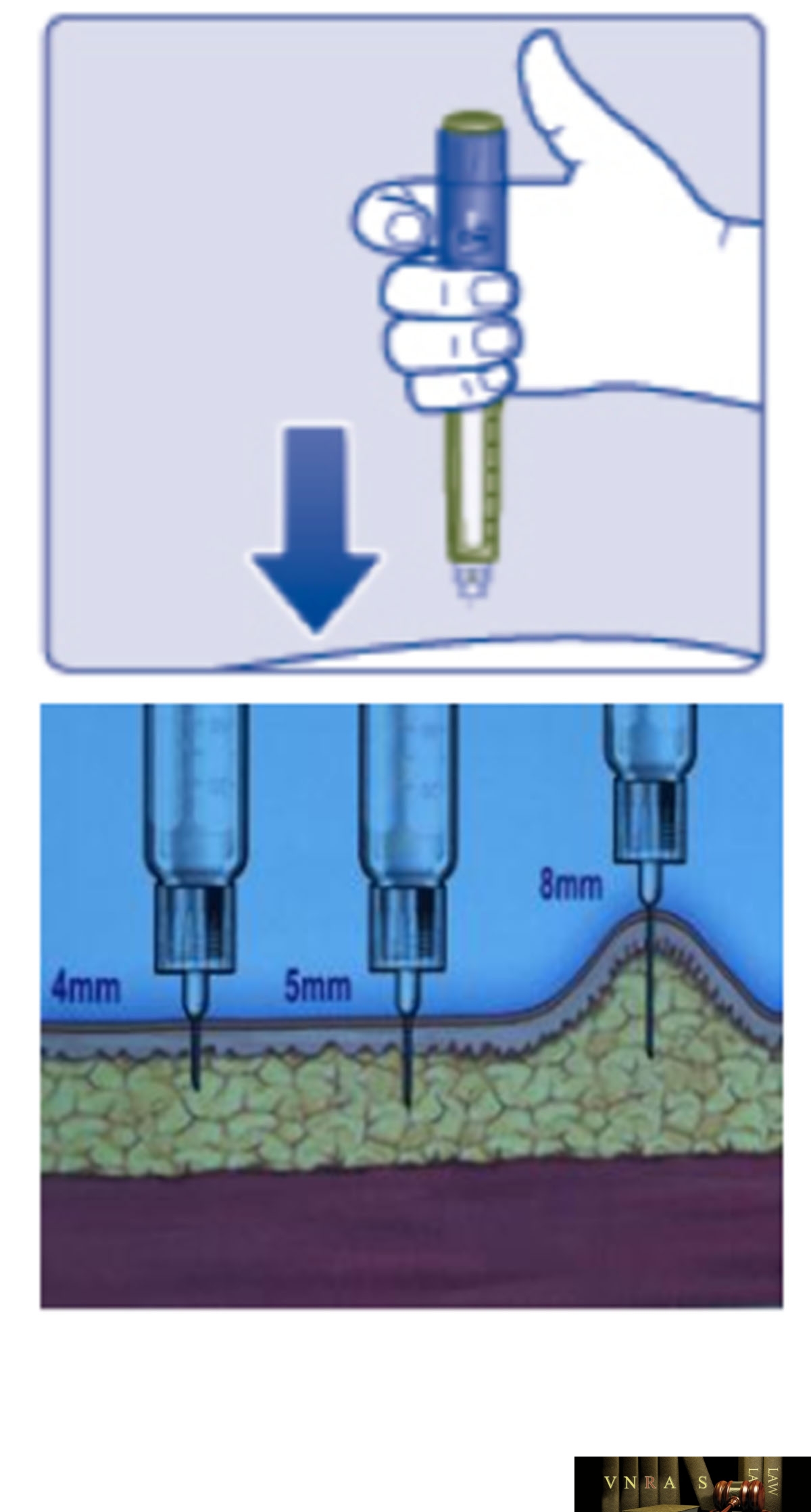 |
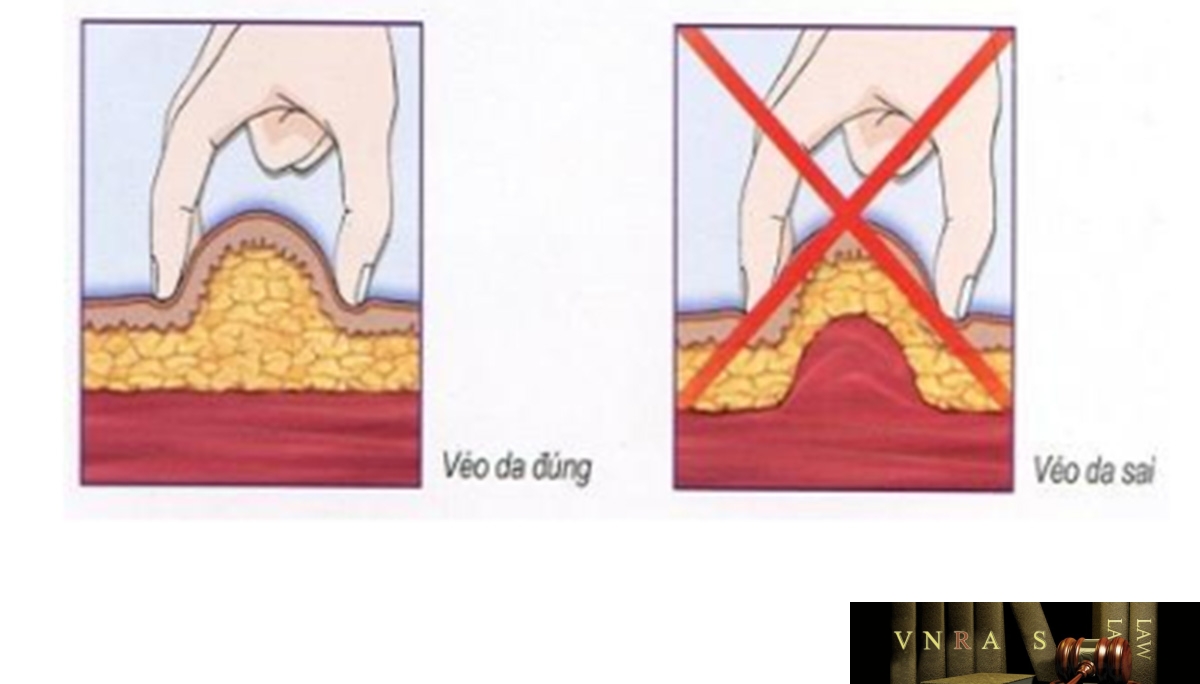
Nên véo da để đảm bảo thuốc không vào lớp cơ |
| 13. | Nhấn và giữ nút liều cho đến khi bộ đếm liều hiển thị “0 ” + “0” phải ngang với con trỏ liều, có thể nghe hoặc cảm thấy tiếng “tách” Giữ kim trong da sau khi bộ đếm liều đã trở về “0” và từ từ đếm đến để đảm bảo đủ liều insulin | 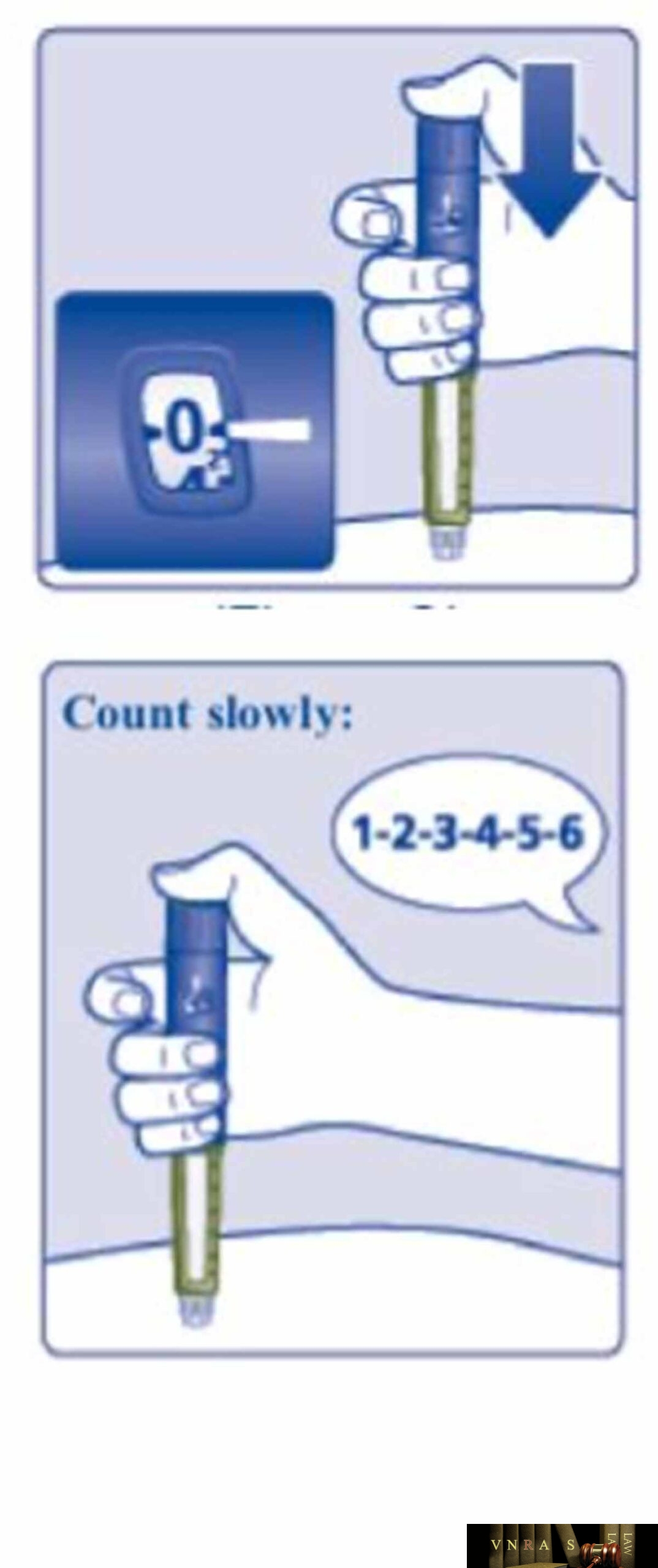 |
|
| 14. | Rút kim tiêm ra khỏi da Có thể thấy một giọt insulin ở đầu kim. Điều này là bình thường và không ảnh hưởng đến liều nhận được. Nếu thấy máu sau khi lấy kim ra khỏi da, hãy ấn chổ tiêm bằng bông alcohol. KHÔNG chà xát, xoa bóp quanh chổ tiêm |
 |
|
| 15. | Hủy kim: – Nếu có bình hủy kim (tại bệnh viện) thì không đậy nắp kim lại tránh bị kim đâm vào tay – Nếu người bệnh dùng thuốc thì cẩn thận trọng cho kim vào nắp kim ngoài, hủy kim an toàn |
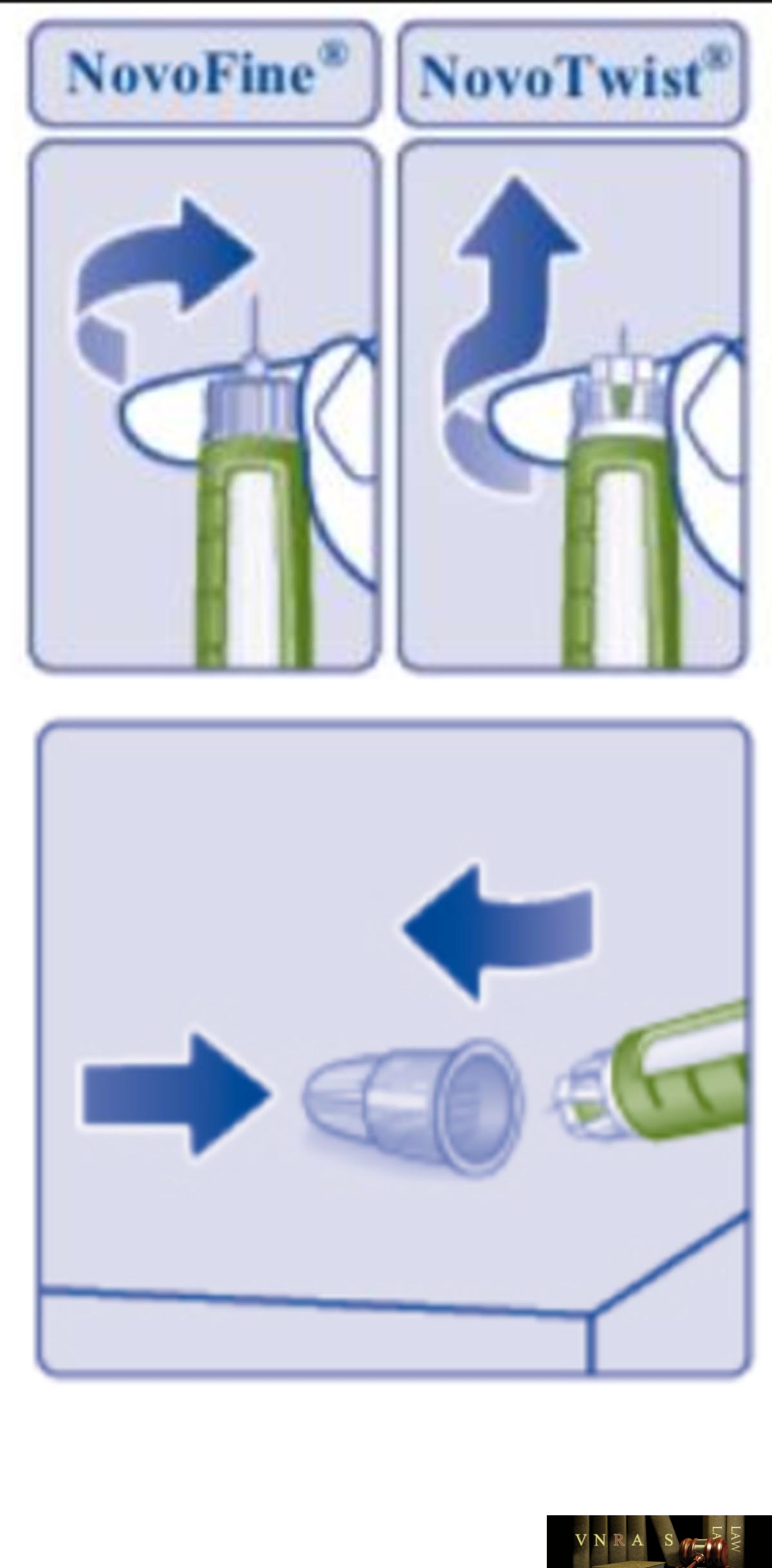 |
|
Phụ lục 2.5. Bảng kiểm tư vấn sử dụng insulin dạng bút tiêm cho người bệnh
| Bước | Nội dung | Tiêu chí đánh giá |
| 1. | Chuẩn bị vật liệu tư vấn:
□ Bút tiêm và kim tiêm insulin □ Bông gòn sát khuẩn □ Thùng đựng rác y tế sắc nhọn □ Hình ảnh/tờ rơi có hình ảnh quy trình kỹ thuật tiêm Insulin □ Tờ rơi phát cho BN sau tư vấn |
Đầy đủ
Đúng tiêu chuẩn |
| 2. | Giới thiệu:
□ Chào hỏi người bệnh □ Tự giới thiệu bản thân □ Nêu mục đích buổi tư vấn |
Thân thiện Tạo lòng tin |
| 3. | Thực hiện nội dung tư vấn:
• Kiểm tra insulin: loại insulin, liều thuốc, thời gian tiêm tùy loại insulin (lưu ý: trước ăn bao nhiêu phút, sáng/ tối) • Hướng dẫn vị trí tiêm insulin và lưu ý thay đổi vị trí tiêm • Hướng dẫn quy trình kỹ thuật tiêm Insulin qua hình ảnh tài liệu • Hướng dẫn bảo quản insulin • Hướng dẫn xử lý rác y tế: đầu kim, bông gòn |
Thông tin đầy đủ và chính xác |
| 4. | Thực hiện kỹ năng:
• Yêu cầu BN tự thực hiện tiêm insulin dưới sự giám sát của nhân viên y tế và điều chỉnh các sai sót của BN |
Thực hiện kỹ năng đúng |
| 5. | Giải đáp thắc mắc của BN (nếu có) | Thông tin đầy đủ và chính xác |
| 6. | Phát các tài liệu giáo dục liên quan cho BN đem về |
Phụ lục 2.6. Bảng kiểm người bệnh ghi lại cách sử dụng insulin dạng bút tiêm
| Bước | Nội dung |
Người bệnh ghi lại thắc mắc |
|||||||||
| 1. | Bạn đánh dấu tick √ sau khi đã kiểm tra 3 nội dung: √ Loại insulin √ Liều insulin √ Thời gian tiêm  |
|
|||||||||
| 2. | A. Bạn đánh dấu tick √ sau khi đã thực hiện từng bước quy trình tiêm insulin (tài liệu kèm theo) B. Bạn ghi số thứ tự vị trí bạn đã tiêm: Luôn luân chuyển, thay đổi vị trí tiêm 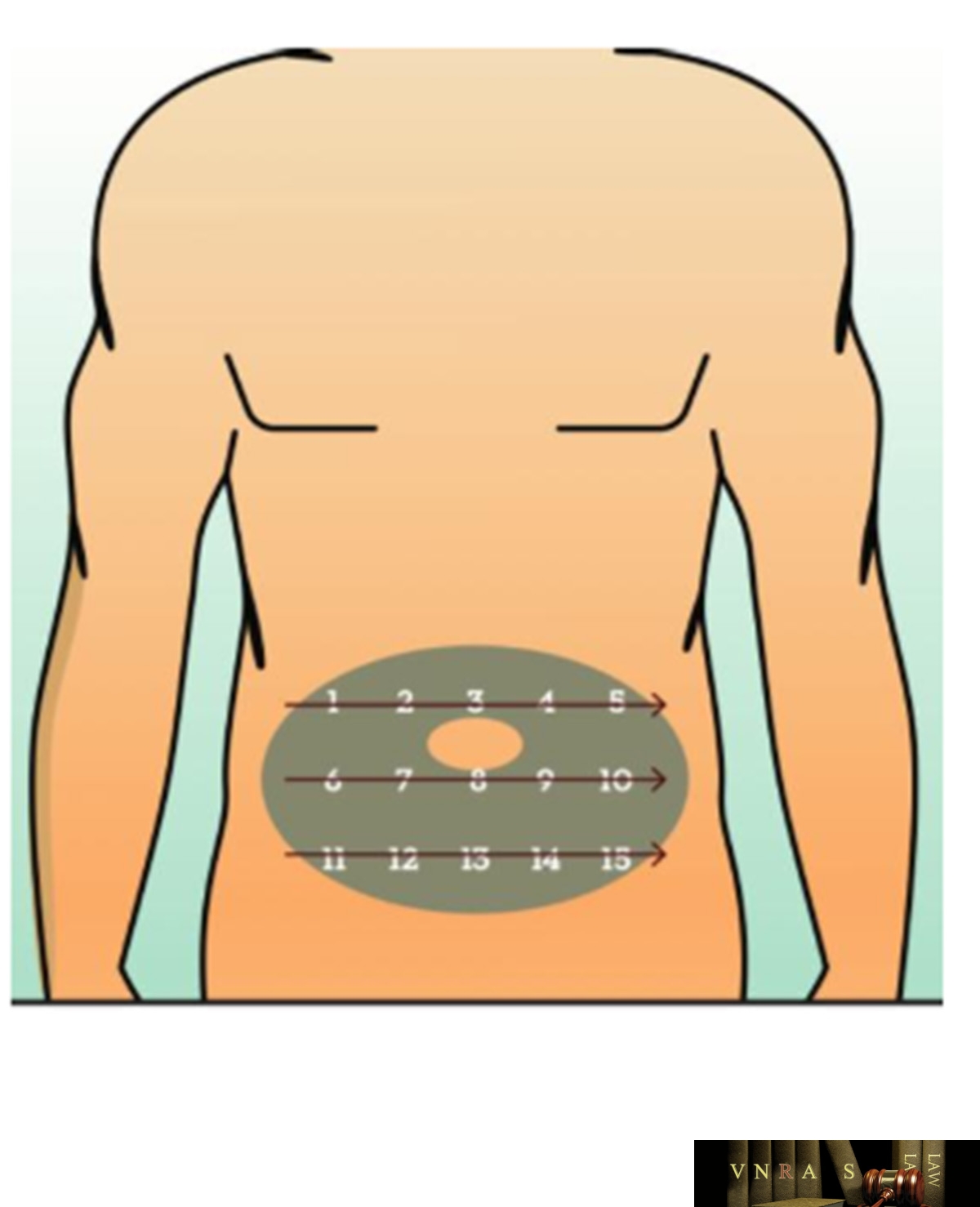
|
|
|||||||||
| 3. | Bạn ghi nhãn ngày bắt đầu, ngày hết hạn cho bút insulin của bạn
|
|
|||||||||
| 4. | Bạn ghi lại đường huyết đã đo vào bảng này
|
|
TÀI LIỆU THAM KHẢO
1. Lexi-Drugs online, truy cập 03/12/2018.
2. Standards of Medical Care in Diabetes, Diabetes Care, 2018
3. Checklist tư vấn sử dụng insulin dạng bút tiêm cho người bệnh, khoa Nội Tiết Bệnh
viện Đại học Y Dược TPHCM năm 2018.
Chương 3. HƯỚNG DẪN THỰC HÀNH DƯỢC LÂM SÀNG TRONG MỘT SỐ BỆNH TIM MẠCH
1. HƯỚNG DẪN THỰC HÀNH DƯỢC LÂM SÀNG TRONG ĐIỀU TRỊ TĂNG HUYẾT ÁP
1.1. Đại cương về bệnh tăng huyết áp
1.1.1. Chẩn đoán
Định nghĩa tăng huyết áp
Tăng huyết áp (THA) được định nghĩa khi huyết áp tâm thu ≥ 140 mmHg và hoặc
huyết áp tâm trương (HATTr) ≥ 90 mmHg. Định nghĩa này được áp dụng cho người ≥
18 tuổi; huyết áp (HA) được đo lúc ngồi ít nhất 2 lần mỗi lần khám và ít nhất 2 lần
khám khác nhau. Bên cạnh chẩn đoán tăng huyết áp tại phòng khám, còn có những định nghĩa khác cho THA ngoài phòng khám.
Bảng 3.1. Định nghĩa THA theo HA đo tại phòng khám, HA Holter và HA đo tại nhà theo Khuyến cáo về chẩn đoán và điều trị THA của Hội Tim mạch học Việt Nam 2018
| Phân loại | HA tâm thu (mmHg) | HA tâm trương (mmHg) | |
| HA tại phòng khám | > 140 | và/hoặc | > 90 |
| Holter HA | |||
| HA trung bình ban ngày (lúc thức) | > 135 | và/ hoặc | > 85 |
| HA trung bình ban đêm (lúc ngủ) | > 120 | và/ hoặc | > 70 |
| HA trung bình 24 giờ | > 130 | và/hoặc | > 80 |
| HA trung bình tại nhà | > 135 | và/hoặc | > 85 |
Phân loại THA
Bảng 3.2 trình bày phân loại THA theo mức HA đo tại phòng khám. Trong trường
hợp HA không cùng mức để phân loại thì chọn mức HATT hoặc HATTr cao nhất.
Bảng 3.2. Phân loại THA theo mức HA đo tại phòng khám theo Khuyến cáo về chẩn đoán và điều trị THA của Hội Tim mạch học Việt Nam 2018
| Phân loại | HA tâm thu (mmHg) | HA tâm trương (mmHg) | |
| Tối ưu | < 120 | và/hoặc | < 80 |
| Bình thường ** | 120 – 129 | và/hoặc | 80 – 84 |
| Bình thường cao ** | 130 – 139 | và/hoặc | 85 – 89 |
| Độ 1 | 140 – 159 | và/hoặc | 90 – 99 |
| Độ 2 | 160 – 179 | và/hoặc | 100 – 109 |
| Độ 3 | > 180 | và/hoặc | > 110 |
| THA tâm thu đơn độc* | > 140 | và | < 90 |
* THA tâm thu đơn độc xếp loại theo mức HATT
** Tiền THA: khi HATT > 120 – 139 mmHg và HATTr > 80 – 89 mmHg.
– Đánh giá lâm sàng và tổn thương cơ quan đích
Người bệnh cần được đánh giá đẩy đủ và toàn diện về tiền sử gia đình và bản thân,
các yếu tố tham gia phát triển THA, yếu tố nguy cơ tim mạch, tổn thương cơ quan đích và các bệnh mắc kèm.
Bảng 3.3. Các yếu tố ảnh hưởng nguy cơ tim mạch ở người bệnh THA
| Đặc điểm người bệnh và thông số cận lâm sàng
Giới tính Tuổi Thuốc lá (đang hút hoặc đã hút) Cholesterol toàn phần và HDL-C Tăng acid uric máu Đái tháo đường Thừa cân hoặc béo phì Tiền sử gia đình bị bệnh tim mạch sớm (nam < 55 và nữ < 65) Tiền sử gia đình hoặc người thân mắc bệnh THA sớm Mãn kinh sớm Lối sống tĩnh tại Yếu tố tâm lý xã hội Nhịp tim (trị số khi nghỉ > 80 lần/phút) |
| Tổn thương cơ quan đích hông triệu chứng
Cứng mạch: HA mạch (người lớn) > 6 0 mmHg Vận tốc sóng mạch (PWV) ĐMC – đùi > 1 0 m/s Điện tâm đồ dày thất trái Siêu âm tim dày thất trái Albumin niệu vi thể hoặc tăng tỷ lệ albumin – creatinin Bệnh thận mạn mức độ vừa (MLCT 30 – 59 ml/phút/1,73 m2) hoặc bệnh thận mạn mức độ nặng (MLCT < 30 ml/phút/1,73 m2) Chỉ số cẳng chân – cổ tay < 0,9 Bệnh võng mạc tiến triển: xuất huyết hoặc xuất tiết, phù gai thị |
| Bệnh tim mạch đã xác định
Bệnh mạch não: đột quỵ thiếu máu cục bộ, xuất huyết não, thiếu mãu não thoáng qua BMV: nhồi máu cơ tim, ĐTN, tái tưới máu cơ tim Mảng xơ vữa qua hình ảnh Bệnh động mạch ngoại biên Rung nhĩ |
– Phân tầng nguy cơ tim mạch
Nguy cơ tim mạch của người bệnh được phân tầng theo mức HA, các yếu tố nguy
cơ, tổn thương cơ quan đích và các bệnh mắc kèm.
Bảng 3.4. Phân tầng nguy cơ tim mạch của người bệnh THA
| Giai đoạn | Các YTNC, TTCQ đích, BMK |
Phân độ HA (mmHg) |
|||
| Bình thường-cao | Độ 1 | Độ 2 | Độ 3 | ||
| Giai đoạn 1 (không biến chứng) | Không có YTNC | Nguy cơ thấp | Nguy cơ thấp | Nguy cơ trung bình | Nguy cơ cao |
| 1 – 2 YTNC | Nguy cơ thấp | Nguy cơ trung bình | Nguy cơ trung bình – cao | Nguy cơ cao | |
| ≥ 3 YTNC | Nguy cơ thấp – trung bình | Nguy cơ trung bình – cao | Nguy cơ cao | Nguy cơ cao | |
| Giai đoạn 2 (bệnh không triệu chứng) | TTCQ đích, BTM giai đoạn 3 hoặc ĐTĐ không TTCQ đích | Nguy cơ trung bình – cao | Nguy cơ cao | Nguy cơ cao | Nguy cơ cao – rất cao |
| Giai đoạn 3 (bệnh có triệu chứng) | Bệnh tim mạch có triệu chứng, BTM giai đoạn ≥ 4 hoặc ĐTĐ có tổn thương cơ quan đích | Nguy cơ rất cao | Nguy cơ rất cao | Nguy cơ rất cao | Nguy cơ rất cao |
Chú thích: YTNC: yếu tố nguy cơ, TTCQ: tổn thương cơ quan, BMK: bệnh mắc kèm, BTM: Bệnh thận mạn, ĐTĐ: Đái tháo đường.
Một số thang điểm đánh giá nguy cơ tim mạch có thể sử dụng như: bảng kiểm SCORE hay thang điểm đánh giá nguy cơ tim mạch do xơ vữa (ASCVD) 10 năm.
Đánh giá nguy cơ tim mạch theo thang điểm SCORE được khuyến cáo cho người bệnh THA không có nguy cơ bệnh tim mạch cao hoặc rất cao, ĐTĐ hoặc có nguy cơ cao rõ ràng (ví dụ cholesterol cao) hoặc dày thất trái do THA.
Người bệnh có nguy cơ tim mạch do xơ vữa (ASCVD) 10 năm > 10% được coi có nguy cơ cao và rất cao.
1.1.2. Điều trị
Ngưỡng HA ban đầu cần điều trị
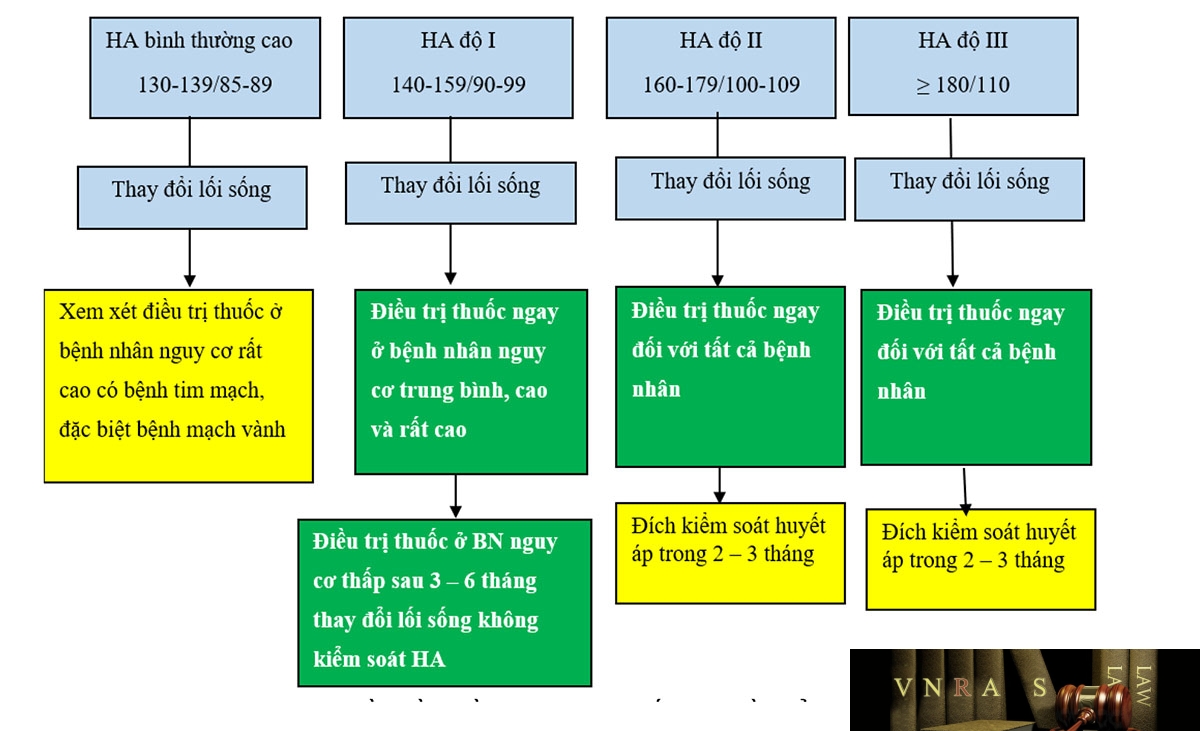
Ngưỡng HA phòng khám ban đầu cần điều trị trong các tình huống lâm sàng
Bảng 3.5. Ngưỡng điều trị dựa trên HA tại phòng khám theo Khuyến cáo về chẩn đoán và điều trị THA của Hội Tim mạch học Việt Nam 2018
| Nhóm tuổi |
Ngưỡng điều trị HA tâm thu tại phòng khám |
Ngưỡng điều trị HATTr tại phòng khám | ||||
| THA | THA+ ĐTĐ | THA + BTM | THA + BMV | THA + Đột quỵ hoặc thiếu máu não thoáng qua | ||
| 18 – 65 | ≥140 | ≥140 | ≥140 | ≥140 | ≥140 | ≥ 90 |
| 65 – 79 | ≥140 | ≥140 | ≥140 | ≥140 | ≥140 | ≥ 90 |
| ≥ 80 | ≥160 | ≥160 | ≥160 | ≥160 | ≥160 | ≥ 90 |
Huyết áp mục tiêu
Bảng 3.6. HA mục tiêu trong các tình huống lâm sàng theo Khuyến cáo về chẩn đoán và điều trị THA của Hội Tim mạch học Việt Nam 2018
| Nhóm tuổi |
Ngưỡng HATT mục tiêu (mmHg) |
HATTr mục tiêu (mmHg) | ||||
| THA | THA+ ĐTĐ | THA + BTM | THA + BMV | THA + Đột quỵ/thiếu máu não thoáng qua | ||
| 18 – 64 | 130 – 120 | 130 – 120 | < 140 – 130 | 130 – 120 | 130 – 120 | < 80 – 70 |
| ≥ 65 | < 140 –
130 |
< 140 – 130 | < 140 – 130 | < 140 – 130 | < 140 – 130 | < 80 – 70 |
| HATTr tại phòng khám | < 80 – 70 | < 80 – 70 | < 80 – 70 | < 80 – 70 | < 80 – 70 | |
Thay đổi lối sống
- Hạn chế muối < 5 g/ ngày.
- Hạn chế lượng cồn uống vào, < 2 đơn vị/ ngày ở nam và < 1 đơn vị/ ngày ở nữ (1 đơn vị cồn chứa 14 g cồn tinh khiết tương đương 345 mL bia (5% cồn) hoặc 150 mL rượu vang (12% cồn) hoặc 45 mL rượu mạnh (40% cồn).
- Nên sử dụng nhiều rau, trái cây tươi, cá, các loại hạt, acid béo không bão hòa (dầu oliu); hạn chế dùng thịt đỏ, nên dùng các sản phẩm ngũ cốc ít béo.
- Tránh béo phì (BMI > 30 kg /m2 hay vòng eo > 102 cm ở nam và > 88 cm ở nữ), duy trì BMI 20-25 kg/ m2 và vòng eo < 94 cm ở nam hay < 80 cm ở nữ.
- Tăng cường hoạt động thể lực (ít nhất 30 phút vận động thể lực mức độ trung bình trong 5-7 ngày trong tuần).
- Ngưng hút thuốc lá và tránh nhiễm độc khói thuốc.
Điều trị bằng thuốc
a) Nguyên tắc điều trị
- Các thuốc ức chế men chuyển (ƯCMC), chẹn thụ thể angiotensin II (CTTA), chẹn beta (CB), chẹn kênh canxi (CKCa) và lợi tiểu (LT) nên được chỉ định do đã có bằng chứng giảm HA và biến cố tim mạch trong các thử nghiệm lâm sàng.
- Bắt đầu điều trị ở hầu hết bệnh nhân bằng phối hợp hai thuốc (ưu tiên viên phối hợp) để đạt HA mục tiêu sớm.
- Ưu tiên phối hợp thuốc ƯCMC hoặc CTTA với CKCa hoặc LT.
- Lựa chọn thuốc CB với một nhóm thuốc khác khi bệnh nhân có đau thắt ngực, sau nhồi máu cơ tim (NMCT), suy tim hay để kiểm soát tần số tim.
- Bắt đầu đơn trị liệu cho bệnh nhân cao tuổi bị lão hóa hoặc bệnh nhân THA độ 1 nguy cơ thấp (HATT < 150 mmHg).
- Nếu HA không kiểm soát bằng hai thuốc nên thêm thuốc thứ ba, thường là ƯCMC/CTTA + CKCa + LT (ưu tiên viên phối hợp).
- Nếu HA không kiểm soát bởi ba thuốc, điều trị thêm spironolacton (hoặc lợi tiểu khác như amilorid nếu không dung nạp), CB hoặc chẹn alpha.
- Không khuyến cáo phối hợp thuốc ƯCMC và CTTA, trừ một số trường hợp đặc biệt.
- Các thuốc điều trị THA khác được dùng trong một sốt ít trường hợp, khi HA không thể kiểm soát bằng các nhóm thuốc điều trị chính.
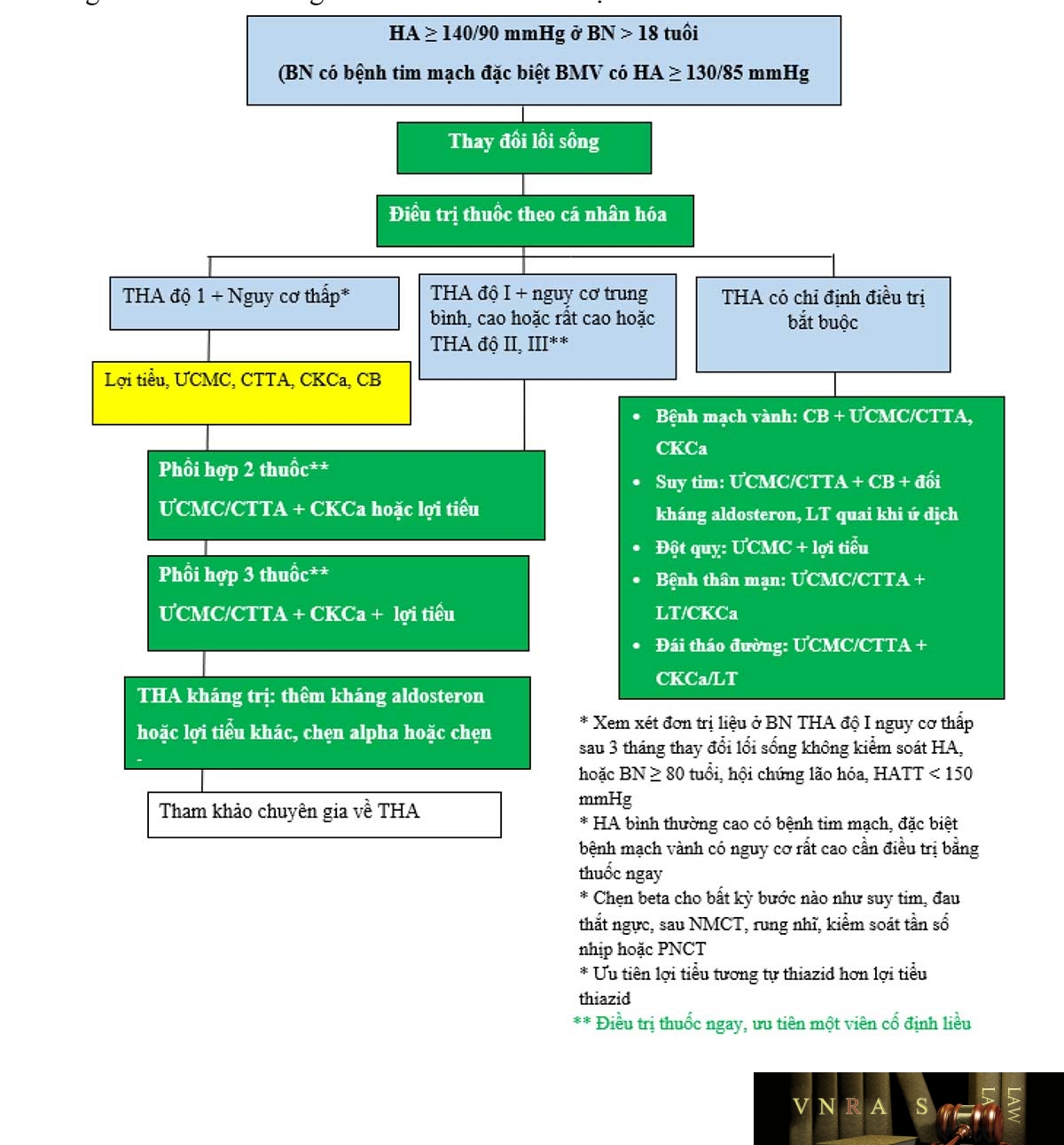
b) Điều trị THA không biến chứng
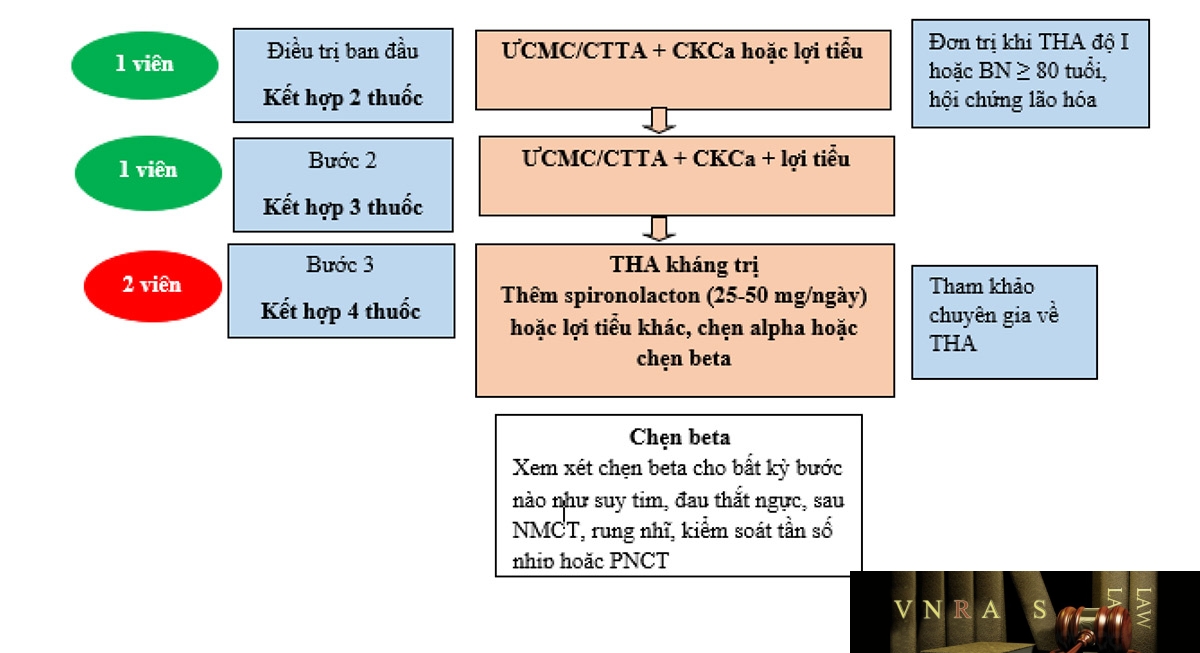
Phác đồ điều trị này cũng thích hợp dùng cho bệnh nhân THA có tổn thương cơ quan đích, bệnh mạch não, đái tháo đường hoặc bệnh động mạch ngoại vi.
1.2. Hướng dẫn thực hành dược lâm sàng trên bệnh nhân tăng huyết áp
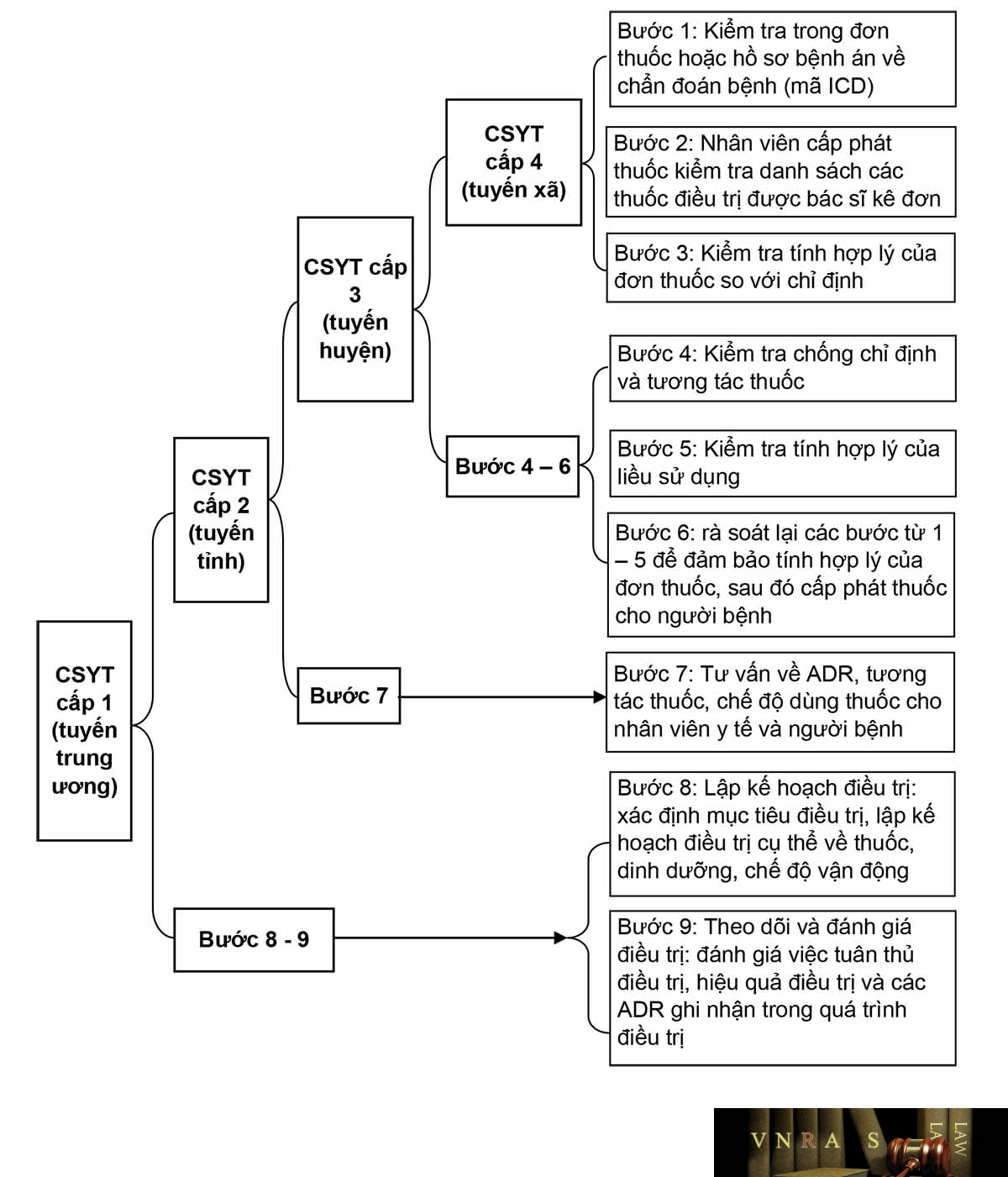
Trong nội dung này, các hoạt động thực hành dược lâm sàng được trình bày theo các bước của quy trình chăm sóc dược đầy đủ trên bệnh nhân. Tùy theo điều kiện của từng cơ sở y tế tại các tuyến khác nhau, có thể triển khai các hoạt động theo hướng dẫn chung được trình bày trong chương 1.
1.2.1. Hướng dẫn thực hành tại cơ sở y tế tuyến 4 (tương đương tuyến xã)
Yêu cầu cần đạt được
Cấp phát thuốc phù hợp với chẩn đoán.
Phạm vi thực hiện
Khuyến khích thực hiện, không quy định cụ thể về mức độ, quy mô thực hiện.
Các bước tiến hành
- Bước 1: Kiểm tra trong đơn thuốc hoặc hồ sơ bệnh án thông tin về chẩn đoán bệnh
- Bước 2: Nhân viên cấp phát thuốc kiểm tra danh sách các thuốc điều trị được bác sĩ kê đơn.
- Bước 3: Kiểm tra tính hợp lý của thuốc so với chỉ định.
+ Nếu người bệnh có chẩn đoán THA nhưng thuốc được kê không phải thuốc điều trị THA, nhân viên cấp phát thuốc thông báo lại cho bác sĩ để làm rõ tính chính xác của chỉ định hoặc bổ sung thuốc điều trị THA.
+ Nếu không có chẩn đoán THA nhưng người bệnh được kê thuốc điều trị THA, nhân viên cấp phát thuốc thông báo lại cho bác sĩ để bỏ thuốc được kê hoặc bổ sung chỉ định (nếu có).
+ Nếu người bệnh có chẩn đoán THA, thuốc được kê là thuốc điều trị THA, nhân viên cấp phát thuốc cấp phát thuốc cho người bệnh.
1.2.2. Hướng dẫn thực hành tại cơ sở y tế tuyến 3 (tương đương tuyến huyện)
Yêu cầu cần đạt được
- Tương tự cơ sở y tế tuyến 4.
- Kiểm tra tương tác thuốc (khuyến khích thực hiện), chặn các chống chỉ định nếu có trong đơn
- Kiểm tra liều thuốc: rà soát liều thuốc không vượt quá giới hạn liều tối đa.
Phạm vi thực hiện
- Cấp phát thuốc phù hợp chẩn đoán: bắt buộc thực hiện với tất cả đơn thuốc.
- Kiểm tra chống chỉ định của các thuốc
- Kiểm tra tương tác thuốc: khuyến khích thực hiện, không quy định cụ thể về mức độ, quy mô thực hiện.
- Kiểm tra liều thuốc: yêu cầu kiểm tra một tỷ lệ nhất định đơn thuốc tuỳ điều kiện nhân lực của cơ sở.
Các bước tiến hành
- Bước 1 đến bước 3: Tương tự hướng dẫn thực hành tại cơ sở y tế tuyến 4.
- Bước 4:
+ Kiểm tra chống chỉ định của các thuốc được kê đơn: Tham khảo phụ lục 3.2
+ Kiểm tra tương tác thuốc: Tham khảo phụ lục 3.5, các phần mềm (Lexicomp, Micromedex) hoặc trang web (drugs.com, medscape.com) hoặc sách (Stockley drug interactions, Tương tác thuốc – BYT).
– Nếu có tương tác thuốc ở mức độ chống chỉ định, dược sĩ cần thông báo lại cho bác sĩ để thay đổi thuốc.
– Nếu có tương tác thuốc cần hiệu chỉnh liều, dược sĩ thông báo lại cho bác sĩ để chỉnh liều thuốc (khuyến khích thực hiện).
– Nếu có những tương tác thuốc khác, cần có tư vấn cho người bệnh sau khi phát thuốc (khuyến khích thực hiện).
- Bước 5: kiểm tra liều sử dụng: Tham khảo phụ lục 3.3
+ Nếu thuốc được kê với liều vượt quá giới hạn liều tối đa theo hướng dẫn, dược sĩ thông báo lại cho bác sĩ để có điều chỉnh hợp lý.
+ Nếu thuốc điều trị THA được kê trong khoảng liều đúng theo hướng dẫn, dược sĩ tiếp tục thực hiện bước 6.
- Bước 6: rà soát lại các bước từ 1 – 5 để đảm bảo tính hợp lý của đơn thuốc, sau đó cấp phát thuốc cho người bệnh.
1.2.3. Hướng dẫn thực hành tại cơ sở y tế tuyến 2 (tương đương tuyến tỉnh)
Yêu cầu cần đạt được
- Tương tự cơ sở y tế tuyến 3.
- Tư vấn chế độ dùng thuốc dựa trên tiền sử dùng thuốc của người bệnh, tư vấn về ADR và tương tác thuốc cho nhân viên y tế và người bệnh.
Phạm vi thực hiện
- Cấp phát thuốc phù hợp chẩn đoán: bắt buộc thực hiện với tất cả đơn thuốc.
- Kiểm tra liều thuốc: Khuyến khích thực hiện với tất cả đơn thuốc. Tuy nhiên, tùy thuộc điều kiện nhân lực của cơ sở và tình hình thực tế, yêu cầu kiểm tra một tỷ lệ đơn nhất định, tập trung trên một số đối tượng nhất định.
- Kiểm tra tương tác thuốc, tư vấn về ADR, chế độ dùng thuốc: yêu cầu kiểm tra và tư vấn trên một tỷ lệ nhất định đơn thuốc tuỳ điều kiện nhân lực của cơ sở, tập trung vào một số đối tượng nhất định (ví dụ: các đơn có nhiều thuốc, đối tượng đặc biệt: phụ nữ có thai, cho con bú,…)
Các bước tiến hành
- Bước 1 đến bước 6: tương tự hướng dẫn thực hành tại cơ sở y tế tuyến 3.
- Bước 7: Tư vấn chế độ dùng thuốc dựa trên tiền sử bệnh và tiền sử dùng thuốc của người bệnh, tư vấn về ADR và tương tác thuốc cho nhân viên y tế và người bệnh.
+ Đánh giá lâm sàng và cận lâm sàng của bệnh nhân: Tham khảo phụ lục 3.1
+ Tư vấn chế độ dùng thuốc: đánh giá chỉ định loại thuốc phù hợp với tình trạng bệnh/đối tượng đặc biệt.
+ Tư vấn về tương tác thuốc cho nhân viên y tế và người bệnh: Tham khảo phụ lục 3.5, các phần mềm (Lexicomp, Micromedex) hoặc trang web (www.drugs.com, www.medscape.com) hoặc sách (Stockley Drug Interactions, Sách “Tương tác thuốc và chú ý khi chỉ định – BYT). Đối với người bệnh, ưu tiên hướng dẫn cách sử dụng thuốc để hạn chế tương tác (ví dụ: tương tác do hấp thu).
+ Tư vấn về ADR: Tham khảo phụ lục 3.4.
Khai thác thông tin về tiền sử bệnh và tiền sử dùng thuốc
Bảng 3.7. Phiếu khai thác tiền sử bệnh và dùng thuốc
| THÔNG TIN BỆNH NHÂN
Họ tên:……………Năm sinh:……………… Giới tính: …………. Chẩn đoán: ……………………………………………………………………………………………… ĐÁNH GIÁ KẾT QUẢ PHỎNG VẤN Dược sĩ phỏng vấn: ……………………………………………………. Ngày phỏng vấn: ………………………………………………………………………………. |
|||
| TT | Nội dung câu hỏi | Thông tin từ bệnh nhân | Cần tư vấn lại |
A. Hiểu biết của bệnh nhân về bệnh tăng HA |
|||
| 1 | Ông/bà bị THA đã bao lâu? Ông/bà được chẩn đoán THA khi nào? | ||
| 2 | Có ai trong gia đình ông/bà bị THA hay bệnh lý tim mạch, rối loạn lipid máu, ĐTĐ không? | ||
| 3 | Ông/bà có biết tác hại của việc không kiểm soát tốt HA? | ||
| 4 | Ông/bà có tự kiểm tra HA tại nhà? Nếu có:
– Mấy lần trong tuần? – Dụng cụ đo HA tại nhà là gì? – Chỉ số HA đo được là bao nhiêu? – Theo bác sĩ, HA mục tiêu (mức HA “tốt”) của ông/bà là bao nhiêu? – Ông/bà có ghi chép lại chỉ số HA vào sổ nhật ký? Nếu có, ông/bà vui lòng cho dược sĩ xem – Nếu HA tại nhà đo được là cao, ông/bà làm gì? Bác sĩ có hướng dẫn ông/bà cách xử trí khi HA cao không? |
||
| B. Các triệu chứng về THA thứ phát | |||
| 5 | Ông/bà có từng mắc bệnh thận, nhiễm trùng đường tiểu, tiểu máu, lạm dụng thuốc giảm đau, bệnh lý tuyến giáp không? | ||
| 6 | Ông/ bà có thường xuyên đổ mồ hôi, nhức đầu, lo lắng, hồi hộp không? | ||
| 7 | Ông/ bà có từng co cứng cơ hoặc nhược cơ không? | ||
| C. Hiểu biết của bệnh nhân về thuốc điều trị tăng HA đang dùng | |||
| 8 | Thuốc HA ông/bà đang sử dụng là thuốc gì? Ông/bà sử dụng như thế nào? | ||
| 9 | Ông/bà có hay quên sử dụng thuốc không? Lý do vì sao? | ||
| 10 | Ông/bà có ngừng sử dụng thuốc không? Lý do vì sao? | ||
| 11 | Loại thuốc HA khác ông/bà đã từng sử dụng trước đây là gì? | ||
| 12 | Ông/bà có sử dụng thuốc không kê đơn hay thực phẩm chức năng nào khác để điều trị tăng HA không? | ||
| D. Thay đổi lối sống | |||
| 13 | Ngoài việc sử dụng thuốc, ông/bà còn sử dụng biện pháp nào khác (như thay đổi lối sống) không? | ||
| 14 | Bác sĩ có đề nghị ông/bà hạn chế sử dụng muối cho bữa ăn không? Nếu có, ông/bà thực hiện và đo lường lượng muối như thế nào? | ||
| 15 | Ông/bà có tập thể dục không? | ||
| E. Khả năng dự phòng của bệnh nhân trước các tình huống khẩn cấp liên quan đến bệnh THA | |||
| 16 | Ông/bà có từng gặp các triệu chứng hạ HA: mờ mắt, lú lẫn, chóng mặt, hoa mắt, té ngã khi thay đổi tư thế (từ ngồi/nằm sang đứng), mệt mỏi, buồn nôn hay không? | ||
| 17 | Bác sĩ có tư vấn ông/bà nên tránh sử dụng một số thuốc không kê đơn có khả năng làm tăng HA không? | ||
| 18 | Ông/bà đã bao giờ nhập viện vì THA chưa? | ||
Tư vấn chế độ dùng thuốc
Bảng 3.8. Lựa chọn thuốc điều trị THA trong một số tình huống lâm sàng
| Tình trạng bệnh/bệnh mắc kèm | Lựa chọn thuốc điều trị tăng huyết áp |
| Không mắc kèm bệnh lý tim mạch khác | Điều trị ban đầu: kết hợp hai thuốc ƯCMC/CTTA + CKCa/LT
Bước 2: kết hợp ba thuốc: ƯCMC CTTA + CKCa + LT Bước 3: kết hợp bốn thuốc (THA kháng trị): Thêm spironolacton ( 5-50 mg ngày) hoặc LT khác, chẹn alpha chẹn beta |
| Bệnh mạch vành | Ưu tiên ƯCMC/CTTA + CB
Nếu chưa kiểm soát được HA: thêm CKCa, LT và/hoặc kháng aldosteron |
| Đái tháo đường | ƯCMC, CTTA, CKCa, LT
Bệnh nhân có protein niệu: ưu tiên ƯCMC/CTTA |
| Suy tim hoặc phì đại thất trái | EF giảm: ƯCMC/ CTTA + CB (bisoprolol, carvedilol, metoprolol succinat hoặc nebivolol) + LT và hoặc kháng aldosteron khi cần Nếu triệu chứng suy tim vẫn còn, xem xét thay thế ƯCMC CTTA bằng valsartan + sacubitril Nếu chưa kiểm soát được HA: thêm CKCa nhóm dihydropyridin
EF bảo tồn + ứ dịch: cần điều trị bằng LT, sau xem xét chỉ định ƯCMC CTTA + CB. Dày thất trái: ƯCMC/CTTA + CB/LT. |
| Bệnh thận mạn | Bước 1 : kết hợp 2 thuốc: ƯCMC/CTTA + CKCa/LT.
Bước : kết hợp 3 thuốc: ƯCMC CTTA + CKCa + LT. Bước 3: kết hợp thuốc: THA kháng trị: thêm spironolacton hoặc LT khác, chẹn alpha hoặc chẹn beta (Bisoprolol). |
| Rung nhĩ | CB hoặc CKCa non-dihydropyridin giúp kiểm soát tần số nhịp.
Dự phòng đột quỵ với thuốc kháng đông được khuyến cáo ở bệnh nhân THA kèm rung nhĩ có thang điểm CHA2DS2-VASc > 2 ở nam và > 3 ở nữ. Dự phòng đột quỵ với thuốc chống đông đường uống phải được xem xét ở bệnh nhân rung nhĩ mắc kèm THA ngay cả khi bệnh nhân chỉ có yếu tố nguy cơ là THA (CHA2DS2-VASC 1 điểm). |
| Đột quỵ | Xuất huyết não cấp:
– HATT > 220 mmHg: xem xét điều trị hạ HA bằng thuốc đường truyền tĩnh mạch đến < 180 mmHg và theo dõi sát HA. – HATT ở giữa 150 – 220 mmHg, trong 6 giờ đầu, cần tránh hạ áp < 140 mmHg. Dự phòng đột quỵ thứ phát: – Sau đột quỵ cấp hoặc thiếu máu não thoáng qua, sử dụng LT, ƯCMC CTTA hoặc kết hợp LT – Bệnh nhân THA đang điều trị bị đột quỵ thiếu máu cục bộ hoặc thiếu máu não thoáng qua, phải khởi trị lại sau giờ khởi phát – Bệnh nhân THA không điều trị mà bị đột quỵ thiếu máu cục bộ hoặc thiếu mãu não thoáng qua: + HA > 140/90 mmHg: phải được điều trị thuốc sau 72 giờ. + HA < 140/90 mmHg: không cần điều trị. |
| Cơn THA: Cấp cứu và khẩn cấp | – THA cấp cứu:
+ Dùng thuốc hạ áp đường tĩnh mạch thích hợp và theo dõi liên tục tổn thương cơ quan đích + Trong những điều kiện bắt buộc (như bóc tách phình động mạch chủ, sản giật hoặc tiền sản giật nặng hoặc cơn THA thượng thận), HATT phải giảm < 140 mmHg trong giờ đầu và hạ xuống đến < 120 mmHg trong trường hợp bóc tách phình động mạch chủ + Nếu không có điều kiện bắt buộc, không hạ HATT quá 25% trong giờ đầu. Sau đó, nếu ổn định, hạ HA đến 160/100 mmHg trong vòng 2-6 giờ tiếp theo và thận trọng hạ đến HA bình thường trong 24-48 giờ – THA khẩn cấp: Bệnh nhân cần điều trị thuốc đường uống tích cực và theo dõi. Đích điều trị là HATTr 100 – 110 mmHg trong nhiều giờ, không cần nằm viện – Thuốc và liều dùng tham khảo Phụ lục 3.3 |
| Bệnh nhân THA cần làm thủ thuật, phẫu thuật | Trước phẫu thuật:
– Bệnh nhân THA trải qua phẫu thuật lớn đang được điều trị CB, phải tiếp tục sử dụng CB. – Bệnh nhân THA đã có kế hoạch phẫu thuật lớn theo chương trình: cần tiếp tục điều trị thuốc hạ áp cho đến khi phẫu thuật – Bệnh nhân THA trải qua phẫu thuật lớn: có thể xem xét ngừng ƯCMC/CTTA trong giai đoạn phẫu thuật. – ƯCMC CTTA đã có kế hoạch phẫu thuật lớn theo chương trình và HATT ≥ 180 mmHg hoặc HATTr > 110 mmHg: có thể xem xét hoãn phẫu thuật. – Không bắt đầu dùng CB trong ngày phẫu thuật ở bệnh nhân chưa bao giờ dùng CB. Trong phẫu thuật: bệnh nhân HA tăng trong lúc phẫu thuật phải được kiểm soát với thuốc hạ áp truyền tĩnh mạch cho đến khi có thể dùng lại thuốc uống. |
| Phụ nữ có thai | Ưu tiên sử dụng methyldopa, niíedipin, hoặc labetalol.
Chống chỉ định: ƯCMC, CTTA, ức chế renin trực tiếp Điều trị cơn tăng HA: labetalol hoặc nicardipin và magnesium truyền tĩnh mạch (IV) THA mức độ nặng: labetalol (IV) hoặc methyldopa, niíedipin đường uống (PO) Tiền sản giật có phù phổi: nitroglycerin (IV) Sau sinh tuần đầu, có thể dùng các thuốc trong 5 nhóm thuốc điều trị THA chính nhưng chú ý tránh dùng methyldopa, propanolol, nifedipin Chống chỉ định thuốc ƯCMC, CTTA trên phụ nữ cho con bú không có biện pháp ngừa thai tin cậy |
1.2.4. Hướng dẫn thực hành tại cơ sở y tế tuyến 1 (tương đương tuyến trung ương)
Yêu cầu cần đạt được
- Tương tự cơ sở y tế tuyến 2
- Lập kế hoạch điều trị
- Theo dõi và đánh giá điều trị
Phạm vi thực hiện
- Cấp phát thuốc phù hợp chẩn đoán: bắt buộc thực hiện với tất cả đơn thuốc.
- Kiểm tra liều thuốc: Khuyến khích thực hiện với tất cả đơn thuốc. Tuy nhiên, tùy thuộc điều kiện nhân lực của cơ sở và tình hình thực tế, yêu cầu kiểm tra một tỷ lệ đơn nhất định, tập trung trên một số đối tượng nhất định.
- Kiểm tra tương tác thuốc, tư vấn về ADR, chế độ dùng thuốc: yêu cầu kiểm tra và tư vấn trên một tỷ lệ nhất định đơn thuốc tuỳ điều kiện nhân lực của cơ sở, tập trung vào một số đối tượng nhất định (ví dụ: các đơn có nhiều thuốc, đối tượng đặc biệt: phụ nữ có thai, cho con bú, trẻ em,…)
- Lập kế hoạch điều trị, theo dõi và đánh giá điều trị: khuyến khích thực hiện khi có đủ điều kiện về nhân lực, tiến hành tại các cơ sở y tế có quy định cụ thể về dịch vụ chăm sóc dược trên các đối tượng có yêu cầu về dịch vụ này.
Các bước tiến hành
- Bước 1 đến bước 7: tương tự hướng dẫn thực hành tại cơ sở y tế tuyến 2.
- Bước 8: Lập kế hoạch điều trị
+ Phát hiện một số vấn đề liên quan đến thuốc trên bệnh nhân THA.
Bảng 3.9. Một số vấn đề liên quan đến sử dụng thuốc ở BN THA
| Vấn đề liên quan đến sử dụng thuốc | Ví dụ |
| Không tuân thủ | Không kiểm soát HA ở mức tối ưu do không thay đổi lối sống (ví dụ hạn chế muối, cai thuốc lá) hoặc do liều thuốc hạ áp chưa đủ Bệnh nhân không dùng thuốc do chi phí cao |
| Thuốc không cần thiết | Liệu pháp phối hợp (ví dụ 2 thuốc ƯCMC) |
| Cần bổ sung thuốc | Đơn trị liệu không kiểm soát HA ở mức tối ưu
Bệnh nhân bị ĐTĐ và albumin niệu không được dùng ƯCMC hoặc CTTA để kiểm soát HA |
| Thuốc không hiệu quả | Thuốc hạ áp mới được thử nghiệm đầy đủ nhưng không có đáp ứng trên lâm sàng
Đơn trị liệu với thuốc chẹn alpha 1 |
| Liều thấp | Không kiểm soát HA ở mức tối ưu do sử dụng liều thuốc hạ áp thấp hơn liều khuyến cáo |
| Liều cao | Bệnh nhân hạ HA tư thế
Bệnh nhân bị nhịp tim chậm với CB |
| Phản ứng có hại của thuốc | Ho do ƯCMC |
– Xác định mục tiêu điều trị, lập kế hoạch điều trị cụ thể về thuốc, dinh dưỡng, chế độ vận động
Lập kế hoạch điều trị
Bảng 3.10. Lập kế hoạch điều trị THA
| Hoạt động chính | Nội dung hoạt động | Hướng dẫn chi tiết | Kế hoạch chăm sóc của dược sĩ lâm sàng cho người bệnh | Thực hiện |
| Xác định mục tiêu điều trị
|
Xác định ngưỡng HA ban đầu cần điều trị | BN cần được đánh giá đẩy đủ và toàn diện về tiền sử gia đình và bản thân, các yếu tố tham gia phát triển tăng huyết áp, yếu tố nguy cơ tim mạch, tổn thương cơ quan đích và các bệnh mắc kèm | Ngưỡng điều trị dựa trên HA tại phòng khám
– BN 18 – 64 tuổi: HA > 140/90 mmHg – BN 65 -79 tuổi: HA > 140/90 mmHg – BN > 8 0 tuổi: HA > 160/90 mmHg – Xem xét điều trị ở bệnh nhân nguy cơ rất cao (ví dụ bệnh mạch vành, đột quỵ, thiếu máu não thoáng qua) khi HATT 130 – 140 mmHg. |
□ |
| Kiểm soát huyết áp | Huyết áp mục tiêu | Đích HA chung cho tất cả bệnh nhân là huyết áp phòng khám < 140/90 mmHg Nếu bệnh nhân dung nạp tốt, xem xét đích huyết áp < 130/80 mmHg.
Đối với bệnh nhân <65 tuổi: – Mục tiêu huyết áp tâm thu cần đạt 120-129 mmHg.
Mục tiêu HATTr cần đạt 70 – 80 mmHg |
□ | |
| Kiểm soát các yếu tố nguy cơ tim mạch và các bệnh đồng mắc theo các khuyến cáo hiện hành
|
Rối loạn lipid máu | Tham khảo phụ lục 3.6
Bệnh nhân nguy cơ tim mạch rất cao: khuyến cáo dùng statin liều cao với đích LDL-C < 1,8 mmol/L (70mg/dL) hoặc giảm > 50% nếu LDL-C ban đầu là từ 1,8-3,5 mmol/L (70-135 mg/dL). Bệnh nhân nguy cơ tim mạch cao: khuyến cáo dùng statin liều trung bình với đích LDL-C < 2,6 mmol/L (100 mg/dL) hoặc giảm > 50% nếu LDL-C ban đầu là 2,6-5,2 mmol/L (100-200 mg/dL). Bệnh nhân có nguy cơ tim mạch thấp – trung bình, khuyến cáo dùng statin liều trung bình với đích LDL-C < 3mmol/L (115mg/dL). |
□ | |
| Đái tháo đường | Tham khảo mục tiêu điều trị chương Đái tháo đường. | □ | ||
| Thừa cân/ béo phì; béo bụng | Giảm cân, duy trì BMI 20-25 kg/m2 và vòng eo < 94 cm ở nam hay <80 cm ở nữ | □ | ||
| Hút thuốc lá | Ngưng hút thuốc lá và tránh nhiễm độc khói thuốc | □ | ||
| Uống nhiều rượu, bia | Hạn chế lượng cồn uống vào, < 2 đơn vị/ngày ở nam và < 1 đơn vị/ngày ở nữ | □ | ||
| Ít hoạt động thể lực | Tăng cường hoạt động thể lực | □ | ||
| Stress và căng thẳng tâm lý | Giảm stress và căng thẳng tâm lý, khám chuyên khoa tâm thần nếu cần | □ | ||
| Chế độ ăn quá nhiều muối | Hạn chế muối < 5 g/ngày | □ | ||
| Điều trị nguyên nhân (nếu có) | Sàng lọc các thể đặc biệt của THA thứ phát | Cần chú ý tìm kiếm nguyên nhân trong các trường hợp:
– Những BN trẻ tuổi (<40 tuổi) THA độ 2 hoặc bất kỳ THA độ nào ở tuổi trẻ.
Các triệu chứng gợi ý u tủy thượng thận hoặc tiền sử gia đình u tủy thượng thận. |
□ | |
| Lập kế hoạch điều trị | Thuốc điều trị |
Nguyên tắc điều trị | Bắt đầu điều trị ở hầu hết BN bằng phối hợp 2 thuốc để đạt huyết áp mục tiêu sớm.
Ưu tiên phối hợp ƯCMC CTTA với CKCa/ LT. Lựa chọn CB với một nhóm thuốc khác khi BN có đau thắt ngực, sau nhồi máu cơ tim, suy tim hay để kiểm soát tần số tim. Bắt đầu đơn trị liệu cho BN cao tuổi bị lão hóa hoặc bệnh nhân tăng huyết áp độ 1 nguy cơ thấp (HATT < 150 mmHg). Không khuyến cáo phối hợp ƯCMC và CTTA, trừ một số trường hợp đặc biệt |
□ |
| Đánh giá chỉ định loại thuốc phù hợp với tình trạng bệnh/ đối tượng đặc biệt | Tương tự cơ sở y tế tuyến 2 | □ | ||
| Liều dùng | Tham khảo Phụ lục 3.3 | □ | ||
| Chế độ sinh hoạt
|
Chế độ dinh dưỡng | Hạn chế muối < 5 g/ngày.
Hạn chế lượng cồn uống vào, < 2 đơn vị/ngày ở nam và < 1 đơn vị/ngày ở nữ (1 đơn vị cồn chứa 14 g cồn tinh khiết tương đương 345 mL bia (5% cồn) hoặc 150 mL rượu vang (12% cồn) hoặc 45 mL rượu mạnh (40% cồn). Nên sử dụng nhiều rau, trái cây tươi, cá, các loại hạt, acid béo không bão hòa (dầu oliu); hạn chế dùng thịt đỏ, nên dùng các sản phẩm ngũ cốc ít béo. |
□ | |
| Luyện tập thể lực | Tăng cường hoạt động thể lực (ít nhất 30 phút vận động thể lực mức độ trung bình trong 5-7 ngày trong tuần) | □ | ||
| Hút thuốc lá | Ngưng hút thuốc lá và tránh nhiễm độc khói thuốc | |||
| Phòng ngừa biến chứng | Các thăm khám giúp tầm soát biến chứng
Thực hiện các xét nghiệm tìm tổn thương cơ quan đích |
Biến chứng của THA hoặc tổn thương cơ quan đích do THA:
– Đột quỵ, thiếu máu não thoáng qua, sa sút trí tuệ, hẹp ĐM cảnh. – Phì đại thất trái (trên điện tâm đồ hoặc siêu âm tim), suy tim. – Nhồi máu cơ tim, cơn đau thắt ngực. – Bệnh mạch máu ngoại vi. – Xuất huyết hoặc xuất tiết võng mạc, phù gai thị. – Protein niệu, tăng creatinin huyết thanh, suy thân,… |
□ | |
| Giáo dục, tư vấn cho người bệnh | Về bệnh và mục tiêu điều trị | Giải thích mục tiêu điều trị | Cung cấp cho người bệnh các thông số mục tiêu của huyết áp, các yếu tố nguy cơ tim mạch cần kiểm soát và phòng ngừa các biến chứng của THA hoặc tổn thương cơ quan đích do THA
Thay đổi lối sống phải được thực hiện ngay ở tất cả các BN với HA bình thường cao và THA. Hiệu quả của thay đổi lối sống có thể ngăn ngừa hoặc làm chậm khởi phát THA và giảm các biến cố tim mạch. Xác định kiểm soát HA đạt đích tối đa trong 2-3 tháng. |
□ |
| Về kế hoạch điều trị | Thuốc – liều dùng | Với mỗi thuốc điều trị được kê, người bệnh được tư vấn về: công dụng, liều dùng và cách nhận biết ADR. | □ | |
| Cách dùng thuốc uống | Với mỗi loại thuốc uống điều trị được kê, BN được tư vấn về: thời điểm uống thuốc, cách uống thuốc và khoảng cách giữa các lần dùng thuốc. | □ | ||
| Chế độ ăn | Tư vấn cho BN về chế độ ăn uống. | □ | ||
| Luyện tập thể dục | Tư vấn cho BN về chế độ luyện tập thể dục. | □ | ||
| Hút thuốc lá | Tư vấn cho BN ngưng hút thuốc lá và tránh nhiễm độc khói thuốc. | □ | ||
| Phòng và điều trị biến chứng | Tư vấn cho BN thăm khám định kỳ giúp tầm soát sớm biến chứng của THA. | □ | ||
| Kiểm soát các yếu tố nguy cơ tim mạch và các bệnh đồng mắc theo các khuyến cáo hiện hành | Tư vấn cho BN về các yếu tố nguy cơ tim mạch và ý nghĩa của việc kiểm soát các bệnh đồng mắc theo các khuyến cáo hiện hành. | □ | ||
| Một số tình huống làm THA | – Ngừng sử dụng đột ngột thuốc chẹn beta hoặc chẹn thụ thể alpha trung ương
– Sử dụng thuốc chẹn beta mà không dùng thuốc chẹn thụ thể alpha trước trong điều trị bệnh u tủy thượng thận – Sử dụng thuốc ức chế monoamin oxidase (isocarboxazid, phenelzin, tranylcypromin) với thức ăn hay thuốc chứa tyramin – Tắc nghẽn đường hô hấp trên, ngưng thở khi ngủ |
□ | ||
| Một số yếu tố ảnh hưởng tới kết quả đo huyết áp tại nhà | – HA thay đổi theo nhịp sinh học của cơ thể (ví dụ: thời gian trong ngày, cảm xúc…)
– Bệnh nhân được tư vấn không đầy đủ hoặc kỹ thuật đo HA sai – Thiếu thời gian nghỉ ngơi trước khi đo HA (HA đo sau khi ngồi nghỉ ngơi 5 phút) – THA ẩn giấu – Bệnh nhân có nhịp thất bất thường (rung nhĩ) – Sử dụng cafein, rượu, nicotin trước khi đo HA (30 phút trước khi đo HA) – Sử dụng sai máy đo HA hoặc máy đo HA không được kiểm tra và hiệu chỉnh định kỳ – THA áo choàng trắng – Bệnh nhân ngồi đo HA sai tư thế (bệnh nhân nên ngồi lưng thẳng, dựa ghế, chân phẳng trên sàn, tay đặt ngang với tim) – Chọn dụng cụ đo có kích thước không phù hợp (bao quanh ít nhất 80% chiều dài của cánh tay trên và 40% chiều rộng) |
□ |
– Bước 9: Theo dõi và đánh giá điều trị
Đánh giá về việc tuân thủ điều trị, hiệu quả điều trị và các ADR ghi nhận trong quá trình điều trị (tham khảo bảng 3.11).
Bảng 3.11. Theo dõi điều trị tăng huyết áp
| Nội dung theo dõi và đánh giá điều trị | Kế hoạch chăm sóc của dược sĩ lâm sàng cho người bệnh | Thực hiện |
| Cách sử dụng máy đo HA tại nhà | Bệnh nhân cần được tư vấn cách sử dụng máy đo HA tại nhà:
– Nghỉ ngơi trước khi đo HA (HA đo sau khi ngồi nghỉ ngơi 5 phút) – Không sử dụng cafein, rượu, nicotin trước khi đo HA (30 phút trước khi đo HA). – Chọn dụng cụ đo có kích thước không phù hợp (bao quanh ít nhất 80% chiều dài của cánh tay trên và 40% chiều rộng). – Đo HA đúng tư thế (bệnh nhân nên ngồi lưng thẳng, dựa ghế, chân phẳng trên sàn, tay đặt ngang với tim), – Sử dụng đúng máy đo HA và máy đo được kiểm tra, hiệu chỉnh định kỳ |
□ |
| Thời gian đạt HA mục tiêu | HA tối ưu: tái đánh giá sau 2 năm
Tiền THA: tái đánh giá sau 1 năm THA độ 1: xác định trong vòng tháng THA độ 2: đánh giá trong vòng tháng THA độ 3: đánh giá và điều trị ngay hoặc trong vòng tuần tùy thuộc vào tình huống lâm sàng và biến chứng |
□ |
| ADR thường gặp của thuốc | Tham khảo phụ lục 3.4 | □ |
TÀI LIỆU THAM THẢO
Tiếng Việt
- Hội Tim mạch học quốc gia Việt Nam (2018), Khuyến cáo về chẩn đoán và điều trị tăng huyết áp 2018.
- Bộ Y tế (2016), Quy trình chuyên môn chẩn đoán và điều trị tăng huyết áp (Ban hành kèm theo quyết định 4068/QĐ-BYT của Bộ trưởng Bộ Y tế).
Tiếng Anh
- Karen Whalen (2018), Chapter 27: Hypertension MTM Data Set, Medication Therapy Management: A Comprehensive Approach, 2e Mc Graw Hill;
- Christopher P. Martin, Robert L. Talbert (2014), Section 1. Cardiology, Pharmacotherapy Bedside Guide; Mc Graw Hill
- Karen J. Mc Connell (2018), Blood Pressure Management of Adult Patients Workbook Supplemental Chapter CARD, ACCP Updates in Therapeutics® 2018: Cardiology Pharmacy Preparatory Review and Recertification Course,
- Saseen JJ, MacLaughlin EJ (2017), Pharmacotherapy: A Pathophysiologic Approach. 10th ed. New York, NY: McGraw-Hill.
2. HƯỚNG DẪN THỰC HÀNH DƯỢC LÂM SÀNG TRONG ĐIỀU TRỊ SUY TIM
2.1. Đại cương về bệnh suy tim mạn
2.1.1. Chẩn đoán
Định nghĩa
Suy tim là hội chứng lâm sàng đặc trưng bởi các triệu chứng điển hình (như khó thở, phù mắt cá chân và mệt mỏi), có thể kèm theo một số dấu hiệu (như tăng áp lực tĩnh mạch, phù ngoại vi) gây ra do các bất thường về cấu trúc và/hoặc chức năng của tim, kết quả làm giảm cung lượng tim và tăng áp lực trong tim khi nghỉ ngơi hoặc căng thẳng.
Các định nghĩa hiện nay về suy tim vẫn tập trung vào giai đoạn bệnh nhân có triệu chứng lâm sàng. Trước khi xuất hiện các triệu chứng lâm sàng này, bệnh nhân có thể có các bất thường về cấu trúc hoặc chức năng của tim (như giảm chức năng thất trái) mà không có triệu chứng kèm theo. Việc phát hiện các dấu hiệu này đóng vai trò rất quan trọng bởi chúng liên quan tới tiên lượng của bệnh nhân và điều trị sớm khi phát hiện ra các bất thường này, làm giảm tỷ lệ tử vong trên bệnh nhân suy giảm chức năng thất trái nhưng chưa có triệu chứng.
Phân loại
a) Phân loại suy tim theo phân suất tống máu
Bệnh nhân suy tim được phân loại dựa trên phân suất tống máu thất trái (LVEF) trên siêu âm như sau:
- Suy tim phân suất tống máu giảm (HFrEF) hay: LVEF < 40%.
- Suy tim phân suất tống máu trung gian (HFmrEF): LVEF 40 – 49%.
- Suy tim phân suất tống máu bảo tồn (HFpEF): LVEF >50%
Suy tim phân suất tống máu giảm (HFrEF) được gọi là suy tim tâm thu và suy tim phân suất tống máu bảo tồn (HFpEF) được gọi là suy tim tâm trương.
b) Phân loại suy tim theo triệu chứng cơ năng
Phân loại suy tim của Hội Tim mạch New York dựa trên triệu chứng cơ năng và khả năng gắng sức của bệnh nhân. Cách phân loại này đơn giản, tiện dụng nhưng tương đối chủ quan. Các tổn thương hoặc bất thường chức năng tim có thể không thể hiện tương ứng với triệu chứng cơ năng của bệnh nhân.
Bảng 3.12. Phân loại suy tim theo Hội Tim mạch New York (NYHA)
| NYHA | Mô tả |
| I | Không hạn chế hoạt động thể lực. Vận động thể lực thông thường không gây mệt, khó thở hay hồi hộp. |
| II | Hạn chế nhẹ hoạt động thể lực. Bệnh nhân khỏe khi nghỉ ngơi; vận động thể lực thông thường dẫn đến mệt, hồi hộp, khó thở hay đau ngực |
| III | Hạn chế nhiều vận động thể lực. Mặc dù bệnh nhân khỏe khi nghỉ ngơi nhưng chỉ cần vận động nhẹ đã có triệu chứng cơ năng . |
| IV | Không vận động thể lực nào không gây khó chịu. Triệu chứng cơ năng của suy tim xảy ra ngay khi nghỉ ngơi, chỉ một vận động thể lực nhẹ cũng làm triệu chứng cơ năng gia tăng |
Chẩn đoán
Trình tự các bước cần thực hiện để khẳng định chẩn đoán suy tim bao gồm: triệu chứng và dấu hiệu của suy tim, điện tâm đồ, peptid lợi niệu Na (NT-proBNP, BNP) và siêu âm tim.
– Triệu chứng và dấu hiệu của suy tim: thường không đặc hiệu và do đó không giúp phân biệt giữa suy tim với bệnh lý khác, chủ yếu dùng để theo dõi đáp ứng điều trị suy tim.
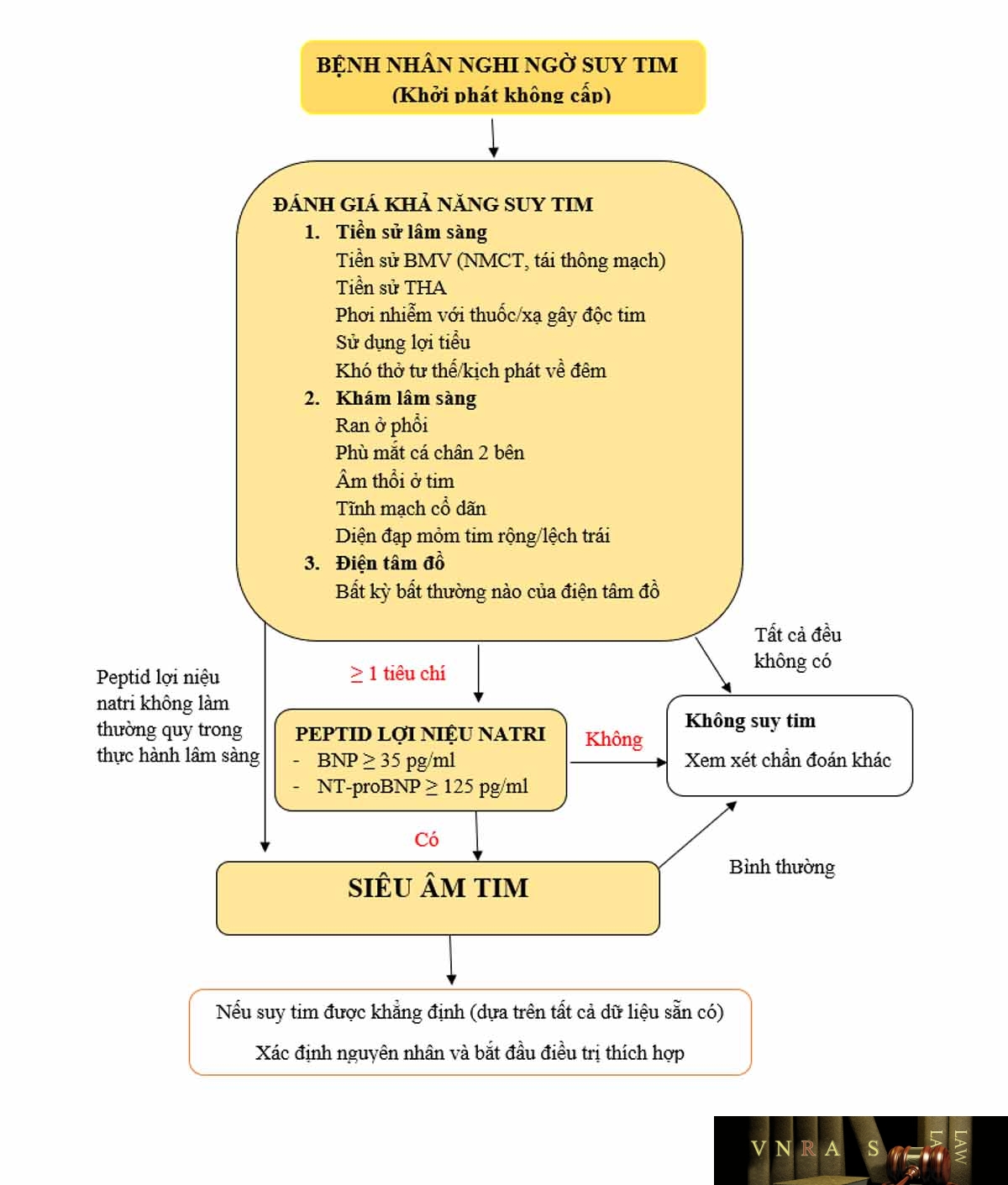
– Điện tâm đồ: điện tâm đồ bất thường làm tăng khả năng chẩn đoán suy tim, nhưng độ đặc hiệu thấp. Một số bất thường trên điện tâm đồ cung cấp thông tin về nguyên nhân (ví dụ: NMCT) và những dấu hiệu trên điện tâm đồ có thể chỉ dẫn cho việc điều trị (ví dụ: thuốc chống đông cho bệnh nhân loạn nhịp). Bệnh nhân suy tim ít khi có điện tâm đồ hoàn toàn bình thường (độ nhạy 89%). Do đó, việc sử dụng thường quy điện tâm đồ chủ yếu là khuyến khích để loại trừ chẩn đoán suy tim.
- Peptid lợi niệu natri: peptid lợi niệu natri tăng cao giúp thiết lập chẩn đoán ban đầu và xác định những đối tượng cần khảo sát tim mạch thêm. Bệnh nhân có giá trị BNP < 35 pg/mL và NT-proBNP < 125 pg/mL có thể loại trừ được các rối loạn chức năng tim mạch quan trọng không cần siêu âm tim. Việc sử dụng peptid lợi niệu natri được khuyến cáo để loại trừ suy tim, nhưng không phải để thiết lập chẩn đoán.
Siêu âm tim: giúp tìm ra những thay đổi về cấu trúc và/hoặc chức năng là nguyên nhân gây nên triệu chứng lâm sàng của bệnh nhân.
2.1.2. Điều trị suy tim mạn tính
Mục tiêu điều trị suy tim mạn tính
Mục tiêu điều trị của suy tim là cải thiện triệu chứng lâm sàng, chất lượng cuộc sống; ngăn ngừa nhập viện và giảm tỷ lệ tử vong.
Thay đổi lối sống
Mặc dù hiện nay có ít nghiên cứu khẳng định vai trò các biện pháp thay đổi lối sống, nhưng một số khuyến cáo sau có thể áp dụng cho bệnh nhân suy tim:
- Chế độ ăn: hạn chế muối thường áp dụng trên bệnh nhân suy tim nặng, suy tim tiến triển, lượng muối tiêu thụ nên < 1.500 mg/ngày trên nhóm đối tượng này. Hạn chế uống rượu, mỗi ngày không quá 2 đơn vị chuẩn (bệnh nhân có bệnh cơ tim do rượu nên ngưng rượu hẳn ); ngưng hút thuốc.
- Giảm cân trên bệnh nhân béo phì; đánh giá tình trạng dinh dưỡng và suy kiệt do suy tim.
- Hoạt động tập luyện: vận động thể lực phù hợp trên bệnh nhân suy tim ổn định làm cải thiện khả năng gắng sức và chất lượng cuộc sống của bệnh nhân. Chế độ luyện tập phải phù hợp với khả năng gắng sức của người bệnh, bắt đầu bằng các hoạt động cơ bắp như đi bộ. Bệnh nhân suy tim nặng được khuyến cáo nghỉ ngơi tại giường.
- Tiêm phòng cúm được khuyến cáo trên tất cả bệnh nhân suy tim.
- Mang thai làm nặng hơn tình trạng suy tim và nguy cơ cao cho cả mẹ và con, đặc biệt trên bệnh nhân suy tim phân độ NYHA III và IV. Lựa chọn phương pháp ngừa thai tùy theo cơ địa và tiền sử bệnh của bệnh nhân.
- Bệnh nhân suy tim nặng nên tránh đến các vùng khí hậu nóng, ẩm; đi du lịch dài ngày hoặc ngồi máy bay lâu vì nguy cơ thuyên tắc tĩnh mạch.
Khuyến cáo điều trị trên bệnh nhân suy tim phân suất tống máu giảm (HFrEF)
Các nhóm thuốc ƯCMC, thuốc CB và thuốc đối kháng thụ thể mineralocorticoid đã chứng minh hiệu quả giảm tỷ lệ tử vong và được khuyến cáo với tất cả bệnh nhân suy tim tâm thu trừ trường hợp chống chỉ định hoặc không dung nạp. Nhóm thuốc CTTA được khuyến cáo với bệnh nhân suy tim tâm thu không dung nạp thuốc ƯCMC hoặc
bệnh nhân sử dụng thuốc ƯCMC nhưng không dung nạp thuốc kháng thụ thể mineralocorticoid do các bằng chứng giảm tỷ lệ tử vong chưa thống nhất giữa các nghiên cứu. Lưu đồ điều trị bệnh nhân suy tim phân suất tống máu giảm của Hội Tim mạch châu Âu năm 2016 được trình bày trong Hình 3.5.
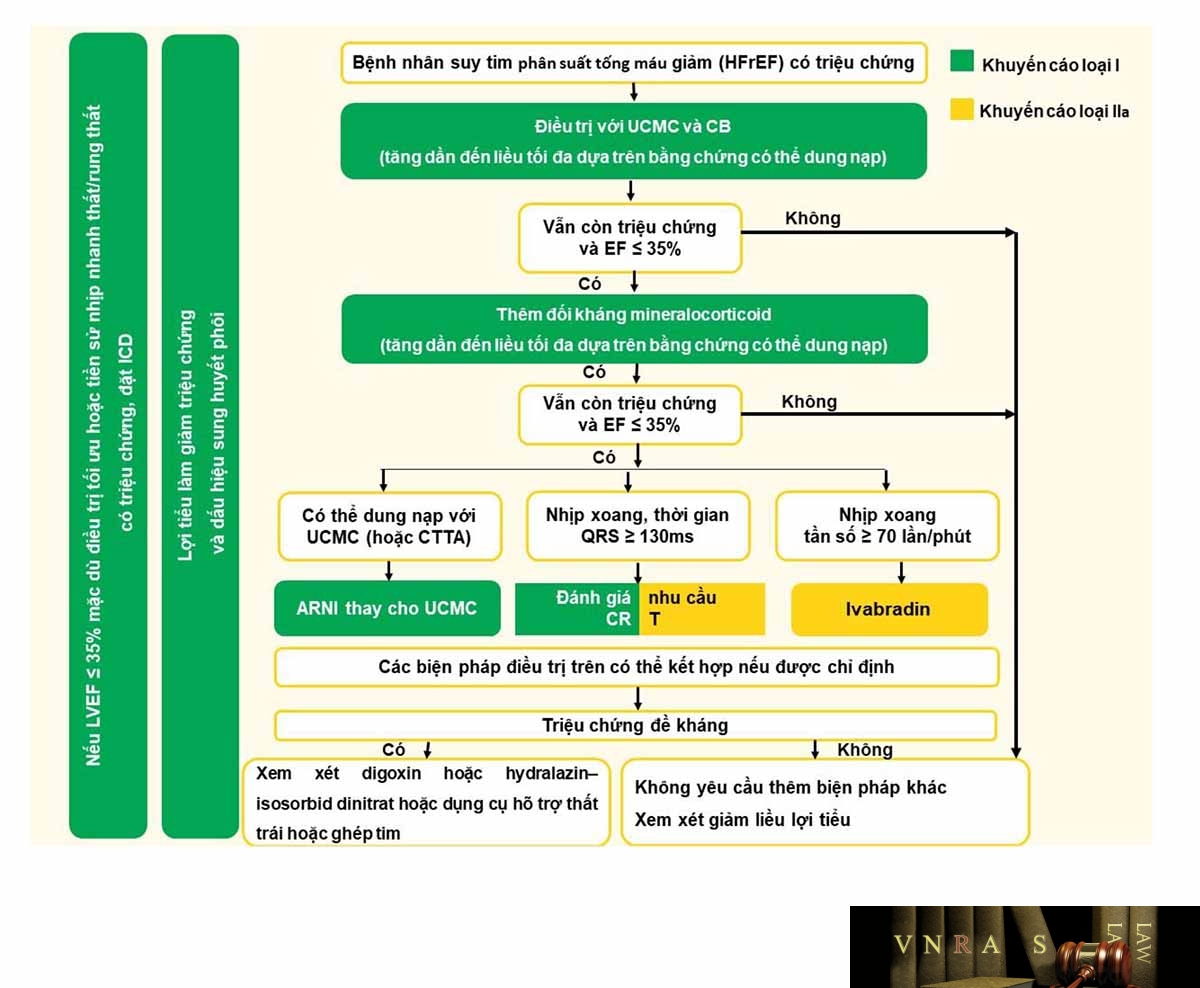
Các thuốc ƯCMC, thuốc CTTA và thuốc CB nên được bắt đầu với liều thấp sau đó tăng dần liều tới liều đích hoặc liều tối đa dung nạp để giảm tử vong và nhập viện trên bệnh nhân suy tim tâm thu.
Một số tác dụng không mong muốn khi sử dụng thuốc ƯCMC hoặc thuốc CTTA và cách xử trí.
– Tăng kali máu (K+ > 5,0 mmol/L) và suy giảm chức năng thận (creatinin máu > 221 mcmol/L hoặc MLCT < 30 mL/phút/1,73 m2).
+ Tăng kali máu và creatinin máu là những tác dụng không mong muốn thường gặp khi sử dụng các thuốc ƯCMC hoặc thuốc CTTA. Trường hợp mức tăng kali, creatinin máu tăng không đáng kể và bệnh nhân không có triệu chứng thì không cần thay đổi phác đồ thuốc ƯCMC hoặc thuốc CTTA.
+ Ngưỡng tăng kali máu < 5,5 mmol/L; creatinin máu tăng tới 266 |imol/L (MLCT < 25 mL/phút/1,73 m2) hoặc tăng 50% so với thời điểm trước khi sử dụng thuốc (tùy theo giá trị nào nhỏ hơn) có thể được chấp nhận khi sử dụng thuốc ƯCMC hoặc thuốc CTTA.
+ Trong trường hợp bệnh nhân tăng kali và creatinin trong máu, cân nhắc dừng sử dụng các thuốc có độc tính trên thận (ví dụ: NSAIDs), các thuốc dùng kèm làm tăng kali máu hoặc giảm liều thuốc lợi tiểu nếu không có dấu hiệu của quá tải dịch. Nếu kali và creatinin trong máu của bệnh nhân vẫn tăng mặc dù đã hiệu chỉnh liều các thuốc dùng kèm, thì cân nhắc giảm một nửa liều thuốc ƯCMC hoặc thuốc CTTA đang dùng và kiểm tra lại kết quả sinh hóa sau 1 – 2 tuần.
+ Trong trường hợp kali máu > 5,5 mmol/L; creatinin máu tăng > 100% so với thời điểm trước khi sử dụng thuốc hoặc creatinin máu > 310 mcmol/L (MLCT < 20 mL/phút/1,73 m2), nên ngừng sử dụng thuốc ƯCMC hoặc thuốc CTTA.
– Huyết áp thấp
+ Thông thường, bệnh nhân sử dụng thuốc ƯCMC hoặc thuốc CTTA có HA thấp nhưng không có triệu chứng thì không cần thay đổi liều thuốc ƯCMC hoặc thuốc CTTA. Tuy nhiên, trong trường hợp bệnh nhân có dấu hiệu tụt HA (chóng mặt, đau đầu) hoặc HATT < 90 mmHg, cần phải đánh giá lại phác đồ thuốc ƯCMC hoặc thuốc CTTA.
+ Xem xét nhu cầu sử dụng các thuốc nitrat, thuốc CKCa và các thuốc giãn mạch khác; giảm liều hoặc dừng sử dụng các thuốc này nếu được.
+ Nếu bệnh nhân không có dấu hiệu và triệu chứng của quá tải dịch thì có thể cân nhắc giảm liều lợi tiểu.
Một số tác dụng không mong muốn khi sử dụng thuốc chẹn beta và cách xử trí
– Triệu chứng suy tim nặng lên
+ Nếu bệnh nhân có dấu hiệu của sung huyết hay quá tải dịch, có thể tăng liều thuốc lợi tiểu hoặc giảm một nửa liều thuốc CB nếu bệnh nhân không đáp ứng khi đã tăng liều thuốc lợi tiểu.
+ Nếu bệnh nhân cảm thấy mệt mỏi, có thể giảm nửa liều thuốc CB và đánh giá lại bệnh nhân sau 1 – 2 tuần. Trong trường hợp bệnh nhân có triệu chứng suy tim mức độ nghiêm trọng, có thể ngừng sử dụng thuốc CB và tham khảo ý kiến của chuyên gia.
– Nhịp tim chậm
Nếu nhịp tim < 50 lần/phút và các triệu chứng suy tim nặng lên, có thể giảm một nửa liều thuốc CB.
+ Đánh giá lại nhu cầu sử dụng các thuốc làm chậm nhịp tim khác của bệnh nhân như: digoxin, amiodaron, diltiazem hay verapamil.
+ Đánh giá điện tâm đồ để loại trừ block tim.
+ Tham khảo ý kiến chuyên gia.
– HA thấp
Nếu bệnh nhân có HA thấp nhưng không xuất hiện triệu chứng thì không cần thay đổi phác đồ thuốc chẹn beta. Trong trường hợp bệnh nhân có HA thấp kèm theo triệu chứng (ví dụ: đau đầu, chóng mặt):
+ Xem xét nhu cầu sử dụng các thuốc nitrat, thuốc CKCa và các thuốc giãn mạch khác; giảm liều hoặc dừng sử dụng các thuốc này nếu được.
+ Nếu bệnh nhân không có dấu hiệu và triệu chứng của quá tải dịch, có thể cân nhắc giảm liều thuốc lợi tiểu.
Một số tác dụng không mong muốn khi sử dụng thuốc đối kháng mineralocorticoid.
– Nếu K+ máu > 5,5 mmol/L hoặc creatinin máu > 221 |imol/L (MLCT < 30 mL/phút/1,73 m2): giảm nửa liều và theo dõi kết quả sinh hóa máu của bệnh nhân.
– Nếu K+ máu > 6,0 mmol/L hoặc creatinin máu > 310 |imol/L (MLCT < 20 mL/phút/1,73 m2): ngừng sử dụng ngay lập tức và tham khảo ý kiến của chuyên gia.
Khuyến cáo điều trị trên bệnh nhân suy tim phân suất tống máu trung gian (HFmrEF) và phân suất tống máu bảo tồn (HFpEF)
Hiện nay, chưa có bằng chứng thuyết phục về sử dụng thuốc điều trị suy tim nhằm giảm tỷ lệ tử vong hay nhập viện ở bệnh nhân suy tim phân suất tống máu trung gian hoặc bảo tồn. Mặc dù vậy, sử dụng thuốc điều trị suy tim có thể giảm triệu chứng và nâng cao chất lượng cuộc sống của bệnh nhân.
– Nên sàng lọc bệnh mắc kèm đối với bệnh nhân suy tim phân suất tống máu giảm hoặc bảo tồn để điều trị hoặc can thiệp thích hợp nhằm cải thiện triệu chứng và tiên lượng.
– Thuốc lợi tiểu được khuyến cáo trên bệnh nhân suy tim phân suất tống máu trung gian hoặc bảo tồn có dấu hiệu sung huyết để giảm triệu chứng và dấu hiệu suy tim.
Lựa chọn thuốc cho bệnh nhân suy tim có bệnh mắc kèm
Bảng 3.13. Một số lưu ý khi lựa chọn thuốc cho bệnh nhân suy tim có bệnh mắc kèm
| Bệnh mắc kèm hoặc dân số đặc biệt | Lựa chọn thuốc |
| Hẹp động mạch chủ | Lựa chọn thuốc
Bệnh nhân hẹp động mạch chủ trung bình đến nặng có thể không dung nạp với thuốc giãn động mạch. Thuốc chẹn beta như bisoprolol và metoprolol succinat phù hợp hơn trong điều trị HFrEF. Các tác dụng trên thụ thể alpha của carvedilol có thể không được dung nạp. Thận trọng khi phối hợp thuốc lợi tiểu để điều trị triệu chứng suy tim. Có thể tiếp tục dùng thuốc ƯCMC hay CTTA nếu bệnh nhân mới chẩn đoán và dung nạp, tuy nhiên nên duy trì ở liều thấp. Tránh sử dụng Thuốc CKCa nhóm dihydropyridin và non-dihydropyridin. |
| Sau NMCT | Lựa chọn thuốc
Trên bệnh nhân HFrEF, carvedilol trong nhóm CB là thuốc ưu tiên được lựa chọn. Tránh sử dụng Thuốc CKCa nhóm dihydropyridin giải phóng nhanh, thuốc CB với hoạt tính giao cảm nội tại (acebutolol, penbutolol, pindolol) |
| Rối loạn nhịp nhĩ | Lựa chọn thuốc
Thuốc CB hay thuốc CKCa nhóm non-dihydropyridin. Trên bệnh nhân HFrEF, sử dụng bisoprolol, carvedilol hoặc metoprolol succinat. Digoxin có thể được chỉ định để hỗ trợ kiểm soát tần số thất Tránh sử dụng Thuốc CKCa dihydropyridin giải phóng nhanh (nhịp tim nhanh phản xạ), thuốc CKCa non-dihydropyridin trên bệnh nhân HFrEF (tác động inotrope âm tính), thuốc CB với hoạt tính giao cảm nội tại (acebutolol, penbutolol, pindolol) |
| Rối loạn nhịp thất | Lựa chọn thuốc
Trên bệnh nhân HFrEF, nhóm CB được sử dụng: bisoprolol, carvedilol, hoặc metoprolol succinat. Amiodaron hoặc sotalol có thể thêm vào để ngăn ngừa rối loạn nhịp và hoặc hạn chế số lần shock điện của máy khử rung. Tránh sử dụng Thuốc CKCa nhóm dihydropyridin giải phóng nhanh, thuốc CKCa nhóm non – dihydropyridin, digoxin, thuốc CB với hoạt tính giao cảm nội tại (acebutolol, penbutolol, pindolol) |
| Nguy cơ cao bệnh mạch vành | Lựa chọn thuốc
Trên bệnh nhân HFrEF, thuốc CB được sử dụng: bisoprolol, carvedilol hoặc metoprolol succinat và thuốc ƯCMC CTTA Tránh sử dụng Thuốc CKCa nhóm dihydropyridin giải phóng nhanh, thuốc CB với hoạt tính giao cảm nội tại (acebutolol, penbutolol, pindolol). |
| Dự phòng đột quỵ thứ phát | Lựa chọn thuốc
Thuốc lợi tiểu phối hợp với ƯCMC hay CTTA nếu HA cao trên bệnh nhân HFpEF. Đối với bệnh nhân HFrEF, chưa có bằng chứng theo thời gian tiến cứu cho thấy cần ưu tiên điều trị đột quỵ. Tuy nhiên, mục tiêu điều trị là kiểm soát HA nghiêm ngặt Điều trị HFrEF theo phác đồ điều trị, nếu HA vẫn còn tăng sau khi đã điều trị tối đa, thêm thuốc CKCa nhóm dihydropyridin hoặc thuốc lợi tiểu. |
| Đau thắt ngực (ĐTN) – nMCt | Lựa chọn thuốc
Trên bệnh nhân HFrEF, thuốc CB là lựa chọn ưu tiên gồm: bisoprolol, carvedilol, metoprolol succinat hoặc nebivolol. Nếu thuốc CB đã dùng đến liều tối đa dung nạp nhưng bệnh nhân đáp ứng kém hoặc BN không dung nạp với thuốc CB: cân nhắc sử dụng ivabradin (nhịp tim khi nghỉ > lần/phút). Trimetazidin có thể được cân nhắc trên bệnh nhân vẫn còn ĐTN mặc dù đã dùng CB hoặc có thể chỉ định thay thế CB. Nicorandil có thể cân nhắc sử dụng ở bệnh nhân không dùng thuốc CB để làm giảm triệu chứng đau ngực. Thêm thuốc nitrat tác dụng kéo dài nếu còn ĐTN. Ranolazin có thể được cân nhắc sử dụng ở bệnh nhân không dung nạp thuốc CB để làm giảm triệu chứng đau ngực, tuy nhiên nên sử dụng thận trọng trên bệnh nhân HFrEF. Bất kể bệnh nhân có hoặc không có ĐTN, nên sử dụng thuốc ƯCMC hoặc CTTA trừ khi chống chỉ định hoặc không dung nạp. Tránh sử dụng Trong trường hợp sử dụng thuốc CKCa khi bệnh nhân có ĐTN: tránh thuốc CKCa nhóm dihydropyridin giải phóng nhanh và tránh thuốc CKCa nhóm non – dihydropyridin trên bệnh nhân HFrEF |
| Tái thông mạch vành | Lựa chọn thuốc
Nếu bệnh nhân ĐTN không tái thông mạch vành thì phối hợp ba thuốc có thể được cân nhắc trên BN vẫn còn đau ngực mặc dù đã điều trị với thuốc CB, ivabradin. Thuốc phối hợp thêm để giảm triệu chứng có thể là: trimetazidin, nicoraldin, thuốc CKCa nhóm dihydropyridin, ranolazin. Tránh sử dụng Bất kỳ phối hợp nào giữa các thuốc ivabradin, ranolazin và nicorandil. Phối hợp giữa nicorandil và nitrat. Thuốc CKCa nhóm non – dihydropyridin trên bệnh nhân HFrEF. |
| Người gốc Phi | Không có khuyến cáo riêng biệt trên bệnh nhân HFpEF. HA có thể kiểm soát tốt với thuốc lợi tiểu và CKCa dihydropyridin.
Trên bệnh nhân HFrEF, tối đa hóa sử dụng chẹn beta và ƯCMC hay CTTA Cân nhắc phối hợp hydralazin và isosorbid dinitrat trên bệnh nhân có phân suất tống máu thấp và ít nhất có những triệu chứng của phân loại NYHA II. |
| Chậm nhịp tim | Tối đa hóa những thuốc điều trị suy tim mà không ảnh hưởng lên nhịp tim. Cân nhắc dùng các thiết bị hỗ trợ trên bệnh nhân có HFrEF (như phương pháp tái đồng bộ mạn tính-CRT). |
| Bệnh thận mạn | Bệnh nhân suy tim mắc kèm bệnh thận mạn có tiên lượng sống còn kém hơn. Bệnh nhân có thể không thể dung nạp liều đích các thuốc điều trị suy tim. Bệnh nhân cũng có nguy cơ tăng kali máu và tổn thương thận cấp khi sử dụng đồng thời với thuốc lợi tiểu.
Lựa chọn thuốc Sử dụng thuốc ƯCMC Trường hợp bệnh nhân không dung nạp thuốc ƯCMC, sử dụng thuốc CTTA |
| ĐTĐ | Lựa chọn thuốc
Khuyến cáo sử dụng thuốc CB ở bệnh nhân HFrEF mặc dù CB có thể làm đường huyết khó kiểm soát hơn Carvedilol có tác động trung tính trên HbA1c. Thuốc CKCa nhóm non-dihydropyridin có thể sử dụng trên bệnh nhân HFpEF nếu gần đây BN không có nhồi máu cơ tim Sử dụng thuốc ƯCMC hay CTTA nếu không có chống chỉ định hoặc không dung nạp Bệnh nhân đái tháo đường sử dụng thuốc đối kháng aldosteron có nguy cơ cao tăng kali máu Metformin là lựa chọn hàng đầu trong điều trị ĐTĐ typ 2 trừ khi có chống chỉ định hoặc không dung nạp. Thuốc ức chế SGLT – 2 được khuyến cáo thêm vào phác đồ metformin nếu không đạt mục tiêu HbA1c sau 3 tháng Tránh sử dụng Khuyến cáo nên tránh sử dụng nhóm thiazolidinedion ở BN suy tim. |
| THA | Bệnh nhân HFrEF: tối ưu hóa trị với thuốc CB và ƯCMC hoặc CTTA nếu không dung nạp ƯCMC
Cân nhắc thuốc đối kháng aldosteron, ARNI và/hoặc phối hợp hydralazin/ isosorbid dinitrat nếu BN có chỉ định. Thêm thuốc lợi tiểu nếu BN có triệu chứng. Thuốc CKCa nhóm dihydropyridin có thể thêm vào phác đồ điều trị suy tim. |
| Bệnh phổi (hen phế quản và COPD) | Hen phế quản là chống chỉ định tương đối của thuốc CB trong điều trị suy tim. Không chống chỉ định thuốc CB trên bệnh nhân suy tim mắc kèm COPD. Bệnh nhân suy tim mắc kèm hen phế quản hoặc COPD có thể dùng các thuốc chẹn thụ thể beta 1 chọn lọc trên tim như: bisoprolol, metoprolol succinat hoặc nebivolol với liều khởi đầu thấp và theo dõi thận trọng các dấu hiệu tắc nghẽn đường hô hấp, đặc biệt trên bệnh nhân cao tuổi. |
| HA thấp | Đánh giá sử dụng thuốc lợi tiểu từ đầu và giảm liều nếu triệu chứng được kiểm soát tốt.
Bệnh nhân HFrEF có thể có HA thấp khi sử dụng các thuốc điều trị suy tim. Bắt đầu dùng liều thấp thuốc CB, ƯCMC, thuốc đối kháng aldosteron và tăng dần liều nếu bệnh nhân không có triệu chứng của HA thấp. |
Hướng dẫn thực hành DLS trên bệnh nhân suy tim
Trong nội dung này, các hoạt động thực hành dược lâm sàng được trình bày theo các bước của quy trình chăm sóc dược đầy đủ trên bệnh nhân. Tùy theo điều kiện của từng cơ sở y tế tại các tuyến khác nhau, có thể triển khai các hoạt động theo hướng dẫn chung được trình bày trong chương 1.
2.1.3. Khai thác thông tin về tiền sử bệnh và tiền sử thuốc
Bảng 3.14. Phiếu khai thác tiền sử bệnh và dùng thuốc
| THÔNG TIN BỆNH NHÂN
Họ tên:……………Năm sinh:……………… Giới tính: …………. Chẩn đoán: ……………………………………………………………………………………………… ĐÁNH GIÁ KẾT QUẢ PHỎNG VẤN Dược sĩ phỏng vấn: ……………………………………………………. Ngày phỏng vấn: ………………………………………………………………………………. |
|||
| TT | Nội dung câu hỏi | Thông tin từ bệnh nhân | Cần tư vấn lại |
| A. Hiểu biết của bệnh nhân về bệnh suy tim mạn | |||
| 1 | Ông/bà đi bộ bao xa thì cảm thấy mệt, khó thở hoặc leo được tối đa bao nhiêu tầng lầu mà không thấy mệt? | ||
| 2 | Ông/bà khi đang nghỉ ngơi (không hoạt động) có mệt không? | ||
| 3 | Những triệu chứng mệt hay khó thở trên có giảm khi ông/bà nằm nghỉ không? | ||
| 4 | Ông/bà đã được chẩn đoán suy tim bao lâu rồi? | ||
| 5 | Ông/bà đã từng bị NMCT chưa? Đã từng phẫu thuật tim chưa? Có đặt stent không? Nếu có, ông bà đặt stent khi nào? | ||
| 6 | Ông/bà có đi tái khám thường xuyên không? Ông/bà có đem theo đơn thuốc gần đây nhất không? | ||
| 7 | Cân nặng bình thường của ông/bà là bao nhiêu? (so sánh với cân nặng lúc nhập viện của ông/bà) | ||
| B. Hiểu biết của bệnh nhân về thuốc điều trị suy tim mạn đang dùng | |||
| 8 | Ông/bà có sử dụng thuốc đúng theo đơn thuốc bác sĩ kê không: về thời điểm dùng, số lượng thuốc? | ||
| 9 | Ông/bà có thường quên liều thuốc của mình không? | ||
| 10 | Ông/bà đã bao giờ tự ngừng dùng bất kỳ loại thuốc nào trong đơn mà không báo cho bác sĩ không? Nếu có, tại sao? | ||
| 11 | Ông/bà có dùng thực phẩm chức năng, các loại thuốc khác trong đơn bác sĩ kê không (ví dụ như thuốc bắc, thuốc nam,…)? | ||
| 12 | Ông/bà có thường ăn mặn không (ví dụ gia vị, nước tương, nước mắm,.)? | ||
| 13 | Ông/bà uống bao nhiêu lít nước mỗi ngày? | ||
| C. Hiểu biết của bệnh nhân về các yếu tố nguy cơ của bệnh suy tim mạn | |||
| 14 | Ông/bà có hút thuốc không? Nếu có, ông/bà hút bao nhiêu điếu một ngày? | ||
| 15 | Hiện tại, HA của ông/bà là bao nhiêu? Nhịp tim là bao nhiêu? | ||
| 16 | Ông/bà có thường xuyên kiểm tra HA, nhịp tim không? | ||
| 17 | HA thông thường của ông/bà là bao nhiêu? Nhịp tim là bao nhiêu? | ||
| 18 | Mức cholesterol của ông/bà như thế nào? | ||
| 19 | Những hoạt động thể lực/môn thể thao nào ông/bà thường tham gia? | ||
| D. Khả năng dự phòng của bệnh nhân trước các tình huống khẩn cấp liên quan đến bệnh suy tim | |||
| 20 | Buổi tối, ông/bà ngủ ngon giấc không? Có thức giấc vì mệt hay khó thở không? Nếu thường xuyên thức giấc vì những triệu chứng trên thì ông bà có đến bác sĩ khám bệnh không? | ||
| 21 | Ông/bà có từng bị HA thấp không? Những lúc đó ông/bà có bị đau đầu, hoa mắt, chóng mặt không? | ||
| 22 | Ông/bà có từng bị nhịp tim nhanh không? | ||
2.1.4. Đánh giá lâm sàng và cận lâm sàng
Tham khảo phụ lục 3.1
2.1.5. Đánh giá sử dụng thuốc
Một số vấn đề liên quan đến thuốc trong điều trị suy tim mạn tính
Bảng 3.15. Một số vấn đề liên quan đến thuốc trong điều trị suy tim mạn tính
| Các vấn đề | Ví dụ |
| Không tuân thủ | Dấu hiệu và triệu chứng suy tim nặng hơn do không tuân thủ biện pháp không dùng thuốc (ví dụ hạn chế muối)
Nhập viện do không tuân thủ dùng thuốc như thuốc chẹn beta, thuốc lợi tiểu. |
| Thuốc không cần thiết | Phối hợp cả thuốc ƯCMC và CTTA trong điều trị suy tim phân suất tống máu bảo tồn |
| Cần bổ sung thuốc | Không bổ sung liều thấp digoxin trên bệnh nhân suy tim phân suất tống máu bảo tồn và rung nhĩ có tần số tim chưa tối ưu đã sử dụng liều tối đa thuốc CB |
| Thuốc không hiệu quả | Sử dụng metoprolol tartrat cho bệnh nhân suy tim phân suất tống máu giảm Sử dụng liều cao furosemid trên bệnh nhân có cổ trướng đang tiến triển xấu hơn, khó thở khi gắng sức và gan to (giảm hấp thu furosemid đường uống) |
| Liều thấp | Sử dụng furosemid 20 mg trên bệnh nhân cổ trướng đang tiến triển xấu hơn |
| Liều cao | Bệnh nhân mắc kèm bệnh thận mạn sử dụng spironolacton liều đích và bị tăng kali máu
Nhịp tim chậm có triệu chứng khi dùng metoprolol succinat 150 mg mỗi ngày |
| Phản ứng có hại của thuốc | Tụt HA tư thế khi sử dụng carvedilol
Tăng kali máu và suy giảm chức năng thận khi dùng thuốc ƯCMC hoặc CTTA. |
Bảng 3.16. Một số thuốc làm nặng thêm tình trạng suy tim
| Cơ chế dự đoán | Thuốc có nguy cơ cao gây suy tim |
| Rối loạn nhịp tim | Cilostazol, citalopram |
| Gây độc tính trên tim trực tiếp | Amphotericin B, các anthracyclin, anagrelid, bevacizumab, cloroquin, clozapin, cyclophosphamid, cytarabin, fluorouracil, hydroxycloroquin, ifosfamid, interferon, interleukin-2, lenalidomid, lithium, pertuzumab, stimulants, trastuzumab, các thuốc ức chế TNFa |
| Giữ dịch/nước | Các corticosteroid, NSAID, thiazolidinedion |
| Tăng HA | Bevacizumab, các NSAID, sorafenib, sunitinib |
| Tương tác với các thuốc điều trị suy tim | Nhóm thuốc NSAID |
| Tác động inotrope/chrorotrope âm tính | Diltiazem, disopyramid, dronedaron, flecainid, itraconazol, propafenon, sotalol, verapamil |
| Phá hủy mạch máu | Bromocriptin, ergotamin |
| Không rõ | Alogliptin, bosentan, epoprostenol, pramipexol, saxagliptin |
2.1.6. Lập kế hoạch điều trị
Bảng 3.17. Kế hoạch điều trị cho bệnh nhân suy tim
| Hoạt động chính | Nội dung hoạt động | Hướng dẫn chi tiết | Kế hoạch chăm sóc của dược sĩ lâm sàng cho người bệnh | Thực hiện |
| Xác định mục tiêu điều trị | Cải thiện triệu chứng lâm sàng, chất lượng cuộc sống, ngăn ngừa nhập viện, giảm tỷ lệ tử vong | □ | ||
| Kiểm soát các yếu tố nguy cơ tim mạch và các bệnh đồng mắc theo các khuyến cáo hiện hành | Rối loạn lipid máu | Tham khảo phụ lục 3.6
– Bệnh nhân có nguy cơ tim mạch rất cao: khuyến cáo dùng statin liều cao với đích LDL-C < 1,8 mmol/L (70 mg/dL) hoặc giảm >50% nếu LDL-C ban đầu là từ 1,8-3,5 mmol/L (70-135 mg/dL). – Bệnh nhân có nguy cơ tim mạch cao: khuyến cáo dùng statin liều trung bình với đích LDL-C < 2,6 mmol/L (100 mg/dL) hoặc giảm > 50% nếu LDL-C ban đầu là 2,6-5,2 mmol/L (100-200 mg/dL). – Bệnh nhân có nguy cơ tim mạch thấp – trung bình, khuyến cáo dùng statin liều trung bình với đích LDL-C < 3 mmol/L (115 mg/dL). |
□ | |
| Đái tháo đường | – Tham khảo chương Đái tháo đường | □ | ||
| Lập kế hoạch điều trị
|
Thuốc điều trị | Chống chỉ định và thận trọng | Phụ lục 3.2 | □ |
| Liều dùng | Phụ lục 3.3 | □ | ||
| Tác dụng không mong muốn | Phụ lục 3.4 | □ | ||
| Tương tác thuốc | Phụ lục 3.5 | □ | ||
| Chế độ sinh hoạt
|
Chế độ ăn | – Tránh nhập lượng dịch quá mức
– Không cần hạn chế dịch thường quy ở bệnh nhân suy tim độ 2,3 – Hạn chế muối ăn vào < 2 g/ngày (khoảng 1/4 muỗng cà phê) – Hạn chế ăn chất béo bão hòa – Hạn chế uống cà phê, uống quá mức có thể làm tăng nhịp tim, tăng huyết áp và khởi phát rối loạn nhịp – Bổ sung thêm omega -3 – Ăn nhiều chất xơ, tránh táo bón (dễ gây đau thắt ngực, khó thở hay rối loạn nhịp) – Nên ăn làm nhiều bữa nhỏ |
□ | |
| Rượu, thuốc lá và các chất cấm | – Rượu gây độc trực tiếp lên tim, có thể làm giảm co bóp cơ tim và làm tăng rối loạn nhịp
– Hạn chế uống rượu bia. Kiêng rượu bia nếu bệnh nhân bị bệnh cơ tim do rượu Giới hạn lượng rượu mỗi ngày: đơn vị cho nam giới và đơn vị cho nữ ( đơn vị tương đương 10 mL rượu nguyên chất hay 1 ly rượu vang hoặc 0,5 lít bia) – Bỏ thuốc lá và hoặc các chất cấm, tránh hút thuốc lá thụ động – Tư vấn và điều trị cai thuốc lá |
□ | ||
|
Lập kế hoạch theo
|
Hoạt động tập luyện | – Hiểu được lợi ích của tập thể dục
– Mức độ và hình thức tập luyện dựa trên từng bệnh nhân cụ thể – Khuyến khích tập luyện khoảng 30 phút/ ngày, từ 5 – 7 ngày trong tuần với cách tăng cường độ từ từ lúc khởi đầu và giảm dần cường độ lúc cuối buổi tập – Khi lâm sàng ổn định, khuyến khích bệnh nhân thực hiện các công việc hàng ngày và các hoạt động lúc nhàn rỗi mà không gây ra triệu chứng |
□ | |
| Hoạt động tình dục | – Quan hệ tình dục có vẻ an toàn ở bệnh nhân có khả năng hoạt động > 6 METs (tương đương leo lên được 2 tầng lầu mà không mệt khó thở hay đau ngực)
– Bệnh nhân có thể dùng nitroglycerin dưới lưỡi để ngừa đau ngực và khó thở trong quá trình giao hợp – Bệnh nhân có thể dùng thuốc điều trị rối loạn cương (tadalafil, sildenafil.) nhưng phải nhớ chống chỉ định dùng nitrat sau đó (chỉ cho nitrat sau khi uống tadalafil ≥ 48 giờ và sildenafil ≥ 24 giờ) hoặc có hạ huyết áp, rối loạn nhịp hay đau thắt ngực. |
□ | ||
| Các nhóm thuốc điều trị
|
Thuốc CB | Đánh giá lại sau hai tuần bắt đầu điều trị hoặc tăng liều Tăng liều trong khoảng thời gian hai tuần một lần Đối với bệnh nhân không ổn định (ví dụ, huyết áp thấp hoặc trung bình hoặc triệu chứng nghiêm trọng), cân nhắc đánh giá khả năng dung nạp trong 2 tuần và điều chỉnh sau 1 tháng. | □ | |
| Thuốc ƯCMC, CTTA hoặc ARNI | Lặp lại các xét nghiệm (ure, creatinin và kali máu) và đánh giá lại 1 – 2 tuần sau khi bắt đầu điều trị hoặc điều chỉnh liều Không điều chỉnh liều sớm hơn tuần. Lặp lại các xét nghiệm trên và đánh giá lại ít nhất mỗi tháng sau đó | □ | ||
| Thuốc đối kháng aldosteron | Lặp lại các xét nghiệm (ure, creatinin và kali máu) và đánh giá lại vào các thời điểm 1 và 4 tuần sau khi bắt đầu điều trị hoặc tăng liều và tại thời điểm 8 và 12 tuần và 6, 9 và 12 tháng, sau đó mỗi 4 tháng. Cân nhắc điều chỉnh các thuốc đối kháng aldosteron trong khoảng thời gian 4 đến 8 tuần. | □ | ||
| Thuốc lợi tiểu | Lặp lại các xét nghiệm (ure, creatinin và kali máu và magie máu và đánh giá lại 1 – 2 tuần sau khi bắt đầu điều trị hoặc điều chỉnh liều. Lưu ý với bệnh nhân mắc bệnh tim mạch cần duy trì nồng độ kali máu ≥ 4,0 mmol/L và nồng độ magie máu ≥ 2,0 mmol/L để hạn chế tối đa nguy cơ loạn nhịp tim. Lặp lại các xét nghiệm và đánh giá lại ít nhất mỗi 4 tháng sau đó | □ | ||
| Phối hợp hydralazin/Isosorbid dinitrat | Đánh giá lại 2 tuần sau khi bắt đầu điều trị hoặc tăng liều Tăng liều trong khoảng thời gian hai tuần một lần Đối với bệnh nhân không ổn định (ví dụ huyết áp thấp), xem xét đánh giá khả năng dung nạp trong 2 tuần và điều chỉnh liều sau 1 tháng. | □ | ||
| Digoxin | Theo dõi chặt chẽ sau khi bắt đầu điều trị hoặc tăng liều digoxin (tần suất theo dõi xét nghiệm chưa được xác định). Nên lặp lại các xét nghiệm (ure, creatinin, kali máu, magie máu và nồng độ đáy digoxin) và đánh giá sau 1 tháng kể từ khi bắt đầu điều trị hoặc điều chỉnh liều. Nếu kết quả nồng độ đáy cả thuốc trong khoảng mục tiêu điều trị (0,5 – 0,8 ng/mL), lặp lại các xét nghiệm và điều chỉnh lại ít nhất mỗi tháng sau đó | □ | ||
| Ivabradin | Đánh giá lại nhịp tim và khả năng dung nạp 2 tuần sau khi bắt đầu điều trị hoặc thay đổi liều. Xem xét thay đổi liều 2 tuần sau khi điều trị. Các thử nghiệm lâm sàng thường đo điện tâm đồ tại mỗi đợt theo dõi. Tuy nhiên điều này có thể không thực sự cần thiết nếu có biện pháp đánh giá chính xác khác thay thế (ví dụ theo dõi huyết áp,…) | □ | ||
| Giáo dục, tư vấn cho người bệnh
|
Về bệnh và mục tiêu điều trị
|
Giải thích về bệnh | Tư vấn cho người bệnh hiểu về bệnh suy tim và một số thuật ngữ chuyên ngành liên quan đến bệnh và các thuốc điều trị suy tim: tham khảo phụ lục chung. | □ |
| Giải thích mục tiêu điều trị | Cải thiện triệu chứng lâm sàng, chất lượng cuộc sống, ngăn ngừa nhập viện, giảm tỷ lệ tử vong | □ | ||
| Thuốc và sự tuân thủ khi dùng thuốc | Với mỗi thuốc điều trị suy tim được kê, người bệnh được tư vấn về: công dụng, liều dùng và cách nhận biết ADR. | □ | ||
| Cách dùng thuốc uống | Với mỗi loại thuốc uống điều trị suy tim được kê, người bệnh được tư vấn về: thời điểm uống thuốc, cách uống thuốc và khoảng cách giữa các lần dùng thuốc.
Hiểu được tầm quan trọng của việc điều trị và lý do phải tuân thủ điều trị lâu dài |
□ | ||
| Chế độ ăn | Tư vấn cho người bệnh về chế độ ăn uống. | □ | ||
| Luyện tập thể dục | Tư vấn cho người bệnh về chế độ luyện tập thể dục | □ | ||
| Rượu, thuốc lá và các chất cấm | Người bệnh được tư vấn và điều trị cai thuốc lá/các chất cấm; hạn chế uống rượu bia | □ | ||
| Hoạt động tình dục | Tư vấn cho người bệnh về chế độ sinh hoạt tình dục phù hợp để tình trạng bệnh suy tim không trở nên trầm trọng hơn | □ | ||
| Mang thai và uống thuốc tránh thai | – Uống thuốc tránh thai liều thấp có nguy cơ (nhưng ít) gây tăng huyết áp và sinh huyết khối
– Mang thai và uống thuốc tránh thai nên cân nhắc nguy cơ và lợi ích mang lại |
□ | ||
| Tiêm chủng | – Nếu không có chống chỉ định, tất cả bệnh nhân suy tim nên được tiêm ngừa phế cầu và cúm hàng năm
– Sung huyết phổi và tăng áp phổi làm tăng nguy cơ viêm phổi (một trong những nguyên nhân chính gây suy tim mất bù cấp, đặc biệt là ở người lớn tuổi) |
□ | ||
| Du lịch | – Cần phải thảo luận kế hoạch trước với bác sĩ điều trị
– Đi máy bay sẽ tốt hơn các phương tiện khác, đặc biệt nếu đi đường dài. Mặc dù vậy, nếu ngồi máy bay lâu, bệnh nhân vẫn có nguy cơ huyết khối tĩnh mạch chi dưới, phù chân – Tránh du lịch lên những nơi độ cao > .500 m vì không khí loãng giảm nồng độ oxy – Mang theo thuốc uống hàng ngày và hồ sơ bệnh tật |
□ | ||
| Các rối loạn thở trong khi ngủ | – Bệnh nhân suy tim có triệu chứng thường có rối loạn thở trong lúc ngủ (ngưng thở khi ngủ do trung ương hoặc do tắc nghẽn)
– Để giảm nguy cơ trên cần phải bỏ thuốc lá, rượu bia và giảm cân nếu có béo phì – Tìm hiểu các biện pháp điều trị nếu có rối loạn thở trong lúc ngủ |
|||
|
|
Lĩnh vực tâm lý xã hội | – Hiểu được triệu chứng trầm cảm và rối loạn nhận thức là khá phổ biến ở những bệnh nhân bị suy tim và quan trọng cần sự giúp đỡ từ xã hội
– Tìm hiểu thêm về các biện pháp điều trị |
□ | |
| Về theo dõi điều trị
|
Theo dõi triệu chứng và tự chăm sóc bản thân | – Theo dõi và nhận biết được các dấu hiệu và triệu chứng
– Ghi lại cân nặng hàng ngày và nhận ra sự tăng cân nhanh chóng – Biết cách thông báo cho cơ sở khám, chữa bệnh và thông báo kịp thời, không chậm trễ – Trong trường hợp tăng khó thở hoặc phù hoặc tăng cân bất ngờ đột ngột trên 2 kg trong 3 ngày, bệnh nhân có thể tăng liều thuốc lợi tiểu và hoặc thông báo cho nhân viên y tế – Sử dụng liệu pháp lợi tiểu linh hoạt nếu phù hợp và được khuyến cáo sau khi đã giáo dục và cung cấp chỉ dẫn chi tiết phù hợp cho bệnh nhân. |
□ | |
| ADR thường gặp của thuốc | Tham khảo phụ lục 3.4 | □ | ||
TÀI LIỆU THAM KHẢO
Tiếng Việt
- Hội Tim mạch học quốc gia Việt Nam (2018), Khuyến cáo về chẩn đoán và điều trị suy tim mạn 2018.
- Bộ Y tế (2016), Quy trình chuyên môn chẩn đoán và điều trị suy tim mạn, NYHA 2 – 3 (Ban hành kèm theo quyết định 4068/QĐ-BYT của Bộ trưởng Bộ Y tế).
Tiếng Anh
- Carie S.Oliphant (2018). Drug-induced cardiovascular disease and drugs to avoid in CV disease. In: ACCP Update in Therapeutics 2018: Cardiology Pharmacy Prepatory Review course. American College of Clinical Pharmacy.
- Clyde W. Yancy, Mariell Jessup et al (2017), 2017 ACC/AHA/HFSA Focused Update of the 2013 ACCF/AHA Guideline for the Management of Heart Failure, Journal of American College Cardiology, 70(6), 776-803.
- Piotr Ponikowski, Adriaan A. Voors et al (2016), 2016 ESC guidelines for the diagnosis and treatment of acute and chronic heart, Eur Heart J, 37, 2129-2200.
- Robert L. (2018), Page II. Chronic Heart Failure. In: ACCP Update in Therapeutics 2018: Cardiology Pharmacy Prepatory Review course. American College of Clinical Pharmacy.
- Shawn D. Anderson, Katherine Vogel Anderson (2018), Chapter 25: Heart Failure MTM Data Set. In: Medication Therapy Management: A Comprehensive Approach, 2e. Mc Graw Hill.
3. HƯỚNG DẪN THỰC HÀNH DƯỢC LÂM SÀNG TRONG ĐIỀU TRỊ RUNG NHĨ KHÔNG DO VAN TIM
3.1. Đại cương về bệnh rung nhĩ không do bệnh van tim
3.1.1. Chẩn đoán
Định nghĩa
Rung nhĩ là rối loạn nhịp trên thất, đặc trưng bởi tình trạng mất đồng bộ điện học và sự co bóp của tâm nhĩ. Đặc trưng của rung nhĩ trên điện tâm đồ là các dao động biên độ thấp quanh đường đẳng điện gọi là sóng f và sự không đều của nhịp thất. Sóng f có tần số 300 đến 600 lần/phút và có sự thay đổi về biên độ, hình dạng và thời gian. Đáp ứng tần số thất trong rung nhĩ có thể thay đổi, phụ thuộc vào trương lực thần kinh tự chủ, yếu tố điện sinh lý của nút nhĩ thất, hiệu quả của thuốc kiểm soát tần số thất trên hệ thống dẫn truyền nhĩ thất và được phân loại thành: < 60 lần/phút là đáp ứng chậm, 60 – 110 lần/phút là đáp ứng trung bình, và > 110 lần/phút là đáp ứng nhanh.
Phân loại
Bảng 3.18. Phân loại rung nhĩ
| Loại rung nhĩ | Định nghĩa |
| Rung nhĩ cơn | – Rung nhĩ kết thúc nhanh chóng hoặc tồn tại trong vòng 7 ngày kể từ khi xuất hiện
– Các cơn rung nhĩ có thể xuất hiện trở lại với tần suất khác nhau |
| Rung nhĩ bền bỉ | Rung nhĩ xuất hiện liên tục kéo dài > 7 ngày |
| Rung nhĩ dai dẳng | Rung nhĩ liên tục > 12 tháng |
| Rung nhĩ mạn tính | – Rung nhĩ mạn tính khi bác sĩ và bệnh nhân cùng chấp nhận việc không thể chuyển nhịp và/hoặc duy trì nhịp xoang
– Rung nhĩ mạn tính thể hiện thái độ về chấp nhận phương pháp điều trị của bệnh nhân và bác sĩ hơn là thuộc tính sinh lý bệnh của rung nhĩ – Việc chấp nhận rung nhĩ mạn tính có thể thay đổi các triệu chứng, hiệu quả của các biện pháp can thiệp và lựa chọn ưu tiên của bệnh nhân cũng như bác sĩ |
| Rung nhĩ không do van tim | Rung nhĩ khi không có hẹp van hai lá do thấp, không có van tim cơ học/sinh học hoặc sửa hẹp van hai lá |
Chẩn đoán
Chẩn đoán rung nhĩ đòi hỏi ghi nhận điện tâm đồ điển hình của rung nhĩ ít nhất 30 giây. Rung nhĩ là rối loạn nhịp trên thất có sự hoạt hóa nhĩ không đồng bộ và co thắt nhĩ không hiệu quả. Trên điện tâm đồ có những đặc điểm:
- Khoảng R-R không đều (trong trường hợp có dẫn truyền nhĩ thất)
- Không có sóng P
- Hoạt động nhĩ không đều biểu hiện bằng sóng f.
Tần số sóng f từ 300-600 lần/phút và thay đổi về biên độ, hình dạng, thời gian. Ngược lại, tần số sóng cuồng nhĩ từ 250-350 lần/phút và cố định về hình dạng và thời gian. Ở V1, sóng f đôi khi đồng dạng và giả như cuồng nhĩ, đặc điểm giúp nhận ra rung nhĩ lúc này là không thấy hoạt động nhĩ ở những chuyển đạo còn lại.
Tần số thất dao động từ 100-160 lần/phút. Khi không có đường dẫn truyền phụ, đáp ứng thất được quyết định bởi đặc tính trơ và dẫn truyền của nút nhĩ thất. Kích thích beta giao cảm làm tăng dẫn truyền qua nút nhĩ thất đối ngược khi kích thích phó giao cảm. Kích thích giao cảm và ức chế phó giao cảm có thể gặp trong các trường hợp như gắng sức, bệnh lý nặng gây ra đáp ứng thất nhanh. Ở bệnh nhân Wolf- Parkinson- White, tần số thất có thể đến 250 lần/phút do dẫn truyền qua đường phụ. Khi tần số thất quá nhanh > 170 lần/phút thì nhịp tim có thể giống như đều.
Chẩn đoán rung nhĩ trước hết cần có bệnh sử và thăm khám cẩn thận. Bệnh nhân cần được đánh giá triệu chứng và diễn tiến của rung nhĩ. Từ đó, phân loại kiểu rung nhĩ (rung nhĩ cơn, rung nhĩ dai dẳng hay rung nhĩ mạn tính); tìm hiểu khởi phát triệu chứng và thời điểm phát hiện rung nhĩ; tìm yếu tố kích thích, tần suất, thời gian và kiểu chấm dứt rung nhĩ; tìm hiểu đáp ứng với thuốc. Đồng thời, cần tìm kiếm bệnh tim cấu trúc cũng như các nguyên nhân có thể hồi phục như cường giáp hay lạm dụng rượu.
- Trên điện tâm đồ, xác định có rung nhĩ hay không, tìm dấu hiệu phì đại thất trái, hội chứng kích thích sớm, block nhánh, nhồi máu cơ tim và những rối loạn nhịp khác.
- Trên siêu âm tim qua thành ngực, cần tìm kiếm bệnh van tim, kích thước các buồng tim, chức năng tâm thu và tâm trương thất trái, áp lực động mạch phổi, phì đại thất trái, huyết khối nhĩ trái và bệnh màng ngoài tim.
- Xét nghiệm máu cần làm: chức năng gan, thận, điện giải và tuyến giáp.
- Một số xét nghiệm khác cần làm thêm như:
+ Test đi bộ 6 phút nếu như khó kiểm soát tần số.
+ Test gắng sức khi kiểm soát tần số khó khăn, xác định rung nhĩ do gắng sức, loại trừ thiếu máu cơ tim trước khi dùng thuốc chống rối loạn nhịp nhóm IC.
+ Theo dõi Holter nếu cần chẩn đoán rối loạn nhịp hoặc giúp đánh giá kiểm soát tần số.
+ Siêu âm tim qua thực quản giúp tìm huyết khối nhĩ trái.
+ Thăm dò điện sinh lý giúp làm rõ cơ chế của nhịp nhanh phức bộ rộng, xác định vị trí cắt đốt.
+ Chụp X-quang ngực giúp tìm những bất thường của mạch máu và nhu mô phổi.
3.1.2. Điều trị
Mục tiêu điều trị
Mục tiêu điều trị của rung nhĩ là cải thiện triệu chứng, phòng ngừa đột quỵ, giảm thời gian và số lần điều trị tại bệnh viện.
Thay đổi lối sống
a) Hút thuốc lá
- Khuyến khích bỏ hút thuốc vì hút thuốc lá và tiếp xúc với khói thuốc lá có thể làm tăng nguy cơ đột quỵ.
- Một số biện pháp để cai thuốc lá: tư vấn, các sản phẩm thay thế nicotin hoặc thuốc kê đơn.
b) Chế độ ăn
- Hạn chế đồ uống có cồn do làm tăng nguy cơ đột quỵ.
- Lượng thức uống có cồn cần hạn chế: Nam < 2 đơn vị/ngày; nữ < 1 đơn vị/ngày (1 đơn vị tương đương 10 mL cồn nguyên chất – 1 ly rượu vang, lon bia, 1 cốc rượu mạnh).
- Chế độ ăn nhiều trái cây, rau quả và các sản phẩm ít chất béo.
- Lượng natri < 2,4 g/ngày; tối ưu < 1,5g muối/ngày.
- Không khuyến cáo bổ sung vitamin hàng ngày.
c)Luyện tập thể dục
- Tập thể dục đều đặn, ít nhất 30 phút/ngày.
- Vật lý trị liệu nếu có khuyết tật do biến chứng của đột quỵ.
Nguyên tắc điều trị
Đối với bệnh nhân rung nhĩ mới chẩn đoán, cần đánh giá 5 khía cạnh sau:
- Có rối loạn huyết động hay triệu chứng nặng
- Yếu tố kích thích (nhiễm độc giáp, nhiễm trùng huyết hay hậu phẫu…) và bệnh tim mạch nền
- Nguy cơ đột quỵ và nhu cầu sử dụng thuốc chống đông
- Tần số tim và nhu cầu kiểm soát tần số
- Đánh giá triệu chứng và quyết định kiểm soát nhịp
Điều trị rung nhĩ bao gồm điều trị yếu tố ảnh hưởng đến tiên lượng (thuốc chống đông và điều trị bệnh lý tim mạch) và cải thiện triệu chứng (kiểm soát nhịp và tần số). Mặc dù đã có nhiều tiến bộ trong điều trị rung nhĩ nhưng bệnh suất vẫn còn khá cao. Thuốc chống đông đường uống làm giảm đáng kể tỷ lệ đột quỵ và tử vong trên bệnh nhân rung nhĩ. Kiểm soát tần số và nhịp giúp cải thiện triệu chứng liên quan đến rung nhĩ và bảo tồn chức năng tim nhưng không cho thấy giảm tử vong và bệnh tật về lâu dài.
Kiểm soát tần số thất
Kiểm soát tần số trong rung nhĩ chia thành hai giai đoạn: cấp và mạn tính.
Trong giai đoạn cấp tính, thuốc CB và nhóm CKCa non-DHP (diltiazem/verapamil) được ưu tiên hơn digoxin do tác dụng khởi phát nhanh. Lựa chọn thuốc và nhịp tim mục tiêu phụ thuộc vào đặc điểm bệnh nhân, triệu chứng, phân suất tống máu và huyết động của bệnh nhân. Với bệnh nhân suy tim phân suất tống máu giảm, có thể phối hợp thuốc chẹn beta và digoxin do diltiazem có tác dụng inotropic âm tính trên bệnh nhân có LVEF < 40%. Đối vối bệnh nhân suy giảm chức năng thất trái nặng, có thể truyền tĩnh mạch amiodaron khi nhịp tim nhanh dẫn tới bất ổn huyết động.
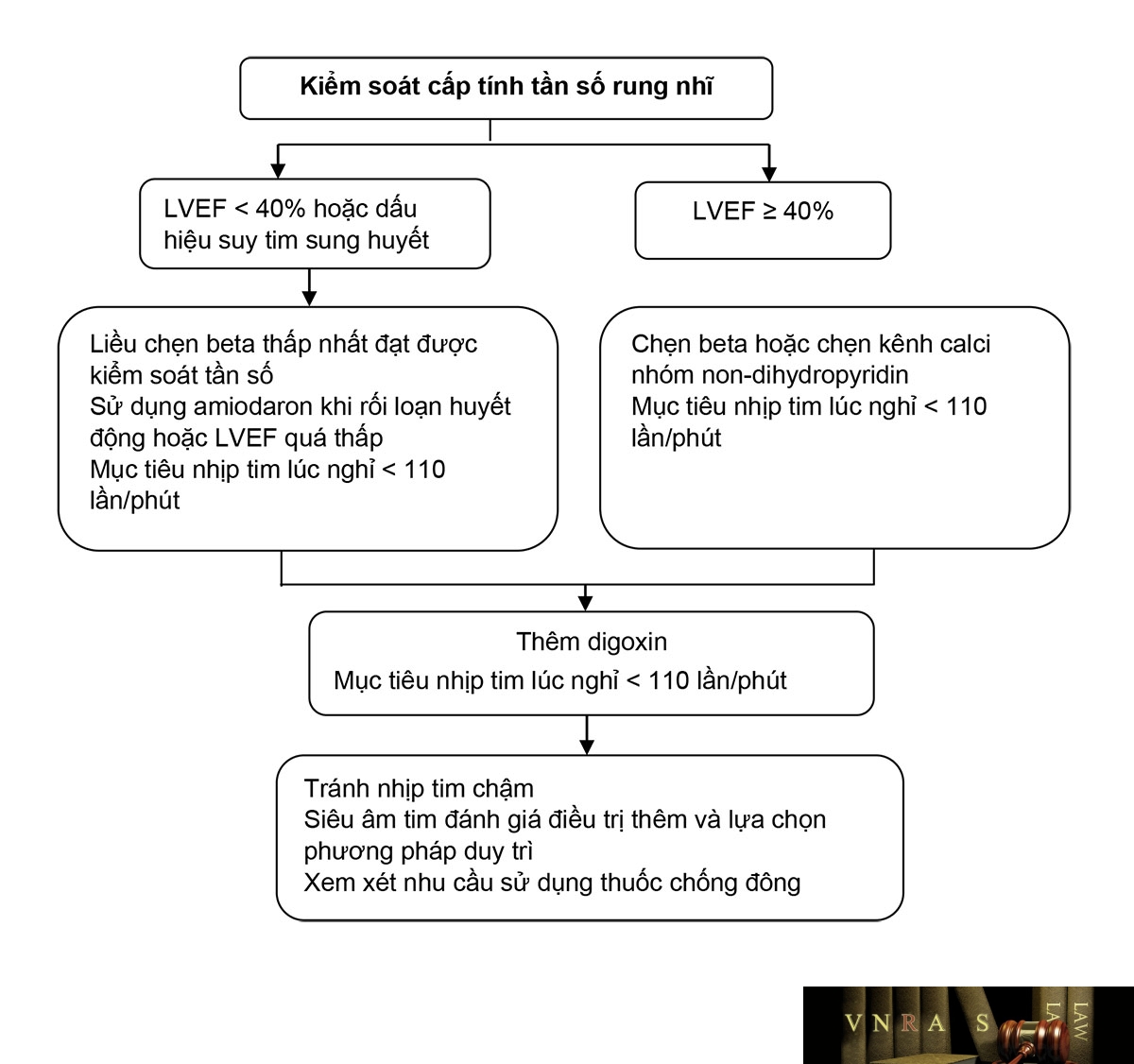
Đối với giai đoạn kiểm soát tần số thất mạn tính, một số khuyến cáo sử dụng thuốc bao gồm:
- Thuốc chẹn beta, digoxin, diltiazem và verapamil được khuyến cáo để kiểm soát tần số thất ở bệnh nhân rung nhĩ có LVEF > 40%.
- Thuốc chẹn beta và/hoặc digoxin được khuyến cáo để kiểm soát tần số thất ở bệnh nhân rung nhĩ có LVEF < 40%.
- Cân nhắc phối hợp thuốc nếu điều trị một thuốc không đạt nhịp tim mục tiêu.
- Nhịp tim khi nghỉ < 110 nhịp/phút có thể được xem là mục tiêu ban đầu của kiểm soát nhịp.
- Cắt đốt nút nhĩ thất nên cân nhắc để kiểm soát tần số tim ở những bệnh nhân không đáp ứng hoặc không dung nạp với điều trị kiểm soát nhịp và kiểm soát tần số tích cực, bệnh nhân sẽ phụ thuộc máy tạo nhịp.
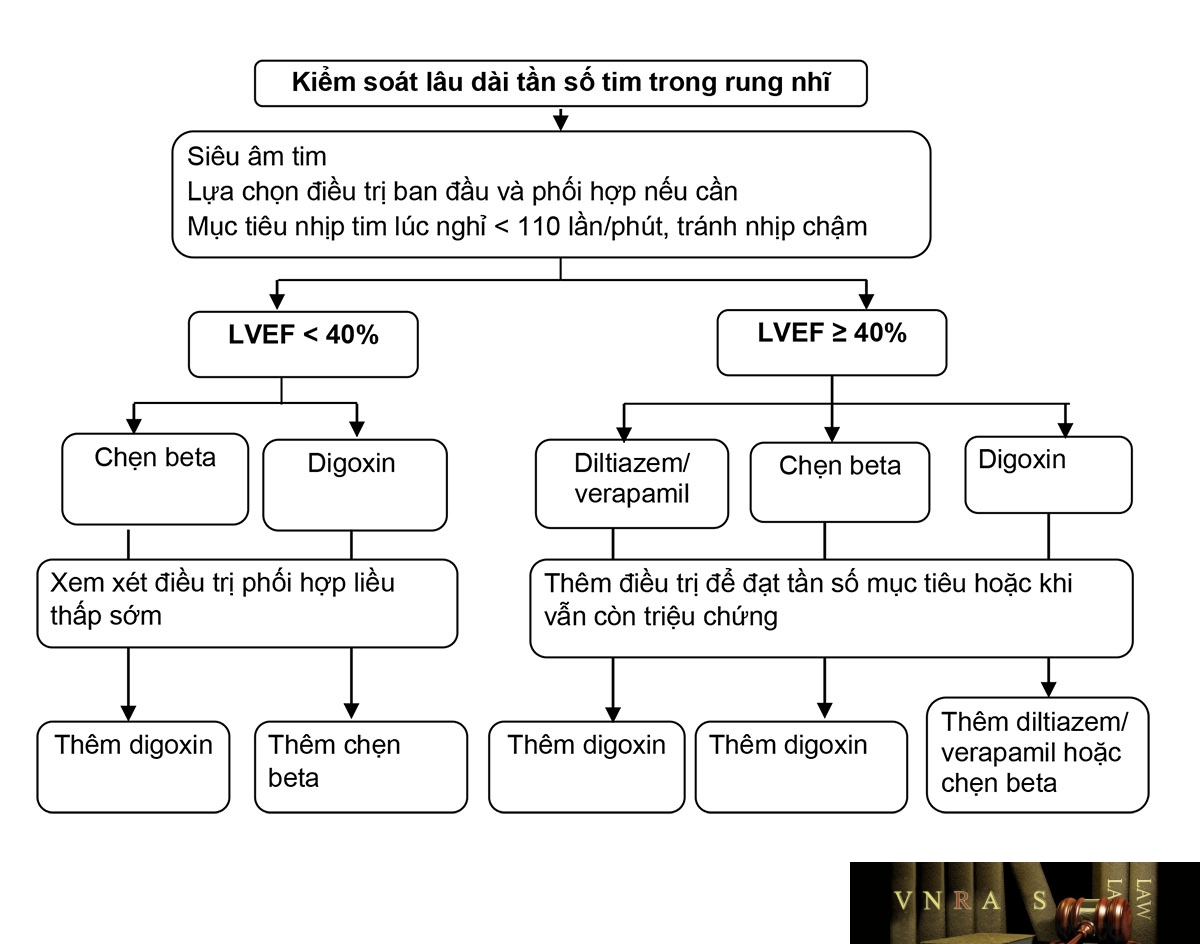
Kiểm soát nhịp
Chuyển nhịp rung nhĩ có thể thực hiện bằng thuốc hoặc bằng điện. Trong những tình huống khẩn cấp như rối loạn huyết động (tụt HA), chuyển nhịp bằng điện được ưu tiên.
Dự phòng huyết khối
a) Phân tầng nguy cơ đột quỵ
Dựa trên các nghiên cứu lớn, các nhà nghiên cứu đã đưa ra các thang điểm đánh giá nguy cơ đột quỵ do huyết khối ở các BN rung nhĩ không do bệnh van tim dựa trên thang điểm CHAD2DS2-VASc.
Bảng 3.19. Thang điểm CHAD2DS2-VASc
| Yếu tố nguy cơ | Điểm |
| Suy tim sung huyết | 1 |
| Tăng HA | 1 |
| Tuổi > 75 | 2 |
| Đái tháo đường | 1 |
| Đột quỵ, thiếu máu não thoáng qua hoặc thuyên tắc mạch | 2 |
| Bệnh mạch máu (tiền sử NMCT, bệnh động mạch ngoại biên, xơ vữa động mạch chủ) | 1 |
| Tuổi 65 – 74 | 1 |
| Nữ giới | 1 |
b) Đánh giá nguy cơ chảy máu theo thang điểm HAS-BLED
Bảng 3.20. Thang điểm HAS-BLED đánh giá nguy cơ chảy máu
| Chứ viết tắt | Đặc điểm lâm sàng | Điểm |
| H | Tăng HA | 1 |
| A | Bất thường chức năng gan và thận (1 điểm cho mỗi bệnh lý) | 1 hoặc 2 |
| S | Đột quỵ | 1 |
| B | Xuất huyết | 1 |
| L | INR bất thường | 1 |
| E | Cao tuổi (> 65 tuổi) | 1 |
| D | Sử dụng thuốc hoặc rượu (1 điểm cho mỗi loại) | 1 hoặc2 |
Chú thích: Tăng HA: HATT > 160mmHg. Bất thường chức năng thận: lọc thận mạn tính hoặc ghép thận hoặc creatinin huyết thanh ≥ 220 mcmol/L; Bất thường chức năng gan: bệnh gan mạn tính (xơ gan) hoặc thay đổi sinh hóa chứng tỏ có giảm chức năng gan đáng kể (bilirubin tăng trên 2 lần giới hạn bình thường trên, đi kèm aspartate aminotransferase/alanine aminotransferase/alkaline phosphatase tăng trên 3 lần giới hạn bình thường trên, .v.v.). Xuất huyết: gồm tiền sử xuất huyết và/hoặc nguy cơ xuất huyết có sẵn như: cơ địa xuất huyết, thiếu máu. Bất thường INR: INR tăng/không ổn định hoặc thời gian đạt ngưỡng thấp (60%). Sử dụng thuốc hoặc rượu: dùng đồng thời các thuốc như kháng ngưng tập tiểu cầu, kháng viêm non- steroid hoặc nghiện rượu.
- Khuyến cáo sử dụng thuốc chống đông trên bệnh nhân rung nhĩ không do van tim
- Sử dụng thuốc chống đông đường uống dự phòng huyết khối được khuyến cáo trên tất cả bệnh nhân rung nhĩ là nam giới có điểm CHA2DS2-VASc từ 2 trở lên.
- Sử dụng thuốc chống đông đường uống dự phòng huyết khối được khuyến cáo trên tất cả bệnh nhân rung nhĩ là nữ giới có điểm CHA2DS2-VASc từ 3 trở lên.
- Cân nhắc sử dụng thuốc chống đông đường uống ở các bệnh nhân rung nhĩ là nam giới có điểm CHA2DS2-VASc là 1, cần dựa trên từng cá thể và sự lựa chọn của bệnh nhân.
- Cân nhắc sử dụng thuốc chống đông đường uống ở các bệnh nhân rung nhĩ là nữ giới có điểm CHA2DS2-VASc là 2, cần dựa trên từng cá thể và sự lựa chọn của bệnh nhân.
- Sử dụng các thuốc kháng vitamin K (INR từ 2.0-3.0 hoặc cao hơn) để dự phòng đột quỵ ở các bệnh nhân rung nhĩ có sử dụng van tim nhân tạo hoặc có hẹp van hai lá mức trung bình và nặng.
- Khi lựa chọn sử dụng các thuốc chống đông đường uống, nên lựa chọn thuốc chống đông thế hệ mới thay vì thuốc kháng vitamin K nếu thích hợp.
- Khi bệnh nhân được sử dụng thuốc kháng vitamin K, khoảng đạt liều điều trị cần được giữ ở mức cao nhất có thể và cần được theo dõi chặt chẽ.
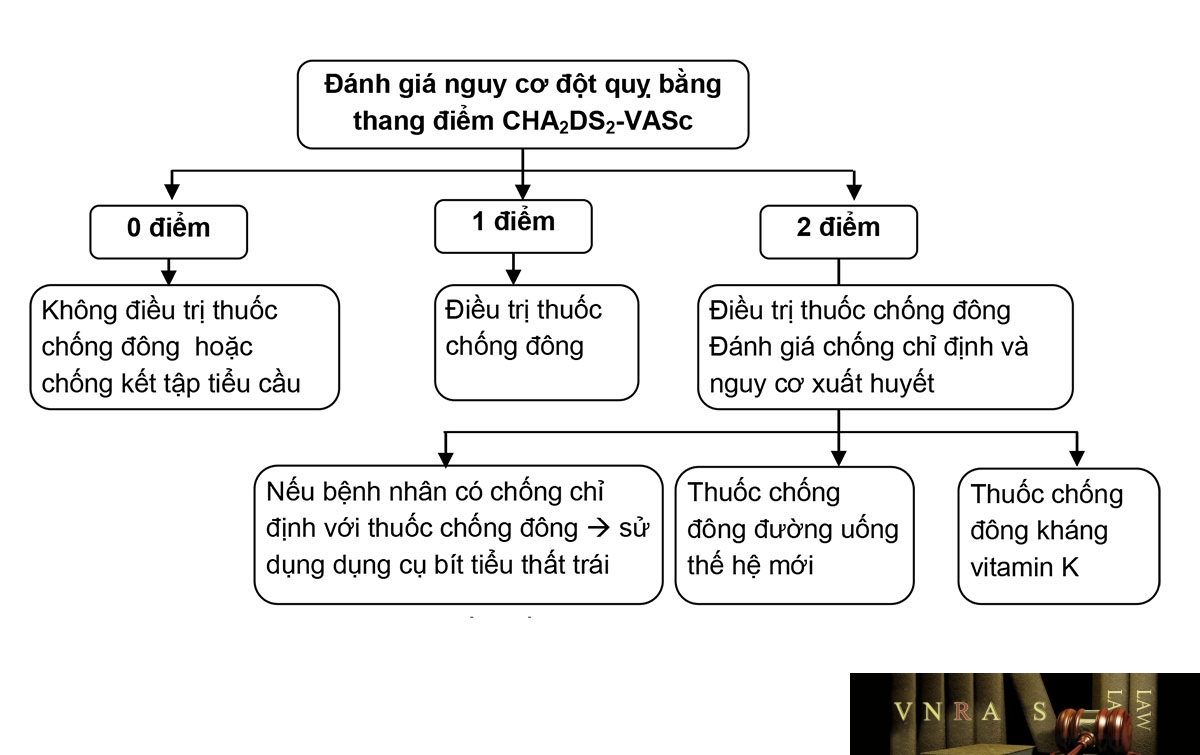
3.2. Hướng dẫn thực hành dược lâm sàng trên bệnh nhân rung nhĩ không do van tim
Trong nội dung này, các hoạt động thực hành dược lâm sàng được trình bày theo các bước của quy trình chăm sóc dược đầy đủ trên bệnh nhân. Tùy theo điều kiện của từng cơ sở y tế tại các tuyến khác nhau, có thể triển khai các hoạt động theo hướng dẫn chung được trình bày trong chương 1.
3.2.1. Khai thác thông tin về tiền sử bệnh và tiền sử thuốc
Bảng 3.21. Phiếu khai thác tiền sử bệnh và dùng thuốc
| THÔNG TIN BỆNH NHÂN
Họ tên:……………Năm sinh:……………… Giới tính: …………. Chẩn đoán: ……………………………………………………………………………………………… ĐÁNH GIÁ KẾT QUẢ PHỎNG VẤN Dược sĩ phỏng vấn: ……………………………………………………. Ngày phỏng vấn: ………………………………………………………………………………. |
|||
| TT | Nội dung câu hỏi | Thông tin từ bệnh nhân | Cần tư vấn lại |
| A. Hiểu biết của bệnh nhân về bệnh rung nhĩ |
|||
| 1 | Ông/bà bị rung nhĩ bao lâu rồi? Ông/bà được chẩn đoán rung nhĩ khi nào? | ||
| 2 | Trong gia đình ông/bà có ai khác bị rung nhĩ không? | ||
| 3 | Ông/bà biết những nguy cơ gì về sức khỏe liên quan đến rung nhĩ? | ||
| 4 | Ông/bà đã bao giờ có các dấu hiệu/ triệu chứng sau của rung nhĩ chưa?
– Đánh trống ngực – Khó thở – Chóng mặt – Đau ngực – Mệt mỏi – Yếu, không thể tập thể dục |
||
| B. Hiểu biết của bệnh nhân về thuốc điều trị rung nhĩ đang dùng | |||
| 5 | Ông/bà sử dụng những loại thuốc nào để điều trị rung nhĩ? Cách sử dụng thuốc như thế nào? | ||
| 6 | Sau khi chẩn đoán ông/bà bị rung nhĩ, bác sĩ có cho ông/bà sử dụng thuốc chống đông máu (chất làm loãng máu) không? | ||
| 7 | Nếu có, liều dùng hoặc lịch dùng thuốc chống đông máu của ông/bà như thế nào? | ||
| 8 | Ông/bà có thường hay quên uống thuốc chống đông máu, lý do quên là gì? | ||
| 9 | Ông/bà đã từng bị chảy máu hoặc bầm da bất thường mà nghi có liên quan đến thuốc chống đông máu không? | ||
| 10 | Thực phẩm chứa vitamin K có thể tương tác với thuốc chống đông máu Do đó, ông/bà có thể cho biết chế độ ăn uống của ông/bà thường gồm những loại thực phẩm nào? | ||
| 11 | Ông/bà có thường hay quên uống thuốc trị rung nhĩ? | ||
| 12 | Trước đây, ông/bà từng dùng những loại thuốc nào khác để điều trị rung nhĩ? | ||
| 13 | Ông/bà đã bao giờ tự ngưng bất kỳ loại thuốc điều trị rung nhĩ nào mà không báo với bác sĩ điều trị không? Nếu có, thì lý do là gì vậy? | ||
| 14 | Ông/bà sử dụng những loại thuốc không kê đơn (OTC, thuốc có thể tự mua ở ngoài nhà thuốc) hoặc thảo dược nào để điều trị rung nhĩ? | ||
| 15 | Bác sĩ có thông báo cho ông/bà biết những loại thuốc không kê đơn nào nên tránh dùng vì có thể làm bệnh rung nhĩ nặng hơn và hoặc gây ra nguy cơ đột quỵ? | ||
| C. Khả năng dự phòng của bệnh nhân trước các tình huống khẩn cấp liên quan đến bệnh rung nhĩ | |||
| 16 | Các dấu hiệu cảnh báo ông/bà bị đột quỵ và nhồi máu cơ tim là gì? Khi đó, ông/bà sẽ xử trí như thế nào? | ||
| 17 | Có bao giờ ông/bà bị ngã, cảm thấy chóng mặt, hoặc nhìn mờ, hoặc đánh trống ngực khi hoạt động hoặc khi nghỉ ngơi không? | ||
| 18 | Ông/bà đã bao giờ nhập viện vì rung nhĩ chưa? | ||
| 19 | (Nếu đang dùng thuốc chống đông máu) Ông/bà đã từng thấy nước tiểu của mình bị sẫm màu đỏ, phân đen đỏ, ho hoặc nôn ra máu hoặc các chất sẫm màu không? Đây là dấu hiệu cho thấy ông/bà bị chảy máu bên trong cơ thể và cần được thông báo ngay. | ||
3.2.2. Đánh giá lâm sàng và cận lâm sàng
Nội dung chi tiết tham khảo phần Nguyên tắc điều trị, một số điểm dược sĩ cần lưu ý:
- Bệnh cảnh rung nhĩ (phân loại, tần suất, tiền sử chuyển nhịp, mức độ nặng của triệu chứng lâm sàng); bệnh lý nền: giúp dược sĩ hiểu được chiến lược điều trị của bác sĩ (chuyển nhịp, duy trì nhịp xoang, kiểm soát tần số thất).
- Thời điểm khởi phát rung nhĩ: Phục vụ thẩm định y lệnh chỉ định thuốc chống đông quanh chuyển nhịp.
- Ý nghĩa một số đánh giá cận lâm sàng liên quan đến bệnh rung nhĩ: theo Phụ lục 3.1.
3.2.3. Đánh giá sử dụng thuốc
Một số vấn đề liên quan đến thuốc trong điều trị rung nhĩ không do van tim
Bảng 3.22. Một số vấn đề liên quan đến thuốc trong điều trị rung nhĩ không do van tim
| Vấn đề liên quan đến sử dụng thuốc | Ví dụ |
| Không tuân thủ | Kiểm soát triệu chứng rung nhĩ không tối ưu do quên dùng thuốc kiểm soát nhịp tim
Tự ý ngưng dùng thuốc chống đông máu do chi phí cao (đối với các chống đông thế hệ mới như dabigatran, rivaroxaban) |
| Thuốc không cần thiết | Sử dụng thuốc chống đông máu khi điểm CHA2DS2-VASc = 0 ở nam; 1 ở nữ. Các thuốc thường được chỉ định: aspirin, clopidogrel, thuốc kháng vitamin K, dabigatran, rivaroxaban
Sử dụng đồng thời aspirin + clopidogrel hoặc aspirin + thuốc chống đông kháng vitamin K hoặc thuốc chống đông kháng vitamin K + clopidogrel khi không có chỉ định phù hợp |
| Cần bổ sung thuốc | Không chỉ định thuốc chống đông máu khi điểm CHA2DS2– VASC ≥ 2 ở nam; ≥ 3 ở nữ |
| Thuốc không phù hợp | Chỉ định thuốc aspirin hoặc clopidogrel khi điểm CHA2DS2– VASC ≥ 2 ở nam; ≥ 3 ở nữ |
| Thuốc không hiệu quả | Sử dụng thực phẩm chức năng nguồn gốc thảo dược thay vì liệu pháp đã được các cơ quan quản lý, hội chuyên môn chấp thuận |
| Liều thấp | Chỉ số INR dưới ngưỡng mục tiêu (INR < 2) khi dùng warfarin/acenocoumarol
Sử dụng các thuốc chẹn beta chỉ ở mức liều khởi đầu khiến cho bệnh nhân còn dấu hiệu đánh trống ngực |
| Liều cao | Chỉ số INR trên ngưỡng mục tiêu (INR > 3) khi đang dùng warfarin/acenocoumarol
Sử dụng đồng thời warfarin/acenocoumarol với các thuốc ức chế enzym chuyển hóa ở gan (ví dụ amiodaron) làm tăng tác dụng của warfarin/acenocoumarol Nhịp tim quá thấp khi đang dùng thuốc chống loạn nhịp (ví dụ diltiazem) Sử dụng liều dabigatran 150 mg ở bệnh nhân > 80 tuổi, suy thận |
| Phản ứng có hại của thuốc | Chảy máu cam khi dùng warfarin/acenocoumarol
Đau đầu, táo bón khi dùng diltiazem Triệu chứng trào ngược dạ dày thực quản khi dùng dabigatran |
Một số thuốc có nguy cơ gây rung nhĩ
Bảng 3.23. Một số thuốc có nguy cơ gây rung nhĩ
| Mức độ chứng cứ | Thuốc có nguy cơ gây rung nhĩ |
| Cao | Adenosin: thời gian bán thải ngắn nên thường không có ý nghĩa lâm sàng, ngoại trừ trường hợp bệnh nhân có đường dẫn truyền phụ như mắc hội chứng Wolff-Parkinson-White
Dobutamin Aminophyllin/theophyllin |
| Trung bình | Milrinon Interleukin-2 Flecainid Propafenon Cisplatin Melphalan Amifostin |
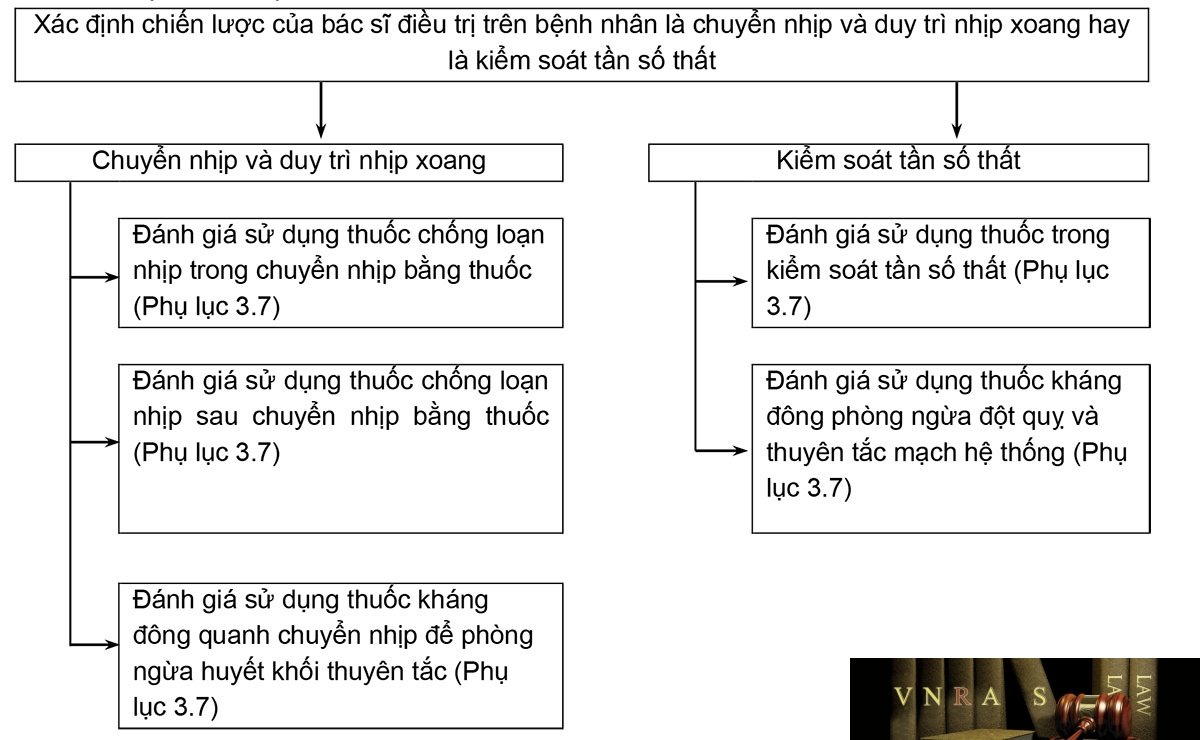
3.2.4. Lập kế hoạch điều trị
Bảng 3.24. Kế hoạch điều trị cho bệnh nhân rung nhĩ
| Hoạt động chính | Nội dung hoạt động | Hướng dẫn chi tiết | Kế hoạch chăm sóc của dược sĩ lâm sàng cho người bệnh | Thực hiện |
| 1. Xác định mục tiêu điều trị | Cải thiện triệu chứng | Kiểm soát tần số thất, nhịp xoang và giảm triệu chứng của bệnh nhân | – Tần số thất lúc nghỉ đạt mục tiêu: < 110 nhịp/phút hoặc < 80 lần/phút nếu bệnh nhân có triệu chứng và chức năng tâm thu thất trái giảm
– Chuyển nhịp và duy trì nhịp xoang: 60-100 lần/phút lúc nghỉ – Giảm các triệu chứng: đánh trống ngực; khó thở; chóng mặt; đau ngực; mệt mỏi; yếu, không thể tập thể dục |
□ |
| Dự phòng đột quỵ | Sử dụng thuốc chống đông dự phòng huyết khối | – Đánh giá nguy cơ đột quỵ của bệnh nhân thông qua thang điểm CHA2DS2-VASC
– Sử dụng thuốc chống đông trên bệnh nhân có nguy cơ cao – Cân nhắc sử dụng chống đông trên bệnh nhân có nguy cơ trung bình |
□ | |
| Giảm thời gian và số lần điều trị tại bệnh viện | Kiểm soát tốt các bệnh tim mạch mắc kèm (nếu có) và các yếu tố nguy cơ gây tái phát rung nhĩ | – Tăng huyết áp
– Phẫu thuật bệnh van tim hoặc bệnh tim bẩm sinh (khi có chỉ định) – Bệnh mạch vành – Suy tim – Cường giáp – Bệnh phổi tắc nghẽn mạn tính |
□ | |
| Xác định thuốc có nguy cơ gây rung nhĩ | Các thuốc có nguy cơ gây rung nhĩ (bảng
3.23) |
□ | ||
| 2. Lập kế hoạch điều trị | Lựa chọn thuốc điều trị | Kiểm soát tần số thất | – Thuốc chẹn beta, digoxin, diltiazem và verapamil được khuyến cáo để kiểm soát tần số thất ở bệnh nhân rung nhĩ có LVEF ≥ 40 % .
– Thuốc chẹn beta và/hoặc digoxin được khuyến cáo để kiểm soát tần số thất ở bệnh nhân rung nhĩ có LVEF < 40 % . – Cân nhắc phối hợp thuốc nếu điều trị một thuốc không đạt nhịp tim mục tiêu. |
□ |
| Duy trì nhịp xoang | – Điều trị yếu tố có thể gây khởi phát rung nhĩ hoặc điều trị nguyên nhân có thể đảo ngược.
– Lựa chọn thuốc tùy thuộc vào bệnh mắc kèm của bệnh nhân. – Các thuốc được khuyến cáo sử dụng ở bệnh nhân rung nhĩ để duy trì nhịp xoang bao gồm: amiodaron, dofetilide, dronedaron, flecanid, propafenon và sotalol |
□ | ||
|
|
Dự phòng huyết khối | – Đánh giá nguy cơ đột quỵ thông qua thang điểm CHA2DS2-VASc
– Sử dụng thuốc chống đông đường uống dự phòng huyết khối được khuyến cáo trên tất cả bệnh nhân nam giới có điểm CHA2DS2-VASc từ 2 trở lên hoặc bệnh nhân nữ giới có điểm CHA2DS2-VASc từ 3 trở lên. – Cân nhắc sử dụng thuốc chống đông đường uống ở các bệnh nhân nam giới có điểm CHA2DS2-VASc là 1 hoặc bệnh nhân nữ giới có điểm CHA2DS2-VASc là 2. Việc lựa chọn thuốc dựa trên từng cá thể và sự lựa chọn của bệnh nhân. – Sử dụng các thuốc kháng vitamin K (INR từ 2.0-3.0 hoặc cao hơn) để dự phòng đột quỵ ở các bệnh nhân rung nhĩ có sử dụng van tim nhân tạo hoặc có hẹp van hai lá mức độ trung bình đến nặng. – Nên lựa chọn thuốc chống đông thế hệ mới thay vì thuốc kháng vitamin K nếu thích hợp. – Khi bệnh nhân được sử dụng thuốc kháng vitamin K, khoảng đạt liều điều trị cần được giữ ở mức cao nhất có thể và cần được theo dõi chặt chẽ. |
□ | |
| Chống chỉ định và thận trọng | Phụ lục 3.2 | □ | ||
| Liều dùng | Phụ lục 3.3 | □ | ||
| Tác dụng không mong muốn | Phụ lục 3.4 | □ | ||
| Tương tác thuốc | Phụ lục 3.5 | □ | ||
| 3. Tư vấn và giáo dục bệnh nhân | Cách sử dụng thuốc | Nhãn của bao bì thuốc xuất viện cần ghi chú tối thiểu các thông tin sau:
– Tên thuốc – Liều dùng – Thời điểm dùng thuốc: đặc biệt lưu ý thuốc kháng đông kháng vitamin K cần dùng trước ăn 3 phút hoặc sau ăn giờ Đối với bệnh nhân được chỉ định thuốc kháng đông kháng vitamin K, cần tư vấn và phát “Phiếu thông tin dành cho bệnh nhân sử dụng thuốc kháng đông kháng vitamin K” (Phụ lục 3.9) |
□ | |
| ADR thường gặp | Thông tin một số phản ứng bất lợi của thuốc mà bệnh nhân có thể nhận biết được và hướng dẫn cách xử lý (tham khảo Phụ lục 3.4) | □ | ||
| Tuân thủ dùng thuốc | Các nội dung cần tư vấn trực tiếp cho bệnh nhân để tăng tính tuân thủ sử dụng thuốc:
– Lý do dùng thuốc: sử dụng ngôn ngữ dễ hiểu (ví dụ: diltiazem dùng để kiểm soát nhịp tim; dabigatran dùng để ngăn ngừa đột quỵ, …) – Dặn dò bệnh nhân ghi lại các thời điểm quên uống thuốc (nếu xảy ra) |
□ | ||
| Chế độ sinh hoạt
|
Hút thuốc lá | Hút thuốc lá:
– Khuyến khích bỏ hút thuốc vì hút thuốc lá và tiếp xúc với khói thuốc lá có thể làm tăng nguy cơ đột quỵ. – Một số biện pháp để cai thuốc lá : tư vấn, các sản phẩm thay thế nicotin hoặc thuốc kê đơn |
□ | |
| Chế độ ăn | – Hạn chế đồ uống có cồn do làm tăng nguy cơ đột quỵ: Nam ≤ 2 đơn vị/ngày; nữ ≤ 1 đơn vị ngày ( đơn vị tương đương mL cồn nguyên chất – 1 ly rượu vang, % lon bia, 1 cốc rượu mạnh).
– Lượng natri ≤ 2,4 g ngày; tối ưu < 1,5g muối/ngày – Không khuyến cáo bổ sung vitamin hàng ngày. – Chế độ ăn nhiều trái cây, rau quả và các sản phẩm ít chất béo. |
□ | ||
| Luyện tập thể dục | Luyện tập thể dục:
– Tập thể dục đều đặn, ít nhất 30 phút/ngày. – Vật lý trị liệu nếu có khuyết tật do biến chứng của đột quỵ |
□ | ||
| 4. Theo dõi, đánh giá điều trị | Đáp ứng điều trị | – Cải thiện triệu chứng lâm sàng
– Nguy cơ đột quỵ, nguy cơ xuất huyết để điều chỉnh chế độ dùng thuốc chống đông – Dấu hiệu, nguy cơ rối loạn nhịp tim – Sự tiến triển rung nhĩ tạm thời thành rung nhĩ vĩnh viễn – Điện tâm đồ 12 chuyển đạo |
□ | |
| Độc tính của thuốc | – Thuốc chống loạn nhịp: theo dõi độc tính sau 2-4 tuần khởi trị hoặc tăng liều thuốc (điện tâm đồ nên được theo dõi để phát hiện tình trạng kéo dài khoảng QT) Đặc biệt, độc tính của thuốc amiodaron cần được theo dõi chặt chẽ
– Thuốc kháng đông: theo dõi tác dụng phụ chảy máu ở mỗi đợt tái khám. + Warfarin/acenocoumarol: Nên theo dõi INR mỗi 1-2 tuần cho đến khi INR ổn định trong khoảng mục tiêu (INR mục tiêu 2-3). Thời gian theo dõi có thể nới rộng ở những bệnh nhân được kiểm soát tốt (tối thiểu mỗi tháng). + Dabigatran/rivaroxaban: nên kiểm tra chức năng thận và công thức máu ít nhất 2 lần/năm hoặc khi có thay đổi lâm sàng. |
□ | ||
TÀI LIỆU THAM KHẢO
Tiếng Việt
- Đỗ Quang Huân, Hồ Huỳnh Quang Trí (2018), Phác đồ điều trị Viện Tim, NXB Y học, Hà Nội.
- Phạm Hữu Văn, “Tóm tắt điều chỉnh rung nhĩ của ESC 2016 được phát triển với sự hợp tác của hội ngoại khoa tim & lồng ngực châu Âu”, http://timmachhoc.vn/huan- luyen-nang-cao-va-chuyen-sau/1353-tom-tat-dieu-chinh-rung-nhi-cua-esc-2016- duoc-phat-trien-voi-su-hop-tac-cua-hoi-ngoai-khoa-tim-long-nguc-chau-au-p4.html, truy cập ngày 20/12/2018.
Tiếng Anh
- January C. T. et al. (2014), “2014 AHA/ACC/HRS Guideline for the Management of Patients With Atrial Fibrillation: Executive Summary A Report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines and the Heart Rhythm Society“, Journal of the American College of Cardiology, 64 (21), pp. 2246-2280.
- Shawn D. Anderson, Kristyn M. Pardo (2018). Chapter 14: Atrial Fibrillation MTM Data Set. In: Medication Therapy Management: A Comprehensive Approach, 2e. Mc Graw Hill.
4. HƯỚNG DẪN THỰC HÀNH DƯỢC LÂM SÀNG TRONG ĐIỀU TRỊ BỆNH MẠCH VÀNH MẠN
4.1. Đại cương về bệnh mạch vành mạn
4.1.1. Chẩn đoán
Định nghĩa
Bệnh mạch vành mạn thường gặp nhất do mảng xơ vữa gây tắc nghẽn hoặc hẹp dần một hay nhiều động mạch vành thượng tâm mạc. Tuy nhiên, những yếu tố khác như: rối loạn chức năng nội mạc, bệnh vi tuần hoàn hay co thắt mạch máu vẫn có thể hiện diện đơn thuần hay phối hợp với xơ vữa động mạch vành và có thể là nguyên nhân chính gây ra thiếu máu cơ tim cục bộ ở một số bệnh nhân.
Về mặt thuật ngữ: suy mạch vành (về mặt chức năng), thiểu năng vành, bệnh động mạch vành (hình thái, giải phẫu), đau thắt ngực (triệu chứng lâm sàng), bệnh tim thiếu máu cục bộ (hệ quả) là những thuật ngữ dùng để chỉ một nhóm các thể lâm sàng gây ra do nhiều nguyên nhân khác nhau nhưng cùng có chung một cơ chế sinh lý bệnh là sự mất cân bằng cung cầu oxy cho cơ tim. Nhu cầu oxy cơ tim phụ thuộc vào nhịp tim, sức co cơ tim, tiền tải, hậu tải trong khi đó cung cấp oxy cho cơ tim phụ thuộc vào lưu lượng tưới máu cơ tim.
Phân loại
Đối với bệnh mạch vành mạn, các thể lâm sàng bao gồm:
- Cơn đau thắt ngực im lặng
- Cơn đau thắt ngực gắng sức hay kinh điển
- Biến thể của cơn đau thắt ngực hay cơn đau thắt ngực Prinzmetal
- Hội chứng tương tự cơn đau thắt ngực
- Hội chứng-X
- Cơn đau thắt ngực khi nằm
- Cơn đau thắt ngực về đêm
Chẩn đoán
a) Dấu hiệu gợi ý chẩn đoán đau thắt ngực ổn định
- Bệnh nhân đau ngực sau xương ức. Khởi phát khi gắng sức hoặc stress và giảm khi nghỉ ngơi hoặc khi dùng nitrat.
- Tình trạng cơn đau ổn định, đã có trước không tăng về tần số, thời gian và mức độ nặng của cơn đau.
b) Đánh giá tiền sử và khám lâm sàng
Đánh giá tính chất, mức độ của cơn đau ngực
- Vị trí cơn đau.
- Thời gian đau.
- Các yếu tố khởi phát cơn.
Đánh giá nguy cơ bệnh mạch vành:
- Hút thuốc lá; rối loạn lipid máu; ĐTĐ; hội chứng chuyển hóa; ít hoạt động thể lực và tiền sử gia đình mắc bệnh tim mạch sớm.
- Tiền sử bệnh mạch máu não hoặc bệnh mạch máu ngoại biên.
Phân loại lâm sàng đau ngực:
- Đau ngực điển hình có đủ ba đặc điểm: đau ngực sau xương ức; đau khi gắng sức hoặc stress và giảm khi nghỉ ngơi hoặc dùng nitrat.
- Đau ngực không điển hình chỉ có hai đặc điểm trên.
- Đau ngực không do tim: chỉ có một hoặc không có những đặc điểm trên.
Phân độ đau ngực theo Hội Tim mạch Canada (CCS):
- Độ I: những hoạt động thể lực bình thường không gây ĐTN
- Độ II: hạn chế nhẹ hoạt động thể lực bình thường. ĐTN xuất hiện khi leo cao >
- tầng gác thông thường bằng cầu thang hoặc đi bộ dài hơn 2 dãy nhà.
- Độ III: hạn chế đáng kể hoạt động thể lực thông thường. ĐTN khi đi bộ dài từ 1-
- dãy nhà hoặc leo cao 1 tầng gác.
- Độ IV: các hoạt động thể lực bình thường đều gây ĐTN. ĐTN khi làm việc nhẹ, khi gắng sức nhẹ.
c) Chẩn đoán cơn ĐTN không ổn định
- Cơn đau ngực xảy ra lúc nghỉ và thường kéo dài trên 20 phút
- Cơn ĐTN mới xảy ra dưới hai tháng, nhưng làm giới hạn hoạt động thể lực
- Cơn ĐTN ổn định trước đó nặng thêm về cường độ (giảm ngưỡng gây đau, tăng độ nặng cơn đau, kéo dài hơn và tần suất tăng hơn).
- Cơn ĐTN tái phát trong vòng 4 – 6 tuần sau nhồi máu cơ tim cấp
4.1.2 Điều trị
Mục tiêu điều trị
- Giảm ĐTN và dự phòng biến cố tim mạch.
- Cải thiện khả năng gắng sức cho người bệnh.
Biện pháp dùng thuốc
Tối ưu hóa điều trị với ít nhất một thuốc giảm ĐTN, giảm thiếu máu cơ tim và thuốc dự phòng biến cố tim mạch.
a) Điều trị giảm thiếu máu cục bộ và giảm ĐTN
- Thuốc nitrat tác dụng ngắn được khuyến cáo để cắt cơn ĐTN
- Thuốc CB và CKCa là các thuốc được lựa chọn ưu tiên để kiểm soát tần số tim và triệu chứng.
- Đối với lựa chọn thay thế, có thể thêm thuốc nitrat tác dụng kéo dài, ivabradin, nicorandil hoặc ranolazin dựa trên tần số tim, HA và dung nạp của bệnh nhân.
- Thuốc trimetazidin có thể được coi là lựa chọn thay thế
- Trong một số trường hợp, cân nhắc lựa chọn thay thế thay vì lựa chọn ưu tiên dựa trên bệnh mắc kèm và dung nạp của bệnh nhân.
- Thuốc CB nên dùng cho bệnh nhân có vùng thiếu máu cục bộ > 10% mặc dù không có triệu chứng.
- Ở bệnh nhân đau ngực do co thắt mạch, nên cân nhắc sử dụng thuốc CKCa và nitrat. Tránh sử dụng thuốc CB.
b) Dự phòng biến cố tim mạch
- Khuyến cáo sử dụng aspirin liều thấp ở tất cả bệnh nhân có BMV ổn định.
- Nếu bệnh nhân không dung nạp aspirin, clopidogrel là thuốc thay thế.
- Statin được khuyến cáo ở tất cả bệnh nhân có BMV ổn định.
- Khuyến cáo sử dụng thuốc ƯMCM, hoặc CTTA nếu bệnh nhân có bệnh mắc kèm như suy tim, THA, ĐTĐ.
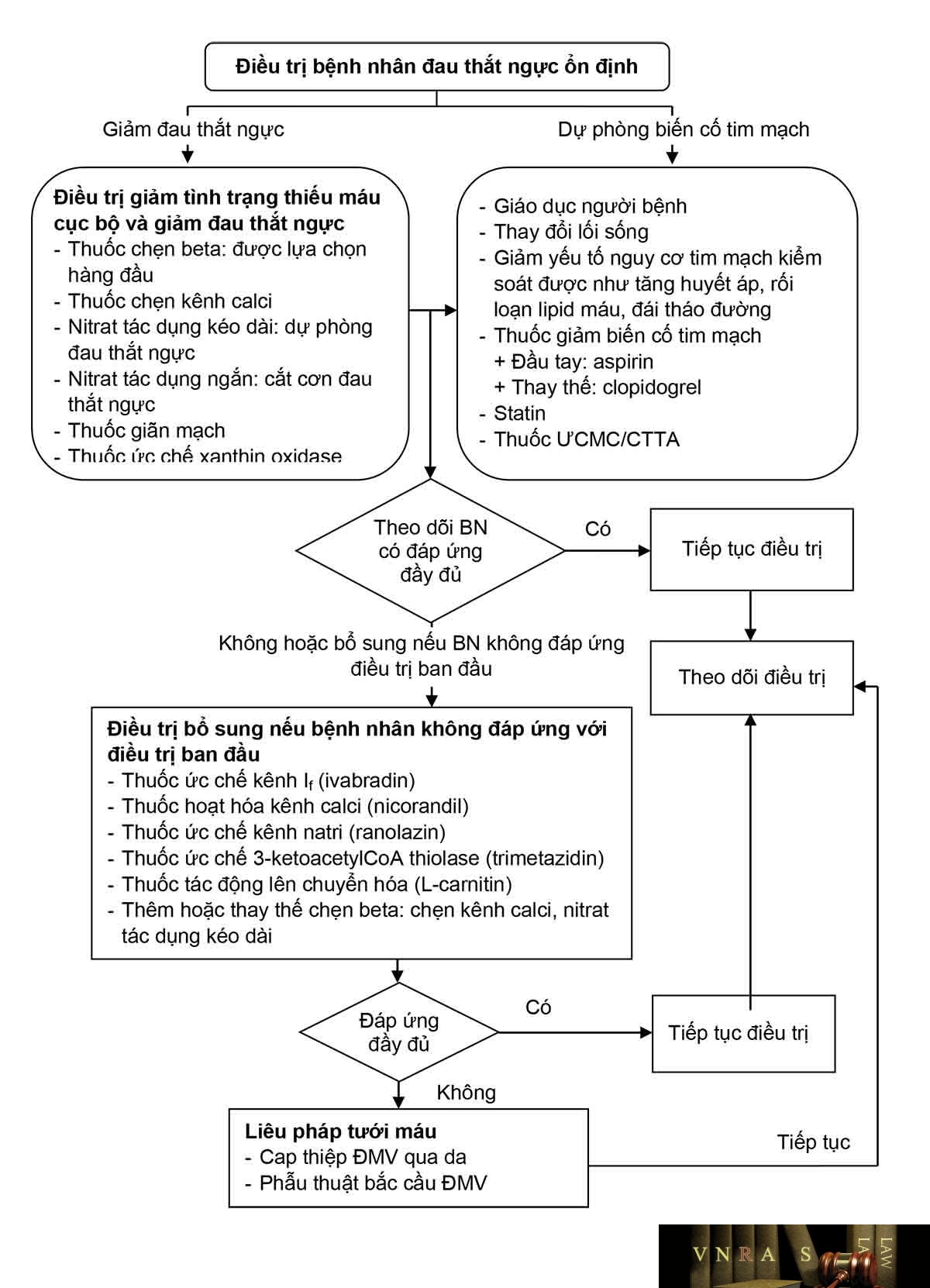
Hướng dẫn thực hành dược lâm sàng trên bệnh nhân bệnh động mạch vành mạn
Trong nội dung này, các hoạt động thực hành dược lâm sàng được trình bày theo các bước của quy trình chăm sóc dược đầy đủ trên bệnh nhân. Tùy theo điều kiện của từng cơ sở y tế tại các tuyến khác nhau, có thể triển khai các hoạt động theo hướng dẫn chung được trình bày trong chương 1.
Khai thác thông tin về tiền sử bệnh và tiền sử thuốc
Bảng 3.25. Phiếu khai thác tiền sử bệnh và dùng thuốc bệnh mạch vành mạn
| THÔNG TIN BỆNH NHÂN
Họ tên:……………Năm sinh:……………… Giới tính: …………. Chẩn đoán: ……………………………………………………………………………………………… ĐÁNH GIÁ KẾT QUẢ PHỎNG VẤN Dược sĩ phỏng vấn: ……………………………………………………. Ngày phỏng vấn: ………………………………………………………………………………. |
|||
| TT | Nội dung câu hỏi | Thông tin từ bệnh nhân | Cần tư vấn lại |
| A. Câu hỏi đánh giá kiểm soát đau ngực |
|||
| 1 | – Mô tả cơn đau ngực của ông/bà: vị trí, thời gian cơn đau kéo dài
– Khi nào ông/bà cảm thấy đau ngực? – Khi nào ông/bà cảm thấy đỡ đau? – Khi nào ông/bà cảm thấy đau nhiều hơn? |
||
| B. Câu hỏi đánh giá tuân thủ dùng thuốc? | |||
| 2 | – Ông/bà đang dùng thuốc gì để điều trị và dự phòng đau ngực? Ông/bà dùng những thuốc đó như thế nào?
– Ông/bà có dùng thêm những thuốc không kê đơn nào khác? – Trong vòng 2 tuần trở lại đây, có bao nhiêu lần ông/bà quên dùng thuốc? – Ông/bà đã từng ngừng thuốc mà không thông báo với bác sĩ bao giờ chưa? Nếu có vì lý do gì? |
||
| 3 | Nếu người bệnh có dùng nitroglycerin:
– Ông/bà dùng nitroglycerin như thế nào? Ông/bà đã dùng thuốc này được bao lâu? – Nếu ông/bà có dùng nitroglycerin dạng xịt thì bao lâu ông/bà thay lọ thuốc? |
||
| C. Câu hỏi đánh giá nguy cơ bệnh | |||
| 4 |
Bác sĩ có ý kiến gì về cân nặng của ông/bà không?
|
||
| D. Câu hỏi về xử trí trong trường hợp khẩn cấp | |||
| 5 | – Dấu hiệu của đột quỵ và nhồi máu cơ tim là gì? Ông/bà sẽ xử trí như thế nào nếu cơn đau ngực xảy ra?
– Ông/bà sẽ làm gì nếu dùng nitroglycerin và không hết đau? |
||
4.2.2. Đánh giá lâm sàng và cận lâm sàng
Tham khảo Phụ lục 3.1
4.2.3. Đánh giá sử dụng thuốc
Một số vấn đề liên quan đến thuốc trong điều trị BMV mạn
Bảng 3.26. Một số vấn đề thường gặp ở bệnh nhân BMV mạn
| Vấn đề liên quan đến sử dụng thuốc | Ví dụ |
| Không tuân thủ | Kiểm soát không tốt do quên liều thuốc, không tuân thủ các thuốc dự phòng như: aspirin, các thuốc statin |
| Thuốc không cần thiết | Trùng lặp thuốc: dùng 2 thuốc chẹn beta hoặc kết hợp ƯCMC và cttA |
| Cần bổ sung thuốc | Bệnh nhân không được dùng aspirin dự phòng |
| Thuốc không hiệu quả | Isosorbid mononitrat dùng 2 lần/ngày không có thời gian không sử dụng nitrat |
| Liều thấp | Chưa tối ưu liều thuốc CKCa nhóm non-dihydropyridin dẫn đến nhịp tim cao |
| Liều cao | Bệnh nhân có triệu chứng hạ HA do sử dụng liều cao Bệnh nhân đau đầu do tăng liều nitrat tác dụng kéo dài |
| Phản ứng có hại của thuốc | Đau cơ khi sử dụng statin
Phù ngoại vi khi dùng thuốc CKCa nhóm dihydropyridin |
Một số thuốc gây thiếu máu cơ tim
Bảng 3.27. Các thuốc gây thiếu máu cơ tim
| Thuốc | Cơ chế | ||
| Ngưng thuốc đột ngột | Tăng nhu cầu oxy | Giảm cung cấp oxy | |
| Adenosin, dipyridamol, regadenoson | Giảm máu trực tiếp đến mạch vành (coronary steal) | ||
| Amphetamin/methamphetamin | Tăng HA, tim đập nhanh | Co thắt mạch máu | |
| CB | √ | ||
| CKCa | Nhịp tim nhanh phản xạ | ||
| Đồng vận alpha ở trung ương | √ | ||
| Cocain | Kết tập tiểu cầu, co thắt mạch máu | ||
| Dobutamin | Tim đập nhanh | ||
| Alkaloid cựa lõa mạch | Hạ HA | Co thắt mạch máu | |
| Hydralazin | Tim đập nhanh phản xạ | ||
| Đồng vận beta | Tim đập nhanh | ||
| Milrinon | Tim đập nhanh | ||
| Nifedipin (giải phóng nhanh) | Hạ HA cấp | ||
| Các chất ức chế P2Y12 | √ | ||
| Phenylephrin | Tăng HA | Co thắt mạch máu | |
| Các chất ức chế PDE-5 + nitrat | Hạ HA cấp | ||
| Các chất ức chế PDE-5 + riociguat | Hạ HA cấp | ||
4.2.4. Lập kế hoạch điều trị
Bảng 3.28. Kế hoạch điều trị cho bệnh nhân BMV
| Hoạt động chính |
Nội dung hoạt động |
Hướng dẫn chi tiết |
Kế hoạch chăm sóc của dược sĩ lâm sàng cho người bệnh |
Thực hiện |
| 1. Xác định mục tiêu điều trị |
Giảm đau thắt ngực và dự phòng biến cố tim mạch Cải thiện khả năng gắng sức cho người bệnh |
| ||
Kiểm soát các nguy cơ đi kèm |
Tăng huyết áp | Tham khảo phần 3.1 Tăng huyết áp | | |
| Đái tháo đường | Tham khảo chương 2- Đái tháo đường | | ||
| Lipid máu | LDL-C < 70 mg/dL (1,8 mmol/L) hay giảm LDL-C trên 50% |
| ||
| 2. Lập kế hoạch điều trị
|
Chiến lược điều trị | Giảm đau thắt ngực | – Thuốc CB được lựa chọn hàng đầu
– Thuốc CKCa là lựa chọn thay thế – Ivabradin – Nitrat tác dụng kéo dài: dự phòng cơn đau thắt ngực – Nitrat tác dụng ngắn: cắt cơn đau thắt ngực |
□ |
| Dự phòng biến cố tim mạch | – Thuốc chống kết tập tiểu cầu: lựa chọn đầu tay là aspirin, có thể thay thế bằng clopidogrel. Chống kết tập tiểu cầu kép có thể dùng ở bệnh nhân có nguy cơ cao hoặc sau khi đặt stent
– Thuốc statin – Thuốc ƯCMC hoặc CTTA |
□ | ||
| Lựa chọn thuốc trong các tình huống lâm sàng
|
Tăng huyết áp | Tất cả các thuốc hạ áp, trừ ranolazin
Nên tối ưu bằng các thuốc hạ áp trước khi bổ sung ranolazin |
□ | |
| Huyết áp thấp hoặc hạ huyết áp | Bệnh nhân có thể dùng các thuốc chống đau thắt ngực liều thấp. Tuy nhiên, nếu bệnh nhân có triệu chứng hạ huyết áp nhiều nên đổi sang ranolazin | □ | ||
| Suy tim phân suất tống máu giảm (EF ≤ 40%) | Thuốc CB (bisoprolol, carvedilol, metoprolol succinat) với liều thấp và tăng liều từ từ đến khi dung nạp thuốc
Thận trọng: ranolazin có thể gây tác dụng inotrope (-) |
□ | ||
| Sau nhồi máu cơ tim | Lựa chọn thuốc CB không có hoạt tính cường giao cảm nội tại
Tránh dùng: thuốc CKCa nhóm dihydropyridin, CB có hoạt tính cường giao cảm nội tại (acebutolol, penbutol, pindolol) |
□ | ||
| Bệnh mạch máu co thắt hoặc đau ngực
Prinzmetal |
Thuốc CKCa là thuốc đơn trị được khuyến cáo Có thể kết hợp thuốc CKCa nhóm non- dihydropyridin và thuốc CKCa nhóm dihydropyridin nếu còn tiếp tục đau ngực khi đã tối ưu hóa liều đơn trị và kết hợp với nitrat Tránh dùng thuốc CB vì có thể làm nặng thêm tình trạng đau ngực do co thắt mạch máu
Có thể dùng thuốc CB có tác dụng chẹn alpha (carvedilol) nhưng là lựa chọn sau cùng |
□ | ||
| Loạn nhịp nhĩ | Thuốc CB không có hoạt tính cường giao cảm nội tại hoặc thuốc CKCa nhóm non- dihydropyridin
Tránh thuốc CKCa nhóm dihydropyridin (làm tim đập nhanh do phản xạ |
□ | ||
| Nhịp tim chậm | Dùng thuốc CKCa nhóm dihydropyridin, nitrat, ranolazin | □ | ||
| Loạn nhịp thất | Thuốc CB không có hoạt tính cường giao cảm nội tại
Verapamil là lựa chọn đầu tay cho nhịp nhanh thất nguyên phát |
□ | ||
| Hẹp động mạch chủ nặng | Tránh sử dụng thuốc CKCa ở bệnh nhân hẹp động mạch chủ nặng
Có thể cân nhắc dùng thuốc CB không có tác dụng trên thụ thể alpha, nitrat, và/hoặc ranolazin |
□ | ||
| Rối loạn cương dương | Chống chỉ định phối hợp nitrat với chất ức chế phosphodiesterase – 5 (sildenafil, tadalafil, vardenafil)
Nếu dùng nitrat, bệnh nhân cần ngưng sildenafil 24 giờ, tadalafil 48 giờ trước khi dùng nitrat Có thể dùng thuốc CB, CKCa, ranolazin |
□ | ||
| Chống chỉ định | Tham khảo phụ lục 3.2 | □ | ||
| Liều dùng | Tham khảo phụ lục 3.3 | □ | ||
| Tác dụng không mong muốn | Tham khảo phụ lục 3.4 | □ | ||
| Tương tác thuốc | Tham khảo phụ lục 3.5 | □ | ||
| Giáo dục tư vấn cho người bệnh |
Thay đổi lối sống |
Hút thuốc | Cai thuốc lá | □ |
| Kiểm soát cân nặng | BMI cần đạt: < 23 kg/m2.
Vòng eo: nam < 90 cm; nữ < 80 cm |
□ | ||
| Chế độ ăn | Hàng ngày ăn nhiều rau, củ, trái cây, ít chất béo, thay chất béo bão hòa bằng chất béo không bảo hòa; tăng ăn cá có dầu
Lượng muối ăn vào: hạn chế 5 – 6 g/ngày Đồ uống có cồn: nam < 20 – 30 g/ngày; nữ < 10 – 20 g/ngày |
□ | ||
| Tiêm phòng | Tiêm phòng vaccin phòng cúm hàng năm | □ | ||
| 4. Theo dõi, đánh giá điều trị | Theo dõi hiệu quả điều trị
|
Theo dõi triệu chứng cơn đau ngực trước và sau khi bắt đầu điều trị:
Đánh giá 2-4 tuần sau điều trị hoặc thay đổi điều trị: đánh giá tần suất và mức độ nặng của cơn đau ngực Theo dõi mỗi 6-12 tháng ở bệnh nhân ổn định Bệnh nhân có triệu chứng nặng, nhiều bệnh đi kèm, tiền sử không tuân thủ điều trị, gặp tác dụng phụ của thuốc cần được theo dõi thường xuyên hơn Theo dõi biến chứng suy tim nếu có Theo dõi huyết áp để đánh giá dung nạp thuốc Theo dõi tần số tim ở nhứng bệnh nhân có dùng thuốc tác động làm giảm tần số tim (thuốc CB, verapamil, diltiazem) và thuốc làm tăng nhịp tim phản xạ (nitrat, thuốc CKCa nhóm dihydropyridin) |
□ | |
| Theo dõi tác dụng không mong muốn, độc tính
|
Theo dõi tác dụng phụ của thuốc sau 2-4 tuần khởi trị hoặc tăng liều thuốc
Theo dõi tác dụng phụ mỗi 6-12 tháng ở bệnh nhân ổn định Theo dõi chức năng thận và kali máu với bệnh nhân dùng thuốc ƯCMC, thuốc CTTA định kỳ như trên, đặc biệt ở bệnh nhân suy thận hoặc đái tháo đường Do ranolazin có thể gây kéo dài khoảng QT, cần theo dõi điện tâm đồ, nồng độ kali, magie trong máu trước khi điều trị và trong vòng 6 tháng sau khi bắt đầu điều trị hoặc tăng liều. Nên làm lại các xét nghiệm trên nếu có tương tác với các thuốc dùng kèm |
□ | ||
TÀI LIỆU THAM KHẢO
Tiếng Việt
- Bộ Y tế (2016), Quy trình chuyên môn chẩn đoán và điều trị bệnh mạch vành mạn (Ban hành kèm theo quyết định 4068/QĐ-BYT của Bộ trưởng Bộ Y tế).
Tiếng Anh
- Shawn D. Anderson, Kristyn M. Pardo (2018). Chapter 18: Chronic Stable Angina MTM Data Set. In: Medication Therapy Management: A Comprehensive Approach, 2e. Mc Graw Hill;
- Bernard J. Gersh, Lionel H. Opie (2013). Which Therapy for Which condition? In: Drug for the heart. Eighth edition. Elsevier.
- Kelly C. Rogers (2018). Stable Atherosclerotic Disease. In: ACCP Update in Therapeutics 2018: Cardiology Pharmacy Prepatory Review course. American College of Clinical Pharmacy.
- Paul P. Dobesh (2017). Chapter 16: Stable Ischemic Heart Disease. In: Pharmacotherapy: A Pathophysiologic Approach, 10e. Mc Graw Hill.
- Gilles Montalescot, Udo Sechtem (2013). 2013 ESC guidelines on the management of stable coronary artery disease. Eur Heart J.
- Fihn SD, Blankenship JC, Alexander KP, Bittl JA, Byrne JG, Fletcher BJ, et al (2014). 2014 ACC/AHA/AATS/PCNA/SCAI/STS Focused Update of the Guideline for the Diagnosis and Management of Patients With Stable Ischemic Heart Disease. J Am Coll Cardiol.;64(18):1929.
- Carie S.Oliphant (2018). Drug-induced cardiovascular disease and drugs to avoid in CV disease. In: ACCP Update in Therapeutics 2018: Cardiology Pharmacy Prepatory Review course. American College of Clinical Pharmacy.
PHỤ LỤC CHƯƠNG 3. HƯỚNG DẪN THỰC HÀNH DƯỢC LÂM SÀNG TRONG MỘT SỐ BỆNH TIM MẠCH
Phụ lục 3.1. Đánh giá cận lâm sàng bệnh nhân tim mạch
| Cận lâm sàng | Ý nghĩa của việc đánh giá các thông số |
| Công thức máu
RBC,Hb, Hct, WBC, Neu, CRP, Pro- calcitonin Tổng phân tích nước tiểu (NIT, bạch cầu, vi khuẩn,…) |
Theo dõi điều trị các bệnh mắc kèm, nếu có
Theo dõi điều trị nhiễm trùng (nếu có) Theo dõi chảy máu (Hb/ Hct), trong trường hợp dùng aspirin, clopidogrel, thuốc chống đông đường uống |
| Chức năng thận | Theo dõi để hiệu chỉnh liều thuốc theo chức năng thận
Theo dõi chức năng thận khi điều trị với ƯCMC/CTTA, statin, diltiazem, verapamil Suy tim: Suy tim nặng hơn có thể dẫn đến tổn thương thận, tổn thương gan cấp (BS đánh giá) Rung nhĩ: Tìm nguyên nhân gây ra và làm nặng thêm rối loạn nhịp Chỉnh liều thuốc chống đông (dabigatran rivaroxaban) |
| Chức năng gan (ASAT, ALAT, bilirubin) | Theo dõi và hiệu chỉnh liều thuốc theo chức năng gan
Rung nhĩ: Theo dõi độc tính amiodaron, tác dụng phụ diltiazem, verapamil, statin |
| Điện giải đồ | Theo dõi rối loạn điện giải do bệnh mắc kèm
Tìm nguyên nhân gây ra và làm nặng thêm rối loạn nhịp Theo dõi kali máu khi điều trị với ƯCMC/CTTA Theo dõi kali, magie, canxi khi dùng digoxin |
| Đường huyết lúc đói, HbA1C | Tối ưu hoá điều trị ĐTĐ để phòng ngừa biến cố tim mạch ở bệnh nhân có BMV
Lưu ý thuốc CB có thể che dấu các dấu hiệu hạ đường huyết Lưu ý các tương tác thuốc có thể gây rối loạn đường huyết |
| Lipid máu (cholesterol toàn phần, triglycerid, HDL -C, LDL -C) | Rối loạn lipid máu:
Ghi nhận các chỉ số lipid máu để đánh giá đáp ứng điều trị với statin Bệnh nhân có BMV mạn: Xác định mục tiêu điều trị LDL-C |
| PT (Prothrombin time)
INR (International Normalized Ratio) |
Đánh giá việc sử dụng thuốc chống đông kháng vitamin K |
| BNP hay NT-proBNP | Suy tim:
Theo dõi độ nặng của suy tim nên trong quá trình điều trị, theo dõi đáp ứng điều trị |
| Men tim | Kết hợp chẩn đoán nhồi máu cơ tim |
| Siêu âm tim | Suy tim:
Tùy theo phân suất tống máu để phân loại suy tim, từ đó dược sĩ dựa vào phác đồ để can thiệp trên lâm sàng Rung nhĩ: Xác định huyết khối trong buồng tim Xác định LVEF: giúp lựa chọn thuốc trong kiểm soát tần số thất |
| Điện tâm đồ, men tim, điện tâm đồ gắng sức, Chụp CT scanner ĐMV hoặc chụp động mạch vành qua thông tim, chụp MRI tim, stress test kết hợp với hình ảnh
Trắc nghiệm tưới máu cơ tim bằng hình ảnh (bằng siêu âm tim, cộng hưởng từ tim, SPECT hoặc pEt) |
Rung nhĩ:
Đánh giá việc dùng thuốc kiểm soát tần số thất có đạt mục tiêu hay không Giúp xác định có mắc kèm các rối loạn nhịp và dẫn truyền khác hay không BMV mạn: Theo dõi và đánh giá độ hẹp, vị trí hẹp của mạch vành, mức độ suy tim do BMV (nếu có) |
| X-quang ngực thẳng | Tổng quát: Theo dõi viêm phổi nếu có
Suy tim: Chẩn đoán suy tim: phù mô kẽ, thâm nhiễm rốn phổi Rung nhĩ: Tìm nguyên nhân rung nhĩ Theo dõi độc tính amiodaron |
| CT scan não | Rung nhĩ:
Trong trường hợp bệnh nhân có triệu chứng thần kinh để chẩn đoán nhồi máu não do thiếu máu trên bệnh nhân rung nhĩ Từ đó, có kế hoạch điều trị thuốc chống đông hay không |
| Xét nghiệm chức năng tuyến giáp TSH, FT3, FT4 | Suy tim:
Cường giáp hay suy giáp có thể dẫn đến suy tim nên cần điều trị bệnh về tuyến giáp ngay khi phát hiện trên bệnh nhân suy tim Rung nhĩ: Tìm nguyên nhân rung nhĩ Theo dõi độc tính amiodaron (xét nghiệm khi khởi đầu và mỗi 6 tháng dùng thuốc) |
Phụ lục 3.2. Chống chỉ định và thận trọng của thuốc tim mạch
TĂNG HUYẾT ÁP
| Nhóm thuốc | Chống chỉ định | Thận trọng |
| LT | Gút | Hội chứng chuyển hóa
Không dung nạp glucose Mang thai Tăng canxi máu, hạ kali máu |
| CB | Hen
Block xoang nhĩ hoặc AV cao độ Nhịp tim chậm (< 60 lần phút) |
Hội chứng chuyển hóa
Không dung nạp glucose Vận động viên |
| CKCa nhóm dihydropyridin | Nhịp tim nhanh
Suy tim (EF giảm, độ II, III) Phù chân nặng trước đó |
|
| CKCa nhóm non – dihydropyridin (verapamil, diltiazem) | Block xoang nhĩ hoặc block nhĩ thất cao độ
Rối loạn chức năng thất trái (EF < 40%) Nhịp tim chậm (< 60 lần phút) |
|
| UCMC | Mang thai, tiền sử phù mạch
Tăng kali máu ( > 5,5mmol/L) Hẹp động mạch thận bên |
PNCCB không có biện pháp ngừa thai tin cậy |
| CTTA | Mang thai
Tăng kali máu Hẹp động mạch thận bên |
PNCCB không có biện pháp ngừa thai tin cậy |
| Đối kháng thụ thể mineralocorticod | Suy thận cấp hoặc nặng (MLCT<30 mL/phút)
Tăng kali máu |
SUY TIM
| Nhóm thuốc | Chống chỉ định | Thận trọng |
| UCMC/CTTA | Phụ nữ có thai
Phù mạch Hẹp động mạch thận hai bên |
Kali máu > 5,0 mmol/L
Natri máu < 130 mmol/L Creatinin máu > 221 mcmol/L Hạ HA có triệu chứng hoặc không triệu chứng nhưng nặng (HATT < 90 mmHg) Ho Hẹp động mạch chủ nặng |
| Thuốc ức chế neprilysin – thụ thể angiotensin (aRni) | Phối hợp với ƯCMC
Tiền sử phù mạch với ƯCMC hoặc CTTA Phù mạch di căn hoặc di truyền Suy gan nặng, xơ gan do bệnh lý đường mật quý thứ và thứ 3 của thai kỳ |
PNCT
Kali máu > 5,0 mmol/L Hẹp động mạch chủ nặng |
| CB | Hen phế quản (trừ thuốc chẹn beta chọn lọc trên tim)
Block nhĩ thất độ II, III (không đặt máy tạo nhịp) Thiếu máu cục bộ chi |
PNCT: phân loại an toàn C
Ngưng thuốc đột ngột Suy tim nặng (NYHA IV), đợt cấp suy tim hiện tại hoặc gần đây (< 4 tuần) Nhịp tim <50 lần phút Hạ HA (HATT < 90 mmHg) U tủy thượng thận (nếu hiện tại không dùng thuốc chẹn thụ thể alpha) Còn dấu hiệu sung huyết, tăng áp lực tĩnh mạch cảnh, phù ngoại biên, bệnh cổ trướng Hội chứng suy nút xoang |
| Thuốc đối kháng aldosteron | Dị ứng/đã bị phản ứng có hại của thuốc nghiêm trọng | PNCT: phân loại an toàn eplerenon (B), spironolacton (C)
Kali máu > 5,0 mmol/L Creatinin máu > 221 mcmol/L hoặc MLCT <30 mL/phút/1,73 m2 |
| Ivabradin | Bệnh tim mạch không ổn định (hội chứng mạch vành cấp, đột quỵ thiếu máu não thoáng qua, hạ HA nghiêm trọng)
Suy gan nặng, suy thận nặng Phụ nữ có thai hoặc cho con bú |
|
| LT | Bệnh nhân không có triệu chứng, dấu hiệu sung huyết | Lợi tiểu thiazid
PNCT: phân loại an toàn B Kali máu ≤ 3,5 mmol/L Creatinin máu > 221 mcmol/L hoặc MLCT < 30 mL/phút/1,73 m2. Hạ HA có triệu chứng hoặc không triệu chứng nhưng nặng (HATT < mmHg) Hạ kali máu Lợi tiểu quai Phụ nữ có thai: phân loại an toàn C Kali máu v 3,5 mmol/L Creatinin máu > 221 mcmol/L hoặc MLCT < 30 mL/phút/1,73 m2 Hạ HA có triệu chứng hoặc không triệu chứng nhưng nặng (HATT < 90 mmHg) Tăng acid uric máu |
| Digoxin | Rung thất | PNCT: phân loại an toàn C
Nhồi máu cơ tim cấp Chậm nhịp tim Hạ kali máu Hạ magie máu Hạ kali máu Tăng canxi máu |
| Hydralazin | Bệnh mạch vành
Bệnh thấp tim Lupus ban đỏ hệ thống vô căn |
Phụ nữ có thai: phân loại an toàn C
Viêm dây thần kinh Tụt HA Rối loạn hệ tạo máu (giảm hồng cầu, giảm bạch cầu) |
| Nitrat | Sử dụng đồng thời với thuốc ức chế phosphodiesterase
Viêm màng ngoài tim co thắt Bệnh cơ tim hạn chế |
PNCT: phân loại an toàn C
Dung nạp có thể xuất hiện ở liều cao hoặc khi không có khoảng thời gian ngưng dùng nitrat. |
RUNG NHĨ
| Nhóm thuốc | Chống chỉ định | Thận trọng |
| Amiodaron | Sốc tim
Suy nút xoang nặng dẫn đến nhịp chậm xoang và blốc xoang nhĩ, blốc nhĩ thất độ II và III, blốc nhánh Chậm nhịp từng cơn gây ngất Bệnh tuyến giáp Hạ HA động mạch Mẫn cảm với các thành phần của thuốc Quý thứ 2 và 3 của thai kỳ (chỉ dùng khi không có thuốc thay thế) PN CCB |
Suy tim sung huyết
Suy gan Hạ kali huyết Rối loạn chức năng tuyến giáp Giảm thị lực Kết hợp với thuốc chẹn beta Kết hợp với thuốc chẹn kênh canxi |
| CB | Suy tim cấp
Tiền sử co thắt phế quản nặng |
Hen phế quản: khuyến cáo dùng CB chọn lọc trên thụ thể beta 1 (tránh dùng carvedilol) |
| CKCa nhóm non- dihydropyridin | Suy thất trái với sung huyết phổi hoặc LVEF < 40%. | Thận trọng khi phối hợp với CB . Giảm liều trên bệnh nhân suy gan và bắt đầu với liều thấp hơn trên bệnh nhân suy thận |
| Glycosid tim (digoxin) | Bệnh nhân có các đường dẫn truyền phụ, nhịp nhanh thất và bệnh cơ tim phì đại tắc nghẽn đường dẫn máu | Nồng độ cao trong huyết tương có liên quan đến gia tăng nguy cơ tử vong Cần kiểm tra chức năng thận trước khi khởi đầu điều trị và hiệu chỉnh liều ở bệnh nhân có bệnh thận mạn |
BỆNH MẠCH VÀNH MẠN
| Nhóm | Chống chỉ định | Thận trọng |
| Chẹn beta
Atenolol Bisoprolol Metoprolol Propranolol Carvedilol Metoprolol |
– Block nhĩ thất (không có máy tạo nhịp)
– Nhịp tim chậm (< 50 lần phút) – Shock tim, suy tim mất bù – Hội chứng suy nút xoang (không có máy tạo nhịp) |
– PNCT: phân loại an toàn C (atenolol: D)
– Hen phế quản (tránh dùng chẹn beta không chọn lọc hoặc dùng chẹn beta chọn lọc liều cao) – Suy tim (trừ bisoprolol, carvedilol, metoprolol succinat) – Hạ huyết áp – U tủy thượng thận |
| Thuốc chẹn kênh canxi nhóm dihydropyridin
Amlodipin Felodipin Nifedipin |
– PNCT: phân loại an toàn C.
– Tránh dùng thuốc chẹn kênh canxi nhóm dihydropyridin tác dụng ngắn có thể làm nặng thêm tình trạng đau ngực (ví dụ nifedipin giải phóng nhanh hoặc nicardipin) – Thận trọng ở bệnh nhân hẹp van động mạch chủ và bệnh cơ tim phì đại – Thận trọng ở bệnh nhân suy tim phân suất tống máu giảm (amlodipin có tác động trung tính trên tỷ lệ tử vong nên thường được dùng ở bệnh nhân có tăng huyết áp hoặc đau thắt ngực ổn định) |
|
| Thuốc chẹn kênh canxi nhóm non- dihydropyridin Diltiazem
Verapamil |
– Suy tim phân suất tống máu giảm
– Tim đập chậm – Suy nút xoang – Block nhĩ thất độ nặng |
– PNCT: phân loại an toàn C
– NMCT – Nhịp nhanh thất – Hội chứng Wolff-Parkinson-White – Shock tim – Hạ huyết áp |
| Nitrat
Nitroglycerin (dưới lưỡi, xịt, miếng dán, kem bôi) Isosorbid dinitrat Isosorbid mononitrat |
– Dùng đồng thời với các chất ức chế phosphodiesterase-5 | – PNCT: phân loại an toàn C .
– Viêm màng tim – Bệnh cơ tim giới hạn vận động – Dung nạp có thể xảy ra ở liều cao hoặc dùng liên tục kéo dài |
| Ivabradin | – Chậm nhịp tim
– Suy gan nặng |
– Tuổi >75
– Suy thận nặng |
| Thuốc chống đau ngực khác:
Ranolazin |
– Xơ gan | PNCT: phân loại an toàn C.
– Chất ức chế hoặc cảm ứng CYP 3A4 – Người bệnh đã có khoảng QT kéo dài (> 500ms) – Suy gan, suy thận |
| Chống kết tập tiểu cầu
Aspirin Clopidogrel |
Xuất huyết tiêu hóa, xuất huyết nội sọ | Tiền sử xuất huyết tiêu hóa với aspirin |
Phụ lục 3.3. Liều dùng các thuốc tim mạch
| Thuốc chẹn bêta | ||
| Tên thuốc | Liều dùng | Lưu ý |
| Chẹn bêta chọn lọc | ||
| Atenolol | Tăng HA: 25 – 100 mg ngày x lần ngày
Rung nhĩ: 25-100 mg X 1 lần/ngày (PO) Hiệu chỉnh liều trên bệnh nhân suy giảm chức năng thận – ClCr15 – 35 mL/phút: tối đa 50 mg/ngày (PO) . – ClCr < 15 mL/phút: tối đa 25 mg/ngày (PO) hoặc 50 mg uống cách ngày – Thẩm phân máu: 25-50 mg sau mỗi lần thẩm phân (PO) |
Ngừng đột ngột sẽ gây tăng HA dội ngược, ức chế chọn lọc thụ thể beta-1 ở liều thấp – trung bình, trường hợp sử dụng liều cao cũng ức chế thụ thể beta-2; làm nặng hơn tình trạng hen phế quản khi mất tính chọn lọc; hiệu quả trên bệnh nhân có nhịp nhanh nhĩ hoặc tăng HA trước phẫu thuật Chỉ bisoprolol, carvedilol và metoprolol succinat được khuyến cáo trong điều trị HFrEF theo Hiệp Hội Tim mạch Hoa Kỳ (ACCF/AHA 2017)
Nebivolol được khuyến cáo trong điều trị HFrEF theo Hội Tim mạch châu Âu (ESC 2016) Những lưu ý trên BN suy tim Tất cả bệnh nhân suy tim đều cần sử dụng chẹn beta nếu không có chống chỉ định. Bắt đầu sử dụng chẹn beta khi tình trạng suy tim của BN ổn định: – Không nằm viện ở khoa chăm sóc tích cực – Không ứ dịch hoặc thiếu dịch – Không phải điều trị bằng thuốc vận mạch gần đây – Khởi đầu liều thấp, và tăng gấp đôi liều mỗi 2 tuần (hoặc chậm hơn nếu cần) để đạt liều mục tiêu sau 8-12 tuần điều trị. Chú ý thuốc CB có thể không cải thiện triệu chứng trong một vài tháng vì thuốc thể hiện tác dụng chậm. Ngay cả khi không cải thiện triệu chứng cơ năng, sử dụng CB trên bệnh nhân suy tim vẫn có lợi do làm giảm biến cố trên lâm sàng. Tránh ngưng thuốc đột ngột vì có thể dẫn đến kết cục lâm sàng xấu. Thuốc CB nên được cân nhắc sử dụng ngay cả khi bệnh nhân có bệnh đường hô hấp hoặc nhịp tim chậm không triệu chứng.
|
| Bisoprolol | – Tăng HA: 5-20mg/ngày x 1 lần/ngày
– Suy tim: + Khởi đầu: 1.25 mg x 1 lần/ngày + Liều đích: 10 mg x 1 lần/ngày – Điều trị suy tim mạn ổn định kèm suy gan suy thận: việc xác định liều cho các trường hợp này cần hết sức thận trọng – BMV mạn: 5-20 mg/ngày x 1lần/ngày – Điều trị tăng HA và bệnh tim thiếu máu cục bộ: không cần điều chỉnh liều đối với bệnh nhân suy chức năng gan hay thận mức độ nhẹ đến trung bình – ClCr < 20 (mL/phút) và suy gan nặng: liều tối đa 10 mg/ngày |
|
| Metoprolol succinat | Tăng HA: 25 – 100mg/ngày x 1 lần/ngày
Suy tim: – Khởi đầu: 12,5-25 mg x 1 lần/ngày – Liều đích: 200 mg x 1lần/ ngày Rung nhĩ: – 50-400 mg X 1 lần/ngày (PO) BMV mạn: – Khởi đầu: 50 mg x 2 lần; Tối đa: 200mg x 2 lần |
|
| Metoprolol tartrat | Tăng HA: 25 – 100mg/ngày x 2 lần/ngày
Rung nhĩ: 25-100 mg X 2 lần/ngày (PO) – BMV mạn Khởi đầu: 50 mg x 2 lần; Tối đa: 20 mg x1 lần/ngày |
|
| Esmolol | Tăng HA cấp cứu: liều tải 500-1000 mcg/kg/phút trong 1 phút tiếp theo truyền 50 mcg/kg/phút Liều bổ sung tiêm bolus lặp lại và truyền 50 mcg/kg/phút tăng dần đến tối đa 2.200mcg/kg/p khi cần
Rung nhĩ: Bolus 500 mcg/kg/phút, sau đó 50 -300 mcg/kg/phút (IV) |
|
| Chẹn bêta không chọn lọc | ||
| Nadolol | Tăng HA: 20- 120mg/ngày x 1 lần/ngày | Ngừng đột ngột sẽ gây tăng HA dội ngược, ức chế thụ thể beta-1 và beta-2 ở liều bình thường; làm nặng hơn tình trạng hen suyễn; hiệu quả trên bệnh nhân bị run, đau nửa đầu, tăng áp suất tĩnh mạch cửa, nhiễm độc tuyến giáp |
| Propranolol | Tăng HA: 40-320mg/ngày x 1-2 lần/ngày
Rung nhĩ: – Tĩnh mạch: Bolus 1 mg/phút, được dùng 3 liều cách 2 phút – Uống: 10-40 mg X 3-4 lần/ngày |
|
| Timolol | Tăng HA: 10-40mg/ngày x 1 lần/ngày | |
| Chẹn beta có hoạt tính giao cảm nội tại | ||
| Acebutalol | Tăng HA: 200-40Omg/ngày x 2 lần/ngày | |
| Pindolol | Tăng HA: 5-15mg/ngày x 2-3 lần/ngày | |
| Chẹn bêta và alpha | ||
| Carvedilola | Tăng HA: 12,5-50 mg/ngày x 2 lần/ngày
Suy tim – Khởi đầu: 3,125 mg X 2 lần/ngày – Liều đích: 25 mg X 2 lần/ngày BMV mạn: 25-50 mg x2 lần ngày Rung nhĩ: 3,125-25 mg X 2 lần/ngày (PO) |
|
| Labetalol | Tăng HA: 200-800 mg/ngày x 2 lần/ngày
Tăng HA cấp cứu: 0,5-1,0 mg kg (tối đa 20 mg) tiêm TM chậm mỗi 10 phút hoặc truyền TM 0,4 -1,0 mg/kg/giờ tăng đến 3 mg/kg/giờ. Tổng liều 300m. Liều này có thể lặp lại mỗi 4-6 giờ |
|
| Chẹn beta chọn lọc và có tác dụng giãn mạch | ||
| Nebivolol | Tăng HA: 2,5-10 mg/ngày x 1 lần/ngày
Suy tim – Khởi đầu: 1,25 mg X 1 lần/ngày – Liều đích: 10 mg X 1 lần/ngày |
|
| Thuốc ức chế men chuyển, ức chế thụ thể angiotensin | ||
| Tên thuốc | Liều dùng | Lưu ý |
| Thuốc ức chế men chuyển | ||
| Benazepril | Tăng HA: 5-40 mg/ngày | Có thể tăng kali máu ở bệnh nhân mắc bệnh thận mạn hoặc bệnh nhân sử dụng thuốc lợi tiểu giữ kali, đối kháng aldosteron, CTTA, hoặc thuốc ức chế trực tiếp renin
Có thể gây suy thận cấp ở bệnh nhân bị hẹp động mạch thận hai bên hoặc hẹp nghiêm trọng động mạch đến thận đơn độc Không sử dụng trong thai kỳ hoặc bệnh nhân có tiền sử phù mạch. Liều khởi đầu nên giảm 50% ở bệnh nhân đang điều trị với thiazid, đang bị giảm thể tích dịch, hoặc người lớn tuổi do nguy cơ hạ HA |
| Captopril | Tăng HA: 12,5 -100 mg/ngày x 2-3 lần/ngày
Suy tim – Khởi đầu: 6,2 5 mg X 3 lần/ngày – Liều đích: 50 mg X 3 lần/ngày |
|
| Enalapril | Tăng HA: 5-40 mg/ngày x 1-2 lần/ngày Suy tim
– Khởi đầu: 2,5 mg X 2 lần/ngày – Liều đích: 20 mg X 2 lần/ngày |
|
| Enalaprilat | Tăng HA cấp cứu: khởi đầu 1,25mg trong khoảng 5 phút. Liều này có thể tăng lên 5 mg mỗi 6 giờ; khi cần để đạt HA đích | |
| Fosinopril | Tăng HA: 10-40 mg/ngày x 1 lần/ngày
Suy tim – Khởi đầu: 5- 10 mg X 1 lần/ngày – Liều đích: N/A |
|
| Lisinopril | Tăng HA: 5-40 mg/ngày x 1 lần/ngày
Suy tim – Khởi đầu: 2,5 – 5 mg X 1 lần/ngày – Liều đích: 20 – 35 mg X 1 lần/ngày |
|
| Perindopril | Tăng HA: 2,5-10 mg/ngày x 1 lần/ngày
Suy tim – Khởi đầu: 2 mg X 1 lần/ngày – Liều đích: N/A |
|
| Quinapril | Tăng HA: 2,5-80 mg/ngày x 1-2 lần/ngày
Suy tim – Khởi đầu: 5 mg X 2 lần/ngày – Liều đích: N/A |
|
| Ramipril | Tăng HA: 1,25-10 mg/ngày x 1 -2 lần/ngày
Suy tim – Khởi đầu: 2,5 mg X 1 lần/ngày – Liều đích: 10 mg X 1 lần/ngày |
|
| Trandolapril | Tăng HA: 1- 4 mg/ngày x 1 lần/ngày
Suy tim – Khởi đầu: 0,5 mg X 1 lần/ngày – Liều đích: 4 mg X 1 lần/ngày |
|
| Imidapril | Tăng HA: 2,5-20mg/ngày | |
| Thuốc ức chế thụ thể angiotensin II | ||
| Candesartan | Tăng HA: 4-32 mg/ngày x 1- lần ngày
Suy tim – Khởi đầu: 4-8 mg X 1 lần/ngày – Liều đích: 32 mg X 1 lần/ngày |
Có thể tăng kali máu ở bệnh nhân BTM, hoặc bệnh nhân sử dụng thuốc lợi tiểu giữ kali, đối kháng aldosteron, ƯCMC, hoặc thuốc ức chế trực tiếp renin; có thể gây suy thận cấp ở bệnh nhân bị hẹp động mạch thận hai bên hoặc hẹp nghiêm trọng động mạch đến thận đơn độc Không gây ho khan như ƯCMC; không sử dụng cho PNCT; liều khởi đầu nên giảm 50% ở bệnh nhân đang điều trị với thiazid, đang bị giảm thể tích dịch, hoặc người lớn tuổi do nguy cơ hạ HA
|
| Irbesartan | Tăng HA: 150-300 mg/ngày x 1 lần/ngày | |
| Losartan | Tăng HA: 25-100 mg/ngày x 1-2 lần/ngày
Suy tim – Khởi đầu: 50 mg X 1 lần/ngày – Liều đích: 150 mg X 1 lần/ngày |
|
| Telmisartan | Tăng HA: 20-160 mg/ngày x 1 lần/ngày | |
| Valsartan | Tăng HA: 80-320 mg/ngày x 1 lần/ngày
Suy tim – Khởi đầu: 40 mg X 2 lần/ngày – Liều đích: 160 mg X 2 lần/ngày |
|
| Azilsartan | Tăng HA: 40-80 mg/ngày x 1 lần/ngày | |
| Eprosatan | Tăng HA: 400-800 mg/ngày x 1-2 lần/ngày | |
| Olmesartan | Tăng HA: 10-40 mg/ngày x 1 lần/ngày | |
| Thuốc ức chế neprilysin kết hợp ức chế thụ thể angiotensin (sacubitril/valsartan) (ARNI) | |||
| Nhóm bệnh nhân | Liều khởi đầu | Liều đích | Lưu ý |
| Chuyển đổi từ ƯCMC | ARNI chỉ có chỉ định duy nhất trong điều trị suy tim mạn
Đối với những bệnh nhân hiện tại không dùng ƯCMC/CTTA, bệnh nhân suy thận nặng (MLCT < 30 ml/phút/1,73 m2) hoặc suy gan trung bình: liều khởi đầu sacubitril/valsartan là 24/26 mg x 2 lần/ngày. Sacubitril ức chế neprilysin và ngăn cản sự giáng hóa của peptid lợi niệu BNP, do đó BNP sẽ tăng sau khi bắt đầu điều trị. Vì vậy, giá trị NT-proBNP cần thiết để đánh giá điều trị suy tim và mức độ suy tim khi sử dụng sacubitril/valsartan.
|
||
| Bệnh nhân đang dùng ƯCMC với tổng liều > 10 mg enalapril hoặc tương đương (lisinopril > mg hoặc ramipril > 5mg) | Ngưng ƯCMC ít nhất 36 giờ trước khi bắt đầu sử dụng sacubitril/valsartan 49/51 mg x 2 lần/ngày | Tăng gấp đôi liều sau 2-4 tuần theo khả năng dung nạp của bệnh nhân để đạt liều mục tiêu 97/103 mg x 2 lần/ngày.
|
|
| Bệnh nhân đang dùng ƯCMC với tổng liều < 10 mg enalapril hoặc tương đương (lisinopril ≤ 10 mg hoặc ramipril ≤ 5mg) | Ngưng ƯCMC ít nhất 36 giờ trước khi bắt đầu sử dụng sacubitril/valsartan 24/26 mg x 2 lần/ngày | ||
| Chuyển đổi từ CTTA | |||
| Bệnh nhân đang dùng CTTA với tổng liều > 160 mg valsartan hoặc tương đương (losartan > 50 mg hoặc olmesartan > 10mg) | Ngưng CTTA và bắt đầu sử dụng sacubitril/valsartan tại thời điểm liều kế tiếp với liều 49/51 mg x 2 lần/ngày | Tăng liều gấp đôi sau 2-4 tuần theo khả năng dung nạp của bệnh nhân để đạt liều mục tiêu 97/103 mg x 2 lần/ngày | |
| Bệnh nhân đang dùng CTTA với tổng liều ≤ 160 mg valsartan hoặc tương đương (losartan ≤ 50 mg hoặc olmesartan ≤ 10 mg) | Ngưng CTTA và bắt đầu sử dụng sacubitril/valsartan tại thời điểm liều kế tiếp với liều 24/26 mg x 2 lần/ngày | ||
| Thuốc chẹn kênh canxi | |||
| Tên thuốc | Liều dùng | ||
| Nhóm dihydropyridin | |||
| Amlodipin | Tăng HA: 2,5- 10 mg/ngày x 1 lần/ngày
BMV mạn: 2,5-10 mg/ngày x 1 lần/ngày |
||
| Felodipin | Tăng HA: 2,5-20 mg/ngày x 1 lần/ngày
BMV mạn: 5- 10 mg/ngày x 1 lần/ngày |
||
| Nifedipin | Tăng HA: 30-90 mg/ngày
BMV mạn (dạng giải phóng kéo dài): 30- 60 mg/lần x 1 lần/ngày |
||
| Lercanidipin | Tăng HA: 10-20 mg/ngày | ||
| Nicardipin | Tăng HA cấp cứu: bắt đầu 5 mg/g, tăng 2,5 mg/giờ mỗi 5 phút đến tối đa 15 mg/giờ
BMV mạn: 10-20 mg/ngày x 3 lần/ngày (PO) |
||
| Nhóm Non-Dihydropyridin | |||
| Diltiazem | Tăng HA: 120-360 mg/ngày x chia 1-2 lần/ngày
Rung nhĩ: 120-360 mg X 1 lần/ngày (PO) |
||
| Verapamil | Tăng HA: 120-480 mg/ngày x chia 2-3 lần/ngày
Rung nhĩ: – Tĩnh mạch: Bolus 0,075-0,15 mg/kg/2 phút, thêm 10 mg sau 30 phút nếu không đáp ứng, rồi truyền 0,005 mg/kg – Đường uống: 180-480 mg X 1 lần/ngày |
||
| Thuốc lợi tiểu | ||
| Tên thuốc | Liều dùng | Lưu ý |
| Nhóm thiazid | ||
| Hydroclorothiazid | Tăng HA: 12,5-50 mg ngày x lần ngày Suy tim
– Khởi đầu: 25 mg X 1-2 lần/ngày – Tối đa: 100 mg/ngày |
Sử dụng vào buổi sáng để tránh tiểu đêm
Những lưu ý trên BN suy tim Phối hợp với giảm muối và nước, lợi tiểu là thuốc điều trị bước đầu cơ bản trong suy tim. Bắt đầu với liều khởi đầu thấp, sau đó có thể tăng liều gấp đôi và điều chỉnh dựa vào cân nặng và chức năng thận của bệnh nhân Lưu ý sự khác biệt trong sinh khả dụng đối với các thuốc đường uống Đối với bệnh nhân có tình trạng quá tải dịch, bắt đầu điều trị bằng thuốc lợi tiểu và điều chỉnh sao cho cân nặng giảm 0,45-0,9 kg/ngày. Có thể phối hợp lợi tiểu quai và lợi tiểu thiazid trong trường hợp ức chế kép thận. Lợi tiểu quai được ưu tiên sử dụng hơn vì tác dụng lợi tiểu tốt hơn, tuy nhiên nó có thể gây suy giảm chức năng thận. Lợi tiểu thiazid chỉ được sử dụng khi có quá tải dịch nhẹ và tăng HA. |
| Metolazon | Suy tim
– Khởi đầu: 2,5 – 5 mg X 1 lần/ngày – Tối đa: 20 mg/ngày |
|
| Clorthalidon | Suy tim
– Khởi đầu: 12,5-25 mg X 1 lần/ngày – Tối đa: 100 mg/ngày |
|
| Clorothiazid | Suy tim
– Khởi đầu: 250 – 500 mg X 1-2 lần/ngày – Tối đa: 2.000 mg/ngày |
|
| Indapamid | Tăng HA: 1,25-2,5 mg/ngày x 1 lần/ngày
Suy tim – Khởi đầu: 2,5 mg/ngày – Liều thường dùng: 2,5-5 mg/ngày |
|
| Nhóm lợi tiểu quai | ||
| Furosemid | Tăng HA: 20-80 mg/ngày x 2 lần/ngày
Suy tim – Khởi đầu: 20-40 mg X 1-2 lần/ngày – Tối đa: 600 mg/ngày |
Liều tương đương furosemid 40 mg ~ bumetanid 1 mg ~ torsemid 10-20 mg ~ acid ethacrynic 50 mg.
Những lưu ý trên BN suy tim Tương tự nhóm thiazid
|
| Bumetanid | Suy tim
– Khởi đầu: 0,5-1 mg X 1-2 lần/ngày – Tối đa: 10 mg/ngày |
|
| Torsemid | Suy tim
– Khởi đầu: 10-20 mg X 1-2 lần/ngày – Tối đa: 200 mg/ngày |
|
| Ethacrynic acid | Suy tim
– Khởi đầu: 25-50 mg X 1-2 lần/ngày – Tối đa: 200 mg/ngày |
|
| Thuốc đối kháng thụ thể mineralocorticoid | ||
| Amilorid | Tăng HA: 5-10 mg/ngày x 1-2 lần/ngày | Tác dụng lợi tiểu yếu, thường được phối hợp với thuốc lợi tiểu thiazid để giảm tác dụng hạ kali máu; tránh dùng ở bệnh nhân bệnh thận mạn (MLCT<30 mL/phút); có thể gây tăng kali máu, đặc biệt khi kết hợp thuốc ƯCMC, CTTA, chất ức chế renin trực tiếp hoặc thực phẩm bổ sung kali
|
| Eplerenon | Tăng HA: 20-25 mg/ngày x 1-2 lần/ngày
Suy tim: xem bảng bên dưới |
|
| Spironolacton | Tăng HA: 12,5-50 mg/ngày x 1-2 lần/ngày
Suy tim: xem bảng bên dưới |
|
| Triamteren | Tăng HA: 25-100 mg/ngày x 1-2 lần/ngày | |
| Thuốc đối kháng thụ thể mineralocorticoid trong điều trị suy tim | |||
| Giá trị | Eplerenon | Spironolacton | Lưu ý |
| MLCT > 50 mL/phú’t/1,73 m2 và kali máu ≤ 5 mmol L | 25 mg x 1 lần/ngày | 12,5-25 mg x 1 lần/ngày |
Liều đích của eplerenon và spironolacton trong điều trị suy tim là 50 mg/ngày Nên khởi đầu liều thấp 12,5mg spironolacton hoặc 5mg eplerenon Nguy cơ tăng kali huyết nếu dùng chung với liều cao thuốc ức chế men chuyển hoặc thuốc ức chế men chuyển phối hợp với thuốc CTTA Phải tránh dùng chung với thuốc kháng viêm không steroid và chất ức chế chọn lọc COX-2 Nếu không có tình trạng hạ kali máu (kali máu < 4,0 mmol/L), không khuyến cáo bổ sung kali khi đang sử dụng một thuốc lợi tiểu giữ kali Tương tác thuốc + Spironolacton: cẩn thận với các thuốc khác có thể gây tăng kali máu + Eplerenon: chuyển hóa qua CYP 3A , tránh dùng chung với các thuốc ức chế mạnh CYP 3A (ketoconazol) và cân nhắc giảm liều với các thuốc ức chế trung bình CYP 3A4 (verapamil, erythromycin, saquinavir, fluconazol); sử dụng thận trọng với các thuốc có thể gây tăng kali máu
|
| Liều duy trì sau 1 tháng nếu kali máu ≤ 5 mmol L và MLCT > 50 mL/phút/1,73 m2 | 50 mg x 1 lần/ngày | 25 mg x 1 lần/ngày hoặc 2 lần ngày | |
| MLCT 30-49 mL/phút/1,73 m2 và kali máu ≤ 5 mmol L | 25 mg cách ngày | 12,5 mg x 1 lần/ngày hoặc cách ngày | |
| Liều duy trì sau 1 tháng nếu kali máu ≤ 5 mmol L và MLCT từ 30-49 mL/phút/1,73 m2 | 25 mg x 1 lần/ngày | 12,5-2 5 mg x 1 lần/ngày | |
| Thuốc điều trị THA khác | ||
| Tên thuốc | Liều dùng | Lưu ý |
| Ức chế renin trực tiếp | ||
| Aliskiren | Tăng HA: 75-300 mg/ngày x 1 lần/ngày | Tăng kali máu ở bệnh nhân BTM và ĐTĐ hoặc bệnh nhân sử dụng thuốc lợi tiểu giữ kali, đối kháng aldosteron, ƯCMC hoặc CTTA
Có thể gây suy thận cấp ở bệnh nhân bị hẹp động mạch thận hai bên hoặc hẹp nghiêm trọng động mạch đến thận đơn độc Không sử dụng cho PNCT |
| Ức chế thụ thể alpha-adrenergic | ||
| Doxazosin | Tăng HA: 1-8 mg/ngày x 1 lần/ngày |
Sử dụng liều đầu tiên khi đi ngủ; bệnh nhân nên đứng lên từ từ khi chuyển tư thế để giảm nguy cơ hạ HA tư thế Hiệu quả trên bệnh nhân nam giới bị tăng sản lành tính tuyến tiền liệt |
| Prazosin | Tăng HA: 1-20 mg/ngày x 2-3 lần/ngày | |
| Terazosin | Tăng HA: 1-20 mg/ngày x 1-2 lần/ngày | |
| Phentolamin | Tăng HA cấp cứu: Tiêm TM liều 5mg. Tiêm bổ sung liều 10 phút khi cần để đạt HA đích | |
| Cường thụ thể Dopamin chọn lọc | ||
| Fenoldapam | Tăng HA cấp cứu: khởi đầu 0,1 -0,3 mcg/kg/p; có thể tăng dần 0,05-0,1 mcg/kg/phút mỗi 15 phút cho đến khi đạt HA đích Truyền tối đa 1,6 mcg/kg/phút. | |
| Giãn mạch, đối kháng a trung ương, giảm adrenergic | ||
| Hydralazin | Tăng HA: 20-100 mg/ngày x 2-4 lần ngày
Tăng HA cấp cứu: khởi đầu 10 mg qua truyền TM chậm (liều ban đầu tối đa 20 mg); lặp lại mỗi 4-6 giờ khi cần |
Nên sử dụng kèm thuốc lợi tiểu thiazid và CB để giảm ứ dịch và giảm phản xạ tim nhanh |
| Minoxidil | Tăng HA: 2,5-40 mg/ngày x 1-2 lần/ngày | |
| Clonidin | Tăng HA: 0,1-0,2 mg/ngày x 2 lần/ngày | Ngừng đột ngột sẽ gây tăng HA dội ngược; hiệu quả nhất khi dùng kèm thuốc lợi tiểu thiazid để làm giảm sự ứ dịch; miếng dán clonidin được sử dụng 1 lần/tuần
|
| Methyldopa | Tăng HA: 250-500 mg/ngày x 2 lần/ngày | |
| Giãn mạch – qua Nitric-oxid | ||
| Sodium nitroprussid | Tăng HA cấp cứu: khởi đầu 0,3-0,5 mcg/kg/phút; tăng dần 0,5 mcg/kg/phút để đạt HA đích; liều tối đa 10 mcg/kg/phút; trong thời gian ngắn nhất có thể
Suy tim cấp – Khởi đầu: 0,3 mcg/kg/phút – Khoảng liều điều trị: 0,3-5 mcg kg phút (thường < 4 mcg/kg/ph) |
Thận trọng ở bệnh nhân thiếu máu cục bộ cơ tim tiến triển, hạ HA, ADR của cyanid (buồn nôn, bồn chồn), ngộ độc thiocyanat, nhạy cảm ánh sáng. |
| Nitroglycerin | Tăng HA cấp cứu: khởi đầu 5 mcg/p; tăng dần 5 mcg/p mỗi 3-5 phút đến liều tối đa 20 mcg.
BMV mạn: viên uống: 2.5-6.5 mg x 3-4 lần/ngày Tối đa: 24mg x 4 lần/ngày BMV mạn: 0,4mg/xịt , 1-2 xịt mỗi 5 phút, tổng cộng 3 liều Suy tim cấp – Khởi đầu: 20 mcg/phút – Khoảng liều điều trị: 40-200 mcg/phút |
Trường hợp không hết đau ngực sau lần xịt đầu tiên cần gọi cấp cứu
Hạ HA, nhức đầu, dung nạp thuốc nếu truyền liên tục trên 24 giờ |
| Isosorbid mononitrat | BMV mạn:
Dạng phóng thích kéo dài: 30 -60 mg x 1 lần/ngày vào buổi sáng Tối đa 240mg x1 lần/ngày Dạng tác dụng tức thời: 20 mg x 2 lần/ngày, uống cách nhau 7 giờ |
Uống thuốc sau khi uống nửa ly nước đầy
Không nhai nghiền thuốc dạng phóng thích kéo dài |
| Isosorbid dinitrat | Suy tim cấp
– Khởi đầu: 1 mg/giờ – Khoảng liều điều trị: 2-10 mg/giờ |
Hạ HA, nhức đầu, dung nạp thuốc nếu truyền liên tục trên 24 giờ |
| Đối kháng adrenergic ngoại biên | ||
| Reserpin | Tăng HA: 0,1-0,25 mg/ngày x 1 lần/ngày | Sử dụng nhiều trong thử nghiệm lâm sàng; nên dùng kèm thuốc lợi tiểu thiazid để làm giảm ứ dịch. |
| Phối hợp hydralazin và isosorbid dinitrat trong điều trị suy tim | ||
| Phối hợp thuốc | Liều khởi đầu | Liều tối đa |
| Viên phối hợp hydralazin/isosorbid dinitrat | 37,5 mg hydralazin/20 mg isosorbid dinitrat X 3 lần/ngày | 75 mg hydralazin/40 mg isosorbid dinitrat X 3 lần/ngày |
| Hydralazin và Isosorbid dinitrat | Hydralazin 25-50 mg X 3-4 lần/ngày,
Isosorbid dinitrat 20-30 mg X 3-4 lần/ngày |
Hydralazin 300 mg chia 2 lần/ngày, Isosorbid dinitrat 120 mg/ngày chia 2 lần/ngày |
| Thuốc chống đông và chống kết tập tiểu cầu | |
| Tên thuốc | Liều dùng |
| Thuốc chống đông đường uống thế hệ mới trong điều trị rung nhĩ | |
| Dabigatran | 150 mg X 2 lần/ngày
Clcr 30-50 mL/phút và tuổi ≥ 75, hoặc nguy cơ xuất huyết tiêu hóa: 110 mg X 2 lần/ngày Không khuyến cáo sử dụng khi: Clcr < 30 mL/phút, đang sử dụng thuốc ức chế, hoặc kích hoạt P-glycoprotein |
| Rivaroxaban | 20 mg X 1 lần/ngày
Clcr 30-50 mL/phút: 15 mg X 1 lần/ngày Tránh sử dụng khi: Clcr < 30 mL/phút, dùng thuốc ức chế, hoặc cảm ứng mạnh CYP3A4 và P-glycoprotein |
| Thuốc chống kết tập tiểu cầu | |
| Aspirin | BMV mạn: 75-100 mg x 1lần/ngày
Dự phòng thứ cấp biến cố tim mạch ở bệnh nhân ĐTĐ: 75-162 mg x 1 lần/ngày Dự phòng thứ cấp ở bệnh nhân sau hậu phẫu bắc cầu mạch vành: 81-325 mg x 1 lần/ngày Bệnh nhân sau đặt stent: 81mg x 1 lần/ngày dùng suốt đời |
| Clopidogrel | BMV mạn: 75 mg x 1 lần/ngày
Dự phòng thứ cấp biến cố tim mạch ở bệnh nhân ĐTĐ: 75 mg x 1 lần/ngày Dự phòng thứ cấp ở bệnh nhân sau hậu phẫu bắc cầu mạch vành: 75 mg x 1 lần/ngày Bệnh nhân đặt stent sau nhồi máu cơ tim cấp: 75 mg x 1 lần/ngày kết hợp aspirin ít nhất 12 tháng Bệnh nhân sau đặt stent (không do nhồi máu cơ tim cấp): 75 mg x 1 lần/ngày Stent kim loại: kết hợp aspirin ít nhất 1 tháng Stent phủ thuốc: kết hợp aspirin ít nhất 6 tháng (3 tháng với bệnh nhân có nguy cơ chảy máu cao) |
| Ticagrelor | Bệnh nhân đặt stent sau nhồi máu cơ tim cấp: 90 mg x 2 lần/ngày ít nhất 12 tháng kết hợp aspirin Stent phủ thuốc: kết hợp aspirin ít nhất 6 tháng với bệnh nhân có nguy cơ chảy máu cao |
| Thuốc chống loạn nhịp khác | ||
| Tên thuốc | Liều dùng | Lưu ý |
| Digoxin | Kiểm soát tần số thất trong rung nhĩ:
– Tĩnh mạch: 0,25 mg tiêm tĩnh mạch, lặp lại đến tối đa 1,5 mg/24 giờ – Đường uống: 0,125-0,25 mg X 1 lần/ngày Suy tim Liều duy trì (không khuyến cáo dùng liều tải): 0,125 – 0,25 mg x 1 lần/ngày |
Những lưu ý trên BN suy tim
– Đối với hầu hết bệnh nhân, liều digoxin 0,125 mg/ngày là đủ để đạt đến nồng đồ điều trị. Liều duy trì của digoxin trên bệnh nhân Việt Nam nên ở khoảng 0,0625- 0,125 mg/ngày tùy theo cân nặng và MLCT. Nếu duy trì liều cao (0,25 mg/ngày), nên có 1-2 ngày trong tuần không uống thuốc. – Cân nhắc liều 0,125 mg cách ngày đối với bệnh nhân trên 70 tuổi, bệnh nhân suy giảm chức năng thận, bệnh nhân có khối lượng cơ thấp. – Không sử dụng liều tải digoxin trong điều trị suy tim. – Tính toán chế độ liều digoxin có thể tham khảo trang web: http://clincalc.com/digoxin/ – Tương tác thuốc: nồng độ digoxin tăng khi sử dụng đồng thời với các thuốc ức chế P-glycoprotein và ức chế nhiều thuốc (clarithromycin, erythromycin, amiodaron, dronedaron, itraconazol, posaconazol, cyclosporin, tacrolimus, verapamil, quinidin, propafenon). – Mảnh Fab miễn dịch digoxin (digoxin immune fab): cân nhắc sử dụng nếu ngộ độc digoxin có khả năng đe dọa tính mạng bao gồm rối loạn nhịp thất nặng, chậm nhịp tiến triển, block tim độ II hoặc độ III không đáp ứng với atropin, kali máu > 5,5 mmol/L với dấu hiệu và triệu chứng ngộ độc digoxin. |
| Amiodaron | Chuyển nhịp trong rung nhĩ:
– Tĩnh mạch: 150 mg/ 10 phút; sau đó 1 mg/phút trong 6 giờ; rồi 0,5 mg/phút trong 18 giờ; sau đó giảm liều tiêm hoặc chuyển sang liều uống – Đường uống: 600-800 mg/ngày (chia nhiều lần, tổng liều có thể: 10 g), sau đó duy trì 100-400 mg/lần/ngày Kiểm soát tần số thất trong rung nhĩ:
|
|
| Ivabradin | ||
| Điều trị BMV mạn | ||
| Liều khởi đầu ở bệnh nhân dưới 75 tuổi: không vượt quá 5 mg x 2 lần/ngày
Liều tối đa: 7,5 mg x 2 lần/ngày Ngưng sử dụng thuốc nếu triệu chứng không cải thiện sau 3 tháng điều trị, đáp ứng kém hoặc bệnh nhân không cần giảm nhịp tim Nếu nhịp tim khi nghỉ dưới 5 lần phút hoặc bệnh nhân có triệu chứng chậm nhịp tim (đau đầu, chóng mặt, mệt mỏi, HA thấp) nên giảm liều ngay cả khi đang dùng liều 5 mg x lần ngày. Theo dõi nhịp tim sau giảm liều Ngừng thuốc nếu nhịp tim khi nghỉ tiếp tục dưới 5 lần phút hoặc bệnh nhân còn triệu chứng chậm nhịp tim |
||
| Điều trị suy tim | ||
| Tần số tim | Điều chỉnh liều | Lưu ý |
| > 60 nhịp/phút | Tăng liều khoảng 2,5 mg X 2 lần/ngày đến tối đa liều 7,5 mg X 2 lần/ngày | Bắt đầu liều 5 mg x 2 lần/ngày và uống thuốc cùng thức ăn. Liều đích ivabradin trong điều trị suy tim là ,5 mg X lần ngày Đối với những bệnh nhân rối loạn dẫn truyền với nhịp tim chậm có thể dẫn đến rối loạn huyết động nên bắt đầu với liều ivabradin 2,5 mg X 2 lần/ngày . Tương tác thuốc
Ivabradin chuyển hóa qua CYP 3A4 vì vậy cần chú ý: – Tránh sử dụng chung với các thuốc ức chế CYP 3A mạnh (itraconazol, clarithromycin, telithromycin, nelfinavir, nefazodon,…) và trung bình (diltiazem, verapamil, nước ép bưởi chùm) – Tránh sử dụng với các thuốc cảm ứng CYP 3A (St John’s wort, rifampicin, barbiturat và phenytoin) Tương tác giữa thuốc và máy tạo nhịp – Bệnh nhân được đặt máy tạo nhịp với thiết lập nhịp phút hoăc cao hơn không thể đạt mục tiêu nhịp tim nhỏ hơn nhịp phút. |
| 50-60 nhịp/phút | Duy trì liều hiện tại | |
| < 50 nhịp/phút hoặc có dấu hiệu và triệu chứng của nhịp chậm | Giảm liều khoảng 2,5 mg X 2 lần/ngày
Ngưng điều trị nếu liều hiện tại là 2,5 mg X 2 lần/ngày |
|
Phụ lục 3.4. Tác dụng không mong muốn của các thuốc tim mạch
| Nhóm thuốc | Tác dụng không mong muốn |
| Ức chế men chuyển/Chẹn thụ thể angiotensin | – Phù mạch: hiếm gặp đối với nhóm thuốc CTTA, CTTA an toàn cho bệnh nhân có tiền sử phù mạch
– Suy thận cấp, suy giảm chức năng thận – Ho khan: tần suất xảy ra ho khan của nhóm bệnh nhân sử dụng CTTA tương đương với placebo và thấp hơn UCMC trong hầu hết các thử nghiệm lâm sàng – Tăng kali máu – Hạ Ha |
| Chẹn beta | – Mệt mỏi, chóng mặt
– Phù, ứ dịch – Tụt HA – Chậm nhịp tim – Làm mờ triệu chứng hạ đường huyết ở bệnh nhân ĐTĐ – Co thắt phế quản (hiếm gặp) |
| Chẹn kênh canxi dihydropyridin | – Chóng mặt
– Đỏ mặt – Tăng sản nướu – Nôn ói – Phù mạch – Tụt HA thế đứng – Tim đập nhanh do phản xạ |
| Chẹn kênh canxi non- dihydropyridin | – Chậm nhịp tim
– Hạ HA – Phù ngoại vi – Diltiazem: chóng mặt, nôn ói – Verapamil: táo bón |
| Lợi tiểu thiazid | – Tụt HA
– Hạ magie máu – Hạ kali máu – Tăng canxi máu – Tăng ure – Suy giảm chức năng thận – Nhạy cảm ánh sáng |
| Lợi tiểu quai | – Tụt HA
– Hạ magie máu – Hạ kali máu – Hạ canxi máu – Tăng ure máu – Suy giảm chức năng thận – Nhạy cảm ánh sáng |
| Kháng aldosteron | – Tăng kali máu
– Nữ hóa tuyến vú ở nam giới, rối loạn kinh nguyệt |
| Hydralazin | – Đau đầu
– Tụt HA – Triệu chứng tương tự lupus |
| Nitrat | – Đau đầu
– Chóng mặt – Tụt HA – Đỏ bừng mặt |
| Ivabradin | – Chậm nhịp tim
– Hiện tượng đom đóm mắt, nhìn mờ – Khởi phát rung nhĩ |
| Amiodaron | – Tụt HA
– Chậm nhịp tim – Kéo dài khoảng QT – Mất sắc tố da – Rối loạn chức năng tuyến giáp – Buồn nôn – Lắng cặn giác mạc |
| Glycosid tim | – Rối loạn tiêu hóa
– Chóng mặt, nhức đầu – Phát ban – Loạn nhịp |
| Chống kết tập tiểu cầu | – Xuất huyết tiêu hóa
– Chảy máu |
| Thuốc chống ĐTN khác: ranoazin | – Chóng mặt, đau đầu
– Kéo dài QT – Phù ngoại vi |
Phụ lục 3.5. Tương tác thuốc của các thuốc tim mạch
Một số tương tác chống chỉ định
| Thuốc | Thuốc ức chế và cảm ứng enzym chuyển hóa thuốc | Chú ý |
| Tương tác thuốc chống chỉ định | ||
| Sildenafil, tadalafil, vardenafil | Isosorbid dinitrat, isosorbid mononitrat, NTG | Phối hợp gây tụt huyết áp sâu, tử vong đã được báo cáo |
| Thioridazin, pimozid | Amiodaron, conivaptan, diltiazem, dronedaron, propafenon, quinidin, ranolazin, verapamil | Ức chế chuyển hóa của thioridazin, pimozid; kéo dài khoảng QT và tăng nguy cơ loạn nhịp |
| Atorvastatin | Telaprevir | Telaprevir làm tăng nồng độ atorvastatin |
| Simvastatin | Gemfibrozil, cyclosporin | Các thuốc ức chế CYP3A4 làm tăng nồng độ simvastatin/lovastatin dẫn tới tăng nguy cơ đau cơ và tiêu cơ vân. Pravastain là lựa chọn thay thế. Giảm nguy cơ khi atorvastatin hoặc rosuvastatin phối hợp với gemfibrozil |
| Lovastatin, simvastatin | Atazanavir, boceprevir, danazol, fosamprenavir, itraconazol, lopinavir, ritonavir, posaconazol, saquinavir, telaprevir, tipranavir | |
| Ranolazin | Clarithromycin, ketoconazol, indinavir, itraconazol, nefazodon, nelfinavir, ritonavir, saquinavir | Các thuốc ức chế CYP3A4 làm tăng nồng độ ranolazin và nguy cơ kéo dài khoảng QT, loạn nhịp |
| Dronedaron, ranolazin | Carbamazepin, phenobarbital, phenytoin, rifampin, rifabutin, rifapentine | Các thuốc cảm ứng CYP3A4 làm giảm nồng độ thuốc trong máu |
| Dronedaron | Cyclosporin, clarithromycin, nước ép bưởi chùm, ketoconazol, itraconazol, nefazodon, ritonavir, telithromycin, voriconazol | Các thuốc ức chế CYP3A4 làm tăng nồng độ dronedaron. Ketoconazol làm tăng Cmax của dronedaron 9 lần |
Một số tương tác có ý nghĩa cần lưu ý trên lâm sàng
| Cặp tương tác | Hậu quả | Cơ chế | Cách xử lý |
| Aspirin (ASA) – Thuốc chẹn bêta | Giảm tác dụng hạ huyết áp và giảm hiệu quả trên phân suất tống máu thất trái (LVEF) ở bệnh nhân suy tim mạn của thuốc chẹn bêta | Giảm hiệu quả làm hạ huyết áp : ASA ức chế sinh tổng hợp prostaglandin.
Suy tim : chưa rõ |
Giảm hiệu quả làm hạ huyết áp : theo dõi huyết áp Nếu nghi ngờ rõ có xảy ra tương tác thì xem xét giảm liều ASA hoặc thay đổi sang thuốc chống kết tập tiểu cầu khác hoặc sử dụng nhóm thuốc điều trị tăng huyết áp khác
Suy tim : Theo dõi LVEF và tình trạng lâm sàng của bệnh nhân Nếu nghi ngờ rõ có xảy ra tương tác thì xem xét giảm liều ASA hoặc thay đổi sang thuốc chống kết tập tiểu cầu khác |
| ASA – Digoxin | Tăng nồng độ kali máu | Hiệp đồng tác dụng làm tăng kali máu | Theo dõi nồng độ kali máu |
| ASA – thuốc ức chế bơm proton (PPI) | Tăng nguy cơ gây hại dạ dày của ASA PPI có thể làm giảm hoạt tính ức chế kết tập tiểu cầu của ASA liều thấp | PPI ức chế bơm proton, làm tăng pH dạ dày nên dễ hòa tan lớp bao phim tan trong ruột của viên thuốc ASA ngay tại dạ dày, giải phóng các phân tử acid salicylic, làm tăng nguy cơ gây hại dạ dày | Hướng dẫn bệnh nhân cách uống viên ASA bao tan trong ruột, đặc biệt khi dùng đồng thời với PPI Bệnh nhân với nguy cơ có hại nghiêm trọng trên dạ dày thì nên tránh sử dụng đồng thời hai thuốc này |
| ASA – Ginkgo biloba | Tăng nguy cơ xuất huyết | Chưa rõ, có thể do hiệp lực hiệu quả tác dụng ức chế kết tập tiểu cầu giữa ASA với một thành phần trong dịch chiết Ginkgo biloba | Khuyên bệnh nhân nên tránh sử dụng đồng thời hai thuốc trên vì tiềm ẩn nguy cơ xuất huyết nghiêm trọng |
| ASA – Glimepirid | Tăng hiệu quả hạ đường huyết của glimepirid | ASA làm giảm nồng độ glucose huyết và tăng cường sự tiết insulin Sự ức chế tổng hợp prostaglandin có thể làm ức chế sự đáp ứng cấp tính insulin với đường huyết ASA cạnh tranh với glimepirid trong việc gắn với protein huyết tương | Theo dõi đường huyết của bệnh nhân Nếu xảy ra hạ đường huyết thì xem xét giảm liều glimepirid Nếu ASA dùng với mục đích giảm đau kháng viêm thì nên cân nhắc thay thế bằng paracetamol hoặc một thuốc kháng viêm không steroid khác (ví dụ như sulindac) |
| ASA – Insulin | Tăng nguy cơ hạ đường huyết | Tăng nồng độ nền của Insulin | Theo dõi đường huyết và điều chỉnh phác đồ insulin khi cần thiết |
| ASA – ACEI | Tác dụng hạ huyết áp và gây giãn mạch của ƯCMC bị giảm | ASA ức chế sự tổng hợp prostaglandin | Nếu bắt buộc phải sử dụng đồng thời hai thuốc này thì cần theo dõi chặt chẽ huyết áp và các thông số huyết động Nếu thông số huyết động được ghi nhận bị ảnh hưởng theo chiều hướng xấu thì cần xem xét các trường hợp sau: giảm liều ASA dưới 100 mg/ngày, hoặc chuyển sang thuốc ức chế kết tập tiểu cầu khác, hoặc nếu tiếp tục sử dụng ASA thì đổi nhóm thuốc ƯCMC sang CTTA. |
| ASA – CTTA | Tăng độc tính trên thận, đặc biệt ở người lớn tuổi hoặc người bị giảm thể tích tuần hoàn Giảm hiệu quả CTTA Tăng nồng độ kali máu | Tăng độc tính các thuốc
Đối kháng dược lực Các thuốc kháng viêm không steroid làm giảm tổng hợp prostaglandin giãn mạch thận nên ảnh hưởng đến cân bằng nội môi và có thể làm giảm tác dụng hạ huyết áp Cả hai thuốc đều làm tăng nồng độ kali máu |
Thận trọng, theo dõi chặt chẽ |
| ASA – Spironolacton | ASA ngăn tác dụng bài tiết natri qua nước tiểu của spironolacton Dữ liệu hạn chế cho thấy ASA không có lợi trên hiệu quả hạ huyết áp của spironolacton | ASA ngăn sự bài tiết canrenon (chất chuyển hóa chưa liên hợp của spironolacton) qua ống thận | Theo dõi huyết áp và nồng độ natri máu ở bệnh nhân được điều trị mãn tính với hai thuốc này
Tăng liều spironolacton có thể làm đảo ngược hậu quả của tương tác |
| ASA – Furosemid | Ảnh hưởng nồng độ kali máu Giảm hiệu quả furosemid. | ASA làm tăng nồng độ kali máu Furosemid làm giảm nồng độ kali máu Đối kháng dược lực | Theo dõi |
| ASA – Lợi tiểu thiazid | Ảnh hưởng nồng độ kali máu Tăng nhẹ nồng độ, hiệu quả của ASA | ASA làm tăng nồng độ kali máu, lợi tiểu thiazid làm giảm nồng độ kali máu Lợi tiểu thiazid cạnh tranh đào thải ở ống thận với các thuốc có tính acid. | Thận trọng, theo dõi |
| Chẹn beta – Diltiazem, verapamil | Có thể gây đau thắt ngực và block tim Tương tác này thường gặp ở người già, rối loạn chức năng thất trái | Hiệp đồng tác dụng | Giám sát chặt chẽ dung nạp thuốc của bệnh nhân Bệnh nhân cần thông báo tới bác sĩ dược sĩ ngay nếu có triệu chứng chậm nhịp tim, đau đầu, mệt mỏi, phù, tăng cân |
| Chẹn beta – Clodinin | Gây hội chứng ngừng clodinin | Chưa rõ ràng | Giám sát chặt chẽ huyết áp bệnh nhân Bệnh nhân cần thông báo tới bác sĩ dược sĩ ngay nếu có triệu chứng chậm nhịp tim, đau đầu, chóng mặt |
| Clopidogrel – Esomeprazol | Giảm hiệu quả ức chế kết tập tiểu cầu của clopidogrel | Cản trở sự chuyển hóa clopidogrel qua CYP2C19 để thành chất có hoạt tính | Các bệnh nhân cần điều trị clopidogrel dài hạn với nguy cơ xuất huyết dạ dày – ruột thấp thì có thể sử dụng thuốc đối kháng histamin H2 thay thế (famotidin, ranitidin; không dùng cimetidin). Các bệnh nhân cần điều trị dài hạn
clopidogrel với nguy cơ xuất huyết dạ dày – ruột cao (tiền sử xuất huyết dạ dày – ruột, cao tuổi, điều trị đồng thời với thuốc chống đông hoặc steroid, kháng viêm không steroid, nhiễm Hecilobacter pylori) hoặc bị bệnh trào ngược dạ dày – thực quản – cần dùng nhóm thuốc ức chế bơm proton – thì nên sử dụng pantoprazol. |
| Clopidogrel – CKCa non- dihydropyridin (diltiazem, nifedipin) | Giảm nồng độ, hiệu quả clopidogrel | Diltiazem/ Nifedipin ức chế CYP3A4, clopidogrel chuyển hóa qua CYP 3A để thành chất có hoạt tính | Theo dõi chặt chẽ |
| Clopidogrel – Meloxicam | Tăng hoạt tính ức chế kết tập tiểu cầu | Hiệp đồng dược lực | Thận trọng, theo dõi chặt chẽ |
| Digoxin – Thuốc ức chế CYP 3A4 (Amiodaron, conivaptan, itraconazol, propafenon, quinidin, verapamil) | Tăng độc tính của digoxin | Thuốc ức chế CYP3A làm tăng nồng độ digoxin trong máu | Giám sát nồng độ digoxin trong máu |
| Digoxin – Indomethacin | Tăng độc tính của digoxin | Giảm thanh thải của digoxin | Giám sát nồng độ digoxin trong máu |
| Digoxin – Lợi tiểu quai và thiazid | Tăng độc tính của digoxin | Hạ kali máu do dùng các thuốc lợi tiểu có thể gây ra độc tính của digoxin ngay cả khi nồng độ digoxin bình thường. | Giám sát nồng độ digoxin trong máu |
| Statin (Atorvastatin, lovastatin, simvastatin) – Thuốc ức chế CYP3A4 (Amiodaron, aprepitant, clarithromycin, conivaptan, erythromycin, fluvoxamin, imatinib, ketoconazol, nefazodon, quinupristin/dalfopristin, telithromycin) | Tăng nguy cơ đau cơ, tiêu cơ vân cấp | Các thuốc ức chế CYP 3A4 có thể làm tăng nồng độ statin trong máu do ức chế chuyển hóa statin | Xem xét pravasatin hoặc giảm liều statin nếu phối hợp; giám sát nồng độ CK và dấu hiệu, triệu chứng đau cơ |
| Warfarin – Acetaminophen | Tăng hiệu quả chống đông của warfarin phụ thuộc vào liều paracetamol Sự tương tác có thể không có ý nghĩa trên lâm sàng nếu dùng acetaminophen liều thấp, hoặc sử dụng không thường xuyên (không quá 6 viên paracetamol 325 mg tuần) | Paracetamol hoặc chất chuyển hóa làm tăng hoạt tính đối kháng vitamin K | Hạn chế sử dụng paracetamol; theo dõi các thông số đông máu 1-2 lần tuần khi bắt đầu hoặc ngừng sử dụng paracetamol, đặc biệt là nếu dùng trên 2,275g acetaminophen mỗi tuần Khi cần thiết có thể cần chỉnh liều warfarin |
| Warfarin – Alopurinol | Allopurinol làm tăng hoạt tính chống đông của một số thuốc chống đông uống, nhưng không rõ là có warfarin hay không | Alopurinol ức chế sự chuyển hóa ở gan | Sự tương tác không đoán trước được, cần theo dõi các thông số chống đông và điều chỉnh liều thuốc chống đông khi cần |
| Warfarin – Amiodaron | Tăng hiệu quả chống đông của warfarin | Amiodaron ức chế sự chuyển hóa qua CYP1A2, CYP2C9 của R- Warfarin và S- Warfarin | Theo dõi chặt chẽ INR trong 6-8 tuần đầu tiên trị liệu với amiodaron
Ở những bệnh nhân dùng amiodaron ở liều duy trì 100, 200, 300 hoặc 400 mg/ngày thì cần giảm liều Warfarin tương ứng khoảng 25%, 30%, 35% hoặc % (thông thường, cần giảm 30%-50% liều) Hiệu quả này có thể tiếp tục kéo dài 1,5-4 tháng sau khi ngưng amiodaron nên cần tiếp tục điều chỉnh liều warfarin sau khi ngưng amiodaron |
| Warfarin – Diltiazem, nifedipin | Tăng nồng độ, hiệu quả warfarin | Ảnh hưởng lên CYP 1A2, 3A4 | Theo dõi chặt chẽ |
| Warfarin – Fenofibrat | Tăng tác dụng làm giảm prothrombin của warfarin Đã xảy ra trường hợp xuất huyết và tử vong Nồng độ warfarin trong máu không bị ảnh hưởng | Ảnh hưởng lên quá trình tổng hợp các yếu tố đông máu | Nếu bắt buộc phải sử dụng đồng thời hai thuốc này thì cần theo dõi thường xuyên INR khi bắt đầu hoặc ngưng dùng fenofibrat.
Chuẩn bị để điều chỉnh liều warfarin Hướng dẫn bệnh nhân cần báo cáo ngay lập tức cho nhân viên y tế khi bị chảy máu bất thường hoặc bầm tím |
| Warfarin – Ginkgo biloba | Tăng nguy cơ xuất huyết | Có thể do hiệp lực hiệu quả chống đông | Căn dặn bệnh nhân tránh sử dụng đồng thời hai thuốc trên vì nguy cơ chảy máu có thể đe dọa tính mạng Căn dặn bệnh nhân khi đang dùng warfarin thì không được tùy ý sử dụng bất kỳ thực phẩm chức năng, thảo dược nào mà chưa có sự tham khảo ý kiến của nhân viên y tế; đồng thời hướng dẫn bệnh nhân cách theo dõi để báo cáo kịp thời các dấu hiệu xuất hướng, bầm tím bất thường |
| Warfarin – Glucosamin + chondroitin | Tăng nguy cơ xuất huyết | Tác dụng phụ có thể khi dùng warfarin với liều cao glucosamin- chondroitin | Nếu bắt buộc phải sử dụng đồng thời warfarin và glucosamin- chondroitin thì cần theo dõi chặt chẽ INR để chỉnh liều warfarin khi bắt đầu hoặc khi ngưng sử dụng glucosamin-chondroitin
Căn dặn bệnh nhân khi đang dùng warfarin thì không được tùy ý sử dụng bất kỳ thực phẩm chức năng, thảo dược nào mà chưa có sự tham khảo ý kiến của nhân viên y tế; đồng thời hướng dẫn bệnh nhân cách theo dõi để báo cáo kịp thời các dấu hiệu xuất hướng, bầm tím bất thường |
| Warfarin – Statin (rosuvastatin, simvastatin) | Tăng hiệu quả chống đông của warfarin | Giảm sự thải trừ S-Warfarin qua CYP2C9, R-Warfarin qua CYP3A4 | Theo dõi các thông số về hoạt tính chống đông khi bắt đầu hoặc ngừng dùng chung với statin. Atorvastatin, pravastatin không có dữ liệu cho thấy có tương tác với warfarin |
| Warfarin – Spironolacton | Hiệu quả làm giảm prothrombin máu của warfarin có thể bị giảm | Spironolacton gây lợi tiểu, làm tăng nồng độ các chất chống đông | Theo dõi các thông số chống đông để điều chỉnh liều warfarin (Có thể tăng liều warfarin) |
| Warfarin – Meloxicam | Tăng hiệu quả chống đông của warfarin | Hiệp đồng hoạt tính chống đông | Thận trọng, theo dõi chặt chẽ |
| Warfarin – Tramadol | Tăng hiệu quả chống đông của warfarin | Chưa rõ | Theo dõi các thông số chống đông khi bắt đầu hoặc ngưng sử dụng tramadol; có thể cần điều chỉnh liều warfarin |
Phụ lục 3.6. Đánh giá nguy cơ tim mạch của bệnh nhân
ĐÁNH GIÁ NGUY CƠ TIM MẠCH
- Đánh giá nguy cơ tim mạch theo thang điểm SCORE
Thang điểm SCORE dự báo tỷ lệ mắc bệnh tim mạch gây tử vong trong 10 năm. Thang điểm được trình bày dạng biểu đồ màu, có 2 biểu đồ riêng cho nhóm các nước nguy cơ cao (chủ yếu là các nước Tây Âu) và nhóm các nước nguy cơ thấp (chủ yếu là các nước Đông Âu). Tại Việt Nam, chúng ta sử dụng biểu đồ cho nhóm các nước nguy cơ thấp.
Ngoài ra, thang điểm SCORE của bệnh nhân có thể tính trực tiếp từ trang web: https://heartscore.escardio.org/2012/calc.aspx?model=europelow
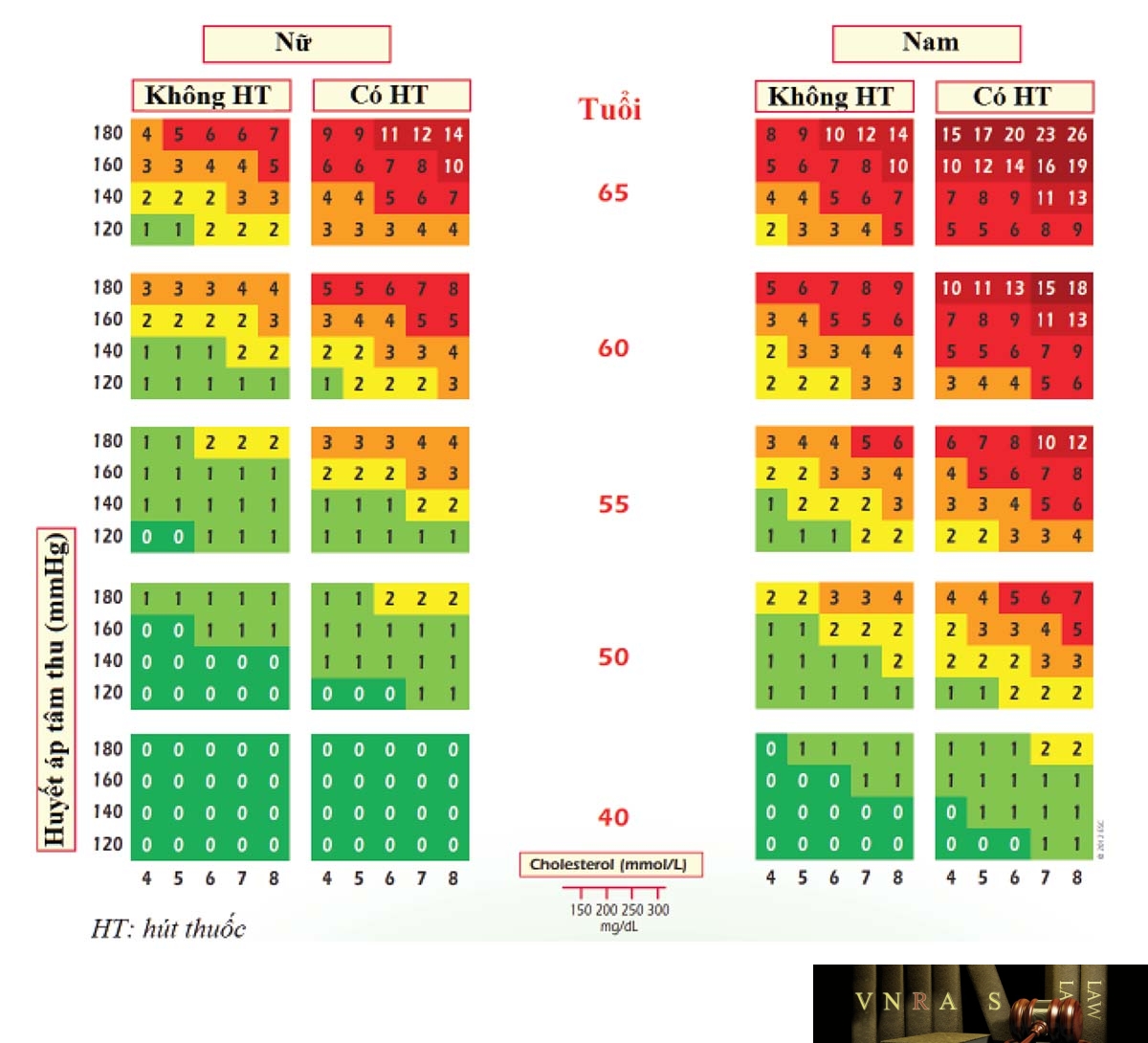
2. Phân tầng nguy cơ tim mạch theo Khuyến cáo chẩn đoán và điều trị tăng huyết áp 2018 của Hội Tim mạch Việt Nam
| Nguy cơ tim mạch | Bệnh nhân |
| Nguy cơ rất cao | Bao gồm các đối tượng có bất kỳ một hoặc những yếu tố nguy cơ sau:
– BTM đã được chẩn đoán xác định bằng các thăm dò xâm lấn hoặc không xâm lấn (như chụp mạch vành, xạ hình tưới máu cơ tim, siêu âm tim gắng sức, mảng xơ vữa động mạch cảnh trên siêu âm), tiền sử NMCT, hội chứng mạch vành cấp, can thiệp mạch vành qua da, phẫu thuật bắc cầu nối chủ – vành và các thủ thuật can thiệp động mạch khác, đột quỵ do thiếu máu cục bộ, bệnh động mạch ngoại biên. – Bệnh nhân ĐTĐ týp 2 hoặc ĐTĐ týp 1 có tổn thương cơ quan đích (Ví dụ: Albumin niệu vi thể). – Bệnh nhân BTM mức độ trung bình-nặng (MLCT < 60 mL/phút/1,73 m2). – Điểm SCORE ≥ 10 % . |
| Nguy cơ cao | Bao gồm các đối tượng có bất kỳ một hoặc những yếu tố nguy cơ sau:
– Có yếu tố nguy cơ đơn độc cao rõ rệt như rối loạn lipid máu có tính gia đình hay tăng HA nặng. – Điểm SCORE ≥ 5% và < 1 0 % . |
| Nguy cơ trung bình | – Điểm SCORE ≥ 1 % và < 5% |
| Nguy cơ thấp | – Điểm SCORE < 1%. |
Phụ lục 3.7. Thẩm định y lệnh các thuốc điều trị rung nhĩ
PHIẾU ĐÁNH GIÁ SỬ DỤNG THUỐC AMIODARON TRONG CHUYỂN NHỊP BẰNG THUỐC
(Amiodaron là lựa chọn hàng 2, các thuốc chống loạn nhịp khác như: flecainid, dofetilid, propafenon, ibutilid hiện không cung ứng được)
| THÔNG TIN BỆNH NHÂN Họ tên: …………Năm sinh:……….. Giới tính:………….. Chẩn đoán: …………………………………………………………………… |
DSLS:……………………………………………………………………… Ngày thẩm định y lệnh: ……………………………………………… |
||||||||||||
| CHỐNG CHỈ ĐỊNH 1. Sốc tim 2. Suy nút xoang nặng dẫn đến nhịp chậm xoang và blốc xoang nhĩ, blốc nhĩ thất độ II và III, blốc nhánh 3. Chậm nhịp từng cơn gây ngất 4. Bệnh tuyến giáp 5. Hạ HA động mạch 6. Mẫn cảm với các thành phần của thuốc 7. PNCT ở 3 tháng thứ 2 và thứ 3 thai kỳ (dùng khi không có thuốc khác) 8. PNCCB |
THẬN TRỌNG 1. Suy tim sung huyết 2. Suy gan 3. Hạ kali huyết 4. Rối loạn chức năng tuyến giáp 5. Giảm thị lực 6. Kết hợp với thuốc chẹn beta 7. Kết hợp với thuốc chẹn kênh canxi |
||||||||||||
LIỀU DÙNG (NGƯỜI LỚN) Phù hợp Không phù hợp
|
DUNG MÔI PHA TIÊM Phù hợp Không phù hợp Chỉ dùng dung dịch glucose 5% NỒNG ĐỘ PHA TIÊM Phù hợp Không phù hợp
|
PHIẾU ĐÁNH GIÁ SỬ DỤNG THUỐC AMIODARON DUY TRÌ SAU CHUYỂN NHỊP
(Amiodaron là lựa chọn hàng 2 nhưng các thuốc chống loạn nhịp khác như: flecainid, dofetilid, propafenon, ibutilid hiện không có nguồn
| THÔNG TIN BỆNH NHÂN Họ tên: …………Năm sinh:……….. Giới tính:………….. Chẩn đoán: …………………………………………………………………… |
DSLS:……………………………………………………………………… Ngày thẩm định y lệnh: ……………………………………………… |
||||
| ĐÁNH GIÁ TÍNH CẦN THIẾT CỦA VIỆC DUY TRÌ THUỐC CHỐNG LOẠN NHỊP SAU CHUYỂN NHỊP Không cần duy trì thuốc chống loạn nhịp sau chuyển nhịp nếu : 1. Rung nhĩ cơn đầu tiên không do bệnh van tim và được bác sĩ điều trị đánh giá có nguy cơ tái phát thấp 2. Nguyên nhân gây rung nhĩ thoáng qua, đã được giải quyết (nhồi máu cơ tim, viêm nội tâm mạc nhiễm trùng, điện giật, cường giáp đã điều trị, …) 3. Thời gian rung nhĩ tái phát xa (> 6 tháng hoặc năm), ít triệu chứng, tiền sử dễ chuyển nhịp |
|||||
| CHỐNG CHỈ ĐỊNH 1. Sốc tim 2. Suy nút xoang nặng dẫn đến nhịp chậm xoang và blốc xoang nhĩ, blốc nhĩ thất độ II và III, blốc nhánh 3. Chậm nhịp từng cơn gây ngất 4. Bệnh tuyến giáp 5. Hạ HA động mạch 6. Mẫn cảm với các thành phần của thuốc 7. PNCT ở 3 tháng thứ 2 và thứ 3 thai kỳ (dùng khi không có thuốc khác) 8. PNCCB |
THẬN TRỌNG 1. Suy tim sung huyết 2. Suy gan 3. Hạ kali huyết 4. Rối loạn chức năng tuyến giáp 5. Giảm thị lực 6. Kết hợp với thuốc chẹn beta 7. Kết hợp với thuốc chẹn kênh canxi |
||||
LIỀU DÙNG (NGƯỜI LỚN) Phù hợp Không phù hợp
|
|||||
PHIẾU ĐÁNH GIÁ SỬ DỤNG THUỐC KHÁNG ĐÔNG QUANH CHUYỂN NHỊP ĐỂ PHÒNG NGỪA HUYẾT KHỐI THUYÊN TẮC
| THÔNG TIN BỆNH NHÂN Họ tên: …………Năm sinh:……….. Giới tính:………….. Chẩn đoán: …………………………………………………………………… |
DSLS:……………………………………………………………………… Ngày thẩm định y lệnh: ……………………………………………… |
||||||||||||||||||||||||||||||
ĐÁNH GIÁ CHỈ ĐỊNH THUỐC KHÁNG ĐÔNG VỀ: SỰ CẦN THIẾT – THỜI GIAN – LOẠI THUỐC
|
|||||||||||||||||||||||||||||||
ĐÁNH GIÁ CHỈ ĐỊNH THUỐC KHÁNG ĐÔNG VỀ: LIỀU DÙNG
|
|||||||||||||||||||||||||||||||
PHIẾU ĐÁNH GIÁ SỬ DỤNG THUỐC TRONG KIỂM SOÁT TẦN SỐ THẤT
| THÔNG TIN BỆNH NHÂN Họ tên: …………Năm sinh:……….. Giới tính:………….. Chẩn đoán: …………………………………………………………………… |
DSLS:……………………………………………………………………… Ngày thẩm định y lệnh: ……………………………………………… |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
CHỈ ĐỊNH LOẠI THUỐC PHÙ HỢP VỚI TÌNH TRẠNG BỆNH LÝ MẮC KÈM
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
KHÔNG VI PHẠM CHỐNG CHỈ ĐỊNH & PHÙ HỢP VỀ LIỀU
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
PHIẾU ĐÁNH GIÁ SỬ DỤNG THUỐC KHÁNG ĐÔNG
PHÒNG NGỪA ĐỘT QUỴ VÀ THUYÊN TẮC MẠCH HỆ THỐNG
| THÔNG TIN BỆNH NHÂN Họ tên: …………Năm sinh:……….. Giới tính:………….. Chẩn đoán: …………………………………………………………………… |
DSLS:……………………………………………………………………… Ngày thẩm định y lệnh: ……………………………………………… |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
ĐÁNH GIÁ CHỈ ĐỊNH THUỐC KHÁNG ĐÔNG VỀ: SỰ CẦN THIẾT – THỜI GIAN – LOẠI THUỐC
NHẬN DIỆN CÁC YẾU TỐ NGUY CƠ GÂY XUẤT HUYẾT CÓ THỂ ĐẢO NGƯỢC:…………………………………………………………………………………………………. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
ĐÁNH GIÁ CHỈ ĐỊNH THUỐC KHÁNG ĐÔNG VỀ: LIỀU DÙNG
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Phụ lục 3.8. Liều warfarin trên bệnh nhân rung nhĩ
| Ngày | INR | Liều hàng ngày |
| 1-3 | Không cần | 5mg
2,5mg nếu suy yếu, bệnh gan, suy dinh dưỡng, dùng chung với các loại thuốc tăng cường hoạt tính wafarin, người châu Á 5-7,5mg ở bệnh nhân tr , khỏe mạnh |
| 3 hoặc 4 | 1,0-1,3 | 7,5mg |
| 1,4-1,5 | 5mg | |
| 1,6-1,8 | 5/2,5mg xen kẽ | |
| > 1,9 | 2,5mg | |
| ≥ 2,0 | Ngưng 1 ngày, sau đó 2,5mg (kiểm tra INR thường xuyên hơn) | |
| 7 và 10 | ≤ 1 ,5 | Tăng 15% liều trung bình mỗi ngày |
| 1,6-1,9 | Tăng 10 % liều trung bình mỗi ngày | |
| 2,0-3,0 | Không thay đổi | |
| 3,1-3,5 | Giảm 10% liều trung bình mỗi ngày | |
| 3,6-4,0 | Giảm 15% liều trung bình mỗi ngày | |
| > 4,1 | Ngưng 1 ngày, sau đó giảm 15% hoặc hơn liều trung bình mỗi ngày (kiểm tra INR thường xuyên hơn) | |
| ≥ 6,0 | Xem xét dùng vitamin K (kiểm tra INR thường xuyên hơn) |
| INR đo được | Chỉnh liều thuốc | Theo dõi INR kế tiếp |
| < 2,0 | Tăng 10-15%
Tăng 15% nếu INR < 1,5 mà không tìm được nguyên nhân |
Trong vòng 1 tuần |
| 3,1-3,5 | Giảm 0-10% | Trong vòng 2 tuần |
| 3,6-4,0 | Ngưng 0-1 liều
Giảm 10-15% |
Trong vòng 1 tuần |
| 4,1-8,9 | Ngưng 0-2 liều
Giảm 10-15% Có thể uống vitamin K 2,5mg |
Trong vòng 2 ngày |
| > 9,0 | Ngưng 2 liều
Giảm 15-20% Uống vitamin K 2,5-5mg |
Sau 1 ngày |
Phụ lục 3.9. Phiếu thông tin dành cho bệnh nhân sử dụng thuốc kháng đông kháng vitamin K
- CÁCH CHIA THUỐC
Xem kỹ đơn thuốc trước khi uống vì liều thuốc chống đông kháng vitamin K có thể thay đổi theo ngày
2. QUÊN UỐNG THUỐC
|
√ – Có thể uống liều bị bỏ quên – Ghi lại việc bỏ quên này vào |
X – Nếu vượt quá 8 giờ, nên bỏ qua liều đã quên và dùng liều tiếp theo vào giờ dự kiến thông thường – KHÔNG dùng liều gấp đôi để bù liều đã quên |
3. THỂ THAO
|
√ Chơi các môn thể thao an toàn như |
X Không chơi các môn thể thao mạnh, đối |
4. LƯU Ý
|
√ – Nên dùng dao cạo điện, bàn chải đánh răng mềm, chỉ nha khoa để xỉa răng – Nên mang dép chống trượt ngã khi ở nhà, mang giày khi ra đường. – Mang bao tay, cẩn thận khi dùng vật sắc nhọn – Khi chấn thương, khám bệnh nơi khác phải báo cho nhân viên y tế biết mình đang uống thuốc kháng đông – Khi mang thai/dự định có thai phải báo ngay với bác sĩ vì thuốc có thể gây dị tật thai nhi |
X – Không tự ý dùng thêm bất kỳ loại thuốc giảm đau, dược liệu – Cẩn thận khi cắt móng tay, – Không leo trèo, đến những |
5. RƯỢU
√ Uống rượu quá nhiều có thể làm tăng INR và tăng nguy cơ chảy máu
X Có thể uống tối đa ly rượu mỗi ngày nếu thường xuyên uống rượu và tối đa -2 ly nhỏ trong dịp đặc biệt
6. THỨC ĂN
X Ăn quá nhiều thực phẩm có chứa nhiều vitamin K có thể làm giảm tác dụng của thuốc chống đông
√ Vẫn có thể ăn thức ăn có vitamin K với chế độ ăn ổn định, ít thay đổi

7. DẤU HIỆU QUÁ LIỀU THUỐC KHÁNG ĐÔNG
| Chảy máu nhẹ | Chảy máu nặng |
| – Chảy máu lợi khi đánh răng – Thỉnh thoảng chảy máu mũi – Dễ bị bầm tím trên da – Chảy máu lâu không cầm sau khi bị rách da nhẹ – Kinh nguyệt kéo dài-> Gọi điện bác sĩ hoặc tái khám để theo dõi ngay |
– Chảy máu lợi, mũi thường xuyên – Bầm tím mà không rõ nguyên nhân – Nôn/ho ra máu – Phân đỏ hoặc đen như bã cafe – Nước tiểu đỏ hoặc nâu đậm – Nhức đầu hoặc đau bụng nhiều – Khi bị ngã gây chấn thương nặng hoặc chấn thương vùng đầu do tai nạn-> Nhập viện cấp cứu ngay |
Phụ lục 3.10. Chuyển đổi giữa các thuốc kháng đông
| Chống đông đang dùng | Chống đông chuyển sang | Cách chuyển đổi |
| Thuốc kháng vitamin K (INR 2 – 3) | Dabigatran | Ngưng thuốc kháng vitamin K và bắt đầu dabigatran khi INR < 2 |
| Thuốc kháng vitamin K (INR 2 – 3) | Rivaroxaban | Ngưng thuốc kháng vitamin K và bắt đầu rivaroxaban khi INR < 3 |
| Rivaroxaban | ThuốcKVK (INR 2- 3) | Tiếp tục rivaroxaban đồng thời với thuốc kháng vitamin K cho đến khi INR ≥ 2 , sau đó ngưng rivaroxaban |
| Dabigatran | Thuốc KVK (INR 2 – 3) | ClCr ≥ 50 mL/phút: bắt đầu dùng thuốc kháng vitamin K 3 ngày trước khi ngưng dabigatran
30 ≤ ClCr ≤ 50 mL/phút: bắt đầu dùng thuốc KVK 2 ngày trước khi ngưng dabigatran |
| Heparin không phân đoạn hoặc trọng lượng phân tử thấp | Dabigatran | Bắt đầu dabigatran 0 – 2 giờ trước liều heparin trọng lượng phân tử thấp cuối, hoặc vào cùng thời điểm ngưng heparin không phân đoạn truyền tĩnh mạch |
| Heparin không phân đoạn hoặc trọng lượng phân tử thấp | Rivaroxaban | Ngưng heparin và khởi đầu rivaroxaban 0 – 2 giờ trước liều heparin trọng lượng phân tử thấp dự kiến tiếp theo hoặc vào cùng thời điểm ngưng heparin không phân đoạn truyền tĩnh mạch. |
| Dabigatran | Heparin không phân đoạn hoặc trọng lượng phân tử thấp | ClCr ≥ 30 mL/ phút: bắt đầu 12 giờ sau liều cuối cùng của dabigatran
ClCr < 30 mL/phút: bắt đầu 24 giờ sau liều cuối cùng của dabigatran |
| Rivaroxaban | Heparin không phân đoạn hoặc trọng lượng phân tử thấp | Ngưng rivaroxaban và bắt đầu liều đầu tiên của heparin không phân đoạn hoặc trọng lượng phân tử thấp vào thời điểm dùng liều rivaroxaban tiếp theo |
Chương 4. THỰC HÀNH DƯỢC LÂM SÀNG TRONG
CHUYÊN NGÀNH UNG THƯ
1. ĐẠI CƯƠNG VỀ BỆNH HỌC UNG THƯ VÀ CÁC PHƯƠNG PHÁP ĐIỀU TRỊ
1.1 Các phương pháp điều trị bệnh ung thư
Ung thư là một nhóm bệnh lý phức tạp, đa dạng về nguyên nhân, biểu hiện lâm sàng và tiến triển. Đây là một bệnh lý ác tính tế bào, trong đó các tế bào phân chia vô hạn độ, không theo sự kiểm soát của cơ thể, không chết theo chương trình, các tế bào ung thư xâm lấn phá hủy tổ chức xung quanh và di căn xa.
Trong những năm gần đây, tỷ lệ người mới mắc và chết do ung thư có xu hướng ngày càng tăng ở hầu hết các quốc gia trên thế giới, nhất là ở các nước nghèo, các nước đang phát triển, trong đó có Việt Nam. Chẩn đoán và điều trị ung thư ở mỗi quốc gia ngày càng được quan tâm, nhiều phương pháp mới, hiện đại đã ra đời và mang lại kết quả khả quan. Tại các nước phát triển, khoảng 70% người bệnh ung thư tránh được tử vong nhờ các tiến bộ của y học trong việc phát hiện sớm và điều trị. Đặc biệt một số loại như: ung thư tuyến giáp, vú, cổ tử cung, vòm mũi họng, đại trực tràng, tuyến tiền liệt,… tỷ lệ chữa khỏi đạt trên 80%.
Tại Việt Nam, theo đánh giá của Cơ quan nghiên cứu ung thư quốc tế (The International Agency for Research on Cancer – IARC), tỷ lệ chữa khỏi bệnh ung thư đạt 40%. Tỷ lệ này chưa được như mong muốn, lý do chủ yếu là phần lớn bệnh nhân ung thư ở nước ta đến khám và điều trị khi bệnh đã ở giai đoạn muộn. Theo Globocan 2018, hàng năm ở Việt Nam có 164.671 trường hợp ung thư mới mắc và 111.874 trường hợp tử vong. Tính chung cả hai giới nam và nữ thì các bệnh ung thư hay gặp là: ung thư gan, phổi, dạ dày, vú, đại trực tràng. Năm loại bệnh ung thư hay gặp ở nam giới là: ung thư gan, phổi, dạ dày, đại trực tràng, vòm mũi họng. Năm loại bệnh ung thư hay gặp ở nữ giới là: ung thư vú, đại trực tràng, phổi, dạ dày, gan.
Hiện nay, việc phòng chống ung thư đi vào ba hướng chính: phòng bệnh, ứng dụng các tiến bộ trong sàng lọc, chẩn đoán, phát hiện sớm bệnh và ứng dụng các tiến bộ trong điều trị ung thư. Việc điều trị ung thư dựa vào nhiều yếu tố như: cơ quan, vị trí bị ung thư, giai đoạn bệnh, thể mô bệnh học, các dấu ấn sinh học phân tử, xét nghiệm gen.cũng như thể trạng của bệnh nhân. Phát hiện sớm, chẩn đoán đúng giai đoạn bệnh, lựa chọn phương pháp điều trị hợp lý có ý nghĩa quan trọng để đem lại hiệu quả điều trị cao cho người bệnh. Việc chẩn đoán dựa vào các triệu chứng lâm sàng, cận lâm sàng như: chẩn đoán hình ảnh, nội soi, sinh hóa, mô bệnh học, y học hạt nhân, sinh học phân tử,… Trong đó, mô bệnh học đóng vai trò quyết định trong chẩn đoán xác định.
Đặc tính chung của bệnh ung thư là phát triển tại chỗ, xâm lấn tổ chức xung quanh, di căn theo đường bạch huyết và di căn xa qua đường máu tới các cơ quan khác. Chính vì vậy, điều trị bệnh ung thư tùy theo loại, giai đoạn bệnh, mô bệnh học, thể trạng người bệnh,.mà cần điều trị một hoặc phối hợp nhiều phương pháp trong đó phẫu thuật là phương pháp điều trị tại chỗ; xạ trị là phương pháp điều trị tại vùng; hóa chất, nội tiết, điều trị đích, miễn dịch là phương pháp điều trị toàn thân.
Người bệnh ung thư khi bị bệnh thường có tâm lý hoang mang, lo lắng về bệnh, thậm chí một số trường hợp có biểu hiện trầm cảm. Bệnh ung thư giai đoạn muộn thường khiến người bệnh suy kiệt do các tế bào ung thư tăng sinh, nhân lên, xâm lấn, di căn. Do đó, ngoài việc điều trị bệnh ung thư, việc điều trị tâm lý và dinh dưỡng cũng cần được lưu ý. Hơn nữa, người bệnh ung thư đa số trên 50 tuổi, một số mắc các bệnh lý phối hợp, việc lựa chọn các thuốc điều trị nhằm mang lại hiệu quả cao, ít tác dụng phụ, ít có sự tương tác thuốc rất quan trọng.
Do vậy, trong điều trị bệnh nhân ung thư cần có sự phối hợp của các chuyên gia y tế trong nhiều lĩnh vực khác nhau: bác sĩ nội khoa ung bướu, bác sĩ xạ trị ung bướu, phẫu thuật viên, bác sĩ giải phẫu bệnh, chẩn đoán hình ảnh, y học hạt nhân, bác sĩ dinh dưỡng, bác sĩ tâm lý, DSLS, điều dưỡng chuyên ngành ung bướu. Hiện nay, tại một số bệnh viện nước ta đã thành lập các nhóm hội chẩn ung bướu đa chuyên khoa (Multidisciplinary tumour board) để đưa ra chẩn đoán và lựa chọn phương pháp điều trị, chăm sóc tối ưu nhất cho từng người bệnh ung thư mang lại hiệu quả.
1.1.1 Các phương pháp điều trị tại chỗ
Phẫu thuật
Phẫu thuật là phương pháp điều trị cơ bản, cho phép loại bỏ tổ chức ung thư, tuy nhiên chỉ thực hiện triệt để khi bệnh ở giai đoạn sớm, tổ chức khối u còn khu trú. Xu hướng hiện nay là tăng cường phẫu thuật bảo tồn u tối đa và phối hợp với các phương pháp điều trị khác (xạ trị, hóa trị, nội tiết, đích, miễn dịch) nhằm nâng cao chất lượng sống cho bệnh nhân.
Các phương pháp phẫu thuật:
Phẫu thuật dự phòng bệnh ung thư là phẫu thuật cắt bỏ những thương tổn tiền ung thư, góp phần tích cực làm hạ thấp tỷ lệ mắc bệnh. Những phẫu thuật dự phòng có thể áp dụng như: cắt bao quy đầu giúp phòng ngừa ung thư dương vật, cắt polyp đại trực tràng giúp phòng tránh ung thư đại trực tràng.
Phẫu thuật chẩn đoán bệnh ung thư: nhằm lấy tổ chức ung thư làm xét nghiệm mô bệnh học, bao gồm nhiều phương pháp khác nhau như phẫu thuật lấy một phần khối u, phẫu thuật lấy hạch.
Phẫu thuật điều trị bệnh ung thư: có hai chỉ định chính là điều trị phẫu thuật triệt căn và phẫu thuật tạm thời.
– Phẫu thuật triệt căn trong ung thư: là phẫu thuật cắt bỏ rộng rãi khối u nguyên phát, các tổ chức lân cận, nạo vét hạch vùng để đảm bảo không còn tế bào ung thư; có thể phẫu thuật đơn thuần (với những trường hợp bệnh ở giai đoạn sớm, khu trú, chưa di căn xa) hoặc phẫu thuật phối hợp với các phương pháp điều trị khác.
– Phẫu thuật tạm thời: là phẫu thuật với mục đích dự phòng hoặc giải quyết biến chứng do bệnh gây ra, chỉ định cho những trường hợp bệnh ở giai đoạn muộn, tổn thương đã lan rộng.
Phẫu thuật tạo hình và phục hồi chức năng: như phẫu thuật tạo hình vú sau cắt tuyến vú để cải thiện chất lượng cuộc sống cho người phụ nữ.
Phẫu thuật điều trị nội tiết: phẫu thuật cắt buồng trứng trong ung thư vú, cắt tinh hoàn trong ung thư tuyến tiền liệt nhằm mục đích điều trị nội tiết.
Phẫu thuật trong trường hợp tái phát, di căn: tùy từng bệnh và vị trí di căn mà có các chỉ định phẫu thuật cụ thể.
Đốt sóng cao tần
Đốt sóng cao tần (Radiofrequency ablation – RFA) là phương pháp phá hủy nhu mô khối u bằng nhiệt của dòng điện dao động với tần số 200-1200 kHz. Người ta đặt một điện cực ở trung tâm khối u và duy trì nhiệt độ phá hủy từ 60 -100°C. Dòng điện từ máy được truyền vào khối u qua một điện cực dạng kim (needle electrode), dòng sóng radio được truyền vào đầu kim và sinh nhiệt. Nhiệt do ma sát làm khô mô xung quanh dẫn đến làm mất nước trong tế bào và hoại tử đông khối u.

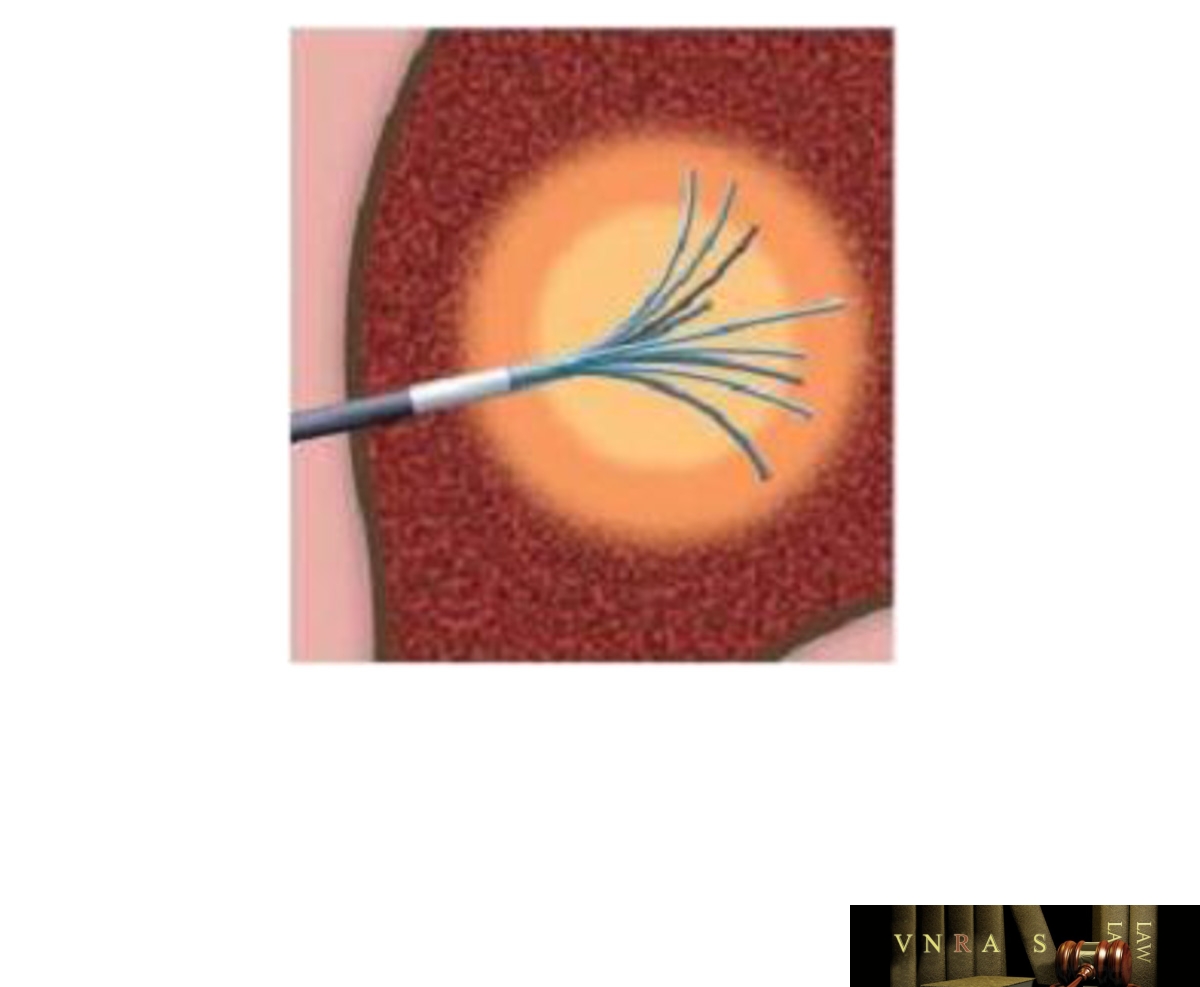
Đốt sóng cao tần được chỉ định cho một số bệnh ung thư như: ung thư gan, ung thư tuyến giáp giai đoạn sớm, các khối u di căn…, có thể kết hợp với phương pháp khác để tăng hiệu quả điều trị.
Nút mạch hóa chất
Nút mạch là đưa vật liệu tắc mạch vào trong động mạch cấp máu cho khối u. Nút mạch hoá chất là vừa nút mạch, vừa đưa hóa chất vào khối u. Do đó, khối u sẽ bị tiêu diệt theo hai cơ chế: thứ nhất, hóa chất được tập trung với nồng độ cao được bơm trực tiếp vào khối u mà không đi qua tuần hoàn của cơ thể nên có tác dụng tại chỗ tốt; ít tác dụng phụ toàn thân. Thứ hai, chất tắc mạch sẽ làm ngăn chặn dòng máu đến nuôi u, làm cho khối u thiếu máu, ngăn cản phát triển khối u. Nút mạch hóa chất thường được áp dụng trong điều trị ung thư gan.
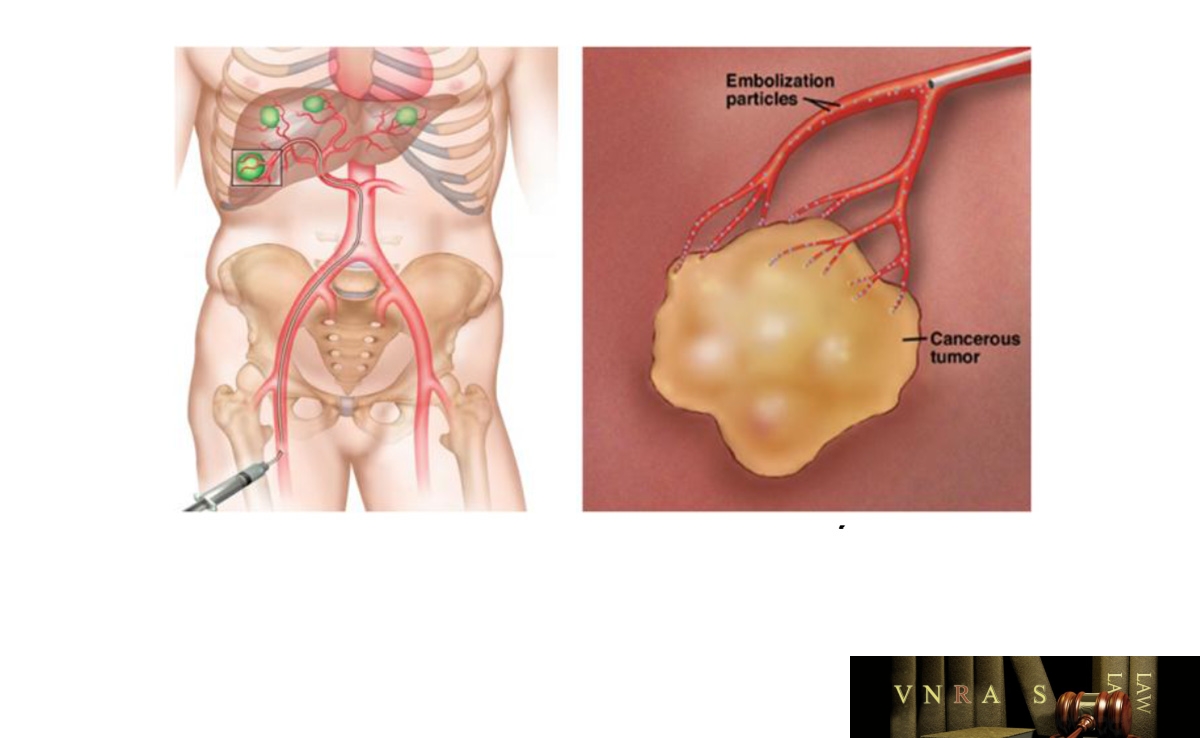
Xạ trị
Xạ trị cũng là một trong các phương pháp cơ bản điều trị bệnh ung thư, phương pháp này sử dụng các tia bức xạ ion hóa có năng lượng cao để tiêu diệt tế bào ung thư. Xạ trị bao gồm: xạ trị chiếu ngoài (Teletherapy, External Beam Radiotherapy – EBRT), xạ trị áp sát (brachytherapy), xạ trị chiếu trong bằng đồng vị phóng xạ hay còn gọi là xạ trị nguồn hở (unsealed source radiotherapy), cấy hạt phóng xạ là sự phối hợp giữa xạ trị áp sát và xạ trị chiếu trong.
❖ Xạ trị chiếu ngoài:
Xạ trị chiếu ngoài: nguồn phát bức xạ từ ngoài cơ thể, đây là phương pháp sử dụng các nguồn bức xạ ion hóa, hội tụ tại khối u và hạch vùng nhằm tiêu diệt tổ chức ung thư nhưng vẫn đảm bảo an toàn cho cơ quan lành xung quanh. Trong những năm gần đây, có nhiều tiến bộ về phương pháp xạ trị chiếu ngoài đó là các kỹ thuật mới như: xạ trị điều biến liều (Intensity Modulated Radiation Therapy – IMRT), xạ trị điều biến thể tích (Volumetric Arc Therapy – VMAT), xạ trị hạt nặng, xạ trị proton, xạ phẫu (radiosurgery), xạ trị định vị thân (Stereotactic Body Radiation Therapy – SBRT), xạ trị với PET/CT mô phỏng nhằm nâng cao liều bức xạ vào khối u và giảm liều bức xạ đến tổ chức lành xung quanh.
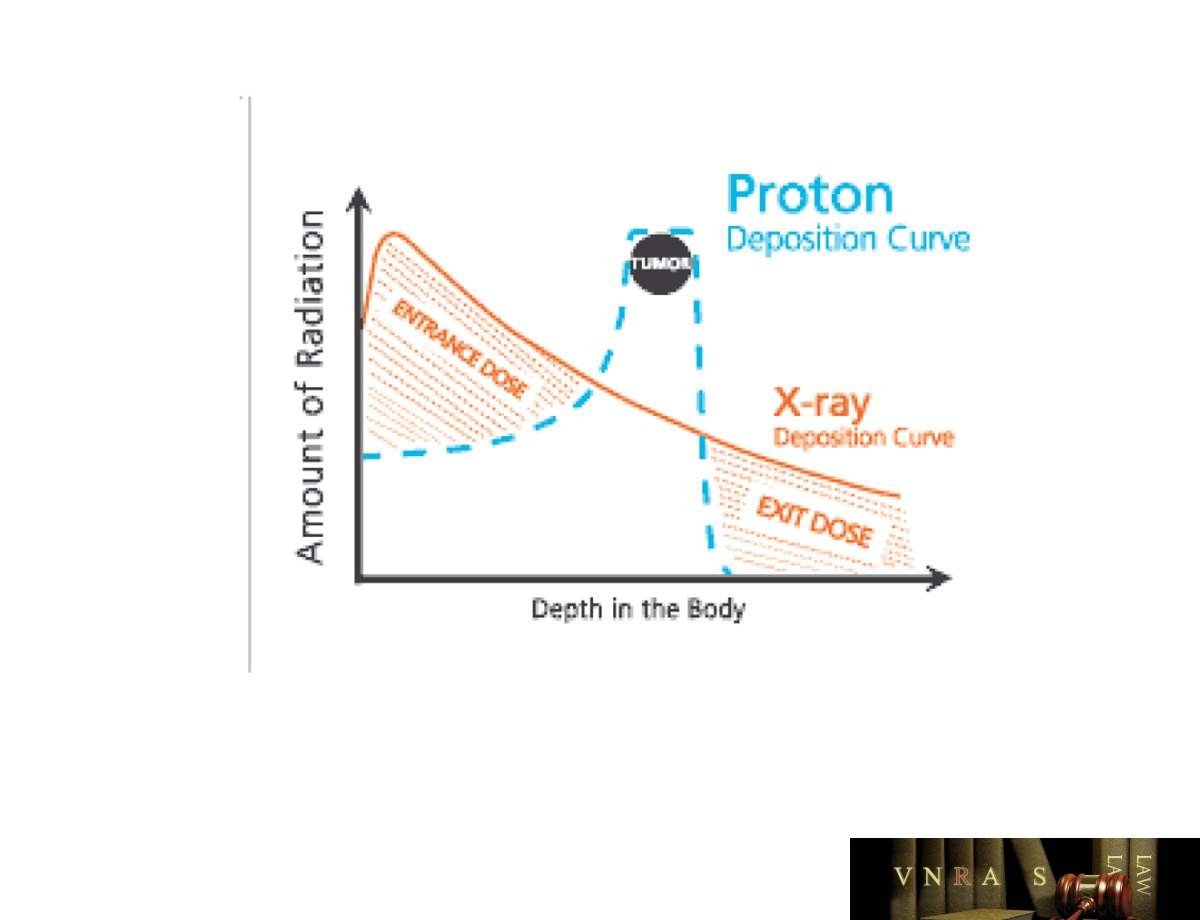
Xạ trị photon (đường da cam, nét liền): Liều lượng bức xạ giảm dần trên đường đi, tổ chức lành trước và sau khối u đều chịu liều bức xạ lớn, biến chứng do xạ trị nhiều, phải sử dụng nhiều trường chiếu hội tụ tại khối u.
Xạ trị proton (đường xanh nét đứt): Liều lượng bức xạ đạt mức tối đa khi đến khối u (điều chỉnh theo mức năng lượng), liều bức xạ trước khối u rất thấp và liều bức xạ sau khối u hầu như không có, do vậy rất ít biến chứng do xạ trị.
Xạ phẫu, đặc biệt kỹ thuật xạ phẫu bằng dao gamma quay là một phương pháp xạ trị đặc biệt, trong đó các nguồn bức xạ quay xung quanh đầu bệnh nhân, hội tụ năng lượng rất lớn tại khối u, độ chính xác cao, gây hủy hoại khối u nhưng rất ít độc tính cho tổ chức lành xung quanh do liều bức xạ tại tổ chức lành rất thấp.
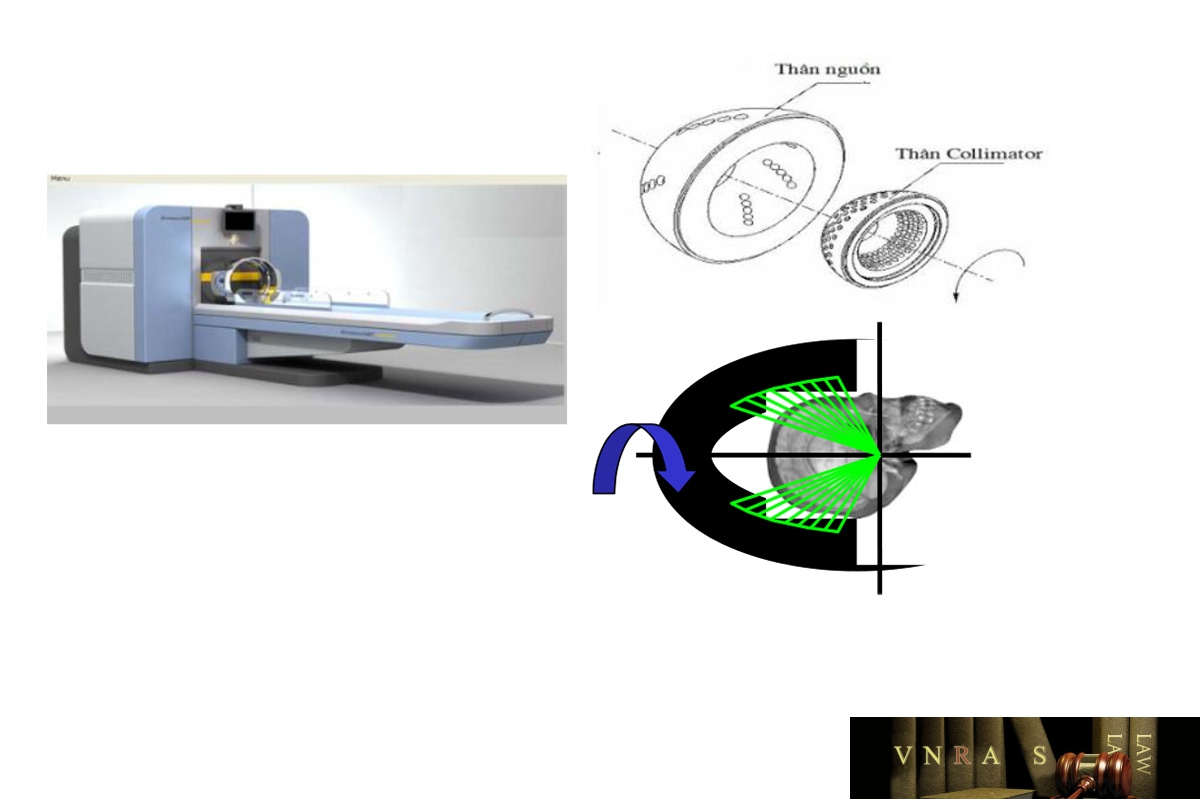

❖ Xạ trị áp sát:
Xạ trị áp sát: các nguồn xạ được đặt áp sát hoặc cắm trực tiếp vào trong vùng tổn thương hoặc đưa vào các khoang trong cơ thể. Ưu điểm của xạ trị áp sát là nâng liều bức xạ vào vị trí tổn thương ung thư (khối u, hạch) lên cao và hạn chế liều bức xạ vào các tổ chức lành xung quanh.
❖ Xạ trị chiếu trong:
Xạ trị chiếu trong: đưa nguồn xạ vào trong mô, tạng bên trong cơ thể qua đường uống, tiêm, truyền tĩnh mạch. Đây là phương pháp xạ trị mà thuốc phóng xạ tập trung vào đích là các tế bào ung thư và ít ảnh hưởng đến cơ quan lành xung quanh. Ví dụ: 131I trong điều trị ung thư tuyến giáp, 32P, 89Sr, 188Re trong điều trị giảm đau ung thư di căn xương
Phương pháp xạ trị trong chọn lọc (Selective Internal Radiation Therapy – SIRT), hay tắc mạch phóng xạ (Radio Embolization – RE) là kỹ thuật sử dụng hạt vi cầu phóng xạ Yttrium-90 (90Y) đưa vào động mạch nuôi khối u gan. Tia beta do 90Y phát ra tại chỗ sẽ tiêu diệt tế bào u mà không hoặc ít ảnh hưởng tới tổ chức lành xung quanh. Phương pháp này được áp dụng trong điều trị ung thư gan nguyên phát hoặc ung thư di căn gan.
Cấy hạt phóng xạ điều trị ung thư tuyến tiền liệt: các hạt phóng xạ (125I hoặc 103Pd) có kích thước nhỏ được cấy trực tiếp vào tuyến tiền liệt, nên các tế bào ung thư sẽ nhận được liều bức xạ cao nhất và giảm thiểu tối đa liều bức xạ tới các cơ quan lành xung quanh. Đây là phương pháp phối hợp giữa xạ trị áp sát và xạ trị chiếu trong.
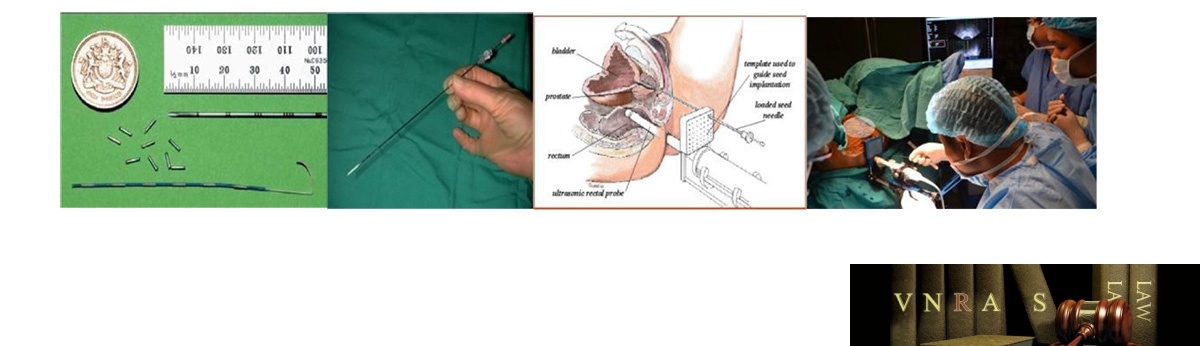
Miễn dịch phóng xạ (radioimmunotherapy – RIT) là phương pháp sử dụng kháng thể đơn dòng đã được đánh dấu đồng vị phóng xạ phát tia beta hoặc alpha để gắn đặc hiệu vào kháng nguyên (nằm trên bề mặt tế bào ung thư). Các đồng vị phóng xạ có mức năng lượng bức xạ thấp và khả năng đâm xuyên ngắn (vài milimet trong tổ chức) nên các tế bào ung thư được nhận liều bức xạ cao nhất và bảo vệ tối đa các tế bào lành xung quanh. Đây là phương pháp phối hợp xạ trị chiếu trong với kháng thể đơn dòng (điều trị toàn thân): ibritumomab tiuxetan gắn với 111In hoặc 90Y (Zevalin), tositumomab gắn với 131I (Bexxar), nimotuzumab gắn với 131I và 90 Y…
1.1.2 Các phương pháp điều trị toàn thân
Hóa trị
Hóa trị là phương pháp sử dụng các thuốc hóa chất dạng uống, tiêm, truyền để điều trị bệnh ung thư. Các thuốc hóa chất là các tác nhân kìm chế sự phát triển của khối u bằng cách can thiệp vào sự nhân lên của tế bào ung thư. Hóa trị phải được xem xét dựa trên các nguyên tắc sau: lựa chọn thuốc thích hợp cho mỗi tình huống lâm sàng cụ thể, cần nắm vững được dược động học, cơ chế tác dụng, liều lượng, cách dùng, tác dụng không mong muốn của từng thuốc; đảm bảo đúng liều và liệu trình điều trị; kết hợp các hóa chất có cơ chế tác dụng khác nhau. Cần theo dõi sát bệnh nhân trong và sau quá trình dùng hóa chất để phát hiện và xử lý kịp thời các tác dụng không mong muốn.
Các phương pháp hóa trị
– Hóa trị bổ trợ trước hay hóa trị tân bổ trợ: là phương pháp điều trị hóa trị trước một phương pháp điều trị chính khác, với mục đích làm giảm kích thước u, giảm giai đoạn bệnh.
– Hóa trị bổ trợ: là sử dụng hóa chất sau khi đã điều trị triệt căn bằng các phương pháp điều trị khác (phẫu thuật, xạ trị). Hóa trị bổ trợ nhằm mục đích tiêu diệt các ổ vi di căn, làm giảm nguy cơ tái phát, tăng thời gian sống của bệnh nhân. Phác đồ hóa trị có thể kết hợp với các thuốc điều trị đích (trastuzumab, bevacizumab…).
– Hóa trị điều trị bệnh ở giai đoạn di căn, lan tràn: nhằm mục đích giảm nhẹ triệu chứng và cải thiện chất lượng sống cho bệnh nhân. Hóa chất toàn thân hoặc tại chỗ: bơm hóa chất vào màng phổi hoặc màng bụng nhằm giảm tràn dịch màng phổi, màng bụng; nếu thể trạng bệnh nhân cho phép, xem xét khả năng hóa trị toàn thân.
Có nhiều nhóm thuốc hóa chất khác nhau, với các cơ chế tác động khác nhau vào chu trình tế bào, các thuốc hóa chất dùng đường toàn thân tiêu diệt tế bào ung thư đồng thời cũng ảnh hưởng đến các cơ quan lành, tuy nhiên các cơ quan lành sẽ hồi phục sau mỗi chu kỳ hóa trị.
Có nhiều phác đồ hóa trị khác nhau, các phác đồ này đều nhằm mục đích tiêu diệt các tế bào ung thư và giảm thiểu tác dụng không mong muốn đến các tế bào lành. Tùy từng loại bệnh ung thư, loại mô bệnh học, thể trạng người bệnh. mà bác sĩ sẽ lựa chọn phác đồ phù hợp cho người bệnh.
Ngoài hóa trị chuẩn thì hóa trị metronomic (sử dụng thuốc liều thấp thường xuyên trong thời gian dài mà không ngắt quãng) mang lại lợi ích rất tốt cho các bệnh nhân không phù hợp với hóa trị chuẩn.
Điều trị đích
Điều trị đích là dùng các chất để ngăn chặn sự phát triển của tế bào ung thư bằng cách tác động vào các phân tử đặc hiệu (các đích phân tử – molecular targets), cần thiết cho quá trình sinh ung thư và phát triển khối u. Điều trị đích có thể tác động vào các thụ thể nằm trên màng tế bào hoặc trong màng tế bào.
Có nhiều cách phân loại thuốc điều trị đích nhưng cách phân loại theo cơ chế tác động vào thụ thể bên ngoài và bên trong màng tế bào hay được sử dụng nhất. Với cách phân loại này, thuốc điều trị đích được chia làm hai loại kháng thể đơn dòng và thuốc có phân tử nhỏ.
– Các kháng thể đơn dòng (monoclonal antibody), tên gọi thường có đuôi là -mab, là kháng thể chỉ gắn với một loại kháng nguyên đặc hiệu ngoài màng tế bào (các kháng nguyên này thường đóng vai trò quan trọng dẫn truyền tín hiệu giúp khối u phát triển).
– Các thuốc loại phân tử nhỏ (small molecule inhibitor), tên gọi thường có đuôi là – ib, đa số là các chất ức chế kinase, tác động vào các con đường tín hiệu bên trong tế bào.
Chỉ định điều trị đích tùy thuộc loại bệnh ung thư, giai đoạn bệnh, các xét nghiệm sinh học phân tử (gen), mô bệnh học (hóa mô miễn dịch).
Điều trị nội tiết
Đây là phương pháp điều trị được áp dụng từ nhiều năm nay, là tiền thân của phương pháp điều trị đích. Phương pháp điều trị nội tiết có nhiều ưu điểm như: đơn giản, dễ thực hiện, ít tác dụng phụ so với các phương pháp điều trị khác. Một số bệnh ung thư được điều trị nội tiết hiện nay: ung thư vú, ung thư tuyến tiền liệt…
Điều trị miễn dịch
Điều trị miễn dịch (miễn dịch trị liệu) có thể được hiểu là phương pháp sử dụng một trong các thành phần của hệ thống miễn dịch của bệnh nhân để chống lại bệnh tật trong đó có bệnh ung thư. Phương pháp này được thực hiện theo hai cách chính: kích thích hệ thống miễn dịch làm việc “nhiều hơn” và “thông minh hơn” để tấn công lại các tế bào ung thư và bổ sung cho bệnh nhân thành phần trong hệ miễn dịch như tế bào miễn dịch, kháng thể.
Trong cơ thể bình thường, CTLA-4 và PD-1 là các điểm ức chế giúp tế bào T không tấn công các tế bào bình thường. Tuy nhiên, tế bào ung thư lại tạo ra các protein có khả năng gắn với “điểm ức chế” CTLA-4 và PD-1, làm cho tế bào T bị tê liệt, giúp các tế bào ung thư trốn thoát khỏi sự kiểm soát của hệ thống miễn dịch. Các nghiên cứu đã mở ra một hướng mới trong điều trị ung thư là sử dụng kháng thể đơn dòng giúp giải phóng các “điểm ức chế” CTLA-4 và PD-1, từ đó tế bào T có thể tiêu diệt các tế bào ung thư.
Ngoài ra, CAR-T (Chimeric Antigen Receptor T-cell) tế bào lympho T chứa thụ thể kháng nguyên dạng khảm cũng là một trong những phương pháp điều trị miễn dịch. Thụ thể là một phân tử protein nằm trên màng hay trong tế bào, nhận tín hiệu hoá học từ bên ngoài vào trong tế bào, tương tự vai trò “cánh tay” hay “đôi mắt” của tế bào lympho T. Kháng nguyên là một phân tử kích thích đáp ứng miễn dịch của cơ thể. Dạng khảm là dạng được lai từ ít nhất hai cá thể khác nhau.
CAR-T là dựa vào hệ miễn dịch để chống lại ung thư bằng cách nâng cao khả năng phát hiện và diệt trừ tế bào ung thư của những tế bào hệ miễn dịch. Các tế bào ung thư giả dạng là tế bào lành (bình thường) nên các tế bào T bỏ sót, không nhận diện được tế bào lạ cần tiêu diệt, từ đó các tế bào ung thư phát triển, tăng sinh hình thành khối u và di căn. Phương pháp CAR-T sẽ tạo lại sự nhận diện tế bào ung thư cho tế bào T, từ đó tế bào miễn dịch của cơ thể nhận biết và tiêu diệt tế bào ung thư.
Như vậy, phương pháp điều trị miễn dịch tác động gián tiếp, tăng cường khả năng của hệ thống miễn dịch, giúp tiêu diệt khối u. Hiện nay, điều trị miễn dịch đã được thực hiện có hiệu quả cho nhiều bệnh ung thư như: ung thư phổi không tế bào nhỏ, ung thư đầu mặt cổ, ung thư dạ dày, ung thư hắc tố, ung thư cổ tử cung, u lympho, ung thư đường niệu, bệnh bạch cầu…
Tuy nhiên, hiện vẫn cần nhiều nghiên cứu để đánh giá hiệu quả và tác dụng không mong muốn của các thuốc thế hệ mới (đích, miễn dịch) trong điều trị bệnh ung thư.
1.2 Các bệnh ung thư cụ thể
Trong khuôn khổ cuốn sách này chúng tôi đề cập đến năm bệnh ung thư có tần suất mắc nhiều nhất tại Việt Nam là: ung thư gan, ung thư phổi, ung thư đại trực tràng, ung thư vú, ung thư dạ dày.
1.2.1 Bệnh ung thư gan
Ung thư gan nguyên phát hay ung thư biểu mô tế bào gan là bệnh lý ác tính của tế bào gan, bệnh có tỷ lệ mắc và tỷ lệ tử vong cao ở các nước Đông Á. Theo Globocan năm 2018 trên thế giới, ung thư gan đứng thứ 7 về tỷ lệ mắc với 841.080 trường hợp nhưng lại đứng thứ 5 về tỷ lệ tử vong với 782.000 (8,2% các nguyên nhân tử vong do ung thư). Tại Việt Nam, ung thư gan là bệnh phổ biến, tỷ lệ mắc ung thư gan tính chung cho cả hai giới đứng hàng số 1 với 25.335 trường hợp mỗi năm, chiếm 16,45% các loại bệnh ung thư. Bệnh thường chẩn đoán ở giai đoạn muộn nên tiên lượng xấu, hằng năm có 25.000 trường hợp ung thư gan tử vong và chiếm 23,48% trường hợp tử vong do ung thư.
Bệnh ung thư gan hay gặp trên đối tượng nguy cơ cao đó là xơ gan do virus (viêm gan B hoặc viêm gan C hoặc cả hai), xơ gan do rượu, nhiễm độc. Vì vậy, điều trị ung thư gan cần bao gồm cả điều trị ung thư và điều trị xơ gan, viêm gan B, C kèm theo điều trị các triệu chứng của bệnh.
❖ Tính chất của bệnh ung thư
Bệnh ung thư gan thường có tiến triển âm thầm, chỉ một số trường hợp phát hiện sớm được bệnh nhờ khám sức khỏe định kỳ, đặc biệt trên các đối tượng có nguy cơ cao như đã nêu ở trên. Hầu hết các trường hợp khác khi có biểu hiện lâm sàng: mệt mỏi, chán ăn, đau tức hạ sườn phải thì khối u tại gan kích thước đã trên 5cm, thậm chí một số trường hợp đã ở giai đoạn muộn: vàng da, vàng mắt, mệt mỏi, suy kiệt, cổ trướng, phù hai chi dưới. Người bệnh ung thư gan ở giai đoạn muộn ngoài các biểu hiện lâm sàng nêu trên thì các xét nghiệm máu cũng có nhiều bất thường như: suy gan, suy thận, rối loạn đông máu, giảm albumin trong máu, tăng bilirubin, ALT, AST,…
Để sàng lọc phát hiện sớm bệnh cần xét nghiệm bộ ba AFP (alpha-fetoprotein), AFP-L3, PIVKA II phối hợp với siêu âm ổ bụng (chụp cắt lớp vi tính hoặc cộng hưởng từ ổ bụng trong các trường hợp nghi ngờ tổn thương).
❖ Chẩn đoán:
Chẩn đoán bệnh dựa vào các đặc điểm lâm sàng và cận lâm sàng.
Triệu chứng lâm sàng:
– Triệu chứng cơ năng: bệnh diễn biến âm thầm không có triệu chứng, nhiều khi phát hiện do tình cờ siêu âm, khám sức khỏe định kỳ. Triệu chứng cơ năng có thể gặp: đầy bụng, khó tiêu, tức hoặc đau âm ỉ vùng hạ sườn phải, mệt mỏi, ăn uống kém, sút cân, ngứa, vàng da, vàng mắt, bụng to do có dịch ổ bụng.
– Triệu chứng thực thể: có thể gặp gan to, lách to, sao mạch, tuần hoàn bàng hệ, giãn tĩnh mạch, chảy máu, suy kiệt, cổ trướng, phù mềm, da niêm mạc vàng.
Xét nghiệm cận lâm sàng
- Công thức máu: có thể giảm tiểu cầu, số lượng tiểu cầu dưới 100 g/L do xơ gan và/hoặc giảm hemoglobin có thể liên quan đến chảy máu.
- Sinh hóa máu: có thể giảm natri, tăng creatinin, tăng men gan, tăng bilirubin, tăng canxi máu, giảm albumin, giảm glucose.
- Đông máu: kéo dài PT/INR, thời gian prothrombin giảm.
- Virus: xét nghiệm HBsAg/anti-HBc, anti-HCV, định lượng HBV-DNA.đánh giá tình trạng nhiễm và tải lượng virus viêm gan B, C.
- Xét nghiệm bộ ba dấu ấn ung thư (chất chỉ điểm khối u): AFP, AFP-L3, PIVKA II.
- Siêu âm, chụp CT, MRI gan, ổ bụng: xác định số lượng, vị trí, kích thước u gan, tính chất xâm lấn, huyết khối tĩnh mạch cửa. Chụp xạ hình xương, PET/CT, chụp CT ngực, MRI sọ não. phát hiện các tổn thương di căn.
- Sinh thiết u gan dưới hướng dẫn của siêu âm hoặc cắt lớp vi tính để xét nghiệm mô bệnh học xác định chẩn đoán khi cần.
- Giải trình tự nhiều gen.
Tiêu chuẩn chẩn đoán xác định:
Chẩn đoán xác định khi có một trong ba tiêu chuẩn sau:
- Có bằng chứng mô bệnh học là ung thư tế bào gan nguyên phát.
- Có hình ảnh điển hình* trên chụp cắt lớp vi tính ổ bụng có cản quang hoặc cộng hưởng từ bụng có cản từ và AFP ≥ 400 ng/mL.
- Có hình ảnh điển hình* trên chụp cắt lớp vi tính ổ bụng có cản quang hoặc cộng hưởng từ bụng có cản từ và AFP tăng cao nhưng chưa đến 400 ng/mL và có nhiễm virus viêm gan B hoặc C. Có thể làm sinh thiết gan để chẩn đoán xác định nếu bác sĩ lâm sàng thấy cần thiết.
- Các trường hợp không đủ các tiêu chuẩn nói trên đều phải làm sinh thiết gan để chẩn đoán xác định.
* Hình ảnh điển hình trên chụp cắt lớp vi tính ổ bụng có cản quang hoặc cộng hưởng từ bụng có cản từ: khối u tăng quang trên thì động mạch gan và thoát thuốc (wash out) trên thì tĩnh mạch cửa hay thì chậm, hoặc khối u giảm quang trên thì chưa tiêm cản quang và tăng quang trên thì động mạch gan.
❖ Chẩn đoán giai đoạn bệnh
Có nhiều phân loại đánh giá giai đoạn bệnh ung thư gan, trong đó phân loại giai đoạn TNM của Hiệp hội Ung thư Hoa Kỳ (American Joint Committee on Cancer- AJCC) và phân loại theo Barcelona hay được sử dụng hơn cả.
Phân loại giai đoạn TNM theo AJCC năm 2017.
T : Khối u nguyên phát
Tx: không đánh giá được khối u nguyên phát
T0: không có bằng chứng của u nguyên phát
T1: khối u ≤ 2 cm hoặc > 2 cm không xâm lấn mạch máu.
T1a: khối u ≤ 2 cm.
T1b: khối u > 2 cm không xâm lấn mạch máu.
T2: khối u > 2 cm có xâm lấn mạch máu hoặc nhiều khối u nhưng kích thước ≤ 5 cm.
T3: nhiều khối u, ít nhất 1 khối > 5 cm.
T4: một khối hoặc nhiều khối u kích thước bất kỳ nhưng đã xâm lấn đến nhánh chính của tĩnh mạch cửa hoặc tĩnh mạch gan, hoặc khối u xâm lấn trực tiếp đến cơ quan lân cận khác ngoài túi mật hoặc thủng phúc mạc tạng.
N: Hạch vùng
N0: không có di căn hạch.
N1: di căn hạch.
M: Di căn xa
M0: không có di căn xa.
M1: có di căn xa.
Bảng 4.1. Phân loại giai đoạn theo TNM bệnh ung thư gan
| Giai đoạn | T | N | M |
| IA | T1a | N0 | M0 |
| IB | T1b | N0 | M0 |
| II | T2 | N0 | M0 |
| IIIA | T3 | N0 | M0 |
| IIIB | T4 | N0 | M0 |
| IVA | bất kỳ T | N1 | M0 |
| IVB | bất kỳ T | bất kỳ N | M1 |
Bảng 4.2. Phân loại giai đoạn bệnh ung thư gan theo phân loại Barcelona
| Giai đoạn | PS | Tình trạng u | Chức năng gan (Child-Pugh) |
| 0 (rất sớm) | 0 | Một u đơn độc < 2 cm | A |
| A (sớm) | 0 | Một u đơn độc ≤ 5 cm hoặc ≤ 3 u, mỗi u ≤ 3 cm | A-B |
| B (trung gian) | 0 | U lớn, nhiều u | A-B |
| C (tiến triển) | 1-2 | U mọi kích thước, huyết khối tĩnh mạch cửa hoặc di căn ngoài gan | A-B |
| D (cuối) | 3-4 | Bất kỳ | C |
PS: Performance Status: chỉ số toàn trạng theo ECOG (Eastern Cooperative Oncology Group)
– Hệ thống điểm Child-Pugh đánh giá chức năng gan:
Bảng 4.3. Đánh giá chức năng gan theo hệ thống điểm Child-Pugh
| Thông số | 1 điểm | 2 điểm | 3 điểm |
| Bilirubin huyết thanh (mg/dL) | < 2 | 2 – 3 | > 3 |
| Albumin huyết thanh (g/dL) | > 3,5 | 2,8 – 3,5 | < 2,8 |
| INR | < 1,70 | 1,71 – 2,2 | > 2,2 |
| Dịch ổ bụng | Không | Kiểm soát được bằng thuốc | Khó kiểm soát |
| Bệnh lý não gan | Không | Kiểm soát được bằng thuốc | Khó kiểm soát |
| Tổng số điểm | Phân loại Child-Pugh |
| 5 – 6 | A (xơ gan còn bù) |
| 7 – 9 | B (xơ gan mất bù) |
| 10 – 15 | C (xơ gan mất bù) |
– Chỉ số đánh giá hoạt động cơ thể (Eastern Cooperative Oncology Group – ECOG):
+ ECOG mức 0: không triệu chứng, hoạt động bình thường.
+ ECOG mức 1: có triệu chứng nhưng vẫn đi lại tương đối bình thường.
+ ECOG mức 2: có triệu chứng, nằm giường bệnh < 50% thời gian trong ngày.
+ ECOG mức 3: có triệu chứng, nằm giường bệnh > 50% thời gian trong ngày.
+ ECOG mức 4: nằm liệt giường.
❖ Điều trị
Các phương pháp điều trị bệnh ung thư gan bao gồm:
Điều trị tại chỗ: phẫu thuật, đốt sóng cao tần, nút mạch, xạ trị trong chọn lọc với Y- 90, vi sóng, áp lạnh, bơm hóa chất động mạch.
Điều trị toàn thân: hóa chất, điều trị đích, miễn dịch. Tùy thuộc vào kích thước khối u, vị trí khối u gan, huyết khối tĩnh mạch cửa, chức năng gan, thể trạng người bệnh, tình trạng di căn xa… mà sẽ áp dụng một hoặc phối hợp các phương pháp điều trị nêu trên.
Song song với việc điều trị ung thư gan thì cần điều trị nguyên nhân gây bệnh ung thư gan và các biến chứng của bệnh; bao gồm điều trị viêm gan B, C, điều trị xơ gan, nâng cao thể trạng, giảm đau, tăng cường miễn dịch, chọc tháo dịch ổ bụng.
Việc lựa chọn các loại thuốc điều trị cần phải dựa vào thể trạng người bệnh, các bệnh lý phối hợp, các triệu chứng của bệnh, chức năng gan, thận, tủy xương. Ví dụ: với các bệnh nhân ung thư gan, có tình trạng rối loạn chức năng đông máu (tiểu cầu và/hoặc tỷ lệ prothrombin thấp) thì cần phải lưu ý đến tình trạng tăng áp lực tĩnh mạch cửa, tình trạng chảy máu có thể xảy ra khi sử dụng một số thuốc để từ đó có sự cân nhắc và lựa chọn thuốc phù hợp.
Điều trị tại chỗ:
- Phẫu thuật cắt bỏ phân thùy gan, phần gan có mang khối u: áp dụng ở bệnh nhân có thể trạng chung tốt PS: 0-1, phần gan có khối u dự kiến cắt bỏ được. Thể tích gan dự kiến còn lại ≥ 50% thể tích gan ban đầu, giai đoạn Child Pugh A, B, không có di căn xa, không có tăng áp lực tĩnh mạch cửa.
- Phẫu thuật ghép gan: được chỉ định khi có một khối u gan kích thước khối u gan không quá 5 cm, hoặc không quá ba u, kích thước mỗi u không quá 3 cm, Child Pugh B, C, không có di căn xa, không có tăng áp lực tĩnh mạch cửa, không có khả năng phẫu thuật cắt bỏ phần gan, phân thùy gan chứa u.
- Phá hủy u tại chỗ bằng bằng vi sóng (microwave), bằng điện đông (cryotherapy): được chỉ định khi khối u gan có số lượng u ≤ 3 và kích thước u ≤ 3 cm, hoặc một u ≤ 5 cm, dễ tiếp cận, thể trạng chung còn tốt, PS 0-2, Child Pugh A, B, khối u không có khả năng cắt bỏ, không có di căn xa, không có tăng áp lực tĩnh mạch cửa, có bệnh lý đi kèm.
- Tiêm cồn tuyệt đối qua da (Percutaneous Ethanol Injection – PEI): chỉ định khi số lượng u ≤ 3 và kích thước u ≤ 3 cm, hoặc một u ≤ 5 cm, dễ tiếp cận. Những trường hợp chỉ định phá hủy khối u kích thước > 5 cm cần được hội chẩn, thể trạng chung còn tốt PS 0-2, Child Pugh A, B, khối u không có khả năng cắt bỏ, không có di căn xa, không có tăng áp lực tĩnh mạch cửa, có bệnh lý đi kèm, khối u ở vị trí không quá sâu, không gần mạch máu lớn trong gan.
- Cắt nguồn máu nuôi khối u phối hợp với diệt tế bào ung thư bằng hóa chất (Transcatheter Arterial Chemoembolization – TACE). Số lượng u ≤ 3 và kích thước u ≤ 3 cm, hoặc một u ≤ 5 cm, thể trạng chung còn tốt PS 0-2, Child Pugh A, B, khối u không cắt được, không có di căn, không có tăng áp lực tĩnh mạch cửa hoặc có nhiều u ở cả hai thùy (có thể có huyết khối tĩnh mạch cửa nhánh nhỏ).
- Xạ trị trong chọn lọc (Selective Internal Radio Therapy – SIRT): được chỉ định điều trị cho các bệnh nhân ung thư biểu mô tế bào gan không thể phẫu thuật, tái phát sau các phương pháp điều trị khác hoặc đã có huyết khối thân tĩnh mạch cửa, u xâm lấn mạch máu gan, Child Pugh A, Shunt lưu thông hoạt độ phóng xạ lên phổi < 20%.
- Xạ trị chiếu ngoài, xạ trị định vị thân vào gan: được chỉ định khi tổn thương tại gan mà không có chỉ định phẫu thuật, đốt sóng cao tần, vi sóng, nút mạch, xạ trị trong chọn lọc, Child Pugh B.
Điều trị toàn thân:
Các thuốc điều trị bệnh ung thư gan bao gồm: hóa chất (gemcitabin, oxaliplatin, 5FU, doxorubicin, epirubicin, cisplatin, capecitabin, thalidomid.); thuốc điều trị đích (sorafenib, lenvatinib, regorafenib, cabozantinib…); thuốc điều trị miễn dịch (nivolumab, ramucirumab, pembrolizumab.). Điều trị đích, miễn dịch: được áp dụng ở giai đoạn tiến triển, di căn:
- Điều trị bước 1 hay sử dụng: sorafenib hoặc lenvatinib.
- Điều trị bước 2 hay sử dụng: sorafenib (sau thất bại bước 1 với lenvatinib), regorafenib (sau thất bại bước 1 với sorafenib), nivolumab, ramucirumab, pembrolizumab.
Một số phác đồ hóa chất:
- Phác đồ PIAF:
Doxorubicin: 40 mg/m2, truyền tĩnh mạch ngày 1.
Cisplatin: 20 mg/m2, truyền tĩnh mạch ngày 1, 2, 3, 4.
5-FU: 400 mg/m2, truyền tĩnh mạch ngày 1, 2, 3, 4.
Interferon a-2a: Tiêm dưới da 5 MUI/m2, ngày 1, 2, 3, 4.
Chu kỳ 3 tuần.
- Phác đồ GEMOX:
Gemcitabin 1.000 mg/m2, truyền tĩnh mạch ngày 1.
Oxaliplatin 100 mg/m2, truyền tĩnh mạch ngày 2.
Chu kỳ 2 tuần.
- Phác đồ FOLFOX4:
Folinic acid 200 mg/m2, truyền tĩnh mạch ngày 1
Oxaliplatin 85 mg/m2, truyền tĩnh mạch ngày 1
5-FU 400 mg/m2, tiêm/truyền tĩnh mạch bolus ngày 1
5-FU 600 mg/m2 truyền tĩnh mạch trong 22 giờ, ngày 1,2.
Chu kỳ 2 tuần.
- Phác đồ thalidomid
Thalidomid 100 mg, uống 2 lần/ngày cho tới khi bệnh tiến triển hoặc xuất hiện các độc tính không chấp nhận được.
- Phác đồ doxorubicin
Doxorubicin: 20-30 mg/m2, truyền tĩnh mạch hàng tuần.
- Phác đồ cisplatin
Cisplatin: 80 mg/m2, truyền tĩnh mạch hàng tuần.
- Phác đồ capecitabin
Capecitabin: 1.000 mg/m2, uống ngày 2 lần, từ ngày 1-14, chu kỳ 21 ngày.
Một số phác đồ điều trị đích, miễn dịch
- Sorafenib: 200 mg x 2 viên/lần, uống 2 lần/ngày cho tới khi bệnh tiến triển. Liều có thể giảm xuống 400 mg hàng ngày hoặc 400 mg cách ngày nếu bệnh nhân xuất hiện nhiều độc tính.
- Lenvatinib: 12 mg/ngày, uống hàng ngày (bệnh nhân trên 60 kg), 8 mg/ngày, uống hàng ngày (bệnh nhân dưới 60 kg).
- Regorafenib: 160 mg/ngày, uống ngày 1-21, chu kỳ 28 ngày.
- Nivolumab: 3 mg/kg, truyền tĩnh mạch chu kỳ 2 tuần.
- Cabozantinib: 60 mg/ngày, uống hàng ngày.
- Ramucirumab: 8 mg/kg, truyền tĩnh mạch chu kỳ 2 tuần.
- Pembrolizumab: 200 mg, truyền tĩnh mạch chu kỳ 3 tuần.
Điều trị phối hợp: thuốc điều trị viêm gan B, C; thuốc nâng cao thể trạng; thuốc tăng cường miễn dịch; thuốc giảm áp lực tĩnh mạch cửa; thuốc giảm đau, lợi tiểu; các thuốc điều trị các bệnh lý phối hợp.
1.2.2 Bệnh ung thư phổi
Ung thư phổi nguyên phát là bệnh lý ác tính tại phổi, đây là bệnh có tỷ lệ mắc có xu hướng ngày càng gia tăng.
Theo Globocan năm 2018, trên thế giới ung thư phổi đứng thứ 1 về tỷ lệ mắc với 2.093.876 trường hợp và cũng đứng thứ 1 về tỷ lệ tử vong với 1.761.007 (18,4% các nguyên nhân tử vong do ung thư). Tại Việt Nam, ung thư phổi là bệnh phổ biến, tỷ lệ mắc ung thư phổi tính chung cho cả hai giới đứng hàng số 2 với 23.667 trường hợp mỗi năm, chiếm 15,37% các loại bệnh ung thư. Hiện nay, người mắc bệnh ung thư phổi ở Việt Nam có xu hướng ngày càng được chẩn đoán sớm hơn, tuy nhiên tỷ lệ người bệnh được chẩn đoán ở giai đoạn muộn còn cao nên tiên lượng xấu, hằng năm có 20.710 trường hợp ung thư phổi tử vong và chiếm 19,14% trường hợp tử vong do ung thư.
Bệnh ung thư phổi hay gặp trên đối tượng nguy cơ cao đó là nam giới trên 50 tuổi, người hút thuốc lá, thuốc lào, người có tiền sử tiếp xúc với các hóa chất độc hại, bụi Amiăng.
Có 2 nhóm: ung thư phổi tế bào nhỏ và ung thư phổi không phải tế bào nhỏ; mỗi nhóm có tiên lượng và chiến lược điều trị khác nhau.
❖ Tính chất của bệnh ung thư
Ung thư phổi ở giai đoạn sớm thường được phát hiện tình cờ hoặc qua thăm khám sức khỏe định kỳ. Ở giai đoạn sớm, bệnh tiến triển âm thầm, ít có các biểu hiện hoặc các biểu hiện không đặc hiệu (ho, đau ngực) dễ lẫn với các triệu chứng bệnh khác. Ở giai đoạn muộn, thường có các biểu hiện đau ngực, ho ra máu, ho kéo dài, khó thở và các biểu hiện do các tổn thương di căn xa (đau tại vùng di căn xương, đau đầu, nôn, yếu, liệt). Ở giai đoạn cuối, người bệnh thường suy kiệt, đau nhiều, khó thở.
❖ Chẩn đoán
Dựa vào các triệu chứng lâm sàng và cận lâm sàng
Triệu chứng lâm sàng: Triệu chứng cơ năng và thực thể:
Ở giai đoạn sớm: bệnh phát triển âm thầm, triệu chứng thường nghèo nàn hoặc không có triệu chứng. Có thể có dấu hiệu gợi ý: ho khan kéo dài, có thể có đờm lẫn máu, điều trị kháng sinh không có kết quả.
Ở giai đoạn tiến triển: triệu chứng đa dạng tùy theo vị trí u, mức độ lan rộng tổn thương. Có thể gặp: đau ngực, đau dai dẳng, cố định một vị trí; khó thở khi khối u to, chèn ép, bít tắc đường hô hấp; hội chứng trung thất; tràn dịch màng tim, rối loạn nhịp tim; tràn dịch màng phổi. Toàn thân: mệt mỏi, gầy sút, sốt.
Các dấu hiệu do di căn: hạch thượng đòn; nốt di căn da thành ngực; di căn não: hội chứng tăng áp lực nội sọ, liệt thần kinh khu trú; di căn xương: đau, gãy xương bệnh lý. Di căn phổi đối bên, di căn gan: thường không có triệu chứng lâm sàng.
Các hội chứng cận ung thư: thường gặp trong ung thư phổi tế bào nhỏ, gồm ngón tay dùi trống; đái tháo nhạt do khối u bài tiết chất giống ADH; hội chứng Cushing do khối u bài tiết chất giống ACTH; tăng canxi máu do khối u bài tiết chất giống PTH; vú to, giọng cao, teo tinh hoàn do khối u bài tiết chất giống gonadotropin; hội chứng giả nhược cơ; hội chứng da liễu-viêm da cơ…
Xét nghiệm cận lâm sàng
- Tế bào học: tìm tế bào ung thư trong đờm, dịch màng phổi, dịch rửa phế quản. Nếu có hạch thượng đòn có thể xét nghiệm tế bào học bằng chọc hút kim nhỏ.
- Chụp X quang lồng ngực thẳng và nghiêng, chụp cắt lớp vi tính lồng ngực: giúp xác định vị trí, hình thái, kích thước tổn thương, mức độ lan rộng của u và tình trạng di căn phổi. Ngoài ra, còn để đánh giá khả năng phẫu thuật.
- Nội soi phế quản: giúp quan sát trực tiếp tổn thương, xác định vị trí, hình thái tổn thương. Qua nội soi tiến hành sinh thiết trực tiếp tổn thương hoặc xuyên thành phế quản để chẩn đoán mô bệnh học.
- Sinh thiết xuyên thành ngực dưới hướng dẫn chụp cắt lớp vi tính: có giá trị với các khối u ngoại vi gần thành ngực. Lấy bệnh phẩm, làm xét nghiệm mô bệnh học và sinh học phân tử.
- Xét nghiệm mô bệnh học, nhuộm hóa mô miễn dịch: là tiêu chuẩn vàng để chẩn đoán bệnh và phân loại mô bệnh học ung thư phổi tế bào nhỏ hoặc không phải tế bào nhỏ (biểu mô tuyến, tuyến-vảy, tế bào lớn…); đồng thời nhuộm hóa mô miễn dịch đánh giá loại tế bào và đánh giá sự bộc lộ PD-L1, ALK.
- Xét nghiệm sinh học phân tử nhằm phát hiện các đột biến gen: Gen EGFR, ALK, ROS-1, BRAF, KRAS, TMB (Tumor Mutational Burden), giải trình tự nhiều gen giúp cho việc lựa chọn các thuốc điều trị đích, miễn dịch.
- Siêu âm ổ bụng, chụp cắt lớp vi tính hoặc cộng hưởng từ sọ não, xạ hình xương, PET/CT. đánh giá giai đoạn bệnh.
❖ Chẩn đoán giai đoạn bệnh
Phân loại giai đoạn TNM theo The American Joint Committee on Cancer (AJCC) năm 2017.
T: U nguyên phát
Tx: không xác định được khối u, có tế bào ác tính trong đờm hoặc dịch rửa phế quản nhưng không nhìn thấy được trên chẩn đoán hình ảnh hay nội soi phế quản.
T0: không có bằng chứng về u nguyên phát.
Tis: ung thư biểu mô tại chỗ.
Ung thư biểu mô tế bào vảy tại chỗ.
Ung thư biểu mô tuyến tại chỗ: kích thước chỗ lớn nhất < 3cm.
T1: kích thước lớn nhất của khối u < 3cm, được bao quanh bởi nhu mô phổi hoặc lá tạng màng phổi, không có bằng chứng về xâm lấn vượt quá đoạn gần của phế quản thuỳ.
T1mi: ung thư biểu mô tuyến xâm lấn tối thiểu. T1a: kích thước lớn nhất ≤ 1 cm. Trên bề mặt, khối u lan rộng về một số kích thước, xâm lấn giới hạn tới thành phế quản và có thể mở rộng ra phế quản chính nhưng được phân loại vào T1a, tuy nhiên không phổ biến. T1b: 1cm < kích thước lớn nhất ≤ 2cm. T1c: 2cm < kích thước chỗ lớn nhất ≤ 3cm.
T2: 3cm < kích thước lớn nhất ≤ 5cm hoặc bất kỳ nhưng: (1) xâm lấn phế quản gốc, cách ngã ba khí phế quản (carina) ≥ 2cm; (2) xâm lấn lá tạng màng phổi; (3) gây xẹp phổi hoặc viêm phổi tắc nghẽn lan đến rốn phổi nhưng chưa lan toàn bộ phổi. Gồm: T2a: 3cm < kích thước lớn nhất ≤ 4cm; T2b: 4cm < kích thước lớn nhất ≤ 5 cm.
T3: 5cm < kích thước lớn nhất ≤ 7 cm hoặc xâm lấn một trong các thành phần: thành ngực (bao gồm cả khối u rãnh liên thùy trên); thần kinh hoành; màng phổi trung thất; màng ngoài tim hoặc có các nốt riêng biệt trên cùng 1 thùy phổi.
T4: khối u ≥ 7cm hoặc u bất kỳ kích thước nhưng xâm lấn 1 trong các thành phần sau: cơ hoành trung thất, tim, mạch máu lớn, khí quản, thần kinh quặt ngược thanh quản, thực quản, thân đốt sống, carina, các nốt khối u khác ở thùy phổi khác cùng bên.
N: Hạch vùng
Nx: không xác định được hạch vùng.
N0: không có di căn hạch vùng.
N1: di căn hạch cạnh phế quản và hoặc hạch trong phổi, hạch rốn phổi cùng bên, bao gồm cả sự xâm lấn trực tiếp.
N2: di căn hạch trung thất cùng bên và hạch dưới carina.
N3: di căn hạch rốn phổi đối bên, hạch trung thất đối bên, hạch cơ bậc thang cùng hoặc đối bên, hạch thượng đòn.
M: Di căn xa
Mx: không xác định được di căn xa.
M0: không có di căn xa.
M1: di căn xa. Gồm M1a: có kèm theo các nốt khối u ở phổi đối bên, u ở màng phổi hoặc màng tim hoặc tràn dịch màng phổi hoặc màng tim ác tính; M1b: di căn ngoài ngực ở một cơ quan đơn thuần. M1c: di căn nhiều nơi ngoài ngực với chỉ một nốt ở một cơ quan hoặc trong nhiều cơ quan.
Bảng 4.4. Phân loại giai đoạn bệnh theo TNM bệnh ung thư phổi
| Giai đoạn | T | N | M |
| 0 | Tis | N0 | M0 |
| IA1 | T1mi, T1a | N0 | M0 |
| IA2 | T1b | N0 | M0 |
| IA3 | T1c | N0 | M0 |
| IB | T2a | N0 | M0 |
| IIA | T2b | N0 | M0 |
| IIB | T1a,1b,1c, T2a,2b | N1 | M0 |
| T3 | N0 | M0 | |
| IIIA | T1a,1b,1c, T2a,2b | N2 | M0 |
| T3 | N1 | M0 | |
| T4 | N0 | M0 | |
| T4 | N1 | M0 | |
| III B | T1a,1b,1c, T2a,2b | N3 | M0 |
| T3, T4 | N2 | M0 | |
| IIIC | T3, T4 | N3 | M0 |
| IVA | T bất kỳ | N bất kỳ | M1a,1b |
| IVB | T bất kỳ | N bất kỳ | M1c |
Ung thư phổi tế bào nhỏ ngoài cách phân loại TNM như trên trong thực hành lâm sàng được chia ra hai giai đoạn:
– Giai đoạn khu trú: khi bệnh còn giới hạn khu trú có thể bao phủ bởi một trường chiếu xạ. Thường đánh giá giới hạn ở 1/2 lồng ngực và hạch vùng kể cả hạch trung thất, hạch thượng đòn cùng bên. Bao gồm giai đoạn I-III (T bất kỳ N bất kỳ M0) loại trừ các trường hợp T3-4 mà khối u quá lan rộng hoặc có khối u hoặc hạch quá lớn vượt quá sự bao phủ một trường chiếu xạ.
– Giai đoạn lan tràn: khi bệnh vượt quá giới hạn các vùng trên. Bao gồm giai đoạn IV và các trường hợp T3-4 mà khối u quá lan rộng hoặc có khối u hoặc hạch quá lớn vượt quá sự bao phủ một trường chiếu xạ.
❖ Điều trị
Điều trị bệnh ung thư phổi là điều trị đa mô thức nhằm đem lại hiệu quả điều trị tối ưu nhất. Tùy thuộc giai đoạn bệnh, thể trạng người bệnh, vị trí, kích thước khối u, loại mô bệnh học, xét nghiệm đột biến gen (EGFR, ALK, ROS-1,…) mà bác sĩ lựa chọn phương pháp điều trị phù hợp bao gồm: phẫu thuật (cắt thùy phổi, cắt thùy phổi và vét hạch, cắt toàn bộ một bên phổi, phẫu thuật lấy tổn thương di căn, sinh thiết tổn thương u, hạch,…) xạ trị tại u, tại hạch, tại tổn thương di căn (xương, não,…), hóa trị (các phác đồ hóa trị khác nhau tùy loại mô bệnh học ung thư biểu mô tế bào nhỏ hay không tế bào nhỏ, với thuốc hay sử dụng: cisplatin, carboplatin, paclitaxel, docetaxel, 5FU, capecitabin, pemetrexed, vinorelbin, gemcitabin, irinotecan, etoposid, topotecan, temozolomid, cyclophosphamid, doxorubicin, vincristin, bendamustin,…) đối với ung thư phổi không tế bào nhỏ ngoài hóa trị chuẩn thì hóa trị metronomic (sử dụng thuốc liều thấp thường xuyên trong thời gian dài mà không ngắt quãng) mang lại lợi ích rất tốt cho bệnh nhân không phù hợp với hóa trị chuẩn, điều trị đích (tùy thuộc xét nghiệm đột biến gen EGFR, ALK, ROS-1, BRAF,…; tùy loại mô bệnh học ung thư biểu mô tuyến hay vảy; thuốc hay sử dụng: erlotinib, gefitinib, afatinib, osimetinib, dacomitinib, alectinib, brigatinib, ceritinib, crizotinib, lorlatinib, trametinib, larotrectinib, vandetanib, cabozantinib, dabrafenib, bevacizumab…), điều trị miễn dịch (tùy thuộc xét nghiệm PD- L1, TMB,… thuốc hay sử dụng: atezolizumab, pembrolizumab, nivolumab, ramucirumab, ipilimumab…), điều trị triệu chứng giảm đau, dinh dưỡng, tâm lý.
Ung thư phổi không tế bào nhỏ:
– Phẫu thuật: chỉ định ở giai đoạn 0, I, II, IIIA. Có thể: phẫu thuật cắt phân thùy, cắt thùy phổi kèm theo vét hạch rốn thùy, cắt lá phổi kèm theo vét hạch rốn phổi và trung thất, có thể cắt một phần màng tim, thành ngực.
– Xạ trị: chỉ định xạ trị đơn thuần triệt căn cho giai đoạn I, II, IIIA có chống chỉ định hoặc bệnh nhân từ chối phẫu thuật, hóa chất. Xạ trị trước mổ: cho giai đoạn IIIB, kích thước u quá lớn để xét khả năng phẫu thuật sau đó. Xạ trị sau mổ: cho giai đoạn II, IIIA và các trường hợp phẫu thuật cắt bỏ không hoàn toàn để lại tổ chức ung thư sau phẫu thuật. Xạ trị triệu chứng: xạ trị giảm đau, xạ trị toàn não, xạ trị chống chèn ép.
– Hóa trị chỉ định cho giai đoạn IV, IIIB, IIIA. Giai đoạn IIB, IIA cần được cân nhắc. Thuốc hay sử dụng: nhóm platin (cisplatin, carboplatin); nhóm taxan (paclitaxel, docetaxel, gemcitabin, vinorelbin; pemetrexed – với nhóm không phải ung thư biểu mô vảy); mitomycin; ifosfamid; vinblastin; 5FU; capecitabin, tegafur + gimeracil + oteracil potassium (TS one), tegafur + uracil (Ufur, Mefuform)
– Điều trị đích:
Thuốc phân tử nhỏ:
Các thuốc nhóm TKI (tyrosin kinase inhibitor):
Thế hệ 1: erlotinib, gefitinib, chỉ định: ung thư phổi không tế bào nhỏ, có đột biến EGFR dương tính đột biến nhạy cảm (thường đột biến trên exon 19, 21).
Thế hệ 2: afatinib chỉ định trong ung thư phổi không tế bào nhỏ có đột biến EGFR dương tính, bao gồm các đột biến thường gặp như L858R, Del 19 và đột biến không thường gặp. Các trường hợp đã thất bại với TKI thế hệ 1 do gặp tác dụng phụ, không dung nạp hoặc không đáp ứng. Các trường hợp có đột biến gen EGFR dương tính nhưng có tăng men gan, có điều trị các thuốc chuyển hóa qua enzym CYP450 hoặc các thuốc điều trị kháng acid dạ dày vì afatinib có bằng chứng không tương tác với CYP450 và các thuốc kháng acid dạ dày. Ung thư phổi không tế bào nhỏ loại biểu mô vẩy sau thất bại với hóa chất phác đồ có platin. Dacomitinib, chỉ định trong ung thư phổi không tế bào nhỏ có đột biến EGFR dương tính, bao gồm các đột biến thường gặp như L858R, Del 19.
Thế hệ 3: osimertinib chỉ định trong ung thư phổi không tế bào nhỏ có đột biến gen EGFR dương tính, bao gồm cả trường hợp có đột biến gen T790M. Ung thư phổi tế bào nhỏ sau thất bại với TKI thế hệ 1, 2.
Các thuốc ức chế ALK, ROS-1, BRAF:
Crizotinib, chỉ định: ung thư phổi không tế bào nhỏ có ALK dương tính và hoặc ROS-1 dương tính.
Alectinib, chỉ định: ung thư phổi không tế bào nhỏ có ALK dương tính; ung thư phổi không tế bào nhỏ sau thất bại với crizotinib.
Ceritinib, chỉ định: ung thư phổi không tế bào nhỏ có ALK dương tính và hoặc ROS-1 dương tính; ung thư phổi không tế bào nhỏ sau thất bại với crizotinib, alectinib.
Brigatinib, chỉ định: ung thư phổi không tế bào nhỏ có ALK dương tính sau thất bại với crizotinib.
Dabrafenib, chỉ định: ung thư phổi không tế bào nhỏ giai đoạn di căn xa có đột biến gen BRAF V600E dương tính.
Trametinib, chỉ định: ung thư phổi không tế bào nhỏ giai đoạn di căn xa có đột biến gen BRAF V600E dương tính.
Kháng thể đơn dòng:
Bevacizumab, chỉ định: ung thư phổi không tế bào nhỏ giai đoạn tiến triển loại không biểu mô vảy.
Ramucirumab, chỉ định: ung thư phổi không tế bào nhỏ giai đoạn tiến triển sau thất bại với hóa chất phác đồ có platin (bước 2). Ung thư phổi không tế bào nhỏ giai đoạn tiến triển sau thất bại với các thuốc điều trị đích nhóm TKI.
– Điều trị miễn dịch:
Pembrolizumab, chỉ định điều trị bước 1: ung thư phổi không tế bào nhỏ giai đoạn di căn xa có PD-L1 dương tính ≥ 50%. Điều trị bước 2: ung thư phổi không tế bào nhỏ giai đoạn di căn xa có PD-L1 dương tính ≥ 1%.
Nivolumab, chỉ định: ung thư phổi không tế bào nhỏ giai đoạn di căn xa, sau thất bại với điều trị hóa chất phác đồ có platin.
Atezolizumab, chỉ định: ung thư phổi không tế bào nhỏ giai đoạn di căn, ung thư phổi tế bào nhỏ.
Durvalumab, chỉ định: ung thư phổi không tế bào nhỏ giai đoạn III, không phẫu thuật được mà bệnh không tiến triển sau ≥ 2 chu kỳ hóa xạ trị đồng thời phác đồ có platin.
Trong thực hành lâm sàng: đối với ung thư phổi không tế bào nhỏ giai đoạn tiến triển (IIIB, IV) thì điều trị như sau:
1) Nếu có đột biến EGFR không có đột biến T790M thì có thể dùng TKI thế hệ 1, 2, 3 (erlotinib, gefitinib, afatinib, dacomitinib, osimetinib), nếu bước 1 dùng erlotinib hoặc gefitinib hoặc afatinib hoặc dacomitinib thì sau khi tiến triển, bước 2 sẽ xét nghiệm lại EGFR nếu xuất hiện đột biến T790M thì chuyển sang dùng thế hệ 3 (osimetinib);
2) Nếu có ALK dương tính: bước 1 dùng alectinib hoặc brigatinib hoặc ceritinib hoặc crizotinib; bước 2 có thể dùng alectinib hoặc brigatinib hoặc ceritinib hoặc lorlatinib;
3) Nếu có ROS-1 dương tính: dùng ceritinib hoặc crizotinib.
Đột biến gen BRAF dương tính có thể điều trị bằng dabrafenib/trametinib. Nếu NTRK dương tính: có thể điều trị bằng larotrectinib. Đối với những người bệnh không có điều kiện kinh tế để sử dụng các thuốc TKI thì hóa trị vẫn là lựa chọn cơ bản ở giai đoạn tiến triển, di căn.
Một số phác đồ hóa chất bệnh ung thư phổi không tế bào nhỏ:
+ Phác đồ PC:
Paclitaxel 175 mg/m2, truyền tĩnh mạch trong 3 giờ ngày 1.
Carboplatin AUC 6, truyền tĩnh mạch ngày 1.
Chu kỳ 3 tuần.
+ Phác đồ DC:
Docetaxel 75 mg/m2, truyền tĩnh mạch, ngày 1.
Carboplatin AUC 6, truyền tĩnh mạch ngày 1.
Chu kỳ 3 tuần.
+ Phác đồ GC:
Gemcitabin 1.000 mg/m2 truyền tĩnh mạch, ngày 1, 8.
Vinorelbin 25 mg/m2, truyền tĩnh mạch ngày 1, 8.
Chu kỳ 3 tuần
+ Phác đồ pemetrexed + platin:
Pemetrexed 500 mg/m2, truyền tĩnh mạch ngày 1.
Carboplatin AUC 6 hoặc cisplatin 75 mg/m2, truyền tĩnh mạch ngày 1.
Chu kỳ 3 tuần.
+ Phác đồ vinorelbin:
Vinorelbin 25 mg/m2, truyền tĩnh mạch ngày 1, 8. Chu kỳ 3 tuần.
Hoặc vinorelbin 60-80 mg/m2, uống hàng tuần.
Hoặc vinorelbin uống 30-50 mg/ lần x 3 lần/tuần.
+ Phác đồ capecitabin:
Capecitabin 1.000-1.250mg/m2/lần, uống 2 lần/ngày, ngày 1-14, chu kỳ 21 ngày
Một số phác đồ điều trị đích, miễn dịch bệnh ung thư phổi không tế bào nhỏ
Các thuốc nhóm TKI (tyrosin kinase inhibitor):
+ Erlotinib: 1 viên 150 mg/ngày, uống hàng ngày, trước ăn ít nhất 1 giờ và sau ăn ít nhất 2 giờ.
+ Gefitinib: 1 viên 250 mg/ngày, uống hàng ngày, trước ăn ít nhất 1 giờ và sau ăn ít nhất 2 giờ.
+ Afatinib: 40 mg/ngày, uống hàng ngày, trước ăn ít nhất 1 giờ và sau ăn ít nhất 2 giờ.
+ Osimertinib: 80 mg/ngày, uống hàng ngày.
+ Crizotinib: uống 2 viên 250 mg/ngày, chia 2 lần, trước ăn ít nhất 1 giờ và sau ăn ít nhất 2 giờ.
+ Alectinib: 600 mg/ngày, uống 2 lần/ngày, uống hàng ngày.
+ Ceritinib: 450 mg/ngày, uống hàng ngày.
+ Brigatinib: 90mg/ngày, hàng ngày x 7 ngày. Nếu độc tính chấp nhận được thì tăng liều 180 mg/ngày, uống hàng ngày.
+ Dabrafenib: dùng phối hợp với trametinib. Liều dùng: 120 mg/ngày, uống 2 lần/ngày, hàng ngày.
+ Trametinib: dùng phối hợp với dabrafenib. Liều dùng: 2 mg/ngày, hàng ngày.
Các thuốc kháng thể đơn dòng
+ Bevacizumab: 15 mg/ kg, truyền tĩnh mạch ngày 1, dùng đơn chất (điều trị duy trì) hoặc kết hợp với hóa chất.
Ramucirumab: dùng phối hợp với docetaxel.
Ramucirumab 10 mg/kg, truyền tĩnh mạch ngày 1.
Docetaxel 75 mg/m2, truyền tĩnh mạch ngày 1. Chu kỳ 21 ngày.
+ Pembrolizumab 200 mg, truyền tĩnh mạch mỗi 3 tuần, dùng đơn chất hoặc kết hợp hóa chất.
+ Nivolumab 3 mg/kg, truyền tĩnh mạch mỗi 2 tuần.
+ Atezolizumab 1.200 mg, truyền tĩnh mạch mỗi 3 tuần, dùng đơn chất hoặc phối hợp với hóa chất.
+ Durvalumab 10 mg/kg, truyền tĩnh mạch ngày 1, trong 1 giờ. Chu kỳ 2 tuần.
Ung thư phổi tế bào nhỏ:
- Phẫu thuật (cắt thùy phổi + vét hạch trung thất): chỉ định ở giai đoạn I-IIA (T1-2N0M0). Sau phẫu thuật, nếu có di căn hạch lựa chọn hóa trị và xạ trị sau mổ; nếu không di căn hạch thì hóa trị.
- Xạ trị: xạ trị dự phòng di căn não, chỉ định ở giai đoạn IIB-IV có đáp ứng với điều trị toàn thân. Xạ trị vào ngực: chỉ định giai đoạn khu trú hoặc giai đoạn I-IIA (T1,2N0M0) kết hợp với hóa trị hoặc giai đoạn lan tràn khi đã đạt đáp ứng hoàn toàn hoặc một phần với hóa trị.
- Hóa trị: giai đoạn khu trú (phối hợp với xạ trị) hoặc giai đoạn lan tràn, tái phát.
- Thuốc hay sử dụng: toposide dạng truyền và uống; nhóm platin: cisplatin, carboplatin; irinotecan; cyclophosphamid; doxorubicin; vincristin; topotecan uống hoặc tĩnh mạch; paclitaxel; docetaxel; temozolomid; vinorelbin dạng truyền và uống; gemcitabin; ifosfamid; bendamustin.
- Điều trị miễn dịch: atezolizumab chỉ định trong ung thư phổi tế bào nhỏ giai đoạn lan tràn. Nivolumab chỉ định ung thư phổi tế bào nhỏ giai đoạn IV sau thất bại với điều trị phác đồ hóa chất có platin. Ipilinumab chỉ định ung thư phổi tế bào nhỏ giai đoạn IV sau thất bại với điều trị phác đồ hóa chất có platin. Pembrolizumab chỉ định ung thư phổi tế bào nhỏ giai đoạn lan tràn, sau thất bại với điều trị hóa chất, có PD-L1 dương tính (CPS ≥ 1).
Một số phác đồ hóa chất bệnh ung thư phổi loại tế bào nhỏ:
+ Phác đồ EP:
Cisplatin 75mg/m2, truyền tĩnh mạch ngày 1.
Etoposid 100mg/m2, truyền tĩnh mạch ngày 1-3; chu kỳ 28 ngày.
Hoặc
Cisplatin 25mg/m2, truyền tĩnh mạch ngày 1-3
Etoposid 100mg/m2, truyền tĩnh mạch ngày 1-3; chu kỳ 28 ngày.
Hoặc
Cisplatin 60mg/m2 truyền tĩnh mạch ngày 1.
Etoposid 120mg/m2, truyền tĩnh mạch ngày 1-3; chu kỳ 28 ngày.
Hoặc
Carboplatin AUC 5-6, truyền tĩnh mạch ngày 1.
Etoposid 100mg/m2, truyền tĩnh mạch ngày 1-3; chu kỳ 28 ngày.
+ Phác đồ IC:
Irinotecan 60mg/m2, truyền tĩnh mạch ngày 1, 8, 15.
Cisplatin 60mg/m2, truyền tĩnh mạch ngày 1; chu kỳ 28 ngày.
Hoặc
Irinotecan 65mg/m2, truyền tĩnh mạch ngày 1, 8
Cisplatin 30mg/m2, truyền tĩnh mạch ngày 1, 8; chu kỳ 28 ngày.
Hoặc
Irinotecan 50mg/m2, truyền tĩnh mạch ngày 1, 8, 15.
Carboplatin AUC 5, truyền tĩnh mạch ngày 1; chu kỳ 28 ngày.
+ Phác đồ CAV:
Cyclophosphamid 1.000mg/m2, truyền tĩnh mạch ngày 1.
Doxorubicin 45mg/m2, truyền tĩnh mạch ngày 1.
Vincristin 1,4mg/m2, truyền tĩnh mạch ngày 1; chu kỳ 21 ngày.
+ Phác đồ CAE:
Cyclophosphamid 1000mg/m2, truyền tĩnh mạch ngày 1.
Doxorubicin 45mg/m2, truyền tĩnh mạch ngày 1.
Etoposid 80-100mg/m2, truyền tĩnh mạch ngày 1-3 hoặc ngày 1, 3, 5; chu kỳ 21 ngày.
+ Phác đồ CEV:
Cyclophosphamid 1.000mg/m2, truyền tĩnh mạch ngày 1.
Epirubicin 70mg/m2, truyền tĩnh mạch ngày 1.
Vincristin 2mg/m2, truyền tĩnh mạch ngày 1; chu kỳ 21 ngày
+ Phác đồ ICE:
Ifosfamid 5.000mg/m2, truyền tĩnh mạch 24 giờ ngày 1 (dùng kèm với mesna)
Carboplatin 300mg/m2, truyền tĩnh mạch ngày 1 trong 1 giờ
Etoposid 120mg/m2, truyền tĩnh mạch ngày 1,2 và 240mg/m2, tĩnh mạch ngày 3
Vincristin 1,0mg/m2, truyền tĩnh mạch ngày 15
Chu kỳ 28 ngày
+ Phác đồ VIP:
Etoposide 75mg/m2, truyền tĩnh mạch ngày 1-4
Ifosfamid 1.200mg/m2, truyền tĩnh mạch ngày 1-4 (với mesna)
Cisplatin 20mg/m2, truyền tĩnh mạch ngày 1-4
+ Phác đồ Topotecan + Cisplatin
Topotecan 1,0mg/m2, truyền tĩnh mạch ngày 1-5
Cisplatin 60mg/m2, truyền tĩnh mạch ngày 1
Chu kỳ 21 ngày
+ Phác đồ: Topotecan 1,0-1,5 mg/m2, truyền tĩnh mạch ngày 1-5. Chu kỳ 21 ngày
Hoặc Topotecan 2,3 mg/m2, uống ngày 1-5. Chu kỳ 21 ngày
+ Phác đồ: Irinotecan 300 mg/m2, truyền tĩnh mạch. Chu kỳ 21 ngày
Hoặc Irinotecan 100 mg/m2, truyền tĩnh mạch hàng tuần
+ Phác đồ: Paclitaxel 175-250 mg/m2, truyền tĩnh mạch trong 24 giờ ngày 1, 8, 15
Hoặc Paclitaxel 80 mg/m2, truyền tĩnh mạch hàng tuần x 6 tuần, sau đó nghỉ 2 tuần
+ Phác đồ: Docetaxel 100 mg/m2, truyền tĩnh mạch ngày 1. Chu kỳ 3 tuần
+ Phác đồ: Temozolomid 75 mg/m2, uống. Chu kỳ 4 tuần
+ Phác đồ: Vinorelbin 25-30 mg/m2, truyền tĩnh mạch ngày 1, hàng tuần
+ Phác đồ: Etoposid uống 50 mg/m2, uống. Chu kỳ 4-5 tuần
+ Phác đồ: Gemcitabin 1.000 mg/m2, truyền tĩnh mạch ngày 1, 8, 15. Chu kỳ 4 tuần
Một số phác đồ điều trị đích, miễn dịch bệnh ung thư phổi loại tế bào nhỏ:
+ Atezolizumab 1.200 mg, truyền tĩnh mạch mỗi 3 tuần, dùng đơn thuần hoặc kết hợp hóa chất.
+ Nivolumab:
– Đơn chất: Nivolumab 3 mg/kg, truyền tĩnh mạch ngày 1. Chu kỳ 2 tuần.
– Phối hợp:
- Nivolumab 1mg/kg, truyền tĩnh mạch ngày 1.
- Ipilimumab 3mg/kg, truyền tĩnh mạch ngày 1.
– Chu kỳ 3 tuần x 4 chu kỳ. Sau đó, nivolumab 3mg/kg, truyền tĩnh mạch ngày
- Chu kỳ 2 tuần.
– Hoặc
- Nivolumab 3mg/kg, truyền tĩnh mạch ngày 1
- Ipilimumab 1mg/kg, truyền tĩnh mạch ngày 1
– Chu kỳ 3 tuần x 4 chu kỳ. Sau đó, nivolumab 3mg/kg, truyền tĩnh mạch ngày
- Chu kỳ 2 tuần.
+ Ipilinumab: dùng phối hợp với nivolumab theo phác đồ như trên.
+ Pembrolizumab: pembrolizumab 200mg, truyền tĩnh mạch ngày 1. Chu kỳ 3 tuần.
1.2.3 Bệnh ung thư đại trực tràng
Ung thư đại trực tràng là bệnh lý ác tính tại đại trực tràng, đây loại ung thư thường gặp của đường tiêu hóa. Theo Globocan năm 2018, trên thế giới ung thư đại tràng đứng thứ 4 về tỷ lệ mắc với 1.096.601 trường hợp và số trường hợp tử vong là 551.269 (5,8% các nguyên nhân tử vong do ung thư). Ung thư trực tràng có tỷ lệ mắc thấp hơn với 704.376 trường hợp và 310.394 trường hợp tử vong. Tại Việt Nam, ung thư đại trực tràng là bệnh phổ biến, tỷ lệ mắc tính chung cho cả hai giới đứng hàng số 5 với 14.733 trường hợp mỗi năm, chiếm 8,9% các loại bệnh ung thư.
Những đối tượng nguy cơ cao mắc bệnh: người trong gia đình mắc bệnh ung thư đại trực tràng, bệnh Crohn, bệnh đa polyp đại trực tràng gia đình, người có chế độ ăn ít rau, nhiều chất béo, bệnh lý đại trực tràng: viêm loét mạn tính, polyp.
- Tính chất của bệnh ung thư:
Bệnh ung thư đại trực tràng ở giai đoạn sớm thường phát hiện tình cờ qua nội soi đại trực tràng khi khám sức khỏe định kỳ. Ở giai đoạn tiếp theo, người bệnh thường có biểu hiện đau bụng, rối loạn tiêu hóa (đi ngoài phân lỏng hoặc táo bón và/hoặc đi ngoài phân nhầy máu mũi, thay đổi khuôn phân, mót rặn); ở giai đoạn muộn hơn, người bệnh có biểu hiện rối loạn tiêu hóa, tự sờ thấy khối ở bụng, đau bụng kèm theo biểu hiện tại các tổn thương di căn: đau tức hạ sườn phải, vàng da (di căn gan), ho, đau ngực (di căn phổi), đau xương (di căn xương), đau đầu, nôn, yếu liệt (di căn não), gầy sút cân, suy kiệt, tắc ruột (đau bụng từng cơn, bí đại tiện, nôn), thủng vỡ u tại đại trực tràng (đau bụng dữ dội, bụng cứng,.).
- Chẩn đoán:
Dựa vào triệu chứng lâm sàng và cận lâm sàng.
Triệu chứng lâm sàng
Triệu chứng cơ năng: tuỳ vị trí u, giai đoạn bệnh mà có bệnh cảnh lâm sàng khác nhau. Nhìn chung có các dấu hiệu sau: đầy bụng, đau bụng, chậm tiêu, rối loạn tiêu hóa, đi ngoài phân nhầy máu mũi; hay gặp ở người bệnh ung thư trực tràng; tự sờ thấy khối u bụng vùng hạ vị, mạng sườn. Ngoài ra, có thể gặp bệnh nhân vào viện do xuất hiện biến chứng như: tắc ruột, viêm phúc mạc do vỡ u: bệnh cảnh lâm sàng rất nặng, tiên lượng xấu.
Người bệnh vào viện khi bệnh ở giai đoạn muộn, triệu chứng tùy thuộc vào cơ quan di căn: cổ trướng số lượng từ ít đến nhiều do di căn phúc mạc; vàng da, đau tức hạ sườn phải,.do tổn thương di căn gan; đau ngực, khó thở, suy hô hấp do tổn thương di căn phổi, hạch trung thất; đau bụng vùng thắt lưng, suy thận do tổn thương di căn hạch; đau vùng xương bị di căn, gãy xương; yếu, liệt, hôn mê, tăng áp lực nội sọ (buồn nôn, nôn, đau đầu) do tổn thương di căn não. Toàn thân: da xanh niêm mạc nhợt do thiếu máu, gầy sút cân, suy kiệt.
Triệu chứng thực thể có thể sờ thấy u qua thành bụng hoặc qua thăm khám trực tràng nếu u ở trực tràng, ống hậu môn. Thăm trực tràng: phát hiện được khối u cách rìa hậu môn dưới 8 cm. Khám toàn thân để phát hiện di căn gan, hạch ngoại vi, dịch cổ trướng, di căn buồng trứng ở phụ nữ, giúp đánh giá mức độ tiến triển bệnh.
Xét nghiệm cận lâm sàng
- Nội soi đại trực tràng với ống soi cứng, ống mềm và sinh thiết làm mô bệnh học là tiêu chuẩn vàng để chẩn đoán xác định.
- Siêu âm ổ bụng, chụp X-quang ngực thẳng, chụp cắt lớp vi tính ổ bụng – lồng ngực, cộng hưởng từ sọ não, SPECT, SPECT/CT, PET/CT để đánh giá giai đoạn bệnh (di căn phổi, hạch, gan, não), đánh giá hiệu quả điều trị, tiên lượng, đánh giá tái phát, di căn sau điều trị. Các thăm dò cận lâm sàng khác như: nội soi dạ dày, soi bàng quang khi nghi ngờ u xâm lấn vào các cơ quan này.
- Xét nghiệm công thức máu, đông máu, sinh hóa máu đánh giá tình trạng thiếu máu, chức năng gan – thận. Xét nghiệm chất chỉ điểm khối u trong máu: CEA, CA 19-9 để tiên lượng, theo dõi đáp ứng điều trị, tái phát và di căn. Xét nghiệm đếm tế bào u trong máu (circulating tumor cell – CTCs) giúp tiên lượng bệnh.
- Xét nghiệm tế bào học dịch màng phổi, màng bụng: ly tâm tìm tế bào ung thư hoặc làm xét nghiệm mô học khối tế bào (cell block) để đánh giá di căn.
- Xét nghiệm đột biến gen KRAS, NRAS, BRAF, PTEN, PIK3CA, Heu-2/neu, APC, TP53, giải trình tự nhiều gen. Đánh giá sự bất ổn định vi vệ tinh và thiếu hụt sửa chữa bắt cặp sai dMMR/MSI (deficient mismatch repair/microsatellite instability).
❖ Chẩn đoán giai đoạn bệnh
Đánh giá giai đoạn theo hệ thống TNM của AJCC ấn bản lần thứ 8 năm 2017.
T: U nguyên phát
- Tx: không thể đánh giá khối u nguyên phát
- T0: không có bằng chứng về khối u nguyên phát
- Tis: ung thư biểu mô tại chỗ
- T1: khối u đã xâm lấn lớp dưới niêm mạc
- T2: khối u xâm lấn lớp cơ
- T3: khối u xâm lấn lớp dưới thanh mạc hoặc đến vùng mô quanh trực tràng hoặc đại tràng không được phủ phúc mạc
- T4: khối u xâm lấn trực tiếp cơ quan hoặc cấu trúc kế cận và/hoặc xâm lấn vào phúc mạc tạng
+ T4a: U xâm lấn vào phúc mạc tạng
+ T4b: U xâm lấn cơ quan kế cận
N: Hạch vùng
- Nx: không thể đánh giá được di căn hạch vùng
- N0: không có di căn hạch vùng
- N1: di căn 1-3 hạch vùng
+ N1a: di căn 1 hạch
+ N1b: di căn 2-3 hạch
+ N1c: không có di căn hạch vùng nhưng có nhân di căn ở dưới thanh mạc hoặc mạc treo hoặc vùng trực tràng không được phúc mạc che phủ.
- N2: di căn 4 hạch vùng trở lên
+ N2a: di căn 4-6 hạch
+ N2b: di căn từ 7 hạch trở lên
M : Di căn xa
- M0: không có di căn xa
- M1: di căn xa
+ M1a: di căn xa chỉ ở một vị trí hoặc cơ quan nhưng không di căn phúc mạc
+ M1b: di căn từ 2 vị trí hoặc cơ quan trở lên nhưng không di căn phúc mạc
+ M1c: di căn phúc mạc có hoặc không kèm theo di căn vị trí hoặc cơ quan khác
Bảng 4.5. Phân loại giai đoạn theo TNM và Dukes bệnh ung thư đại trực tràng
| Giai đoạn | T | N | M | Dukes |
| 0 | Tis | N0 | M0 | _ |
| I | T1 | N0 | M0 | A |
| T2 | N0 | M0 | A | |
| IIA | T3 | N0 | M0 | B |
| IIB | T4a | N0 | M0 | B |
| IIC | T4b | N0 | M0 | B |
| IIIA | T1-T2 | N1/N1c | M0 | C |
| T1 | N2a | M0 | C | |
| IIIB | T3-T4a | N1/N1c | M0 | C |
| T2-T3 | N2a | M0 | C | |
| T1-T2 | N2b | M0 | C | |
| IIIC | T4a | N2a | M0 | C |
| T3-T4a | N2b | M0 | C | |
| T4b | N1- N2 | M0 | C | |
| IVA | Bất kỳ T | Bất kỳ N | M1a | _ |
| IVB | Bất kỳ T | Bất kỳ N | M1b | _ |
| IVC | Bất kỳ T | Bất kỳ N | M1c | _ |
❖ Điều trị
Tùy thuộc giai đoạn bệnh, vị trí khối u, thể trạng người bệnh mà có thể áp dụng các phương pháp phẫu thuật, hóa trị, xạ trị, điều trị đích, miễn dịch.
Phẫu thuật là biện pháp cơ bản điều trị ung thư đại trực tràng: phẫu thuật triệt căn, phẫu thuật điều trị triệu chứng (làm hậu môn nhân tạo trên u, điều trị trong trường hợp thủng vỡ u gây viêm phúc mạc).
Hóa trị được áp dụng: 1) Điều trị bổ trợ sau mổ, nhằm diệt nốt những tế bào ung thư còn sót lại, hạn chế tiến triển, tái phát, di căn; 2) Điều trị trước mổ (hóa trị tiền phẫu) nhằm thu nhỏ kích thước u và tổn thương di căn, tạo điều kiện thuận lợi để phẫu thuật triệt căn; 3) Điều trị ở giai đoạn muộn: thường phối hợp hóa trị với điều trị đích (kháng thể đơn dòng).
Xạ trị được chỉ định chủ yếu trong ung thư trực tràng thấp, trung bình giai đoạn tiến triển tại chỗ; áp dụng: 1) Điều trị bổ trợ sau mổ, nhằm diệt nốt những tế bào ung thư còn sót lại, hạn chế tiến triển, tái phát, di căn; 2) Điều trị trước mổ (xạ trị tiền phẫu) hoặc hóa xạ trị trước mổ, nhằm thu nhỏ kích thước u, tạo điều kiện thuận lợi để phẫu thuật triệt căn; 3) Điều trị ở giai đoạn muộn: thường phối hợp với hóa trị nhằm điều trị chống chảy máu, chèn ép hoặc xạ trị vào não, xương, gan, phổi.trong trường hợp có di căn các vị trí trên.
Điều trị đích, miễn dịch: thường áp dụng ở giai đoạn muộn: đã có tổn thương di căn xa; việc lựa chọn phác đồ điều trị cần xem xét đến các xét nghiệm đột biến gen và hóa mô miễn dịch.
Phác đồ điều trị:
Giai đoạn I, II: phẫu thuật cắt đoạn đại trực tràng và vét hạch.
Giai đoạn II nguy cơ cao, giai đoạn III: phẫu thuật cắt đoạn đại trực tràng, vét hạch và hóa trị bổ trợ.
Giai đoạn IV: nếu phẫu thuật được sẽ phẫu thuật cắt đoạn đại trực tràng, kèm theo cắt bỏ tổn thương di căn sau đó hóa trị. Nếu có tiềm năng phẫu thuật: hóa trị bổ trợ 3 chu kỳ trước mổ, sau đó đánh giá lại và xét phẫu thuật và hóa trị tiếp. Nếu có tiềm năng phẫu thuật: hóa trị. Phác đồ hóa trị ở giai đoạn IV thường hóa chất có thể kèm thêm các kháng thể đơn dòng (bevacizumab, cetuximab, panitumumab), nếu sử dụng bevacizumab thì phải dừng thuốc này ít nhất 4 tuần trước phẫu thuật vì bevacizumab làm chậm liền vết thương.
Các thuốc hay sử dụng: 5 FU, leucovorin, capecitabin, oxaliplatin, irinotecan, tegafur + gimeracil+ oteracil potassium (TS one), tegafur + uracil (Ufur, Mefuform), trifluridin + tipiracil (TAS 102), bevacizumab, cetuximab (dùng khi xét nghiệm đột biến gen KRAS, NRAS, BRAF không đột biến), panitumumab (dùng khi xét nghiệm đột biến gen KRAS, NRAS, BRAF không đột biến), regorafenib, ramucirumab, ziv-aflibercept, vemurafenib (dùng khi có đột biến gen BRAF), dabrafenib (chỉ dùng khi có đột biến gen BRAF), trametinib (dùng khi có đột biến gen BRAF), encorafenib (dùng khi có đột biến gen BRAF), binimetinib (chỉ dùng khi có đột biến gen BRAF), nivolumab (chỉ dùng trong trường hợp dMMR/MSI-high), ipilimumab (dùng trong trường hợp dMMR/MSI- high), pembrolizumab (dùng trong trường hợp dMMR/MSI-high).
Phác đồ hay sử dụng:
Điều trị bổ trợ: Phác đồ FOLFOX, XELOX, FUFA, capecitabin.
Điều trị ở giai đoạn di căn: tân bổ trợ, bổ trợ, triệu chứng: Điều trị bước 1: Phác đồ FOLFOX, XELOX, FOLFIRI ± kháng thể đơn dòng bevacizumab hoặc FOLFOX, XELOX, FOLFIRI ± cetuximab hoặc panitumumab (chỉ trong trường hợp không có đột biến gen KRAS, NRAS, BRAF). Điều trị bước 2: tùy vào điều trị bước 1 là phác đồ có oxaliplatin thì bước 2 là phác đồ có irinotecan và ngược lại, có thể kèm hoặc không kèm kháng thể đơn dòng (bevacizumab, cetuximab, panitumumab). Với người bệnh thể trạng yếu, bác sĩ thường lựa chọn phác đồ đơn chất.
Một số phác đồ hóa chất:
+ Phác đồ FOLFOX4:
Oxaliplatin: 85 mg/m2, truyền tĩnh mạch, ngày 1.
Leucovorin: 200 mg/m2, truyền tĩnh mạch, ngày 1, 2.
5 FU: 400 mg/m2, truyền tĩnh mạch, ngày 1, 2.
5 FU: 600 mg/m2, truyền tĩnh mạch trong 22 giờ, ngày 1, 2.
Nhắc lại sau mỗi 2 tuần.
+ Phác đồ FOLFOX6:
Oxaliplatin: 100 mg/m2, truyền tĩnh mạch, ngày 1.
Leucovorin: 200 mg/m2, truyền tĩnh mạch, ngày 1, 2.
5 FU: 400 mg/m2, tiêm tĩnh mạch, ngày 1, 2.
5 FU: 600 mg/m2, truyền tĩnh mạch trong 22 giờ, ngày 1, 2.
Nhắc lại sau mỗi 2 tuần.
+ Phác đồ mFOLFOX6:
Oxaliplatin: 85mg/m2, truyền tĩnh mạch, ngày 1.
Leucovorin: 350mg/m2, truyền tĩnh mạch, ngày 1.
5 FU: 400mg/m2, tiêm tĩnh mạch ngày 1, sau đó 5 FU: 2,4g/m2 truyền tĩnh mạch trong 46 giờ liên tục.
Nhắc lại sau mỗi 2 tuần.
+ Phác đồ FOLFIRI:
Irinotecan: 180 mg/m2, truyền tĩnh mạch, ngày 1.
Leucovorin: 200 mg/m2, truyền tĩnh mạch, ngày 1, 2.
5 FU: 400 mg/m2, tiêm tĩnh mạch chậm, ngày 1, 2.
5 FU: 600mg/m2, truyền tĩnh mạch, ngày 1, 2.
Nhắc lại sau mỗi 2 tuần.
+ Phác đồ FOLFOXIRI:
Irinotecan: 165 mg/m2, truyền tĩnh mạch, ngày 1.
Oxaliplatin: 85 mg/m2, truyền tĩnh mạch, ngày 1.
Leucovorin 200 mg/m2, truyền tĩnh mạch, ngày 1.
5 FU: 3.200 mg/m2, truyền tĩnh mạch trong 48 giờ.
Lặp lại sau mỗi 02 tuần.
+ Phác đồ XELOX:
Oxaliplatin: 130 mg/m2, truyền tĩnh mạch, ngày 1
Capecitabin: 1.000 mg/m2 uống, 2 lần/ngày x 14 ngày.
Chu kỳ 3 tuần.
+ Phác đồ XELIRI:
Irinotecan: 240-250 mg/m2, truyền tĩnh mạch trong 90 phút, ngày 1
Capecitabin: 1.000 mg/m2 uống, 2 lần/ngày x 14 ngày.
Chu kỳ 3 tuần
hoặc
Irinotecan: 175 mg/m2, truyền tĩnh mạch trong 30 phút, ngày 1
Capecitabine: 1.000 mg/m2 uống, 2 lần/ngày x 7 ngày.
Chu kỳ 2 tuần
+ Phác đồ Capecitabin:
Capecitabin: 1.250 mg/m2 uống, 2 lần/ngày x 14 ngày.
Hoặc Capecitabin 500 mg, 3 lần/ngày, uống hàng ngày liên tục.
Hoặc Capecitabin 625 mg, 2 lần/ngày uống hàng ngày liên tục.
Chu kỳ 3 tuần.
+ Phác đồ TS 1 đơn thuần:
TS – one 60-80 mg/m2, uống ngày 1-14, chu kỳ 3 tuần (21 ngày). hoặc TS – one: 60-80mg/m2, uống ngày 1-28, chu kỳ 6 tuần (42 ngày).
+ Phác đồ UFT:
UFT (Tegafur + Uracil): 100 mg/m2, uống/ lần x 3 lần/ngày, ngày 1-28
Folinic acid: 30mg/m2, uống/lần x 3 lần/ngày, ngày 1-28
Chu kỳ 5 tuần.
hoặc
UFT (Tegafur + Uracil): 100 -125mg/m2, uống/lần x 3 lần/ngày, ngày 1-14, chu kỳ 21 ngày.
+ Phác đồ Triíluridin/Tipiracil (TAS 102): 35mg/m2, tối đa 80mg/lần, uống 2 lần/ngày, ngày 1-5, 8-12, chu kỳ 28 ngày.
Một số phác đồ điều trị đích, miễn dịch:
+ Bevacizumab: Liều dùng thông thường: 5-15 mg/kg, truyền tĩnh mạch từng đợt, phối hợp với các phác đồ hóa chất 14-21 ngày/lần.
+ Cetuximab: Liều dùng: 400 mg/m2 ngày 1 sau đó 250 mg/m2 hàng tuần, truyền tĩnh mạch phối hợp với các phác đồ hóa chất.
+ Panitumumab: Liều dùng: 6 mg/kg, truyền tĩnh mạch trong 60-90 phút, mỗi hai tuần hoặc 2,5mg/kg, truyền tĩnh mạch hàng tuần, phối hợp với các phác đồ hóa chất.
+ Regorafenib: Liều dùng: Regorafenib 40 mg x 4 viên /ngày, uống một lần/ngày, uống từ ngày 1-21, chu kỳ 28 ngày, có thể điều chỉnh liều tùy thuộc bệnh nhân.
+ Ziv-aflibercept: Liều dùng 4 mg/kg truyền tĩnh mạch > 1 giờ mỗi 2 tuần.
+ Ramucimumab: Liều dùng 8 mg/kg truyền tĩnh mạch > 1 giờ mỗi 2 tuần.
+ Pembrolizumab: 200 mg hoặc 2 mg/kg truyền tĩnh mạch > 30 phút mỗi 3 tuần cho đến khi bệnh tiến triển hoặc độc tính không chấp nhận được hoặc dùng đến 24 tháng ở người bệnh không tiến triển bệnh.
+ Nivolumab: 240mg hoặc 3mg/kg truyền tĩnh mạch > 60 phút mỗi 2 tuần cho đến khi bệnh tiến triển hoặc độc tính không chấp nhận được.
1.2.4 Bệnh ung thư vú
Ung thư vú là bệnh lý ác tính tại tuyến vú, đây là bệnh ung thư có tỷ lệ mắc cao nhất ở nữ giới Việt Nam và thế giới. Theo Globocan năm 2018, trên thế giới ung thư vú đứng thứ 1 về tỷ lệ mắc ở nữ giới với 2.088.849 trường hợp và số trường hợp tử vong là 626.679 (6,6% các nguyên nhân tử vong do ung thư). Tại Việt Nam, ung thư vú là bệnh phổ biến, với 15.229 trường hợp mỗi năm, chiếm 20,6% trong số các loại bệnh ung thư ở nữ giới.
Những đối tượng nguy cơ cao mắc bệnh: tiền sử gia đình có mẹ, con gái, chị/em gái bị ung thư vú, có đột biến gen BRCA1 và BRCA2; tuổi cao: phụ nữ > 40 tuổi; phụ nữ có hành kinh sớm (trước 12 tuổi) và mãn kinh muộn (sau 55 tuổi); phụ nữ mang thai muộn (> 30 tuổi), không mang thai, không cho con bú; phụ nữ béo phì, hút thuốc lá; phụ nữ có tiền sử chiếu xạ vào vùng ngực; phụ nữ có tiền sử bị ung thư trước đó: phụ nữ đã bị ung thư một bên vú, ung thư buồng trứng, ung thư nội mạc tử cung, ung thư đại tràng.
Các phương pháp sàng lọc phát hiện sớm ung thư vú bằng tự khám vú hàng tháng, khám bác sĩ chuyên khoa ung thư định kỳ hằng năm sau tuổi 40 phối hợp với chụp X quang tuyến vú và siêu âm vú 3D để phát hiện sớm bệnh.
- Tính chất của bệnh ung thư
Bệnh ung thư vú ở giai đoạn sớm thường phát hiện tình cờ qua thăm khám sức khỏe định kỳ hoặc tự sờ thấy tổn thương nhỏ tại vú, ở giai đoạn này, có thể điều trị khỏi hoàn toàn. Ở giai đoạn tiếp theo, người bệnh thường có biểu hiện tự sờ thấy u vú, hoặc đau tại vú, chảy dịch đầu vú; ở giai đoạn muộn hơn, người bệnh có biểu hiện khối u tại vú to dần và/hoặc kèm theo biểu hiện tại các tổn thương di căn: đau tức hạ sườn phải, vàng da (di căn gan), ho, đau ngực (di căn phổi), đau xương (di căn xương), đau đầu, nôn, yếu liệt (di căn não), gầy sút cân, suy kiệt, loét tại vú.
- Chẩn đoán
Dựa vào các triệu chứng lâm sàng và cận lâm sàng
Triệu chứng lâm sàng
Triệu chứng cơ năng
Các triệu chứng thường là người bệnh tự sờ thấy khối u ở vú hoặc tình cờ phát hiện qua các lần khám sức khỏe định kỳ hoặc bệnh đã ở giai đoạn tiến triển.
- Dấu hiệu tại chỗ: đau, chảy dịch hoặc chảy máu tại đầu núm vú, co kéo da vùng vú, giai đoạn muộn khối u có thể xâm lấn gây lở loét, hoại tử ra ngoài da gây chảy dịch, mùi hôi thối, xâm lấn thành ngực gây đau nhiều.
- Hạch ngoại vi: thường là hạch nách hoặc hạch thượng đòn với kích thước khác nhau, chắc, di động hoặc không di động, có thể biểu hiện viêm, hoại tử.
- Toàn thân: gầy sút cân, suy kiệt, da xanh, niêm mạc nhợt do thiếu máu.
- Dấu hiệu di căn xa: tùy thuộc từng vị trí di căn mà có biểu hiện lâm sàng khác nhau. Di căn phổi: đau ngực, khó thở, có thể có suy hô hấp. Di căn phúc mạc: cổ trướng. Di căn xương: đau xương, gãy xương tự nhiên. Vàng da, đau tức hạ sườn phải,.do tổn thương di căn gan. Đau bụng vùng thắt lưng, suy thận do tổn thương di căn hạch trong ổ bụng. Di căn lên não: tùy vị trí di căn có biểu hiện lâm sàng khác nhau, phần lớn biểu hiện hội chứng tăng áp lực nội sọ: đau đầu, buồn nôn và nôn, yếu hoặc liệt nửa người, hội chứng tiểu não, co giật, hôn mê.
Thực thể
Khám vú
- Sờ thấy u vú có ranh giới không rõ, mật độ chắc. U có thể xâm lấn vào thành ngực làm hạn chế di động hoặc xâm nhiễm da tạo hình ảnh “sần da cam” hoặc vỡ loét, đôi khi ung thư vú cũng biểu hiện như một viêm tấy lan tỏa vùng vú (ung thư vú thể viêm).
- Có thể thấy sẹo mổ cũ sưng nề, thâm nhiễm vùng da ngực xung quanh.
Khám hạch ngoại vi
- Thường gặp hạch nách, hạch thượng đòn, hạch thường cứng, chắc, di động kém, kích thước to nhỏ khác nhau, có thể có biểu hiện viêm, hoại tử.
Khám toàn thân phát hiện các tổn thương di căn xa
Xét nghiệm cận lâm sàng:
Xét nghiệm để chẩn đoán xác định
- Chụp X quang tuyến vú: tổn thương điển hình có dạng hình sao nhiều chân, co kéo tổ chức tuyến vú, có nhiều chấm vi canxi hóa tập hợp thành đám.
- Xét nghiệm tế bào học: thường thấy các tế bào ung thư mất sự kết dính, đa hình thái, tỷ lệ nhân/nguyên sinh chất tăng, nhiều nhân quái nhân chia, bào tương kiềm tính.
- Sinh thiết u bằng kim sinh thiết hoặc sinh thiết hút chân không hoặc sinh thiết mở: cho phép lấy mảnh tổ chức làm xét nghiệm mô bệnh học và các xét nghiệm hóa mô miễn dịch, gen.
Các xét nghiệm đánh giá di căn xa
- Siêu âm ổ bụng, chụp cắt lớp vi tính ổ bụng – lồng ngực, cộng hưởng từ sọ não để đánh giá giai đoạn bệnh (di căn hạch, di căn xa).
- Ghi hình với SPECT, SPECT/CT, PET/CT để đánh giá giai đoạn bệnh, hiệu quả điều trị, tiên lượng, đánh giá tái phát, di căn sau điều trị.
Xét nghiệm cơ bản đánh giá toàn thân
- Xét nghiệm công thức máu đánh giá tình trạng thiếu máu, nhiễm trùng. Xét nghiệm sinh hoá máu đánh giá chức năng gan, thận.
- Xét nghiệm chất chỉ điểm khối u trong máu: CEA, CA 15-3.
- Xét nghiệm đếm tế bào u trong máu (circulating tumor cell – CTCs) giúp tiên lượng bệnh.
Mô bệnh học và hóa mô miễn dịch
- Đánh giá tình trạng thụ thể nội tiết: ER, PR, Her-2/neu, P53, Ki-67.
Xét nghiệm gen: BRCA1, BRCA2, giải trình tự nhiều gen
❖ Chẩn đoán giai đoạn bệnh
Đánh giá giai đoạn theo hệ thống TNM của AJCC năm 2017.
T: khối u
Tx: không đánh giá được u nguyên phát.
T0: không có dấu hiệu u nguyên phát.
Tis: ung thư biểu mô nội ống tại chỗ (DCIS), bệnh Paget của núm vú.
T1: đường kính lớn nhất của u ≤ 2 cm.
T1mi: đường kính lớn nhất của khối u ≤ 1mm.
T1a: 1mm < đường kính lớn nhất của khối u ≤ 5mm.
T1b: 5mm < đường kính lớn nhất của khối u ≤ 10mm.
T1c: 10mm < đường kính lớn nhất của khối u ≤ 20mm.
T2: 2cm < đường kính u ≤ 5 cm.
T3: đường kính u > 5 cm.
T4: u với mọi kích thước nhưng xâm lấn trực tiếp tới thành ngực hoặc da (thành ngực bao gồm xương sườn, cơ gian sườn, cơ răng trước, không tính cơ ngực lớn). T4a: u xâm lấn tới thành ngực.
T4b: phù da cam, loét da vú, hoặc có nhiều u nhỏ vệ tinh ở vú cùng bên.
T4c: bao gồm cả T4a và Tab.
T4d: ung thư vú dạng viêm.
N: Hạch vùng
Nx: hạch vùng không xác định được.
N0: không có di căn tới hạch vùng được xác định hoặc chỉ xác định được lượng rất ít (lượng có tế bào ác tính rất nhỏ ≤ 0,2mm).
N1: vi di căn vào hạch (< 2mm) hoặc di căn 1-3 hạch nách và/hoặc lâm sàng chưa có di căn hạch vú trong kèm theo có di căn hạch cửa.
pN1mi: vi di căn (khoảng 200 tế bào, 0,2mm < vi di căn < 2mm).
pN1a: di căn 1-3 hạch nách, có ít nhất 1 hạch > 2mm.
pN1b: di căn gác là hạch vú trong cùng bên.
pN1c: gồm cả pN1a và pN1b.
N2: di căn 4-9 hạch nách cùng bên hoặc di căn hạch vú trong cùng bên trên chẩn đoán hình ảnh mà không có di căn hạch nách.
pN2a: di căn 4-9 hạch nách (có ít nhất 1 hạch ≤ 2mm).
pN2b: trên lâm sàng phát hiện di căn hạch vú trong mà có hoặc không khẳng định bằng mô bệnh học; kèm theo không di căn hạch nách được khẳng định bằng mô bệnh học.
N3: di căn ≥ 10 hạch nách hoặc hạch nách nhóm III (hạch hạ đòn), hoặc di căn hạch vú trong cùng bên kèm theo có di căn ≥ 1 hạch nách nhóm I, II trên chẩn đoán hình ảnh hoặc di căn > 3 hạch nách và di căn hạch cửa nhưng không di căn hạch vú trong cùng bên hoặc di căn hạch thượng đòn cùng bên.
pN3a: di căn ≥ 10 hạch nách (ít nhất 1 hạch > 2mm) hoặc di căn hạch hạ đòn (hạch nách nhóm III).
pN3b: pN1a hoặc pN2a với cN2b (hạch vú trong dương tính trên chẩn đoán hình ảnh) hoặc pN2a với pN1b.
pN3c: di căn hạch thượng đòn cùng bên.
M: Di căn xa
Mx: không xác định được di căn xa ở thời điểm chẩn đoán.
M0: không có di căn xa.
cM1: di căn xa được phát hiện bằng lâm sàng hoặc chẩn đoán hình ảnh.
pM1: di căn xa được khẳng định bằng mô bệnh học hoặc di căn vào hạch không thuộc nhóm hạch vùng có kích thước > 0,2mm.
Bảng 4.6. Chẩn đoán giai đoạn theo TNM bệnh ung thư vú
| Giai đoạn | T | N | M |
| 0 (tại chỗ) | Tis | N0 | M0 |
| IA | T1 | N0 | M0 |
| IB | T0, T1 | N1mi | M0 |
| IIA | T0 | N1 | M0 |
| T1 | N1 | M0 | |
| T2 | N0 | M0 | |
| IIB | T2 | N1 | M0 |
| T3 | N0 | M0 | |
| IIIA | T0 | N2 | M0 |
| T1 | N2 | M0 | |
| T2 | N2 | M0 | |
| T3 | N1 | M0 | |
| T3 | N2 | M0 | |
| IIIB | T4 | N0 | M0 |
| T4 | N1 | M0 | |
| T4 | N2 | M0 | |
| IIIC | T bất kỳ | N3 | M0 |
| IV | T bất kỳ | N bất kỳ | M1 |
❖ Điều trị
Điều trị ung thư vú là sự phối hợp của nhiều phương pháp điều trị ung thư (điều trị đa mô thức) bao gồm: phẫu thuật, xạ trị, hoá trị, nội tiết, đích, miễn dịch. Ở giai đoạn sớm, phẫu thuật đóng vai trò chủ đạo, tùy thuộc vị trí, kích thước khối u vú, tuổi… có thể phẫu thuật lấy rộng u, vét hạch nách (phẫu thuật bảo tồn) hoặc phẫu thuật cắt toàn bộ tuyến vú kèm theo vét hạch nách (phẫu thuật Patey). Phẫu thuật tạo hình cũng được áp dụng để tạo sự tự tin cho người bệnh, nhất là các phụ nữ trẻ. Ở giai đoạn tiếp theo, cần có sự phối hợp phẫu thuật, hóa trị và/hoặc xạ trị, nội tiết (tùy giai đoạn bệnh, loại mô bệnh học, tuổi, thụ thể nội tiết…) Ở giai đoạn muộn: điều trị toàn thân (hóa trị, nội tiết, đích, miễn dịch) giữ vai trò chủ đạo, trong đó hóa trị là biện pháp cơ bản nhất để điều trị ở giai đoạn này, ngoài hóa trị chuẩn thì việc sử dụng hóa trị metronomic (sử dụng thuốc liều thấp thường xuyên trong thời gian dài mà không ngắt quãng) mang lại lợi ích rất tốt cho bệnh nhân không phù hợp với hóa trị chuẩn. Nội tiết và điều trị đích, miễn dịch được áp dụng tùy thuộc vào các kết quả xét nghiệm thụ thể nội tiết ER, PR, Heu2/neu… Xạ trị được áp dụng điều trị phối hợp khi đã có tổn thương di căn (hạch, di căn xa: xương, não…); xạ trị cũng có thể được áp dụng trong mổ hoặc sau mổ đối với trường hợp phẫu thuật bảo tồn. Xạ trị triệu chứng nhằm giảm đau, giảm chảy máu với khối u xâm lấn thành ngực, khối u gây chảy máu, hoại tử.
Các thuốc hay sử dụng điều trị bệnh ung thư vú: doxorubicin, epirubicin, cyclophosphamid, 5FU, capecitabin, vinorelbin, gemcitabin, paclitaxel, docetaxel, methotrexat, vinblastin, adriamycin, mitomycin C, carboplatin, trastuzumab (chỉ định khi Heu2/neu dương tính), pertuzumab (chỉ định khi Heu2/neu dương tính), ado- trastuzumab emtansine (T-DM1), liposomal doxorubicin, eribulin, albumin-bound paclitaxel, cisplatin, lapatinib, olaparid, atezolizumab, bevacizumab.
Điều trị nội tiết: phụ nữ trẻ chưa mãn kinh: tamoxifen; đã mãn kinh: anastrozol, letrozol, exemestane, fulvestran.
Thuốc ức chế mTor: everolimus, sirolimus, tesmirolimus.
Thuốc ức chế PI3K: taselisib, alpelisib, buparlisib.
Thuốc ức chế đặc hiệu PARP: olaparib, rucaparib, talazoparib, veliparib: người bệnh có BRCA dương tính.
Một số phác đồ hóa chất
+ Phác đồ AC
Doxorubicin 60 mg/m2, truyền tĩnh mạch ngày 1.
Cyclophosphamid 60 mg/m2, truyền tĩnh mạch ngày 1.
Chu kỳ 21 ngày.
+ Phác đồ CAF
Cyclophosphamid 500 mg/m2, truyền tĩnh mạch ngày 1.
Doxorubicin 50 mg/m2, truyền tĩnh mạch ngày 1.
5-Fluorobicin 500 mg/m2, truyền tĩnh mạch ngày 1.
Chu kỳ 21 ngày
+ Phác đồ CMF
Cyclophosphamid 10 mg/m2, uống, ngày 1-14.
Methotrexat 40 mg/m2, truyền tĩnh mạch ngày 1-8.
5-Fluorouracil 600 mg/m2, truyền tĩnh mạch ngày 1, 8.
Hoặc
Cyclophosphamid 100 mg/m2, truyền tĩnh mạch ngày 1-14.
Methotrexat 30 mg/m2, truyền tĩnh mạch ngày 1, 8.
5-Fluorouracil 400 mg/m2, truyền tĩnh mạch ngày 1, 8.
Chu kỳ 28 ngày, điều trị 6 đợt.
+ Phác đồ TA:
Doxorubicin 50 mg/m2, truyền tĩnh mạch ngày 1.
Docetaxel 75 mg/m2, truyền tĩnh mạch ngày 1.
+ Phác đồ TAC:
Doxorubicin 50 mg/m2, truyền tĩnh mạch ngày 1.
Sau đó, docetaxel 75 mg/m2, truyền tĩnh mạch ngày 1.
Cyclophosphamid 500 mg/m2, truyền tĩnh mạch ngày 1.
+ Phác đồ VC:
Vinorebin 30 mg/m2, truyền tĩnh mạch ngày 1, 8.
Cisplatin 75 mg/m2, truyền tĩnh mạch ngày 1.
Nhắc lại mỗi đợt sau 21 ngày.
+ Phác đồ AC liều dày sau đó dùng paclitaxel.
Doxorubicin 60 mg/m2, truyền tĩnh mạch ngày 1.
Cyclophosphamid 600 mg/m2, truyền tĩnh mạch ngày 1.
Chu kỳ 14 ngày x 4 chu kỳ. Sau đó:
Paclitaxel 175 mg/m2, truyền tĩnh mạch trong 3 giờ, ngày 1.
Chu kỳ 14 ngày x 4 chu kỳ.
Hoặc sau đó:
Paclitaxel 80 mg/m2, truyền tĩnh mạch trong 1 giờ, hàng tuần đến 12 tuần.
+ Phác đồ TC
Doxetaxel 75 mg/m2, truyền tĩnh mạch ngày 1.
Cyclophosphamid 600 mg/m2, truyền tĩnh mạch ngày 1.
Chu kỳ 21 ngày x 4 chu kỳ.
+ Phác đồ TAC
Docetaxel 75 mg/m2, truyền tĩnh mạch ngày 1.
Doxorubicin 50 mg/m2, truyền tĩnh mạch ngày 1.
Cyclophosphamide 500 mg/m2, truyền tĩnh mạch ngày 1.
Chu kỳ 21 ngày x 6 chu kỳ.
+ Phác đồ AC, sau đó docetaxel
Doxorubicin 60 mg/m2, truyền tĩnh mạch ngày 1.
Cyclophosphamide 600 mg/m2, truyền tĩnh mạch ngày 1.
Chu kỳ 21 ngày x 4 chu kỳ.
Sau đó: Docetaxel 100 mg/m2, truyền tĩnh mạch ngày 1.
Chu kỳ 21 ngày x 4 chu kỳ
+ Phác đồ EC
Epirubicin 100 mg/m2, truyền tĩnh mạch ngày 1.
Cyclophosphamid 830 mg/m2, truyền tĩnh mạch ngày 1.
Chu kỳ 21 ngày x 8 chu kỳ.
Hoặc Epirubicin 100 mg/m2, truyền tĩnh mạch ngày 1.
Cyclophosphamid 600 mg/m2 truyền tĩnh mạch ngày 1.
Chu kỳ 21 ngày
+ Phác đồ Vinorelbin
Vinorelbin: 25 mg/m2, truyền tĩnh mạch ngày 1 mỗi tuần hoặc 30-35 mg/m2, truyền tĩnh mạch ngày 1, 8 chu kỳ 21 ngày.
Hoặc Vinorelbin: 60-80 mg/m2, uống ngày 1, 8, 15 chu kỳ 28 ngày.
Hoặc Vinorelbin: 60-80 mg/m2, uống hàng tuần.
Hoặc Vinorelbin: 30-50 mg/lần, uống 3 lần/tuần.
+ Phác đồ capecitabin
Capecitabin 1.000-1.250 mg/m2/lần, uống 2 lần mỗi ngày, ngày 1-14.
Một số phác đồ điều trị đích, miễn dịch:
+ Trastuzumab
Dùng kết hợp với hóa trị: trastuzumab 4 mg/kg truyền tĩnh mạch lần đầu, sau đó trastuzumab 2 mg/kg truyền tĩnh mạch hàng tuần.
Hoặc trastuzumab 8 mg/kg truyền tĩnh mạch lần đầu, sau đó, trastuzumab 6 mg/kg truyền tĩnh mạch mỗi 21 ngày.
+ Pertuzumab
Dùng kết hợp với hóa trị và trastuzumab.
Pertuzumab 840 mg/kg, truyền tĩnh mạch ngày 1 trong 60 phút, sau đó, 420 mg/kg, truyền tĩnh mạch trong 30-60 phút, chu kỳ mỗi 21 ngày.
+ Ado-trastuzumab emtansine (T-DM1)
3,6 mg/kg truyền tĩnh mạch ngày 1 chu kỳ mỗi 21 ngày.
+ Atezolizumab
Atezolizumab 1.200 mg, truyền tĩnh mạch mỗi 3 tuần, dùng đơn chất hoặc phối hợp với hóa chất.
+ Lapatinib
Lapatinib 1.250 mg uống hàng ngày, đơn chất hoặc phối hợp với capecitabin hoặc kháng thể đơn dòng.
1.2.5 Bệnh ung thư dạ dày
Ung thư dạ dày là bệnh lý ác tính tại dạ dày, là một trong các loại ung thư phổ biến trong các ung thư đường tiêu hóa.
Theo Globocan năm 2018, thế giới hàng năm có 1.033.701 trường hợp ung thư dạ dày mới mắc và 782.685 trường hợp tử vong (chiếm 8,2% nguyên nhân tử vong do ung thư). Tại Việt Nam, bệnh thường gặp ở cả hai giới, đứng hàng thứ 3 sau ung thư gan, phổi ở nam và đứng hàng thứ 4 sau ung thư vú, đại trực tràng, phổi ở nữ về tỷ lệ mắc; hàng năm có 17.527 trường hợp mới mắc.
Những đối tượng nguy cơ cao mắc bệnh: Những người có tiền sử phẫu thuật cắt dạ dày do loét có nguy cơ mắc bệnh cao gấp 2 – 4 lần người bình thường. Người có các tổn thương như viêm teo dạ dày, vô toan, thiếu máu ác tính, dị sản ruột, u tuyến dạ dày cũng được xem là có nguy cơ mắc bệnh cao hơn.
❖ Tính chất của bệnh ung thư
Bệnh ung thư dạ dày ở giai đoạn sớm thường phát hiện tình cờ qua nội soi dạ dày qua thăm khám sức khỏe định kỳ, ở giai đoạn này, có thể chỉ cần cắt hớt tổn thương qua nội soi và theo dõi định kỳ. Ở giai đoạn tiếp theo, người bệnh thường có biểu hiện đau bụng, ợ hơi, ợ chua, đau tức vùng thượng vị; giai đoạn muộn hơn người bệnh có biểu hiện tự sờ thấy khối ở bụng, đau bụng kèm theo biểu hiện tại các tổn thương di căn: sờ thấy hạch thượng đòn, đau tức hạ sườn phải, vàng da (di căn gan), ho, đau ngực (di căn phổi), đau xương (di căn xương), đau đầu, nôn, yếu liệt (di căn não), gầy sút cân, suy kiệt, tắc ruột (đau bụng từng cơn, bí đại tiện, nôn), thủng vỡ u dạ dày (đau bụng dữ dội, bụng cứng,.).
❖ Chẩn đoán:
Dựa vào các triệu chứng lâm sàng và cận lâm sàng.
Triệu chứng lâm sàng
Giai đoạn sớm: Triệu chứng nghèo nàn. Biểu hiện: đau tức vùng thượng vị, cảm giác đầy bụng, chậm tiêu, ợ hơi, chán ăn hoặc không có triệu chứng gì.
Giai đoạn tiến triển: đau bụng là dấu hiệu thường gặp nhất, đau không có chu kỳ, không liên quan đến bữa ăn. Buồn nôn, nôn nếu khối u ở môn vị và tâm vị. Khó nuốt nếu khối u ở tâm vị. Suy nhược toàn thân, gầy sút nhanh. Hội chứng thiếu máu: da xanh, niêm mạc nhợt. Hội chứng xuất huyết: nôn ra máu, đi ngoài phân đen. Khám có thể sờ thấy khối u hoặc đám cứng ở trên rốn. Phát hiện các dấu hiệu di căn: cổ trướng, gan to, di căn hạch thượng đòn.
Xét nghiệm cận lâm sàng
Nội soi thực quản- dạ dày ống mềm
Qua nội soi có thể quan sát trực tiếp tổn thương, xác định vị trí, hình dạng, kích thước tổn thương. Đồng thời, tiến hành sinh thiết tổn thương để chẩn đoán mô bệnh học.
Siêu âm, chụp cắt lớp vi tính ổ bụng-lồng ngực, cộng hưởng từ sọ não, xạ hình xương, PET/CT: đánh giá tổn thương di căn hạch, gan, buồng trứng, phổi, não,.
Xét nghiệm máu:
Công thức máu, đông máu, sinh hóa máu: đánh giá bilan, tình trạng thiếu máu,.
Xét nghiệm chất chỉ điểm khối u trong máu: CEA, CA72-4, CA 19-9,. có giá trị theo dõi, đánh giá kết quả điều trị.
Mô bệnh học và hóa mô miễn dịch
Giúp đánh giá thể mô bệnh học, mức độ biệt hóa, nhuộm hóa mô miễn dịch để đánh giá thụ thể Heu-2/neu, PD-L1.
Xét nghiệm sinh học phân tử: Xét nghiệm đột biến gen, giải trình tự nhiều gen.
❖ Chẩn đoán giai đoạn
Đánh giá giai đoạn theo hệ thống TNM của Hiệp hội Ung thư Hoa Kỳ (American Joint Committee on Cancer-AJCC) năm 2017.
T: U nguyên phát
Tis: ung thư biểu mô tại chỗ.
T1: u xâm lấn đến lớp niêm mạc, dưới niêm mạc.
T1a: u xâm lấn lớp niêm mạc.
T1b: u xâm lấn lớp dưới niêm mạc.
T2: u xâm lấn đến lớp cơ.
T3: u xâm lấn lớp dưới thanh mạc.
T4: u xâm lấn thanh mạc hoặc các cấu trúc lân cận.
T4a: u xâm lấn lớp thanh mạc.
T4b: u xâm lấn các cấu trúc lân cận.
N: Hạch vùng
N0: không có hạch.
N1: di căn 1-2 hạch.
N2: di căn 3-6 hạch.
N3: di căn trên 6 hạch vùng.
N3a: di căn 7-15 hạch.
N3b: di căn từ 16 hạch trở lên.
M: Di căn xa
M0: chưa di căn xa.
M1: di căn xa.
Bảng 4.7. Xếp loại giai đoạn theo TNM lâm sàng (cTNM) bệnh ung thư dạ dày
| Giai đoạn | cT | cN | M |
| 0 | Tis | N0 | M0 |
| I | T1, T2 | N0 | M0 |
| IIA | T1, T2 | N1,2,3 | M0 |
| IIB | T3, 4a | N0 | M0 |
| III | T3, 4a | N1,2,3 | M0 |
| IVA | T4b | N bất kỳ | M0 |
| IVB | T bất kỳ | N bất kỳ | M1 |
Bảng 4.8. Xếp loại giai đoạn bệnh sau mổ theo TNM (pTNM) bệnh ung thư dạ dày
| Giai đoạn | pT | pN | M |
| 0 | Tis | N0 | M0 |
| IA | T1 | N0 | M0 |
| IB | T1 | N1 | M0 |
| T2 | N0 | M0 | |
| IIA | T1 | N2 | M0 |
| T2 | N1 | M0 | |
| T3 | N0 | M0 | |
| IIB | T1 | N3a | M0 |
| T2 | N2 | M0 | |
| T3 | N1 | M0 | |
| T4a | N0 | M0 | |
| IIIA | T2 | N3a | M0 |
| T3 | N2 | M0 | |
| T4a | N1,2 | M0 | |
| T4b | N0 | M0 | |
| IIIB | T1,2 | N3b | M0 |
| T3, 4a | N3a | M0 | |
| T4b | N1,2 | M0 | |
| IIIC | T3, 4a | N3b | M0 |
| T4b | N3a,3b | M0 | |
| IV | T bất kỳ | N bất kỳ | M1 |
❖ Điều trị
Tùy thuộc giai đoạn bệnh, vị trí khối u, thể trạng người bệnh mà có thể áp dụng các phương pháp phẫu thuật, hóa trị, xạ trị, điều trị đích, miễn dịch.
Phẫu thuật là biện pháp cơ bản điều trị ung thư dạ dày: phẫu thuật triệt căn: cắt đoạn dạ dày và nạo vét hạch, phẫu thuật điều trị triệu chứng (nối vị tràng, mở thông hỗng tràng điều trị trong trường hợp thủng vỡ u gây viêm phúc mạc,.).
Xạ trị được chỉ định trong ưng thư dạ dày giai đoạn muộn hoặc di căn hạch, tuy nhiên ít được áp dụng.
Hóa trị được áp dụng:
- Điều trị trước mổ (hóa trị tiền phẫu) nhằm thu nhỏ kích thước u và tổn thương di căn, tạo điều kiện thuận lợi để phẫu thuật triệt căn;
- Điều trị bổ trợ sau mổ, nhằm diệt nốt những tế bào ung thư còn sót lại, hạn chế tiến triển, tái phát, di căn;
- Điều trị ở giai đoạn muộn: hóa trị giữ vai trò chủ đạo, có thể phối hợp với điều trị đích (kháng thể đơn dòng). Các thuốc hay sử dụng trong điều trị bệnh ung thư dạ dày bao gồm: cisplatin, carboplatin, oxaliplatin; leucovorin, etoposid, 5FU, doxorubicin, farmorubicin, paclitaxel, docetaxel, irinotecan, capecitabin, tegafur + gimeracil + oteracil potassium (TS one), tegafur + uracil (Ufur, Mefuform), triíluridm + tipiracil,…
Điều trị đích, miễn dịch: thường áp dụng ở giai đoạn muộn: đã có tổn thương di căn xa; việc lựa chọn phác đồ điều trị cần xem xét đến các xét nghiệm hóa mô miễn dịch và đột biến gen. Các thuốc hay sử dụng: trastuzumab, ramucirumab, pembrolizumab.
Một số phác đồ hóa chất:
+ Phác đồ FLOT:
Oxaliplatin 85 mg/m2, truyền tĩnh mạch ngày 1.
Leucovorin 200 mg/m2, truyền tĩnh mạch ngày 1.
5FU 2.600 mg/m2, truyền tĩnh mạch liên tục 24 giờ ngày 1.
Docetaxel 50 mg/m2, truyền tĩnh mạch ngày 1.
Chu kỳ 14 ngày.
+ Phác đồ EOX:
Epirubicin 50 mg/m2, truyền tĩnh mạch ngày 1.
Oxaliplatin 135 mg/m2, truyền tĩnh mạch ngày 1 trong 2 giờ.
Capecitabin 625 mg/m2/ngày, uống 2 lần/ngày, ngày 1-21.
Chu kỳ 21 ngày.
+ Phác đồ PC:
Paclitaxel 50 mg/m2, truyền tĩnh mạch ngày 1.
Carboplatin AUC 2, truyền tĩnh mạch ngày 1.
Hàng tuần x 5 tuần.
+ Phác đồ XELOX:
Capecitabin 1.000 mg/m2, uống 2 lần/ngày, ngày 1-14.
Oxaliplatin 130 mg/m2, truyền tĩnh mạch ngày 1.
Chu kỳ 21 ngày.
+ Phác đồ DCF:
Docetaxel 40 mg/m2, truyền tĩnh mạch ngày 1.
Leucovorin 400 mg/m2, truyền tĩnh mạch ngày 1.
5 FU 400 mg/m2, truyền tĩnh mạch ngày 1.
5 FU 1.000 mg/m2, truyền tĩnh mạch 24 giờ ngày 1.
Cisplatin 40 mg/m2, truyền tĩnh mạch ngày 3.
Chu kỳ 14 ngày.
+ Phác đồ docetaxel
Docetaxel 75-100 mg/m2, truyền tĩnh mạch ngày 1.
+ Phác đồ paclitaxel
Paclitaxel 135-250 mg/m2, truyền tĩnh mạch ngày 1. Chu kỳ 21 ngày.
Hoặc:
Paclitaxel 80 mg/m2, truyền tĩnh mạch hàng tuần. Chu kỳ 28 ngày.
+ Phác đồ irinotecan
Irinotecan 250-350 mg/m2, truyền tĩnh mạch ngày 1. Chu kỳ 21 ngày.
Hoặc:
Irinotecan 150-80 mg/m2, truyền tĩnh mạch ngày 1. Chu kỳ 14 ngày.
Hoặc:
Irinotecan 125 mg/m2, truyền tĩnh mạch ngày 1, 8. Chu kỳ 21 ngày.
+ Phác đồ IC:
Irinotecan 65 mg/m2, truyền tĩnh mạch ngày 1, 8.
Cisplatin 25-30 mg/m2, truyền tĩnh mạch ngày 1, 8. Chu kỳ 21 ngày.
Hoặc:
Irinotecan 65 mg/m2, truyền tĩnh mạch ngày 1, 8.
Cisplatin 25-50 mg/m2, truyền tĩnh mạch ngày 1. Chu kỳ 21 ngày.
+ Phác đồ docetaxel + irinotecan
Docetaxel 35 mg/m2, truyền tĩnh mạch ngày 1, 8.
Irinotecan 50 mg/m2, truyền tĩnh mạch ngày 1, 8. Chu kỳ 21 ngày.
+ Phác đồ irinotecan + capecitabin
Irinotecan 250 mg/m2, truyền tĩnh mạch ngày 1.
Capecitabin 1.000 mg/m2, uống 2 lần/ngày, ngày 1-14. Chu kỳ 21 ngày.
+ Phác đồ TS-one + cisplatin
TS-one 80 mg/m2, uống ngày 1-21.
Cisplatin 60 mg/m2, tĩnh mạch ngày 8. Chu kỳ 5 tuần.
Hoặc:
TS-one 80 mg/m2, uống ngày 1-14.
Cisplatin 60 mg/m2, tĩnh mạch ngày 1. Chu kỳ 3 tuần.
Hoặc:
TS-one 80 mg/m2, uống ngày 1-14.
Oxaliplatin 100 mg/m2, tĩnh mạch ngày 1. Chu kỳ 3 tuần.
+ Phác đồ TS one đơn chất
TS-one 80 mg/m2, uống ngày 1-28. Chu kỳ 6 tuần.
Hoặc:
TS-one 80 mg/m2, uống ngày 1-14. Chu kỳ 3 tuần.
+ Phác đồ capecitabin đơn chất
Capecitabine 1.000-1.250mg/m2, uống 2 lần/ngày, ngày 1-14. Chu kỳ 3 tuần.
Hoặc capecitabin 500mg, 3 lần/ngày, uống liên tục hàng ngày
Hoặc Capecitabin 625 mg, 2 lần/ngày uống liên tục hàng ngày
+ Phác đồ tegafur
Tegafur 360 mg/m2 (Ufur, Mefuform), uống ngày 1-14. Chu kỳ 3 tuần.
Một số phác đồ điều trị đích, miễn dịch:
+ Trastuzumab:
Trastuzumab 8 mg/kg, truyền tĩnh mạch lần đầu sau đó 6mg/kg mỗi 21 ngày phối hợp với hóa trị ở người bệnh có Heu-2/neu dương tính.
Hoặc trastuzumab 4 mg/kg truyền tĩnh mạch tuần 1 sau đó trastuzumab 2mg/kg hàng tuần phối hợp với hóa trị ở người bệnh có Heu-2/neu dương tính.
+ Ramucirumab:
Ramucirumab 8 mg/kg, tĩnh mạch ngày 1. Chu kỳ 14 ngày.
Hoặc:
Ramucirumab 8 mg/kg, tĩnh mạch ngày 1, 15. Chu kỳ 28 ngày.
+ Pembrolizumab:
Pembrolizumab 200 mg, truyền tĩnh mạch ngày 1. Chu kỳ 21 ngày.
2. HƯỚNG DẪN THỰC HÀNH DƯỢC LÂM SÀNG TRONG ĐIỀU TRỊ UNG THƯ
2.1 Nguyên tắc sử dụng, đường dùng và cơ chế kháng thuốc của các thuốc điều trị ung thư
❖ Nguyên tắc hóa trị ung thư
- Sử dụng thuốc ung thư cần phải tuyệt đối tuân thủ chế độ điều trị vì đây là các thuốc có hệ số an toàn điều trị thấp.
- Liều dùng thường được tính toán dựa vào diện tích bề mặt cơ thể. Có một số thuốc dùng theo thể trọng, AUC.
- Điều chỉnh liều dùng theo diện tích bề mặt cơ thể hoặc cân nặng; chức năng gan thận, độc tính của hóa trị (chủ yếu là tiểu cầu và bạch cầu trung tính).
- Cần đánh giá thể trạng của bệnh nhân, tác dụng phụ của chu kỳ hóa trị trước, xét nghiệm máu trước mỗi đợt hóa trị.
- Các hóa trị ung thư đều gây tác dụng không mong muốn nặng nề cho người bệnh, nên trong điều trị việc sử dụng thuốc/biện pháp dự phòng để giảm thiểu tác dụng không mong muốn của các hóa chất điều trị ung thư là rất quan trọng và cần được áp dụng đầy đủ.
❖ Đường dùng thuốc:
Đường uống: đa số là các thuốc viên điều trị nhắm đích.
Tiêm tĩnh mạch: phải thận trọng và cần có kinh nghiệm để đảm bảo thuốc chảy dễ dàng vào trong mạch máu. Nếu tiêm truyền tĩnh mạch thì tiêm vào tĩnh mạch chi trên có đường kính lớn. Nên đặt buồng tiêm truyền tĩnh mạch để truyền hoá chất cho người bệnh.
Vì lưu lượng máu tới khối u thấp nên phải sử dụng đường đưa thuốc thích hợp để đạt nồng độ điều trị mục tiêu tại mô và hạn chế vào tuần hoàn để tránh sinh độc tính.
- Đưa thuốc vào màng phổi hay phúc mạc
- Đưa thuốc vào bàng quang điều trị ung thư bàng quang
- Đưa thuốc vào động mạch gan điều trị ung thư gan, ung thư di căn gan
- Đưa thuốc vào động mạch cổ điều trị u não, u đầu cổ
- Đưa thuốc vào tĩnh mạch cửa điều trị ung thư di căn gan
- Đưa thuốc vào phúc mạc điều trị ung thư di căn phúc mạc
❖ Đề kháng thuốc
Sự đề kháng thuốc theo các cơ chế sau đây:
- Giảm thu nhận vào và tăng đẩy thuốc ra khỏi tế bào u. Sự đẩy thuốc ra khỏi tế bào thông qua glycoprotein. Nhiều thuốc đề kháng theo cách này.
- Tăng enzym mục tiêu: như tăng số lượng enzym dihydrofolat reductase (methotrexat).
- Thay đổi ái lực với enzym mục tiêu: methotrexat.
- Giảm hoạt hóa tiền thuốc: mercaptopurin và fluorouracil.
- Tăng quá trình làm mất hoạt tính của thuốc: cytarabin.
- Tăng sửa chữa ADN bị tổn thương: thuốc alkyl hóa, cisplatin.
- Tăng sinh tổng hợp pyrimidin và purin: thuốc kháng chuyển hóa.
- Tăng tạo glutathion do đó làm tăng phức hợp glutathion – thuốc: thuốc alkyl hóa, hợp chất platin và một số kháng sinh kháng u.
2.2 Vai trò của dược sĩ lâm sàng trong điều trị ung thư
Mục tiêu quản lý sử dụng thuốc trong điều trị ung thư là đảm bảo sử dụng đúng thuốc cho đúng người bệnh theo đúng liều và đúng dạng dùng của thuốc vào đúng thời điểm để đạt được kết quả mong muốn giúp cải thiện thời gian và/hoặc chất lượng cuộc sống của người bệnh. Để đạt được mục tiêu này đòi hỏi một cách tiếp cận toàn diện và có hệ thống bởi nhiều nhân viên y tế. Bác sĩ, điều dưỡng, dược sĩ, kỹ thuật viên dược và các nhân viên y tế khác phải phối hợp cùng nhau tạo thành một nhóm đa ngành để đảm bảo việc điều trị an toàn và đạt hiệu quả tối ưu cho người bệnh. Trong nhóm này, vai trò của dược sĩ chuyên khoa ung thư là không thể thiếu để cung cấp dịch vụ chăm sóc toàn diện cho người bệnh.
DSLS chuyên khoa ung thư cần tham gia tất cả các hoạt động lâm sàng như thẩm định y lệnh, đi buồng, giao ban, báo cáo ca lâm sàng, hội chẩn đa chuyên ngành, tham gia ý kiến về điều trị cho bệnh nhân ung thư, thông tin thuốc, báo cáo ADR, nghiên cứu khoa học, viết báo, đào tạo và tập huấn.
2.3 Thực hành DLS tại chuyên khoa ung thư
Mục này nêu các công việc cụ thể và kỹ năng cần có của một dược sĩ chuyên khoa ung thư. Mức độ áp dụng các nội dung này phụ thuộc vào sự kết hợp giữa tính chất của dược sĩ lâm sàng với đặc điểm của từng cơ sở thực hành như quy mô bệnh viện, bệnh viện đại học, bệnh viện đa khoa, trung tâm ung thư, bệnh viện chuyên ngành ung thư.
2.3.1. Các kiến thức và kỹ năng cần có của DSLS chuyên khoa ung thư
- Các loại bệnh ung thư
- Dịch tễ của các bệnh ung thư
- Tính chất của bệnh ung thư
- Đặc điểm lâm sàng của các bệnh ung thư
- Chẩn đoán bao gồm giải phẫu bệnh và mô bệnh học của từng kiểu ung thư
- Lựa chọn điều trị bao gồm cả lợi ích và nguy cơ của các phác đồ khác nhau
- Tác dụng không mong muốn và độc tính của các thuốc điều trị ung thư
- Nguyên tắc an toàn trong sử dụng thuốc điều trị ung thư
- Quy định điều trị và sử dụng thuốc điều trị ung thư tại từng nơi
- Kỹ năng tổng hợp và phân tích để liên kết các thông tin và bằng chứng với các quyết định dùng thuốc theo từng người bệnh
2.3.2 Công việc cụ thể DSLS trong điều trị ung thư
Ngoài các nội dung công việc chung như trong phần chương 1 của cuốn sách này, dược sĩ chuyên khoa ung thư cần lưu ý thêm các dữ liệu sau:
Bảng 4.9. Công việc cụ thể của dược sĩ lâm sàng trong điều trị ung thư
| Công việc | Cụ thể | Phụ lục |
| Khai thác tiền sử sử dụng thuốc và kiểm tra thông tin người bệnh | Kiểm tra thông tin trong bệnh án và hỏi người bệnh hoặc gia đình người bệnh:
– Các thuốc đã và đang sử dụng: thời gian dùng thuốc độ dài các phác đồ điều trị – Các kết quả xét nghiệm thường xuyên của người bệnh – Các thuốc người bệnh dùng mà không cần kê đơn – Sử dụng các phác đồ thay thế bổ sung – Chiều cao, cân nặng và diện tích bề mặt da (công thức Dubois hoặc Mosteller), nếu cân nặng của người bệnh thay đổi nhiều trong quá trình điều trị cần tính lại diện tích bề mặt cơ thể và tính lại liều – Chu kỳ điều trị thứ mấy |
Công thức Dubois: Diện tích bề mặt da (BSA) (m2) = 0,007184 x cân nặng0,425 x chiều cao0,725
Công thức Mosteller: Diện tích bề mặt da (BSA) (m2) = 0,016667 x cân nặng0,5 x chiều cao0,5 |
| Xem xét sử dụng thuốc | Thu thập các thông tin trong bệnh án:
– Chẩn đoán, giai đoạn bệnh, kết quả mô bệnh học,… – Phác đồ điều trị tuân theo hướng dẫn nào (của bệnh viện, BYT, hiệp hội,…). – Xem xét các kết quả xét nghiệm (như bạch cầu, tiểu cầu, chức năng gan, thận, mật độ xương, nước tiểu,…). – Đơn vị tính của thuốc là mg, g hay đơn vị quốc tế – Liều của thuốc tính theo mg/m2 hay theo mg/kg cân nặng hoặc AUC với carboplatin hoặc liều cố định – Liều được kê cho người bệnh có được tính toán chính xác (kiểm tra lại diện tích bề mặt cơ thể, cách tính liều thuốc, tình trạng bệnh nhân, chức năng gan, thận) – Kiểm tra chỉ định về loại và thể tích dung môi pha truyền, nồng độ dung dịch thuốc sẽ đạt được sau khi pha và tốc độ truyền được bác sĩ chỉ định có chính xác không. – Kiểm tra bổ sung đầy đủ dịch và các thuốc hỗ trợ theo từng phác đồ Bổ sung đầy đủ dịch là cần thiết trong các phác đồ: + Cyclophosphamid (với liều > 1000 mg/m2) + Cisplatin + Liều cao methotrexat – Khả năng tương tác, tương kỵ của các thuốc điều trị ung thư – Kiểm tra phác đồ chống nôn, chống sốc, chống dị ứng,. theo từng phác đồ ung thư – Kiểm tra việc sử dụng các thuốc chăm sóc giảm nhẹ |
– Phụ lục 4.1: tra cứu thông tin về chỉ định, dược động học và độc tính thường gặp của các thuốc điều trị 5 bệnh ung thư phổ biến tại Việt Nam
– Phụ lục 4.2: tra cứu về hiệu chỉnh liều thuốc cho bệnh nhân suy gan, thận – Phụ lục 4.3: tra cứu thông tin về dung môi, thể tích pha truyền và độ ổn định của dung dịch thuốc sau khi pha loãng của các thuốc điều trị 5 bệnh ung thư phổ biến tại Việt Nam. – Phụ lục 4.4: tra cứu hướng dẫn bù nước cho bệnh nhân dùng cisplatin – Phụ lục 4.5: tra cứu thời điểm sử dụng thuốc viên điều trị ung thư
|
| Giám sát sử dụng thuốc cho người bệnh | – Với các thuốc tiêm: kiểm tra tính tương hợp của các dung dịch pha thuốc, thể tích cần pha loãng có phù hợp, an toàn và kỹ thuật vô khuẩn trong quá trình pha chế và thực hiện thuốc
– Với thuốc uống: kiểm tra thời điểm uống thuốc so với bữa ăn, sử dụng các dạng bào chế đặc biệt, sử dụng trên bệnh nhân cần nuôi dưỡng qua sonde |
Sử dụng bảng kiểm tra dữ liệu pha chế thuốc điều trị ung thư theo phụ lục 4.9, bảng pha truyền và độ ổn định sau khi pha theo phụ lục 4.3, thời điểm uống thuốc viên theo phụ lục 4.5
Phụ lục 4.17 và 4.18 cung cấp thông tin về tiêu chuẩn trong giai đoạn chuẩn bị và thực hiện thuốc điều trị ung thư mà dược sĩ cần phổ biến cho nhân viên y tế tại chuyên khoa ung thư |
| Theo dõi đáp ứng của người bệnh | Đánh giá người bệnh về các vấn đề liên quan đến thuốc trong suốt quá trình điều trị của người bệnh, bao gồm các vấn đề sau:
– Đáp ứng của người bệnh với thuốc điều trị và đạt được hiệu quả điều trị dựa trên các triệu chứng, thay đổi kết quả xét nghiệm, hóa mô miễn dịch, gen,… – Các tác dụng không mong muốn của thuốc bao gồm dị ứng, độc tính nghiêm trọng đe doạ tính mạng hoặc độc tính chưa dự đoán được của các thuốc điều trị ung thư, tương tác thuốc tiềm tàng Thay đổi tình trạng lâm sàng của người bệnh (làm thay đổi dược động học của thuốc) dẫn đến cần thay đổi phác đồ hoặc chế độ liều điều trị Thay đổi hoàn cảnh của người bệnh dẫn đến trì hoãn hoặc ngừng điều trị |
– Phụ lục 4.10: cung cấp thông tin về độc tính thường gặp của thuốc điều trị ung thư
– Sử dụng bảng kiểm phụ lục 4.11 để theo dõi tác dụng không mong muốn – Phụ lục 4.12, 4.13, 4.14, 4.15, 4.16: cung cấp các thông tin về tác dụng không mong muốn gây tiêu chảy, giảm bạch cầu, thoát mạch, thiếu máu do các thuốc điều trị ung thư và các cách dự phòng, xử trí |
| Tư vấn cho người bệnh | – Thuốc điều trị ung thư có độc tính cao nên người bệnh ung thư cần hiểu đầy đủ để sử dụng đúng và an toàn
– Dược sĩ chuyên khoa ung thư nên tư vấn cho tất cả các người bệnh tối thiểu một lần trong quá trình điều trị – Tư vấn cho người bệnh ung thư và gia đình người bệnh về thuốc điều trị, thông tin cụ thể về an toàn và sự phù hợp của thuốc điều trị, thông tin để theo dõi, phòng ngừa và xử trí các tác dụng không mong muốn hay gặp của thuốc và thúc đẩy tuân thủ điều trị, bao gồm các thông tin sau (nếu có thể, nên cung cấp thông tin bằng văn bản): • Tên của thuốc và mục đích sử dụng cho người bệnh • Hình dạng, đóng gói và bảo quản thuốc • Đường dùng, liều các dùng (đặc biệt với thuốc uống) và độ dài đợt điều trị • Cần làm gì nếu lỡ quên một liều thuốc uống • Tác dụng không mong muốn, độc tính có thể gặp, cách theo dõi và phát hiện chúng, các thận trọng khi dùng thuốc • Các biện pháp để ngăn ngừa độc tính và tác dụng không mong muốn của thuốc • Cung cấp thông tin và cách liên lạc với nhân viên y tế để người bệnh người nhà người bệnh chủ động liên lạc và được tư vấn về các tác dụng không mong muốn DSLS đánh giá hiệu quả của việc tư vấn các kiến thức về thuốc cho người bệnh thông qua bộ câu hỏi và theo dõi Khi có thể, dược sĩ lâm sàng chuyên khoa ung thư cần củng cố kiến thức về thuốc và kỹ năng cho người bệnh bằng cách tư vấn lặp lại nhiều lần cho người bệnh – Báo cáo, ghi chép tóm tắt lại các lần tư vấn về thuốc cho người bệnh trong hồ sơ bệnh án |
Phụ lục 4.19: cung cấp chi tiết một số nội dung tư vấn cho người bệnh |
PHỤ LỤC CHƯƠNG 4. HƯỚNG DẪN THỰC HÀNH DƯỢC LÂM SÀNG TRONG CHUYÊN NGÀNH UNG THƯ
Phụ lục 4.1. Chỉ định, dược động học, độc tính thường gặp của các thuốc điều trị năm bệnh ung thư phổ biến tại Việt Nam
| Tên thuốc | Chỉ định | Các thông số dược động học | Độc tính chủ yếu | Lưu ý |
| Nhóm alkyl hóa | ||||
| Cyclophosphamid (Endoxan) | Tờ hướng dẫn sử dụng (Được phê duyệt tại Mỹ và châu Âu): các bệnh bạch cầu (bạch cầu cấp dòng lympho, bạch cầu mạn dòng lympho, bạch cầu cấp dòng tủy, bạch cầu mạn dòng tủy); u lympho Hodgkin; u lympho không Hodgkin; đa u tủy; ung thư vú; ung thư buồng trứng; ung thư phổi tế bào nhỏ; sarcom Ewing; u nguyên bào thần kinh
Một số chỉ định khác (sử dụng khác): ung thư bàng quang; ung thư não; ung thư cổ tử cung; ung thư nội mạc tử cung; u nguyên bào nuôi; sarcom xương; sarcom mô mềm; ung thư tinh hoàn; u Wilm |
Liên kết protein huyết tương 60-70%; t1/2 3-12 giờ;
< 15% thải trừ qua nước tiểu sau 24giờ |
Nôn, buồn nôn, tiêu chảy, sạm da, đen móng, rụng tóc, ức chế tủy xương, mệt mỏi, viêm bàng quang xuất huyết | |
| Nhóm chống chuyển hóa | ||||
| Capecitabin (Xeloda) | Tờ hướng dẫn sử dụng (được phê duyệt tại Mỹ và châu Âu): ung thư vú; ung thư đại trực tràng; ung thư dạ dày
Một số chỉ định khác (sử dụng khác): ung thư tụy |
Sinh khả dụng 80%; Liên kết protein huyết tương 50%;
t1/2 0,85-3,25 giờ; > 95% thải trừ qua nước tiểu |
Tiêu chảy, hội chứng bàn tay – bàn chân, suy tủy, viêm niêm mạc, độc tính trên thần kinh, co thắt động mạch vành | Chống chỉ định với bệnh nhân có Clcr < 30ml/phút. Cần hiệu chỉnh liều warfarin và kiểm tra các chỉ số đông máu hàng tuần cho người bệnh điều trị đồng thời warfarin và capecitabin. |
| Fluorouracil (Adrucil) | Tờ hướng dẫn sử dụng (được phê duyệt tại Mỹ và châu Âu): ung thư đại trực tràng; ung thư dạ dày; ung thư thực quản; ung thư vú; ung thư vùng đầu cổ; ung thư tụy
Một số chỉ định khác (sử dụng khác): ung thư bàng quang; ung thư buồng trứng; ung thư tinh hoàn; ung thư cổ tử cung; ung thư thận |
t1/2 8-14 phút;
85% bị bất hoạt bởi enzym dihydropyrimidin dehydrogenase (DPD); 90% thải trừ qua nước tiểu sau 1 giờ |
Nôn, buồn nôn, viêm niêm mạc, tiêu chảy, suy tủy, độc tính trên thần kinh, co thắt động mạch vành, viêm kết mạc | Người thiếu hụt DPD có thể gặp các độc tính nghiêm trọng khi điều trị với fluorouracil do kéo dài thời gian thải trừ fluorouracil. |
| Methotrexat (Otrexup) | Tờ hướng dẫn sử dụng (được phê duyệt tại Mỹ và châu Âu): bệnh bạch cầu cấp dòng lympho; u lympho không Hodgkin; ung thư vú; ung thư đầu và cổ; ung thư bàng quang, sarcom xương; u nguyên bào nuôi.
Một số chỉ định khác (sử dụng khác): ung thư dạ dày; ung thư phổi; ung thư tinh hoàn; ung thư thực quản |
Hấp thu gần như hoàn toàn ở liều thấp;
Liên kết protein huyết tương 50%; t1/2 3-10 giờ; 80-90% thải trừ qua nước tiểu sau 24 giờ |
Viêm niêm mạc, tiêu chảy, suy tủy, suy thận cấp, tăng men gan và bilirubin thoáng qua, viêm phổi, độc tính trên thần kinh, độc tính trên da do ánh sáng. | Thải trừ chủ yếu qua thận
Cần kiềm hóa nước tiểu, bù nước và điện giải đầy đủ để giảm độc tính của methotrexat. Lưu ý một số thuốc ức chế quá trình bài tiết của methotrexat như aspirin, NSAID, cephalosporin, penicillin, probenecid. |
| Gemcitabin (Gemzar) | Tờ hướng dẫn sử dụng (được phê duyệt tại Mỹ và châu Âu): ung thư tụy, ung thư phổi không tế bào nhỏ; ung thư vú; ung thư bàng quang; ung thư buồng trứng
Một số chỉ định khác (sử dụng khác): ung thư cổ tử cung; ung thư vùng đầu cổ; u lympho Hodgkin; u trung biểu mô màng phổi |
t1/2 42-94 phút;
70-90% thải trừ qua nước tiểu sau 24 giờ |
Nôn, buồn nôn, suy tủy, hội chứng giả cúm, tăng men gan và bilirubin, viêm phổi, phản ứng tiêm truyền, protein niệu, hội chứng tan máu-tăng ure máu và xuất huyết giảm tiểu cầu (hiếm gặp) | Không truyền kéo dài trên giờ để tránh độc tính trên tủy xương |
| Pemetrexed (Alimta) | Tờ hướng dẫn sử dụng (được phê duyệt tại Mỹ và châu Âu): u trung biểu mô màng phổi; ung thư phổi không tế bào nhỏ | Liên kết protein huyết tương 81%; t1/2 3,5 giờ | Suy tủy, phát ban, viêm niêm mạc, tiêu chảy, mệt mỏi | Cần dự phòng corticoid để giảm độc tính trên da, bổ sung acid folic và vitamin B12 để giảm độc tính trên máu của pemetrexed. |
| Các alkaloid thực vật và các sản phẩm tự nhiên khác | ||||
| Các alkaloid | ||||
| Vinblastin (Velban) | Tờ hướng dẫn sử dụng (được phê duyệt tại Mỹ và châu Âu): u lympho Hodgkin và không Hodgkin; ung thư vú; ung thư tinh hoàn; ung thư thận
Một số chỉ định khác (sử dụng khác): ung thư phổi không tế bào nhỏ; sarcom Kaposi; ung thư bàng quang; u nguyên bào nuôi |
Liên kết protein huyết tương 99%; t1/2 (pha cuối) 25 giờ;
95% thải trừ qua phân. |
Suy tủy, táo bón, rụng tóc, mệt mỏi, đau xương | |
| Vincristin (Oncovin) | Tờ hướng dẫn sử dụng (được phê duyệt tại Mỹ và châu Âu): các bệnh bạch cầu (bạch
cầu cấp dòng lympho, bạch cầu mạn dòng lympho, bạch cầu cấp dòng tủy, bạch cầu mạn dòng tủy); u lympho Hodgkin và không Hodgkin; đa u tủy; ung thư vú; ung thư đầu cổ; sarcom mô mềm; sarcom Ewing; u nguyên bào thần kinh; u Wilm; u nguyên bào tủy; u nguyên bào võng mạc Một số chỉ định khác (sử dụng khác): ung thư cổ tử cung; ung thư đại trực tràng; sarcom xương; ung thư buồng trứng; u nguyên bào nuôi; u nguyên bào gan. |
Liên kết protein huyết tương 75%;
t1/2 (pha cuối) 23-85 giờ; 80% thải trừ qua phân. |
Táo bón, buồn nôn, nôn, rụng tóc, nhìn đôi, suy tủy. | |
| Vinorelbin (Navelbin) | Tờ hướng dẫn sử dụng (được phê duyệt tại Mỹ và châu Âu): ung thư phổi không tế bào nhỏ; ung thư vú
Một số chỉ định khác (sử dụng khác): ung thư cổ tử cung; ung thư buồng trứng; ung thư phổi tế bào nhỏ |
Liên kết protein huyết tương 13,5%; t1/2 (pha cuối) 40 giờ;
Chủ yếu thải trừ qua phân. |
Rụng tóc, tiêu chảy, buồn nôn, nôn, mệt mỏi, độc tính trên thần kinh. | |
| Các taxan | ||||
| Docetaxel (Taxotere) | Tờ hướng dẫn sử dụng (được phê duyệt tại Mỹ và châu Âu): ung thư vú; ung thư phổi không tế bào nhỏ; ung thư tuyến tiền liệt; ung thư dạ dày; ung thư vùng đầu cổ
Một số chỉ định khác (sử dụng khác): ung thư buồng trứng; sarcom xương; u nguyên bào thần kinh; sarcom Ewing |
Liên kết protein huyết tương > 80%; t1/2 11,1-18,5 giờ;
>70% thải trừ qua phân. |
Suy tủy, quá mẫn, phù, rụng tóc, phát ban, tiêu chảy, buồn nôn, nôn, mệt mỏi, độc tính trên thần kinh | Cần dự phòng với corticoid trước khi dùng docetaxel. |
| Paclitaxel (Anzatax) | Tờ hướng dẫn sử dụng (được phê duyệt tại Mỹ và châu Âu): ung thư vú; ung thư buồng trứng; ung thư phổi không tế bào nhỏ; sarcom Kaposi liên quan đến AIDS .
Một số chỉ định khác (sử dụng khác): ung thư phổi tế bào nhỏ; ung thư thực quản; ung thư bàng quang; ung thư vùng đầu cổ; ung thư cổ tử cung; ung thư nội mạc tử cung |
Liên kết protein huyết tương 89-98%; t1/2 (pha cuối) 3-52,7 giờ;
71% thải trừ qua phân. |
Suy tủy, quá mẫn, buồn nôn và nôn, rụng tóc, đau khớp, đau cơ, độc tính trên thần kinh ngoại biên | Cần dự phòng với corticoid, thuốc kháng H2 và kháng histamin trước khi dùng paclitaxel. |
| Các kháng sinh độc tế bào và các chất liên quan | ||||
| Doxorubicin (Adriamycin) | Tờ hướng dẫn sử dụng (được phê duyệt tại Mỹ và châu Âu): ung thư phổi tế bào nhỏ; ung thư vú; ung thư buồng trứng; ung thư nội mạc tử cung; ung thư bàng quang; ung thư tuyến giáp; ung thư dạ dày; sarcom xương; sarcom mô mềm; sarcom Ewing; u lympho Hodgkin và không Hodgkin tuyến tiền liệt; bạch cầu cấp tính dòng tủy; u nguyên bào thần kinh; khối u Wilm; đa u tủy
Một số chỉ định khác (sử dụng khác): ung thư đầu và cổ; ung thư gan; ung thư tinh hoàn; ung thư biểu mô đường niệu; ung thư tuyến tiền liệt; ung thư tuyến ức |
Liên kết protein huyết tương 70%; t1/2 20-48 giờ;
40-50% thải trừ qua phân. |
Nôn, buồn nôn, rụng tóc, viêm niêm mạc, suy tủy, độc tính trên tim. | |
| Epirubicin (Ellence) | Tờ hướng dẫn sử dụng (được phê duyệt tại Mỹ và châu Âu): ung thư vú; ung thư buồng trứng; ung thư phổi tế bào nhỏ; ung thư dạ dày; ung thư bàng quang
Một số chỉ định khác (sử dụng khác): ung thư phổi không tế bào nhỏ; sarcom mô mềm; u lympho Hodgkin và không Hodgkin. |
Liên kết protein huyết tương 77%; t1/2 33 giờ;
9-10% thải trừ qua nước tiểu sau 48 giờ Thải trừ chủ yếu qua mật |
Suy tủy, độc tính trên tim. | |
| Mitomycin (Mutamycin) | Tờ hướng dẫn sử dụng (được phê duyệt tại Mỹ và châu Âu): ung thư vú; ung thư dạ dày; ung thư tụy; ung thư phổi không tế bào nhỏ.
Một số chỉ định khác (sử dụng khác): ung thư đại tràng, ung thư bàng quang; ung thư vùng đầu và cổ; ung thư cổ tử cung |
t1/2 50 phút. | Giảm bạch cầu, tiểu cầu, độc tính trên thận. | |
| Các chất chống ung thư khác | ||||
| Hợp chất platin | ||||
| Cisplatin (Platinol) | Tờ hướng dẫn sử dụng (được phê duyệt tại Mỹ và châu Âu): ung thư tinh hoàn; ung thư bàng quang; ung thư buồng trứng; ung thư phổi không tế bào nhỏ; ung thư tế bào vảy vùng đầu cổ; ung thư cổ tử cung
Một số chỉ định khác (sử dụng khác): ung thư thực quản; ung thư dạ dày; u nguyên bào nuôi; ung thư túi mật; ung thư gan; ung thư phổi tế bào nhỏ; u lympho Hodgkin và không Hodgkin; u thần kinh nội tiết; ung thư vòm họng; sarcom xương; ung thư biểu mô đường niệu; ung thư tuyến tiền liệt; ung thư tuyến ức; ung thư nội mạc tử cung |
Liên kết protein huyết tương > 90%; t1/2 10-30 phút (pha đầu) và 1-5 ngày (pha cuối);
23-50% thải trừ qua nước tiểu sau 24 giờ |
Nôn, buồn nôn, độc tính trên thận, tai, thần kinh, ức chế tủy xương | Bù nước và điện giải đầy đủ để tránh độc tính trên thận |
| Carboplatin (Paraplatin) | Tờ hướng dẫn sử dụng (được phê duyệt tại Mỹ và châu Âu): ung thư buồng trứng; ung thư phổi tế bào nhỏ
Một số chỉ định khác (sử dụng khác): ung thư cổ tử cung; ung thư nội mạc tử cung; ung thư tinh hoàn; ung thư đầu và cổ; ung thư bàng quang; sarcom Ewing; u lympho không Hodgkin; ung thư phổi không phải tế bào nhỏ; u nguyên bào nuôi; u Wilms; sarcom xương |
Liên kết protein huyết tương 24-50%; t1/2 12-98 phút (pha đầu) và 8-40 giờ (pha cuối);
54-82% thải trừ qua nước tiểu sau giờ |
Nôn, buồn nôn, rụng tóc, ức chế tủy xương | i t độc tính hơn so với cisplatin |
| Oxaliplatin (Eloxatin) | Tờ hướng dẫn sử dụng (được phê duyệt tại Mỹ và châu Âu): ung thư đại trực tràng Một số chỉ định khác (sử dụng khác): ung thư vú; ung thư dạ dày; ung thư đầu và cổ; ung thư phổi không phải tế bào nhỏ; u lympho không Hodgkin; ung thư buồng trứng; ung thư tụy; ung thư tinh hoàn | Liên kết protein huyết tương 85%; t1/2 26 phút (pha đầu) và 38-47 giờ (pha cuối);
> 50% thải trừ qua nước tiểu sau 24giờ |
Nôn, buồn nôn, dị cảm | |
| Các chất ức chế topoisomerase | ||||
| Etoposid (Etopophos) | Tờ hướng dẫn sử dụng (được phê duyệt tại Mỹ và châu Âu): ung thư phổi tế bào nhỏ; ung thư tinh hoàn; u lympho Hodgkin và không Hodgkin; ung thư buồng trứng; u nguyên bào nuôi; bạch cầu cấp dòng tủy Một số chỉ định khác (sử dụng khác): ung thư bàng quang; ung thư cổ tử cung; ung thư vùng đầu cổ; ung thư phổi không phải tế bào nhỏ; ung thư tiền liệt tuyến; sarcom Ewing; bạch cầu cấp dòng lympho; u thần kinh nội tiết; u Wilms. | Đạt đỉnh nồng độ sau 1- 1,5 giờ;
Liên kết protein huyết tương 95%; t1/2 (pha cuối) 7 giờ; 44-60% thải trừ qua nước tiểu |
Buồn nôn, nôn, rụng tóc, mệt mỏi, suy tủy | |
| Irinotecan (Campto) | Tờ hướng dẫn sử dụng (được phê duyệt tại Mỹ và châu Âu): ung thư đại trực tràng Một số chỉ định khác (sử dụng khác): ung thư tụy; ung thư phổi; ung thư thực quản; ung thư dạ dày; ung thư cổ tử cung; u thần kinh đệm | Liên kết protein huyết tương 1-65%; t1/2 12 phút (pha đầu) và 14,2 giờ (pha cuối) | Tiêu chảy, suy tủy . | Dự phòng độc tính cholinergic cấp của irinotecan bằng atropin. |
| Topotecan (Hycamtin) | Tờ hướng dẫn sử dụng (được phê duyệt tại Mỹ và châu Âu): ung thư cổ tử cung; ung thư buồng trứng; ung thư phổi tế bào nhỏ
Một số chỉ định khác (sử dụng khác): bệnh bạch cầu cấp dòng tủy; bệnh bạch cầu mạn dòng tủy; u thần kinh đệm; ung thư phổi không phải tế bào nhỏ; đa u tủy; sarcom Ewing; u nguyên bào thần kinh; ung thư tụy |
Liên kết protein huyết tương 35%; t1/2 2-3 giờ; 20-60% thải trừ qua nước tiểu | Suy tủy | Giảm liều 50% cho bệnh nhân suy thân |
| Các kháng thể đơn dòng | ||||
| Atezolizumab (Tecentriq) | Tờ hướng dẫn sử dụng (được phê duyệt tại Mỹ và châu Âu): ung thư biểu mô tiết niệu; ung thư phổi không tế bào nhỏ sau điều trị hoá chất | t1/2 27 ngày. | Buồn nôn, nôn, tiêu chảy, ho, nhiễm khuẩn tiết niệu, phát ban, đau khớp, đau lưng, mệt mỏi | |
| Bevacizumab (Avastin) | Tờ hướng dẫn sử dụng (được phê duyệt tại Mỹ và châu Âu): ung thư đại trực tràng; ung thư vú; ung thư thận; ung thư buồng trứng, ống dẫn trứng, phúc mạc; ung thư cổ tử cung; ung thư phổi không tế bào nhỏ Một số chỉ định khác (sử dụng khác): ung thư vùng đầu cổ; ung thư tuyến tiền liệt | t1/2 18 ngày với nữ và 20 ngày với nam | Thủng đường tiêu hóa, xuất huyết, huyết khối động mạch Giảm bạch cầu, sốt do giảm bạch cầu Hạ magie máu, khô da, mất màu da. Protein niệu Mệt mỏi | |
| Cetuximab (Erbitux) | Tờ hướng dẫn sử dụng (được phê duyệt tại Mỹ và châu Âu): ung thư đại trực tràng di căn thuộc type RAS tự nhiên, có biểu lộ EGFR; ung thư tế bào vảy vùng đầu và cổ | t1/2 70- 100 giờ. | Hạ Magie máu, tăng men gan, phản ứng ngoài da, phản ứng tiêm truyền, viêm kết mạc | Dự phòng corticoid và thuốc kháng histamin ít nhất giờ trước khi truyền cetuximab. |
| Nivolumab (Yervoy) | Tờ hướng dẫn sử dụng (được phê duyệt tại Mỹ và châu Âu): u hắc tố; ung thư thận; ung thư biểu mô tiết niệu; ung thư phổi không tế bào nhỏ; ung thư vùng đầu cổ; u lympho Hodgkin; ung thư đại trực tràng; ung thư tế bào gan. | t1/2 25 ngày. | Mệt mỏi, tiêu chảy, nôn, buồn nôn, tiêu chảy, phát ban, ngứa | |
| Panitumumab (Opdivo) | Tờ hướng dẫn sử dụng (được phê duyệt tại Mỹ và châu Âu): ung thư đại trực tràng có type RAS tự nhiên. | t1/2 7,5 ngày. | Viêm kết mạc, viêm quanh móng, ho, rối loạn tiêu hóa, buồn nôn, nôn, độc tính trên da, mệt mỏi | |
| Pembrolizumab (Keytruda) | Tờ hướng dẫn sử dụng (được phê duyệt tại Mỹ và châu Âu): u hắc tố; ung thư phổi không tế bào nhỏ; u lympho Hodgkin; ung thư biểu mô đường tiết niệu; ung thư dạ dày; ung thư vùng đầu cổ; ung thư cổ tử cung | t1/2 22 ngày. | Nôn, buồn nôn, rối loạn tiêu hóa, nổi ban, đau cơ, đau khớp, mệt mỏi, suy giáp | |
| Pertuzumab (Perjeta) | Tờ hướng dẫn sử dụng (được phê duyệt tại Mỹ và châu Âu): ung thư vú | t1/2 18 ngày. | Viêm mũi họng, sốt giảm bạch cầu, phản ứng tiêm truyền, độc tính trên thần kinh, nôn, buồn nôn, rối loạn tiêu hóa. | |
| Trastuzumab (Herceptin) | Tờ hướng dẫn sử dụng (được phê duyệt tại Mỹ và châu Âu): ung thư vú, ung thư dạ dày và ung thư miệng nối dạ dày – thực quản có HER dương tính | t1/2 28,5 ngày. | Sụt cân, mất ngủ, độc tính trên huyết học | |
| Các chất ức chế protein kinase | ||||
| Afatinib (Giotrif) | Tờ hướng dẫn sử dụng (được phê duyệt tại Mỹ và châu Âu): ung thư phổi không tế bào nhỏ | Liên kết protein huyết tương 95%;
t1/2 37giờ; 85,4 % thải trừ qua phân |
Chảy máu cam, tiêu chảy, buồn nôn, nôn, đau dạ dày, độc tính trên da. | Dùng trước bữa ăn ít nhất 1 giờ hoặc sau bữa ăn ít nhất 3 giờ |
| Crizotinib (Xalkori) | Tờ hướng dẫn sử dụng (được phê duyệt tại Mỹ và châu Âu): ung thư phổi không tế bào nhỏ có đột biến ALK hoặc ROS1. | Sinh khả dụng 43%, sinh khả dụng giảm khi uống cùng bữa ăn có hàm lượng chất béo cao;
Liên kết protein huyết tương 91%; t1/2 42 giờ (pha cuối); 63% thải trừ qua phân. |
Nôn, buồn nôn, tiêu chảy, táo bón, phù, mệt mỏi, tăng men gan. | |
| Erlotinib (Tarceva) | Tờ hướng dẫn sử dụng (được phê duyệt tại Mỹ và châu Âu): ung thư phổi không tế bào nhỏ; ung thư tụy | Sinh khả dụng 59%, sinh khả dụng tăng khi uống thuốc cùng bữa ăn;
Liên kết protein huyết tương 95%; t1/2 36,2 giờ; > 90% thải trừ qua phân. |
Tiêu chảy, nổi ban, rối loạn chức năng gan | Dùng trước bữa ăn ít nhất 1 giờ hoặc sau bữa ăn ít nhất 2 giờ |
| Gefitinib (Iressa) | Tờ hướng dẫn sử dụng (được phê duyệt tại Mỹ và châu Âu): ung thư phổi không tế bào nhỏ có đột biến EGFR
Một số chỉ định khác (sử dụng khác): ung thư vùng đầu cổ |
Sinh khả dụng 59%; Liên kết protein huyết tương 90%; t1/2 41 giờ;
Thải trừ chủ yếu qua phân. |
Mệt mỏi, chán ăn, tiêu chảy, tăng men gan, độc tính trên da | |
| Osimertinib (Tagrisso) | Tờ hướng dẫn sử dụng (được phê duyệt tại Mỹ và châu Âu): ung thư phổi không tế bào nhỏ có đột biến EGFR; ung thư phổi không tế bào nhỏ có đột biến EGFR T M | Sinh khả dụng 80%;
Liên kết protein huyết tương 94,7 %; t1/2 44giờ; 67,8% thải trừ qua phân. |
Tiêu chảy, đau dạ dày, độc tính trên da, độc tính trên huyết học. | |
| Regorafenib (Stivarga) | Tờ hướng dẫn sử dụng (được phê duyệt tại Mỹ và châu Âu): ung thư tế bào gan; ung thư đại trực tràng; u mô đệm đường tiêu hóa | Sinh khả dụng 69-83%;
Liên kết protein huyết tương >99%; t1/2 20-30 giờ; 71% thải trừ qua phân. |
Hội chứng bàn tay-bàn chân, mệt mỏi, tiêu chảy, tăng huyết áp, nhiễm trùng | Nên uống thuốc sau bữa ăn nhẹ, ít béo. |
| Sorafenib (Nexavar) | Tờ hướng dẫn sử dụng (được phê duyệt tại Mỹ và châu Âu): ung thư tế bào gan; ung thư thận; ung thư tuyến giáp | Sinh khả dụng 38 – 49%;
Liên kết protein huyết tương > 99%; t1/2 25-48 giờ; 77% thải trừ qua phân. |
Tiêu chảy, mệt mỏi, rụng tóc, nhiễm trùng, hội chứng bàn tay- bàn chân và nổi ban | Tránh uống thuốc sau bữa ăn giàu chất béo |
| Hormon và các chất liên quan | ||||
| Thuốc đối kháng chọn lọc trên thụ thể estrogen | ||||
| Fulvestrant (Faslodex) | Tờ hướng dẫn sử dụng (được phê duyệt tại Mỹ và châu Âu): ung thư vú có thụ thể hormon dương tính | Hấp thu chậm và đạt đỉnh nồng độ sau 5 ngày;
Liên kết protein huyết tương 99%; Thải trừ chủ yếu qua phân. |
Phản ứng tại vị trí tiêm truyền, nóng bừng, rối loạn tiêu hóa | Tiêm bắp chậm (cơ mông) |
| Tamoxifen (Nolvadex) | Tờ hướng dẫn sử dụng (được phê duyệt tại Mỹ và châu Âu): ung thư vú
Một số chỉ định khác (sử dụng khác): ung thư tụy |
Sinh khả dụng 30%; t1/2 (pha cuối) 4-11 ngày;
Nồng độ thuốc tập trung cao tại gan, phổi, não, tụy, da và xương |
Nóng bừng, xuất huyết âm đạo | Tamoxifen làm tăng nguy cơ ung thư nội mạc tử cung Nguy cơ này phụ thuộc vào thời gian dùng tamoxifen (3,1% với điều trị bổ trợ tamoxifen 10 năm) |
| Thuốc ức chế aromatase | ||||
| Anastrozol (Arimidex) | Tờ hướng dẫn sử dụng (được phê duyệt tại Mỹ và châu Âu): ung thư vú có thụ thể hormon dương tính ở phụ nữ mãn kinh | Liên kết protein huyết tương 40%; t1/2 50 giờ;
85% thải trừ qua nước tiểu |
Nóng bừng, nổi ban, loãng xương | Có thể sử dụng biphosphonat để ngăn ngừa nguy cơ gãy xương |
| Letrozol (Femara) | Tờ hướng dẫn sử dụng (được phê duyệt tại Mỹ và châu Âu): ung thư vú có thụ thể hormon dương tính ở phụ nữ mãn kinh | Sinh khả dụng 99%; Đạt nồng độ đỉnh sau 1 giờ;
Liên kết protein huyết tương 80%; t1/2 (pha cuối) 2-4 ngày; 88% thải trừ qua nước tiểu |
Nóng bừng, nổi ban, loãng xương | Có thể sử dụng biphosphonat để ngăn ngừa nguy cơ gãy xương |
| Exemestan (Aromasin) | Tờ hướng dẫn sử dụng (được phê duyệt tại Mỹ và châu Âu): ung thư vú có thụ thể hormon dương tính ở phụ nữ mãn kinh | Thức ăn làm tăng sinh khả dụng 40%;
Liên kết protein huyết tương 90%; t1/2 (pha cuối) 24 giờ; Thải trừ qua gan và thận |
Nóng bừng, mệt mỏi, đau khớp, nôn | Uống cùng bữa ăn |
| Thuốc ức chế mTOR | ||||
| Everolimus (Afinitor) | Tờ hướng dẫn sử dụng (được phê duyệt tại Mỹ và châu Âu): ung thư thận; ung thư vú; u thần kinh nội tiết | Sinh khả dụng giảm khi uống cùng bữa ăn có hàm lượng chất béo cao; Chuyển hóa bởi CYP3A4;
Thải trừ chủ yếu qua phân. |
Mệt mỏi, khô da, buồn nôn, nôn, viêm niêm mạc, tăng lipid máu, tăng đường máu, quá mẫn, độc tính trên phổi | Chống chỉ định trên bệnh nhân có Childpugh C. |
| Thuốc tương tự hormon giải phóng gonadotropin | ||||
| Goserelin (Zoladex) | Tờ hướng dẫn sử dụng (được phê duyệt tại Mỹ và châu Âu): ung thư tuyến tiền liệt; ung thư vú | Liên kết protein huyết tương thấp; t1/2 5 giờ;
Thải trừ chủ yếu qua nước tiểu |
Nóng bừng, rối loạn cương dương, tăng tiết mồ hôi | |
Phụ lục 4.2. Hiệu chỉnh liều trên bệnh nhân suy thận, suy gan
Các chỉ số dược động học công bố trong các tài liệu về thuốc là những giá trị thu được từ các thử nghiệm trên người tình nguyện khỏe mạnh. Ở những đối tượng có những bất thường về chức năng của hai cơ quan chính đảm nhận chức năng thải trừ thuốc là gan và thận, số phận của thuốc trong cơ thể bị thay đổi đáng kể, do đó không thể sử dụng mức liều hoặc nhịp đưa thuốc như khi điều trị cho bệnh nhân không tổn thương gan, thận. Mặt khác, việc sử dụng thuốc điều trị ung thư rất phức tạp do thuốc có phạm vi điều trị hẹp, độc tính cao dù ở liều điều trị và bệnh nhân ung thư là nhóm bệnh nhân dễ xuất hiện phản ứng có hại do họ có khả năng chịu đựng kém.
Chính vì vậy, việc hiệu chỉnh liều trên đối tượng bệnh nhân ung thư có suy giảm chức năng gan, thận có ý nghĩa quan trọng.
Bảng 1.PL4.2. Chỉnh liều của một số thuốc điều trị ung thư trên bệnh nhân suy thận, suy gan
| STT | Hoạt chất | Khoảng liều trên bệnh nhân có chức năng gan – thận bình thường | Chỉnh liều trên bệnh nhân suy thận dựa trên MLCT (ml/phút) | Chỉnh liều trên bệnh nhân suy gan dựa trên xét nghiệm chức năng gan (Bilirubin huyết thanh (mg/dl) và/hoặc Transaminase (AST, ALT)) |
| 1 | Crizotinib | 250 mg/lần x 2 lần/ngày | Không có thông tin về hiệu chỉnh liều trong các tài liệu đã tham khảo* | – AST > ULN và bilirubin huyết thanh ≤ ULN hoặc bất kỳ AST và ULN < bilirubin huyết thanh ≤ 1,5xULN: không cần hiệu chỉnh liều
– AST bất kỳ, 1,5xULN < bilirubin huyết thanh ≤ 3xULN: khuyến cáo liều 200 mg/lần x 2 lần/ngày – AST bất kỳ và bilirubin huyết thanh > 3xULN: 250 mg/lần/ngày |
| 2 | Bleomycin | 15-30 IU/m2 | – MLCT >50: Không cần chỉnh liều
– MLCT (41-4 9): giảm 30% liều bình thường – MLCT (31-40): giảm 40% liều bình thường – MLCT (20-30): giảm 45% liều bình thường – MLCT (10-20): giảm 55% liều bình thường – MLCT (5- 10): giảm 60% liều bình thường |
Không có thông tin về hiệu chỉnh liều trong các tài liệu đã tham khảo* |
| 3 | Carboplatin | 300-400 mg/m2 | – MLCT > 60: Không cần hiệu chỉnh liều
– MLCT (41-60): 250 mg/m2 – MLCT (20-40): 200 mg/m2 – MLCT < 20: Chống chỉ định |
Không có thông tin về hiệu chỉnh liều trong các tài liệu đã tham khảo* |
| 4 | Capecitabin | 1.000-1.250 mg/m2 | – MLCT >50: Không cần hiệu chỉnh liều
– MLCT (30-50): Giảm 25% liều bình thường khi liều khởi đầu là 1.250 mg/m2, không cần hiệu chỉnh liều khi liều khởi đầu là 1.000 mg/m2 – MLCT <30: Chống chỉ định |
– Không có thông tin đầy đủ trong các tài liệu về hiệu chỉnh liều
– Nên ngừng thuốc nếu bilirubin tăng 3xULN có liên quan đến điều trị hoặc AST, ALT tăng 2,5xULN có liên quan đến điều trị |
| 5 | Cisplatin | 10-90 mg/m2 (Liều tối đa 120 mg/m2) | – MLCT >50: Không cần hiệu chỉnh liều
– MLCT (10-50): Giảm 25% liều bình thường – MLCT < 10: Giảm 50 % liều bình thường – Lọc máu: Giảm 50 % liều bình thường, cần bổ sung liều sau lọc máu vào ngày lọc máu – Lọc màng bụng: Giảm 50 % liều bình thường – Lọc máu liên tục: Giảm 25% liều bình thường |
Không có thông tin về hiệu chỉnh liều trong các tài liệu đã tham khảo* |
| 6 | Cyclophosphamid | Liều thấp: 80-240 mg/m2
Liều trung bình: 400-600 mg/m2 Liều cao: 800- 1.600 mg/m2 |
MLCT < 10: Giảm 50% liều bình thường | Bilirubin huyết thanh (3,1-5mg/dl): giảm 25% liều bình thường |
| 7 | Docetaxel | 75-100 mg/m2 | Không có thông tin về hiệu chỉnh liều trong các tài liệu đã tham khảo* | – ALT, AST >1,5xULN và ALP > 2,5xULN: 75 mg/m2
– Bilirubin huyết thanh >ULN và/hoặc ALT, AST > 3,5xULN và ALP > 6xULN: không nên sử dụng |
| 8 | Doxorubicin | Điều trị đơn độc: 60-75 mg/m2
Điều trị phối hợp: 30-40 mg/m2 |
Không có thông tin về hiệu chỉnh liều trong các tài liệu đã tham khảo* | – Bilirubin 1,2-3,0 mg/dl: giảm 50% liều bình thường
– Bilirubin >3 mg/dl: giảm 75% liều bình thường |
| 9 | Epirubicin | Dùng đơn độc: liều khởi đầu 60 -120 mg/m2 | Không có thông tin về hiệu chỉnh liều trong các tài liệu đã tham khảo* | – Bilirubin 1,2-3,0 mg/dl hoặc AST tăng 2-4 lần so với ULN: giảm 50% liều bình thường
– Bilirubin >3 mg/dl hoặc AST tăng 4 lần ULN: giảm 75% liều bình thường |
| 10 | Etoposid | 50-150 mg/m2 | – MLCT >50: không cần hiệu chỉnh liều
– MLCT (15-50): giảm 25% liều bình thường – MLCT <15: không có dữ liệu, cần xem xét giảm liều nhiều hơn |
Không có thông tin về hiệu chỉnh liều trong các tài liệu đã tham khảo* |
| 11 | Erlotinib | 100-150 mg | Không sử dụng thuốc trên người bệnh có MLCT <15 | Không sử dụng thuốc trên bệnh nhân suy gan nặng |
| 12 | Everolimus | 10 mg | Không có thông tin về hiệu chỉnh liều trong các tài liệu đã tham khảo* | – Suy gan nhẹ (Child-Pugh A): 7,5 mg/ngày
– Suy gan trung bình (Child-Pugh B): 5 mg/ngày – Suy gan nặng (Child-Pugh C): không khuyến cáo sử dụng . Nếu lợi ích vượt trội nguy cơ, liều dùng không quá 2,5 mg/ngày |
| 13 | Ifosfamid | 1,2-2,4 g/m2 | – MLCT >50: không cần hiệu chỉnh liều
– MLCT (10-50): giảm 25% liều bình thường – MLCT <10: giảm 50 % liều bình thường – Lọc máu: Giảm gần 50 % liều bình thường – Lọc màng bụng: Giảm 50 % liều bình thường |
Không có thông tin về hiệu chỉnh liều trong các tài liệu đã tham khảo* |
| 14 | Methotrexat | – Liều thấp: <100mg/m2
– Liều trung bình: 100-1.000mg/m2 – Liều cao: >1.000mg/m2 |
– MLCT > 80: 100% liều
– MLCT (61-80): 75% liều – MLCT (51-60): 70% liều – MLCT (10-50): 30-50% liều – MLCT <10: chống chỉ định |
Chống chỉ định ở người bệnh có bilirubin > 5mg/dL |
| 15 | Oxaliplatin | 85 mg/m2 da, lặp lại mỗi 2 tuần trong 12 chu kỳ (6 tháng) | – Suy thận nhẹ đến trung bình: không cần hiệu chỉnh liều
– Suy thận nặng: chống chỉ định |
Không có thông tin về hiệu chỉnh liều trong các tài liệu đã tham khảo* |
| 16 | Paclitaxel | 100-300 mg/m2 | Không có thông tin về hiệu chỉnh liều trong các tài liệu | AST, ALT > 10xULN hoặc bilirubin > 5xULN: chống chỉ định |
| 17 | Pamidronat | 15-90 mg | – MLCT ≥30: không cần chỉnh liều
– MLCT <30: không khuyến cáo sử dụng |
Không có thông tin về hiệu chỉnh liều trong các tài liệu đã tham khảo* |
| 18 | Pemetrexed | 500 mg/m2 | – MLCT >45: không cần hiệu chỉnh liều
– MLCT <45: không khuyến cáo sử dụng |
Không có thông tin về hiệu chỉnh liều trong các tài liệu ở người bệnh có bilirubin > 1,5xULN kèm ASAT/ALAT > 3xULN |
| 19 | Topotecan | 1,5 mg/m2 | – MLCT (40-60): không cần hiệu chỉnh liều
– MLCT (20-39): giảm liều 50% – MLCT <20: dữ liệu không đầy đủ để khuyến cáo liều thuốc sử dụng |
Không có thông tin về hiệu chỉnh liều trong các tài liệu đã tham khảo* |
| 20 | Regorafenib | 80-160 mg | Không có thông tin về hiệu chỉnh liều trong các tài liệu đã tham khảo* | – AST, ALT tăng ≤ 5xULN: giám sát chức năng gan hàng tuần cho đến khi AST, ALT < 3xULN hoặc trở về giá trị trước khi điều trị .
– 5xULN < AST, ALT ≤ 20xULN: ngừng thuốc, giám sát chức năng gan hàng tuần cho đến khi AST, ALT < 3xULN hoặc trở về giá trị trước khi điều trị – Bắt đầu dùng lại: nếu lợi ích lớn hơn nguy cơ độc tính gan . Khởi đầu điều trị lại với liều 40 mg và giám sát chức năng gan hàng tuần trong ít nhất 4 tuần. Nếu tái xuất hiện tăng men gan, ngừng hẳn điều trị. – AST, ALT > 20xULN: ngừng hẳn điều trị. – AST, ALT > 3xULN kèm theo bilirubin > 2xULN: ngừng hẳn điều trị. |
| 21 | Vinorelbin | 25-30 mg/m2/lần, liều tối đa cho mỗi lần dùng 35,4 mg/m2 | Không có thông tin về hiệu chỉnh liều trong các tài liệu đã tham khảo* | – Bilirubin (2,1-3 mg/dl): Giảm 50% liều bình thường
– Bilirubin >3 mg/dl: Giảm 75% liều bình thường |
| 22 | Vinblastin | 3,7 mg/m2 | Không có thông tin về hiệu chỉnh liều trong các tài liệu đã tham khảo* | – Bilirubin huyết thanh 1,5-3 mg/dl: giảm 50% liều bình thường
– Bilirubin huyết thanh 3,1 -5mg/dl: chống chỉ định |
| 23 | Vincristin | 1,4 mg/m2 | Không có thông tin về hiệu chỉnh liều trong các tài liệu đã tham khảo* | – Bilirubin huyết thanh 1,5-3 mg/dl: giảm 50% liều bình thường
– Bilirubin huyết thanh 3,1 -5mg/dl: chống chỉ định |
[ULN: giới hạn trên của giá trị xét nghiệm bình thường]
Đánh giá chức năng gan, thận của bệnh nhân dựa trên công thức và các chỉ số sau:
1. Bệnh nhân được đánh giá chức năng thận dựa trên MLCT (độ thanh thải creatinin-CLcr), được tính theo công thức:
Người lớn (>18 tuổi): Sử dụng công thức Cockroft & Gault:
CLcr = [(140-tuổi) x cân nặng(kg)]/[72 x creatnin huyết thanh (mg/dl)] x 0,85 (đối với nữ) hoặc
CLcr = [(140-tuổi) x cân nặng(kg)]/[0,815 x creatnin huyết thanh (mcmol/l)] x 0,85 (đối với nữ)
2. Bệnh nhân được đánh giá chức năng gan dựa trên xét nghiêm hóa sinh gan, bao gồm: Bilirubin huyết thanh, transaminase (AST, ALT), ALP (alkaline phosphatase)
Khoảng liều trên bệnh nhân có chức năng gan thận bình thường là liều lượng được tính theo diện tích bề mặt cơ thể.
*: AHFS drugs information 2011, Dược thư quốc gia Việt Nam 2015, Renal Pharmacotherapy_ Dosage Adjustment of Medications Eliminated by the Kidneys 2013, Martindale- The Complete Drug Reference, 36th Edition, tờ hướng dẫn sử dụng của các biệt dược gốc
Phụ lục 4.3. Bảng pha truyền và độ ổn định sau khi pha của các thuốc điều trị 5 loại ung thư thường gặp tại Việt Nam
| TT | Hoạt chất | Tên thuốc | Dạng bào chế | DM pha truyền | Hướng dẫn cách pha | Thời gian truyền | Độ ổn định sau khi pha loãng | Lưu ý | |
| Bước 1: Hoàn nguyên | Bước 2: Pha loãng | ||||||||
| 1 | Bevacizumab | Avastin | Dung dịch đậm đặc để pha truyền tĩnh mạch 100mg/4mL; 400mg/16mL | NaCl 0,9% | NaCl 0,9% để đạt dung dịch có nồng độ 1,4 -16,5 mg/mL. | – Liều khởi đầu: phút
– Nếu lần truyền đầu dung nạp tốt, lần truyền thứ hai: 60 phút. – Nếu lần 2 dung nạp tốt, những lần truyền tiếp theo: 30 phút |
2-8oC/24 giờ | ||
| 2 | Carboplatin | Carboplatin sindan; Bocartin 150 | Dung dịch đậm đặc để pha truyền tĩnh mạch 150mg/15mL | G 5% | Pha loãng thêm với G 5% đến nồng độ 0,5 mg/mL | ≥ 15 phút. Có thể truyền liên tục trong 24 giờ | ≤ 8giờ ở 15 -25oC | Không sử dụng dụng cụ pha truyền thuốc có chứa nhôm | |
| 3 | Cetuximab | Erbitux | Dung dịch tiêm truyền 100mg/20mL | NaCl 0,9% | – Liều đầu tiên: truyền chậm ≤ 5 mg/phút, Thời gian truyền 120 phút.
– Với các liều tiếp theo: truyền tốc độ ≤ 10 mg/phút trong 60 phút |
Thường không quá 24 giờ ở nhiệt độ từ 2- 8°C | |||
| 4 | Cisplatin | Cisplaton | Dung dịch để pha truyền tĩnh mạch 50mg/100mL | NaCl 0,9%;
NaCl 0,9% và G 5% (1:1); NaCl 0,9% và Mannitol 5% (1:1) |
Pha loãng bằng dung môi đến nồng độ 0,1 mg/mL | 6-8 giờ | 48 giờ 2-8oC | Không sử dụng các dụng cụ pha, truyền thuốc có chứa nhôm | |
| DBL Cisplatin injection | Dung dịch để pha truyền tĩnh mạch 50mg/50mL | NaCl 0,9% | Pha vào 1 lít dung dịch truyền tĩnh mạch NaCl 0,9% | 1-2 giờ Thời gian truyền 6-8 giờ có thể giảm độc tính trên thận và đường tiêu hóa. | Chai chứa dịch truyền phải được bọc kín tránh ánh sáng | ||||
| 5 | Cyclophosp hamid | Endoxan | Bột để pha dung dịch tiêm truyền 200mg, 500mg. | NaCl 0,9% | Lọ 200 mg: Thêm 10mL NaCl 0,9%, Lọ 500mg: Thêm 25 mL. Sau khi thêm dung môi phải lắc mạnh để hoà tan thuốc Nếu bột không hoà tan hoàn toàn ngay, phải chờ trong vài phút. | NaCl 0,9%; G 5% với tổng thể tích 500mL | Thời gian truyền (từ 30 phút đến 2 giờ) tương ứng với thể tích và dung môi pha truyền | 2-8oC/24giờ | Để giảm nguy cơ tác dụng phụ theo tốc độ truyền (sưng mặt, đau đầu, nghẹt mũi): truyền rất chậm cyclophospha mid. |
| 6
|
Docetaxel
|
Taxotere; Docetaxel “Ebewe” | Dung dịch đậm đặc để pha truyền tĩnh mạch 20mg/mL, 80 mg/4 mL | NaCl 0,9%; G 5% | – | 250 mL G 5% hoặc NaCl 0,9 % để có nồng độ 0,3 mg/mL-0,74 mg/mL.
Nếu liều docetaxel >190 mg: tính toán thể tích dung dịch pha loãng để dung dịch cuối cùng có nồng độ < 0,74 mg/mL |
Thời gian truyền thường là giờ và có thể nhanh hơn nếu bệnh nhân không bị phản ứng ở lần truyền đầu tiên.
Không truyền trong thời gian quá lâu (ví dụ: 6-24 giờ) hoặc các liều truyền gần nhau (ví dụ: cách nhau 5 ngày) |
4 giờ ở 2-25oC (bao gồm cả 1 giờ tiêm truyền) | |
| Daxotel | Dung dịch đậm đặc để pha truyền tĩnh mạch mg 4 mL và 120 mg/6mL | ||||||||
| 7 | Doxorubicin liposome | Chemodox | Dung dịch tiêm 2mg/mL | G 5% | <90 mg: 250 mL G 5%
>90 mg: 500 mL G 5% |
Khởi đầu nên truyền với tốc độ mg phút để giảm nguy cơ xảy ra phản ứng liên quan đến truyền thuốc Nếu không ghi nhận được những tác dụng phụ do truyền thuốc, nên tăng tốc độ truyền để hoàn tất việc truyền thuốc trong vòng 1 giờ | 24 giờ/ 2-8°C | Không lọc thuốc trong khi tiêm truyền | |
| 8 | Epirubicin | Farmorubicina | Bột đông khô pha tiêm 50 mg | NaCl 0,9%, G 5% | – Hòa tan bột thuốc trong dung dịch NaCl 0,9% hoặc G 5% | 3 – 20 phút tùy thuộc vào liều lượng và thể tích dịch truyền | Khuyến cáo không tiêm tĩnh mạch nhanh toàn bộ lượng thuốc 1 lần do có nguy cơ thuốc thoát mạch
– Dung dịch sau hoàn nguyên ổn định ở 24 giờ nhiệt độ phòng hoặc 48 giờ/2-8oC |
||
| 9 | Etoposid | Sintopozid | Dung dịch đậm đặc để pha truyền tĩnh mạch 100mg/5mL | NaCl 0,9%; G 5% | – | 250mL G 5% hoặc NaCl 0,9% đến nồng độ cuối cùng < 0,25 mg/mL | 30 – 60 phút | ||
| 10 | Fluorouracil | Biluracil | Dung dịch để pha truyền 500mg/10mL | NaCl 0,9%; G 5% | – | 500 mL NaCl 0,9% hoặc G 5% Không quá 1g cho 1 lần truyền | Truyền trên 4 giờ, hoặc truyền trong 30 – 60 phút, hoặc truyền liên tục trong 24giờ | 24 giờ/ nhiệt độ phòng | |
| 11 | Gemcitabin | Gemita | Bột pha dung dịch tiêm truyền 200 mg; 1 g; 1,4g | NaCl 0,9% | Lọ 200 mg: 5 mL NaCl 0,9%; Lọ 1g: 25 mL NaCl 0,9%; Lọ 1,4g: 35mL NaCl 0,9% để đạt nồng độ thuốc là 38 mg/mL (tối đa mg/mL) | Không cần pha loãng hoặc tiếp tục pha loãng thêm bằng dung dịch NaCl 0,9% để đạt nồng độ 0,1 mg/mL | 30-60 phút.
Không truyền lâu quá 60 phút vì làm tăng độc tính của thuốc |
Pha xong để ở nhiệt độ phòng, không bảo quản trong tủ lạnh do kết tinh
Dùng trong 24 giờ |
|
| 12 | Irinotecan | Campto | Dung dịch đậm đặc để pha truyền 40mg/2mL; 100mg/5mL | NaCl 0,9%; G 5% | – | 250 – 500 mL NaCl 0,9% để được dung dịch có nồng độ cuối cùng 0,12 – 2,8 mg/mL | 30 – 90 phút | < 24 giờ/2-8oC | Trộn đều dung dịch tiêm truyền bằng cách xoay vòng nhẹ nhàng bằng tay |
| 13
|
Oxaliplatin | Oxalipatin Hospira | Dung dịch đậm đặc để pha truyền tĩnh mạch 5mg/mL (50 mg hoặc 100 mg)
|
G 5%
|
–
|
250-500 mL dung dịch G 5% để đạt nồng độ ≥ 0,2 mg/mL
|
2- giờ Có thể phải thay đổi liều hoặc thời gian truyền oxaliplatin để hạn chế một số tác dụng không mong muốn của thuốc. Tăng thời gian truyền oxaliplatin từ 2 giờ lên 6 giờ có thể giảm thiểu độc tính cấp
|
Dùng ngay | Không sử dụng các dụng cụ pha/truyền thuốc có chứa nhôm
|
| Oxitan | 6 giờ/20 -25oC | ||||||||
| Eloxatin | 24 giờ/2 -8oC | ||||||||
| 14 | Paclitaxel
|
Paclitaxel actavis;
Paclitaxel ‘ebewe’ |
Dung dịch đậm đặc để pha tiêm truyền tĩnh mạch 6mg/mL
|
NaCl 0,9%; G 5 %
|
|
Pha loãng tới nồng độ 0,3-1,2 mg/mL
|
≥ 3 giờ (tùy phác đồ)
|
<27 giờ/ 25oC | Dung dịch Paclitaxel phải được truyền bằng dây truyền có gắn màng lọc với lỗ lọc < 0,22 micron
|
| Anzatax | Dung dịch trong NaCl 0,9%: 2- 8oC/28 ngày, 25oC/7 ngày;
Dung dịch trong G 5%: 2- 8oC/14 ngày, 25oC/72 giờ (điều kiện: tránh ánh sáng; túi truyền không có PVC) |
||||||||
| Hepargitol 30mg, 100mg, 150mg | Dùng ngay hoặc trong vòng 3 giờ sau khi pha xong.
Không để dịch đã pha loãng vào tủ lạnh |
||||||||
| 15 | Pembrolizu mab | Keytruda | Dung dịch tiêm truyền tĩnh mạch 100mg/4mL | NaCl 0,9%; G 5 % | – | – Để lọ thuốc cân bằng nhiệt độ với nhiệt độ phòng (≤25°C) -Rút lượng dịch cần pha vào chai dịch truyền NaCl 0,9% hoặc G 5% để được dung dịch pha loãng có nồng độ cuối cùng từ 1-10 mg/mL | ≥ 30 phút | 2-8°C/ không quá 24 giờ | Xoay nhẹ chai dịch truyền để hoà tan thuốc, không lắc |
| 16 | Pemetrexed | Alimta | Bột để pha dung dịch tiêm truyền 100 mg | NaCl 0,9% | 4,2 mL NaCl 0,9% | NaCl 0,9% để đủ 100 mL dung dịch | ≥ 10 phút | 2-8oC/ không để quá 24 giờ | Khi hoàn nguyên lắc xoáy lọ nhẹ nhàng tới khi bột thuốc hòa tan hoàn toàn |
| Bột để pha dung dịch tiêm truyền 500 mg | 20 mL NaCl 0,9% | ||||||||
| 17 | Pertuzumab | Perjeta | Dung dịch đậm đặc dùng để pha loãng 420mg/14mL | NaCl 0,9% | – | Pha vào 250 mL NaCl 0,9% Với liều ban đầu 2 lọ dung dịch sau khi pha đạt nồng độ là 3,0 mg/mL, liều tiếp theo 1 lọ dung dịch sau khi pha đạt nồng độ 1,6 mg/mL. Pha trộn bằng cách xoay ngược túi thuốc nhẹ nhàng để tránh tạo bọt | Liều tải 840mg: 60 phút
Liều duy trì 420 mg: 30-60 phút |
2-8oC/không quá 24giờ | Perjeta và herceptin có thể sử dụng theo bất kỳ thứ tự nào Khi dùng docetaxel thì liều docetaxel phải được dùng sau Perjeta và herceptin Không để đông lạnh Không lắc lọ thuốc |
| 18 | Topotecan | Hycamtin | Bột để pha dung dịch tiêm truyền 1mg, 4mg |
NaCl 0,9%; G5 % |
Lọ mg: 1,1 mL nước cất pha tiêm Lọ mg: 4 mL nước cất pha tiêm. |
Pha loãng với NaCl 0,9 % hoặc G 5% để được nồng độ cuối cùng 25-50 mcg/ml |
> 30 phút | 12 giờ/ nhiệt độ phòng (tính đến lúc truyền xong) |
|
| 19 | Trastuzumab | Herceptin | Bột để pha dung dịch tiêm truyền 150 mg | NaCl 0,9% | Lọ 150 mg: 7,2 mL nước cất pha tiêm, xoay vòng lọ thuốc, không lắc | 250 mL NaCl 0,9% | – Liều tải: > 90 phút
– Liều tiếp theo: 30 phút nếu dung nạp tốt liều tải |
– Lọ 150mg: 24 giờ/2-8oC;
– Lọ 440mg: + Nước cất pha tiêm: 24 giờ/2-8°C; + Lọ dung môi đi kèm (Herticad): 28 ngày/2-8oC |
Xoay vòng lọ thuốc một cách nhẹ nhàng để hòa tan. Không được lắc |
| Herticad | Bột để pha dung dịch tiêm truyền 150mg, 440 mg | Lọ 440mg: 20 mL có dung môi chứa chất kìm khuẩn đi kèm. | |||||||
| 20 | Trastuzumab emtansine | Kadcyla | Bột để pha dung dịch tiêm truyền 100mg, 160mg | NaCl 0,9%; NaCl 0,45% | Lọ 100 mg: 5mL nước cất pha tiêm.
Lọ 160mg: 8mL nước cất pha tiêm |
Lấy lượng dịch tương ứng với liều cần dùng pha vào 250 mL dung môi pha truyền | – Liều nạp: 90 phút
– Liều tiếp theo: 30 phút nếu dung nạp tốt liều nạp |
24 giờ/ 2°C – 8°C
Không làm đông lạnh hoặc lắc dịch truyền khi bảo quản |
– Xoay lọ thuốc nhẹ đến khi hòa tan hoàn toàn.
Không lắc – Cần có lọc polyethersulfon e 0.20/0.22 trong dây truyền với dung môi NaCl 0,9%; Với dung môi NaCl 0,45% thì không cần lọc |
| 21 | Vinorelbine | Navelbine | Dung dịch đậm đặc để pha truyền 10mg/mL | NaCl 0,9%; G 5 % | – | Pha loãng với 50 mL NaCl 0,9% hoặc G 5% | 6-10 phút | 24 giờ /2°C – 8°C | |
NaCl 0,9%: Natri clorid 0,9%; G 5%: Glucose 5%
Lưu ý:
Về mặt vi sinh vật, khuyến cáo nên sử dụng ngay các thuốc sau khi hoàn nguyên. Trong trường hợp kiểm soát tốt và đảm bảo vô khuẩn thì có thể bảo quản trong thời gian ổn định về mặt lý hóa.
Dung dịch NaCl 0,9%, G 5% và các dung dịch pha khác là dạng dung dịch vô khuẩn dùng cho tiêm truyền.
Phụ lục 4.4. Hướng dẫn bù nước và điện giải khi truyền cisplatin
| Liều cisplatin (mg/m2) | Bù nước và điện giải trước truyền cisplatin | Bù nước và điện giải sau truyền cisplatin |
| >80 | 1.000mL dung dịch NaCl 0,9 % + 20mmol KCl + 10mmol MgSO4 truyền trên 2 giờ | 1.000mL dung dịch NaCl 0,9 % + 20mmol KCl + 10mmol MgSO4 truyền trên 2 giờ |
| 61-79 | 1.000mL dung dịch NaCl 0,9 % + 20mmol KCl truyền trên 1 giờ | 1.000mL dung dịch NaCl 0,9 % + 20mmol KCl + 10mmol MgSO4 truyền trên 2 giờ |
| 41-60 | 500mL dung dịch NaCl O,9 % truyền trên 30 phút | 1.000mL dung dịch NaCl 0,9 % + 20mmol KCl + 10mmol MgSO4 truyền trên 2 giờ |
| ≤40 | 500mL dung dịch NaCl O,9 % truyền trên 30 phút | Yêu cầu bệnh nhân uống 500mL nước |
NaCl 0,9%: Natri clorid 0,9%; KCl: Kali clorid; MgSO4: Magie sulphat
Lưu ý: Nếu phác đồ có phối hợp thêm thuốc khác ví dụ etoposid, có thể dùng dung môi pha thuốc khác để bù nước và điện giải trước truyền cisplatin (etoposid pha loãng trong 1.000mL dung dịch NaCl 0,9%).
Có thể sử dụng furosemid khi bù nước và điện giải nếu bệnh nhân bị suy tim.
Dặn bệnh nhân về nhà uống ít nhất 2 lít nước trong vòng 24 giờ sau truyền hóa chất.
Phụ lục 4.5. Bảng hướng dẫn thời điểm sử dụng thuốc đường uống
| STT | Hoạt chất | Tên thuốc | Hàm lượng | Dạng bào chế | Thời điểm dùng |
| 1. | Afatinib | Giotrif | 20 mg | Viên nén bao phim | Cách xa bữa ăn (không ăn ít nhất 3 giờ trước và 1 giờ sau uống thuốc )
Không được nghiền viên thuốc |
| 2. | Anastrozol | Anastrozole Stada | 1 mg | Viên nén bao phim | Không phụ thuộc vào bữa ăn |
| Aremed | |||||
| Arimidex | |||||
| 3. | Bicalutamid | Bicalutamide FCT | 50 mg | Viên nén | Không phụ thuộc vào bữa ăn
Nên uống cùng bữa ăn để hạn chế rối loạn tiêu hóa (buồn nôn, đau bụng) |
| Casodex | Không phụ thuộc vào bữa ăn
Uống vào một thời điểm cố định trong ngày |
||||
| 4. | Capecitabin | Xalvobin | 500 mg | Viên nén bao phim | Trong vòng 30 phút sau khi ăn |
| Xeloda | |||||
| 5. | Erlotinib | Nokati | 150 mg | Viên nén bao phim | Trước bữa ăn ít nhất 1 giờ hoặc sau bữa ăn 2 giờ |
| Tarceva | |||||
| 6. | Everolimus | Afinitor | 10 mg | Viên nén | Uống một lần vào một thời điểm cố định trong ngày
Không phụ thuộc vào bữa ăn Không nên nhai hoặc nghiền viên |
| 5 mg | |||||
| 7. | Exemestan | Aromasin | 25 mg | Viên nén | Sau bữa ăn |
| 8. | Gefitinib | Iressa 250 mg | 250 mg | Viên nén bao phim | Không phụ thuộc vào bữa ăn
Uống một lần vào một thời điểm cố định trong ngày Không nghiền viên thuốc |
| 9. | Imatinib | Glivec Tab | 100 mg | Viên nén bao phim | Uống cùng bữa ăn và cốc nước đầy để giảm kích ứng dạ dày |
| 10. | Letrozol | Femara | 2,5 mg | Viên nén bao phim | Không phụ thuộc vào bữa ăn |
| Letrozole Stada | |||||
| Lezra | |||||
| 11. | Nilotinib | Tasigna | 200 mg | Viên nang cứng | Không ăn ít nhất hai giờ trước và một giờ sau khi uống thuốc |
| 12. | Osimertinib | Tagrisso | 40 mg | Viên nén bao phim | Không phụ thuộc vào bữa ăn
Nên dùng vào cùng một thời điểm trong ngày Không được nghiền viên thuốc |
| 13. | Pazopanib | Voltrient | 200 mg | Viên nén bao phim | Uống ít nhất một giờ trước hoặc hai giờ sau khi ăn Không nhai hoặc nghiền viên |
| 14. | Regorafenib | Stivarga | 40mg | Viên nén bao phim | Nên dùng vào cùng một thời điểm trong ngày Uống nguyên viên thuốc sau một bữa ăn nhẹ ít chất béo |
| 15. | Sorafenib | Nexavar | 200 mg | Viên nén bao phim | Trước bữa ăn ít nhất 1 giờ hoặc sau bữa ăn 2 giờ |
| 16. | Sunitinib | Sutent | 12,5 mg | Viên nang cứng | Không phụ thuộc vào bữa ăn |
| 17. | Tamoxifen | Rolnadez | 20 mg | Viên nén | Không phụ thuộc vào bữa ăn |
| Tamifine | 10 mg | Viên nén | Không phụ thuộc vào bữa ăn | ||
| 18. | Tegafur+uracil | Mefuform | 100 mg + 224 mg | Viên nang | Uống trước hoặc sau bữa ăn giờ |
| 19. | Temozolomid | Temodal Cap 100 mg | 100 mg | Viên nang cứng | Uống khi đói Nuốt viên thuốc với nước, không nghiền hoặc nhai |
| 20. | Thalidomid | Domide | 50 mg | Viên nang | Uống sau bữa ăn ít nhất giờ, nên uống vào buổi tối trước khi đi ngủ |
| 21. | Vinorelbin | Navelbine | 20 mg | Viên nang mềm | Uống cùng bữa ăn
Không nhai, nghiền hoặc hòa tan viên thuốc |
Phụ lục 4.6. Tương tác thuốc-thuốc trong điều trị cho bệnh nhân ung thư
Bệnh nhân ung thư thường được điều trị kết hợp nhiều thuốc nên tiềm ẩn nhiều nguy cơ tương tác thuốc. Nguy cơ tương tác thuốc – thuốc tăng lên theo tuổi của bệnh nhân (bệnh nhân ung thư trên 65 tuổi có nguy cơ tương tác thuốc là khoảng 60%) do thiếu dinh dưỡng, kém hấp thu, suy thận hoặc suy chức năng gan làm thay đổi dược động học của thuốc đồng thời mắc nhiều BMK nên phải dùng phối hợp nhiều thuốc. Tương tác thuốc có thể làm tăng tác dụng điều trị hoặc giảm tác dụng điều trị hoặc gây tác dụng không mong muốn. Do đó, cần có kiến thức toàn diện về tương tác thuốc để có thể phòng ngừa, theo dõi bệnh nhân trong quá trình sử dụng thuốc làm giảm nguy cơ tác dụng phụ, giảm biến chứng và tăng hiệu quả điều trị.
Trong phạm vi phụ lục của cuốn sách này xin đề cập đến hai phần, phần A nêu hậu quả và xử trí của các cặp tương tác cần thận trọng và chống chỉ định của thuốc điều trị năm loại bệnh ung thư phổ biến tại Việt Nam với các thuốc khác mà các nhân viên y tế cần lưu ý trong quá trình kê đơn và sử dụng thuốc cho người bệnh mắc bệnh ung thư; phần B nêu các tài liệu để tra cứu tương tác thuốc và so sánh ưu nhược điểm của các tài liệu này:
Phần A: Hậu quả và xử trí của các cặp tương tác thuốc điều trị ung thư cần thận trọng và chống chỉ định.
Bảng 1.PL4.6. Các tương tác thuốc của thuốc điều trị ung thư cần thận trọng và chống chỉ định
| Thuốc điều trị ung thư | Thuốc tương tác | Hậu quả | Xử trí |
| Ức chế tyrosine kinase: dasatinib, imatinib, nilotinib, sorafenib, sunitinib | Vaccin sống: BCG, sởi, quai bị, rotavirus, rubella, đậu mùa, thương hàn, varicella- zoster, sốt vàng da | Tăng nguy cơ nhiễm khuẩn | Tránh phối hợp |
| Ức chế tyrosine kinase: dasatinib, erlotinib, gefitinib, nilotinib | Các thuốc ức chế bơm proton (PPI), đối kháng thụ thể H2 | Giảm sinh khả dụng của thuốc ức chế tyrosine kinase | Không kết hợp, cân nhắc thay thế sang các thuốc kháng acid |
| Ức chế tyrosine kinase: dasatinib, erlotinib, gefitinib, nilotinib, nilotinib, sunitinib, regorafenib | Clarithromycin, erythromycin, itraconazol, ketoconazol, voriconazol | Tăng nồng độ của thuốc ức chế tyrosine kinase | Sử dụng thuốc khác thay thế hoặc giảm liều thuốc tyrosine kinase |
| Ức chế tyrosine kinase: dasatinib, erlotinib, imatinib, gefitinib, lapatinib, nilotinib, sunitinib, sorafenib | Carbamazepin*, dexamethason, phenytoin*, phenobarbital*, rifampin, rifabutin, hypericum | Giảm nồng độ thuốc trong máu của thuốc tyrosine kinase | Sử dụng thuốc khác thay thế cho các thuốc cảm ứng CYP3A hoặc theo dõi tác dụng của thuốc ức chế tyrosine kinase hoặc tăng liều thuốc ức chế tyrosine kinase |
| Tất cả các thuốc gây độc tế bào*: bleomycin, cytarabin, daunorubicin, ifosfamid, cisplatin, carboplatin, cyclophosphamid, doxorubicin, etoposid, fluorouracil, gemcitabin, methotrexat, vincristin, vinblastin | Vaccin sống: BCG, sởi, quai bị, rotavirus, rubella, đậu mùa, thương hàn, varicella- zoster, sốt vàng da | Tăng nguy cơ nhiễm khuẩn | Tránh phối hợp |
| Tất cả các thuốc gây độc tế bào*: bleomycin, cytarabin, daunorubicin, ifosfamid, cisplatin, carboplatin, cyclophosphamid, doxorubicin, etoposid, fluorouracil, gemcitabin, methotrexat, vincristin, vinblastin | Các coumarin*: acenocoumarol, phenprocoumon, warfarin | Giảm hoặc tăng tác dụng của coumarin | Sử dụng thuốc khác thay thế coumarin (heparin trọng lượng phân tử thấp), hoặc theo dõi INR |
| Tất cả các thuốc gây độc tế bào*: bleomycin, cytarabin, daunorubicin, ifosfamid, cisplatin, carboplatin, cyclophosphamid, doxorubicin, etoposid, fluorouracil, gemcitabin, methotrexat, vincristin, vinblastin | Carbamazepin*, phenytoin*, acid valproic* | Giảm nồng độ trong máu của carbamazepin, phenytoin, acid valproic | Theo dõi nồng độ trong máu của carbamazepin, phenytoin, acid valproic |
| Các anthracyclin: daunorubicin, doxorubicin*, epirubicin, idarubicin, | Cyclosporin* | Tăng nồng độ trong máu của các anthracyclin | Tránh phối hợp nếu có thể, thay thế cyclosporin bằng thuốc khác |
| Doxorubicin* | Các thuốc chống virus: atazanavir, darunavir, fosamprenavir, indinavir, lopinavir, nelfinavir, ritonavir, saquinavir, tipranavir | Tăng độc tính của doxorubicin | Theo dõi độc tính của doxorubicin |
| Cyclophosphamid | Cyclosporin* | Giảm nồng độ trong máu của cyclosporin | Theo dõi chức năng gan, thận |
| Etoposid* | Cyclosporin* | Tăng nồng độ trong máu của etoposid | Giảm liều truyền tĩnh mạch etoposid |
| Fluorouracil* | Metronidazol | Tăng độc tính của fluorouracil | Sử dụng thuốc khác thay thế metronidazol hoặc theo dõi tình trạng huyết học |
| Methotrexat* | Cyclosporin* | Tăng nồng độ của cả hai thuốc | Theo dõi tác dụng không mong muốn của methotrexat, chức năng thận và nồng độ trong máu của cyclosporin |
| Kháng sinh nhóm Penicillin | Tăng độc tính của methotrexat | Tránh phối hợp, sử dụng thuốc khác thay thế | |
| Co-trimoxazol, trimethoprim | Tránh phối hợp, sử dụng thuốc khác thay thế co- trimoxazol hoặc trimethoprim | ||
| Các thuốc NSAID | Tăng nồng độ trong máu của methotrexat | Tránh phối hợp, hoặc theo dõi nồng độ thuốc trong máu của methotrexat, tác dụng không mong muốn và chức năng thận | |
| Probenecid | Tránh phối hợp, hoặc theo dõi tác dụng không mong muốn của methotrexat và chức năng thận | ||
| Tamoxifen | Các coumarin* | Tăng tác dụng của các coumarin | Theo dõi INR |
| Vinblastin, vincristin | Itraconazol | Tăng độc tính trên thần kinh của vinblastin hoặc vincristin | Sử dụng thuốc khác thay thế cho itraconazol hoặc theo dõi độc tính trên thần kinh của vinblastin hoặc vincristin |
| Kháng thể đơn dòng:
atezolizumab, pembrolizumab |
Các thuốc corticoid | Giảm tác dụng của thuốc | Không dùng đồng thời |
BCG: bacille Calmette-Guerin; CYP3A4: cytochrome P450 3A4; INR: international normalized ratio; *Thuốc có phạm vi điều trị hẹp
Phần B: Hướng dẫn tra cứu tương tác thuốc trong các tài liệu tham khảo
Lựa chọn tài liệu tra cứu
Hiện nay, trên thế giới có nhiều cơ sở dữ liệu (CSDL) tra cứu tương tác thuốc đã được xây dựng và phát triển. Các CSDL được trình bày dưới dạng sách hoặc phần mềm dễ sử dụng, thuận lợi cho việc tra cứu nhanh để phát hiện và xử trí tương tác thuốc. Dưới đây là những đặc điểm của một số CSDL thường được dùng trên thế giới và tại Việt Nam:
Drug interactions – Micromedex® Solutions (MM): là một phần mềm tra cứu tương tác thuốc trực tuyến cung cấp bởi Truven Health Analytics và được dùng phổ biến tại Mỹ. Tại Việt Nam, phần mềm này ít phổ biến do phải trả phí. Phần mềm này cung cấp thông tin về tất cả các dạng tương tác: tương tác thuốc – thuốc, thuốc – thực phẩm chức năng, thuốc – thức ăn, thuốc – ethanol, thuốc – thuốc lá, thuốc – bệnh lý, thuốc – thời kỳ mang thai, thuốc – thời kỳ cho con bú, thuốc – xét nghiệm và thuốc – phản ứng dị ứng. Mỗi kết quả tra cứu về một tương tác thuốc bao gồm các phần sau: tên thuốc (hoặc nhóm thuốc) tương tác, mức độ nặng của tương tác, mức độ y văn ghi nhận về tương tác, cảnh báo (hậu quả của tương tác), biện pháp xử trí, thời gian tiềm tàng, cơ chế, mô tả tương tác trong y văn và tài liệu tham khảo.
Stockley’s Drug Interactions và Stockley’s Interaction Alerts (SDI): là CSDL dưới dạng sách/phần mềm tra cứu trực tuyến, là nguồn tài liệu toàn diện về tương tác thuốc và có trích dẫn các nguồn tài liệu có bản quyền trên toàn thế giới. Tương tác trong CSDL này bao gồm tương tác của các loại thuốc điều trị, dược liệu, thực phẩm, đồ uống, thuốc trừ sâu và một số thuốc bị lạm dụng. Mỗi kết quả tra cứu về một tương tác thuốc trong Stockley’s Interaction Alerts bao gồm các phần sau: tên thuốc (nhóm thuốc) tương tác, mức độ ý nghĩa của tương tác, hậu quả của tương tác, biện pháp kiểm soát tương tác và mô tả ngắn gọn về tương tác qua ba tiêu chí: mức độ can thiệp, mức độ nặng và mức độ y văn ghi nhận về tương tác.
Sau đây là các bảng phân loại mức độ nặng và mức độ y văn ghi nhận về tương tác của hai CSDL MM và SDI:
Bảng 2.PL4.6. So sánh phân loại mức độ nặng của tương tác trong MM và SDI
| Mức độ tương tác | Ý nghĩa trong MM | Mức độ tương tác | Ý nghĩa trong SDI |
| Chống chỉ định | Chống chỉ định các thuốc dùng đồng thời. | Nặng | Mất hoàn toàn khả năng hoạt động, gây ra ảnh hưởng bất lợi lâu dài hoặc đe dọa tính mạng |
| Nặng | Tương tác gây hậu quả đe dọa tính mạng và/hoặc cần can thiệp y khoa để hạn chế tối thiểu phản ứng có hại nghiêm trọng xảy ra. | Trung bình | Tương tác có thể ảnh hưởng ở mức độ trung bình hoặc giảm một phần khả năng hoạt động của bệnh nhân. Những tương tác này không gây đe dọa tính mạng hoặc gây ảnh hưởng lâu dài. |
| Trung bình | Tương tác dẫn đến hậu quả làm nặng thêm tình trạng của bệnh nhân và/hoặc cần thay đổi thuốc điều trị. | Nhẹ | Tương tác có thể ảnh hưởng ở mức độ nhẹ và không quá đáng lo ngại hoặc không làm giảm khả năng hoạt động ở đa số bệnh nhân |
| Nhẹ | Tương tác ít có ý nghĩa trên lâm sàng Tương tác có thể làm tăng tần suất hoặc mức độ nặng của phản ứng có hại nhưng thường không cần thay đổi thuốc điều trị. | Không có khả năng | Tương tác không chắc chắn ảnh hưởng đến bệnh nhân hoặc đôi khi không có tương tác |
| Không rõ | Không rõ. | Không rõ | Chỉ được sử dụng như phương án cuối cùng. Áp dụng cho những tương tác được dự đoán có khả năng xảy ra nhưng không có đủ bằng chứng. |
Bảng 3.PL4.6. Phân loại mức độ y văn ghi nhận về tương tác trong MM và SDI
| MM | SDI | ||
| Mức độ y văn ghi nhận về tương tác thuốc | Ý nghĩa | Mức độ y văn ghi nhận về tương tác thuốc | Ý nghĩa |
| Rất tốt | Các nghiên cứu có kiểm soát tốt đã chứng minh rõ ràng sự tồn tại của tương tác. | Mở rộng | Tương tác được ghi nhận dựa trên nhiều nghiên cứu quy mô vừa và nhỏ hoặc một số nghiên cứu lớn, thường có các báo cáo ca lâm sàng. |
| Tốt | Các tài liệu tin cậy cho thấy có tồn tại tương tác nhưng vẫn còn thiếu các nghiên cứu có kiểm soát tốt | Nghiên cứu | Tương tác được ghi nhận dựa trên các nghiên cứu chính thống, có thể là một nghiên cứu có quy mô vừa và nhỏ, hoặc một số nghiên cứu nhỏ Có thể có hoặc không có báo cáo ca lâm sàng. |
| Khá | Dữ liệu hiện có nghèo nàn, nhưng dựa vào đặc tính dược lý, các chuyên gia lâm sàng nghi ngờ có tương tác hoặc có bằng chứng tốt về dược lý đối với một loại thuốc tương tự. | Ca lâm sàng | Tương tác được ghi nhận dựa trên một hoặc một số ít báo cáo ca lâm sàng Không có thử nghiệm lâm sàng nào được thực hiện |
| Không rõ | Không rõ. | Lý thuyết | Tương tác được ghi nhận dựa trên lý thuyết hoặc thiếu thông tin về tương tác Thông tin này bắt nguồn từ các nghiên cứu in vitro liên quan đến thuốc đang được thử nghiệm hoặc dựa các thuốc khác trong nhóm có cùng cơ chế tác dụng |
Hansten and Horn’s drug interaction analysis and management 2013 (HH): là CSDL trình bày dưới dạng sách của hai tác giả Philip D. Hansten và John R. Horn. do Wolters Kluwer Health® phát hành. Tài liệu này tập trung vào việc quản lý tương tác thuốc để cải thiện kết quả trên lâm sàng. Các chuyên luận của HH cung cấp thông tin về tên thuốc tương tác, hậu quả, cơ chế, tóm tắt dữ liệu về tương tác trong y văn và đặc biệt là các yếu tố nguy cơ, biện pháp xử trí tương tác và tài liệu tham khảo. Mức độ của tương tác được đánh giá dựa trên mức độ can thiệp của tương tác trên lâm sàng. Năm mức độ của tương tác trong CSDL này được trình bày trong bảng 4.PL.4.6.
Bảng 4.PL4.6. Bảng phân loại mức độ của tương tác trong HH
| Mức độ | Mức độ can thiệp | Ý nghĩa |
| 1 | Tránh phối hợp | Nguy cơ luôn luôn vượt trội lợi ích. |
| 2 | Thường tránh phối hợp | Thường chỉ phối hợp trong một số trường hợp đặc biệt. |
| 3 | Giảm thiểu rủi ro | Cần tiến hành can thiệp để giảm thiểu nguy cơ cho bệnh nhân. |
| 4 | Không cần can thiệp | Nguy cơ xuất hiện tác dụng bất lợi nhỏ. |
| 5 | Không tương tác | Dữ liệu hiện có cho thấy không xảy ra tương tác. |
Tương tác thuốc và chú ý khi chỉ định: là sách chuyên khảo về tương tác thuốc bằng tiếng Việt, giúp tra cứu nhanh, thuận lợi trong thực hành, với mỗi tương tác thuốc được trình bày hai lần, mỗi lần 1 họ khác nhau. Tương tác thuốc và chú ý khi chỉ định chỉ đề cập đến tương tác thuốc – thuốc. Mức độ chú ý khi sử dụng và mức độ tương tác thuốc được xếp theo 4 mức độ trong bảng 5.PL4.6.
Bảng 5.PL4.6. Phân loại mức độ chú ý khi sử dụng và mức độ tương tác thuốc
| Mức độ | Chú ý khi chỉ định | Ý nghĩa của tương tác thuốc |
| 1 | Cần theo dõi | Tương tác cần theo dõi |
| 2 | Thận trọng | Tương tác cần thận trọng |
| 3 | Cân nhắc nguy cơ/lợi ích | Cân nhắc nguy cơ/lợi ích |
| 4 | Chống chỉ định | Phối hợp nguy hiểm |
Mỗi một cơ sở dữ liệu có các ưu nhược điểm khác nhau. Bảng 6.PL4.6 sẽ so sánh ưu nhược điểm của bốn cơ sở dữ liệu ở trên.
Bảng 6.PL4.6. So sánh ưu và nhược điểm các cơ sở dữ liệu
| STT | Tên cơ sở dữ liệu | Loại CSDL | Ngôn ngữ | Ưu điểm | Nhược điểm |
| 1 | Drug interactions – Micromedex® Solutions (MM) | Phần mềm tra cứu trực tuyến | Tiếng Anh | Nhanh, cập nhật và liên kết các vùng CSDL tốt Đưa ra khuyến cáo dựa trên bằng chứng | Trình bày khá phức tạp Chi phí cao |
| 2 | Stockley’s Drug Interactions và Stockley’s Interaction Alerts (SDI) | Sách phần mềm tra cứu trực tuyến | Tiếng Anh | Nhanh, chính xác, dễ hiểu, đưa ra khuyến cáo dựa trên bằng chứng và có ý nghĩa lâm sàng | Không cập nhật Chi phí cao nhưng rẻ hơn MM |
| 3 | Hansten and Horn’s Drug Interactions Analysis and Management (HH) | Sách | Tiếng Anh | Cập nhật, có cơ chế, biện pháp xử trí | Chi phí cao, không có sẵn tại Việt Nam |
| 4 | Tương tác thuốc và chú ý khi chỉ định | Sách | Tiếng Việt | Nhanh, dễ sử dụng, chi phí thấp | Không cập nhật Chỉ đề cập đến tương tác thuốc- thuốc |
Phụ lục 4.7. Thuốc chăm sóc giảm nhẹ không opioid và chế độ liều
Bảng 1.PL4.7. Thuốc giảm đau không opioid
| Tên thuốc và đường dùng | Liều bắt đầu | Khoảng cách giữa các lần dùng thuốc | Liều tối đa hàng ngày | Lưu ý |
| Các thuốc được khuyến cáo: | ||||
| Acetaminophen (Paracetamol viên nén, xi-rô dành cho trẻ em hàm lượng tuỳ theo từng nhà sản xuất)
Đường uống |
Người lớn: 500-1.000 mg | 4-6 giờ/ lần | 4.000 mg | – Giảm liều hoặc không dùng cho người bị bệnh gan.
– Dùng quá liều có thể gây ngộ độc với gan. |
| Trẻ em: 10-15 mg/kg | Trẻ em:
Không quá 60 mg/kg |
|||
| Thuốc chống viêm không steroid | ||||
| Ibuproten
(Viên nén các hàm lượng 200, 300, 400, 600, 800mg; xi-rô dành cho trẻ em hàm lượng tùy theo từng nhà sản xuất) Đường uống |
Người lớn: 400-800 mg | 6-8 giờ/lần | Người lớn: 2.400 mg | – Nếu dùng kéo dài phải dùng kèm các thuốc dự phòng các phản ứng có hại của thuốc này đối với dạ dày, ruột (trướng bụng, buồn nôn, nôn, chảy máu dạ dày ruột, loét dạ dày tiến triển)
– Dùng liều thấp ở người bị bệnh gan nặng. |
| Trẻ em: 5-10 mg/kg | Trẻ em: không dùng quá liều quy định | |||
| Các thuốc có thể cân nhắc lựa chọn khác: | ||||
| Choline magne trisalicylate Đường uống | Người lớn: 500-1.000mg | 8-12 giờ/lần | Người lớn 3.000 mg | – Không có tác dụng hủy tiểu cầu.
– Ít độc tính đối với dạ dày, ruột hơn các thuốc NSAID khác. – Giảm liều khi chức năng thận suy giảm. |
| Trẻ em: 25 mg/kg | Trẻ em: không dùng quá liều quy định. | |||
| Diclofenac (dạng giải phóng nhanh) Đường uống | Người lớn: 25-75 mg | 8-12 giờ/lần | 200 mg | – Nếu dùng kéo dài phải dùng kèm thuốc dự phòng các phản ứng có hại của thuốc này đối với dạ dày, ruột.
– Giảm liều khi chức năng thận suy giảm. |
| Diflunisal Đường uống | Người lớn: 500 mg | 12 giờ/lần | 1.000 mg | |
| Etodolac (dạng giải phóng nhanh) Đường uống | Người lớn: 200-400 mg | 8 giờ/lần | 1.200 mg | |
| Fenoprofen Đường uống | Người lớn: 200 mg | 6 giờ/lần | 3.200 mg | |
| Ketoprofen (dạng giải phóng nhanh) Đường uống | Người lớn: 25- 75mg | 6-8 giờ/lần | 225 mg | – Không nên dùng kéo dài quá 5 ngày.
– Nếu dùng kéo dài phải dùng kèm thuốc dự phòng các phản ứng có hại của thuốc này đối với dạ dày, ruột. – Giảm liều khi chức năng thận suy giảm. |
| Ketorolac
Tiêm bắp/tĩnh mạch Đường uống |
Người lớn:
– Lần đầu: tiêm liều cao 30-6 mg, sau đó 15-30mg; hoặc – Uống: 10 mg |
6 giờ/lần | – Tiêm: 120 mg
– Uống: 40 mg |
– Có nguy cơ gây xuất huyết dạ dày, ruột.
– Chỉ dùng được trong thời gian ngắn (tối đa 5 ngày). – Nên sử dụng thuốc dự phòng các phản ứng có hại đối với dạ dày, ruột. – Giảm liều khi chức năng thận suy giảm. |
| Meloxicam
Đường uống |
Người lớn: 7,5-15 mg | 24 giờ/lần | 30 mg | – Nếu dùng kéo dài phải dùng kèm thuốc dự phòng các phản ứng có hại của thuốc này đối với dạ dày, ruột.
– Giảm liều khi chức năng thận suy giảm. |
| Piroxicam
Đường uống |
Người lớn: 20 mg | 24 giờ/lần | 20 mg | – Nguy cơ gây xuất huyết dạ dày, ruột.
– Nếu dùng kéo dài phải dùng kèm thuốc dự phòng các phản ứng có hại của thuốc này đối với dạ dày, ruột. – Giảm liều khi chức năng thận suy giảm. – Tránh dùng cho người bị bệnh gan. |
| Thuốc giảm đau tác dụng kiểu opioid | ||||
| Tramadol
Đường uống |
Người lớn: 50-100 mg | 4-6 giờ/ lần | Là một thuốc giảm đau tác dụng giống opioid nhẹ. | |
Bảng 2.PL4.7. Các thuốc hỗ trợ trong điều trị đau và cách sử dụng
| Tên thuốc | Liều lượng và cách dùng | Tác dụng không mong muốn |
| Nhóm corticosteroid | ||
| Prednisolon | Người lớn: 20-80 mg, uống vào buổi sáng sau khi ăn | Tăng đường máu, lo âu, chứng loạn thần steroid, bệnh cơ, tiêu hóa,… |
| Trẻ em: 1 mg/kg x 1-2 lần/ngày, uống sau khi ăn | ||
| Dexamethason | Người lớn: 8 – 20 mg uống vào buổi sáng sau khi ăn hoặc tiêm tĩnh mạch | |
| Trẻ em: 0,3 mg/kg/ngày chia 1-2 lần/ngày, uống sau khi ăn hoặc tiêm tĩnh mạch | ||
| Nhóm thuốc chống trầm cảm ba vòng | ||
| Amitriptylin | Người lớn: 5- 25mg (tối đa 200 mg)/ngày.
Uống trước khi ngủ. |
Lơ mơ, hạ huyết áp tư thế đứng, nếu quá liều có thể gây độc thần kinh tim. |
| Trẻ em: 0,5 mg/kg một lần/ngày. Nếu cần thiết tăng liều thêm 0,2-0,4 mg/kg sau 2-3 ngày.
Uống trước khi ngủ. |
||
| Nhóm thuốc chống co giật | ||
| Valproat natri | 15 mg/kg/ngày chia 3 lần. Tối đa: 60 mg/kg/ngày | Gây ngủ gà.
Không dùng nếu người bệnh có bệnh gan. Giảm liều với người già. |
| Gabapentin | Người lớn:
Liều khởi đầu 300 mg trước khi ngủ. Sau ngày, tăng lên 300 mg/lần x 2 lần/ngày. Sau 2 ngày tiếp theo tăng lên 300 mg/lần x 3 lần/ngày. Tiếp tục tăng lên theo nhu cầu. Liều tối đa 3.600 mg/ngày |
Gây ngủ gà mỗi khi tăng thêm liều. |
| Trẻ em:
Liều khởi đầu 5 mg/kg uống 1 lần ngày trước khi ngủ. Khi cần có thể tăng liều lên đến 2-3 lần/ ngày, sau đó có thể tăng thêm 2-5 mg/kg/ngày, liều tối đa 2.400 mg/ngày |
||
| Nhóm chẹn đường dẫn truyền thần kinh (gây tê tại chỗ) | ||
| Lidocain (hydroclorid) | Bắt đầu mg kg, sau đó có thể tăng thêm 0,5-3 mg/kg.
Liều tối đa 50-15 mg/ngày |
Hạ huyết áp, chậm nhịp tim, yếu cơ |
| Bupivicain hydroclorid | 10-20mg, 3-5 lần/ngày | |
| Thuốc chống co thắt cơ trơn | ||
| Scopolamin (hyoscine)
butylbromid |
10-20 mg uống 3-4 lần/ngày; hoặc 10 mg tiêm dưới da 3-4 lần/ngày, tối đa 60 mg/ngày | Kháng muscarin ngoại vi gây khô miệng, táo bón, nhịp tim nhanh |
| Scopolamin (hyoscine)
hydrobromid |
10-20 mg, uống 3-4 lần/ngày; hoặc 0,2-0,4 mg, tiêm dưới da 3-4 lần/ngày; hoặc 2 mg/ngày tiêm dưới da liên tục; hoặc 1,5-6 mg/72 giờ bôi hoặc dán ngoài da | Scopolamin hydrobromid có thể gây buồn ngủ |
| – Phloroglucinol hydrat 80 mg + Trimethylphloroglucinol 80 mg (viên) | 4-6 viên/ngày; hoặc 1-3 ống tiêm bắp hoặc tĩnh mạch | |
| – Phloroglucinol hydrat 40 mg + Trimethylphloroglucinol 0,04 mg (ống) (Spasfon) | ||
| Nhóm thuốc giãn cơ vân | ||
| Diazepam | 2-10 mg uống hoặc tiêm tĩnh mạch 2-3 lần/ngày | Ngủ gà, mất điều hoà vận động |
| Baclofen | Bắt đầu 5 mg uống 3 lần/ngày, tối đa 20 mg x 3 lần/ngày | |
| Nhóm bisphosphonat (dùng cho giảm đau trong ung thư di căn xương) | ||
| Pamidronat | 60-90 mg, truyền tĩnh mạch, 4 tuần/ một lần | Giảm canxi máu
Sốt, giả cúm trong 1-2 ngày Nhuyễn xương hàm
|
| Acid zoledronic | 4mg, truyền tĩnh mạch, 4- 8 tuần/một lần | |
Phụ lục 4.8. Thuốc chăm sóc giảm nhẹ opioid và cách chuyển đổi các thuốc giảm đau opioid
Bảng 1.PL4.8. Các thuốc opioid và cách sử dụng
| Tên thuốc và Đường dùng | Liều bắt đầu | Khoảng cách giữa các lần dùng thuốc | Lưu ý |
| Codein
(Viên nén 30 mg dạng đơn chất, hoặc phối hợp với thuốc giảm đau không opioid như aspirin, paracetamol) Đường uống |
Người lớn: 30-60 mg | 3 – 4giờ/ lần | – Không dùng quá 360 mg/ngày; trẻ em không dùng quá 6 lần/ngày
– Có thể gây táo bón – Thường gây buồn nôn – Giảm liều với người suy thận |
| Trẻ em: 0,5 – 1 mg/kg | |||
| Morphin sulfat
(dạng tác dụng nhanh) Đường uống |
Người lớn: dò liều từ 2-5 mg, sau 15-30 phút đánh giá lại, có thể tăng lên đến 10mg | Sau khi xác định được liều, dùng 4 giờ/lần | Có thể tăng liều lên 1,5-2 lần sau mỗi ngày nếu vẫn đau dai dẳng. |
| Trẻ em: dò liều từ 0,15 mg, có thể lên đến 0,3 mg/kg | |||
| Morphin sulfat (dạng tác dụng kéo dài)
Đường uống |
Người lớn: 10-15 mg | 12 giờ/lần | |
| Morphin clohydrat
Tiêm tĩnh mạch hoặc tiêm dưới da |
Người lớn: 2 – 5 mg | 3-4 giờ/lần | |
| Trẻ em: 0,05 – 0,1 mg/kg | |||
| Oxycodon
(dạng tác dụng nhanh) Đường uống |
Người lớn 5-10 mg | 3-4 giờ/lần | Là thuốc có hiệu lực mạnh hơn morphin. |
| Trẻ em: 0,1mg/kg | |||
| Oxycodon
(dạng tác dụng kéo dài) (Oxycontin) Đường uống |
Người lớn 10mg | 12 giờ/lần | |
| Trẻ em: 0,1 mg/kg | |||
| Hydromorphon
Đường uống |
Người lớn: 1 – 3 mg | 3-4 giờ/lần | Là thuốc có hiệu lực mạnh hơn morphin. |
| Hydromorphon
Tiêm tĩnh mạch hoặc tiêm dưới da |
Người lớn: 0,5 – 1 mg | ||
| Fentanyl
Miếng dán hấp thu qua da (Duragesic) |
Người lớn: 25 mcg/giờ | Dán 72 giờ/một miếng tại vùng ngực và đùi | – Chỉ dùng trong đau mạn tính.
– Không dùng cho cơn đau đột xuất. – Không dùng khi người bệnh đang sốt, ra nhiều mồ hôi, thể trạng gầy. – Thuận tiện trong xử trí đau cho người bệnh quá yếu, không thể uống hay tiêm thuốc thường xuyên. – Cần dùng thêm thuốc giảm đau tác dụng nhanh cho đến khi miếng dán phát huy tác dụng sau 12-18 giờ. – Thuốc có giá thành cao, khó bảo quản ở điều kiện khí hậu nóng ẩm. |
Bảng 2.PL4.8. Quy đổi đường tiêm sang đường uống
| Thuốc opioid | Liều đường tiêm | Liều đường uống | Tỷ lệ chuyển đổi tiêm sang uống | Thời gian tác dụng |
| Morphin | 10mg | 30mg | 3 | 3-4 giờ |
| Hydromorphon | 1,5mg | 7,5mg | 5 | 2-3 giờ |
| Fentanyl | – | – | – | – |
| Methadon | – | – | – | – |
| Oxycodon | – | 15-20mg | – | 3-5 giờ |
| Hydrocodon | – | 30-45mg | – | 3-5 giờ |
| Oxymorphon | 1mg | 10mg | 10 | 3-6 giờ |
| Codein | – | 200mg | – | 3-4 giờ |
Bảng 3.PL4.8. Quy đổi liều các opioid khác sang morphin
| Từ opioid uống khác sang morphin uống | Từ opioid tiêm khác sang morphin tiêm |
| Hydromorphon x 4 | Hydromorphon x 6,7 |
| Codein x 0,15 | Codein x 0,08 |
| Oxycodon x 2 | Fentanyl x 100 |
Bảng 4.PL4.8. Quy đổi morphin đường tiêm sang fentanyl dán
| Morphin clohydrat tiêm (mg/24giờ) | Fentanyl dán (mcg/giờ) |
| 18-35 | 25 |
| 36-59 | 50 |
| 60-83 | 75 |
| 84-107 | 100 |
| 108-131 | 125 |
| 132-156 | 150 |
Bảng 5.PL4.8. Opioid yếu dùng đường uống
| Thuốc/chế phẩm | Liều tối đa hàng ngày | Liều giảm đau tương đương của morphin dạng uống trong 24 giờ so với liều tối đa hàng ngày của chế phẩm |
| Codydramol* | 8 viên | 8 mg |
| Cocodamol 8/500* | 8 viên | 5 mg |
| Cocodamol 30/500* | 8 viên/viên nang | 20 mg |
| Codein phosphat | 240 mg | 20 mg |
| Dihydrocodein | 240 mg | 25 mg |
| Tramadol | 400 mg | 40 mg |
(* Chứa 500 mg paracetamol trong mỗi viên / nang)
Bảng 6.PL4.8. Opioid mạnh dùng đường uống và dưới da
| Thuốc | Tỉ số chuyển đổi từ morphin đường uống | Liều giảm đau tương đương so với 30 mg morphin đường uống | Ví dụ chuyển đổi (Áp dụng đối với đơn liều hoặc tổng liều hàng ngày) |
| Morphin (uống) | 1 | 30 mg | 1 . Để chuyển đổi 60 mg morphin đường uống sang morphin dùng dưới da, ta lấy 60 mg chia 2 được 30mg .
2 . Để chuyển đổi 30 mg morphin đường uống sang oxycodon đường uống, ta lấy 30 chia 2 được 15 mg. |
| Morphin (dưới da) | 2 : 1 | 15 mg | |
| Morphin (tĩnh mạch) | 3 : 1 | 10 mg | |
| Diamorphin (dưới da) | 3 : 1 | 10 mg | |
| Oxycodon (uống) | (1,5 – 2) : 1 | 15 – 20 mg | |
| Oxycodon (dưới da) | 3 : 1 | 10 mg | |
| Alfentanil (dưới da) | 30 : 1 | 1 mg | |
| Fentanyl (dưới da) | 150 : 1 | 200 mcg | |
| Hydromorphon (uống) | 7,5 : 1 | 4 mg | |
| Hydromorphon (dưới da) | 15 : 1 | 2 mg |
Bảng 7.PL4.8. Opioid dùng ngoài da
| Miếng dán fentanyl (mcg/giờ) | Miếng dán Buprenorphin (mcg/giờ) | Liều morphin đường uống trong 24 giờ (mg) | Liều morphin đường uống giảm đau cấp tính tạm thời (mg) |
| 12 | <60 | 5-10 | |
| 25 | 35 | 61-90 | 10-15 |
| 37 | 52,5 | 91-134 | 15-20 |
| 50 | 70 | 135-224 | 30 |
| 75 | 105 | 225-314 | 40 |
| 100 | 140 | 315-404 | 60 |
| 125 | Sự chuyển đổi liều này vẫn đang được bàn luận, liều chuyển đổi có thể cao hơn số liệu ghi ở đây | 405-494 | 80 |
| 150 | 495-584 | 90 | |
| 175 | 585-674 | 100 | |
| 200 | 675-764 | 120 | |
| 225 | 765-854 | 130 | |
| 250 | 855-944 | 150 |
(Chú ý: Ở mức liều thấp hơn, sự chuyển đổi liều của fentanyl kém chính xác hơn)
Phụ lục 4.9. Bảng kiểm tra thông tin trước pha chế thuốc điều trị ung thư
| I. Thông tin chung | |
| 1 | Mã bệnh án:…………………………………………………………………………………………. |
| 2 | Khoa/Phòng:…………………………………………………………………………………………. |
| 3 | Dược sĩ kiểm tra:…………………………………………………………………………………………. |
| 4 | Ngày kiểm tra:…………………………………………………………………………………………. |
| II. Thông tin kiểm tra | |
| 1 | Phác đồ:…………………………………………………………………………………………. |
| – Có phù hợp với chẩn đoán | |
| □ Có
□ Không |
|
| – Có phù hợp với các hướng dẫn điều trị của đơn vị đang dùng | |
| □ Có
□ Không |
|
| 2 | Bệnh nhân: |
| – Có tiền sử dị ứng với thuốc nào trong phác đồ hay không | |
| □ Có
□ Không |
|
| (Nếu có biểu hiện cụ thể như thế nào……………………………………….. ) | |
| – Cân nặng:………………. kg | |
| – Chiều cao:…………….. cm | |
| – Có bệnh về gan thận hay không | |
| □ Có
□ Không |
|
| – Kết quả xét nghiệm máu | |
| □ Có bất thường. Cụ thể:…………………………………………………. | |
| □ Không | |
| 3 | Cách dùng thuốc |
|
|
a/Liều có phù hợp với cân nặng hiện tại và tiền sử ADR cho các lần trước |
| □ Có
□ Không |
|
| b/Liều tích lũy (với anthracyclin) có phù hợp | |
| □ Có
□ Không |
|
| c/Khoảng cách liều có phù hợp | |
| □ Có
□ Không |
|
| d/Đường dùng có phù hợp | |
| □ Có
□ Không |
|
| e/Dung môi pha có tương hợp với hoạt chất pha | |
| □ Có
□ Không |
|
| f/Thể tích dung môi pha có đáp ứng yêu cầu | |
| □ Có
□ Không |
|
| Một số thông tin cần cảnh báo lưu ý khác | |
|
|
Phụ lục 4.10. Độc tính và tác dụng không mong muốn thường gặp của thuốc điều trị ung thư
Thuốc điều trị ung thư thường tác động không phân biệt đối với tế bào bình thường hay tế bào ung thư nên thường gây nhiều tác dụng phụ và độc tính. Một số tác dụng phụ thường gặp như: nôn và buồn nôn, ức chế tủy xương, tiêu chảy, viêm loét niêm mạc, giảm bạch cầu, giảm tiểu cầu, thiếu máu, thoát mạch,…Do đó, thường phải dùng các liệu pháp hỗ trợ để hạn chế tác dụng không mong muốn đã được biết trước của một số thuốc điều trị ung thư.
Trong phạm vi cuốn sách này xin hướng dẫn dự phòng, xử trí, chỉnh liều các tác dụng không mong muốn đặc trưng như: thoát mạch, dị ứng, nôn, buồn nôn, ỉa chảy, nổi mụn, giảm ba dòng (bạch cầu, hồng cầu, tiểu cầu), suy thận, suy gan, hội chứng bàn chân bàn tay của thuốc điều trị ung thư theo từng nhóm.
❖ Độc tính/tác dụng phụ của thuốc điều trị ung thư
Một số độc tính chính của các thuốc điều trị ung thư được tóm tắt ở bảng dưới đây:
Bảng 1.PL4.10. Tóm tắt độc tính chính của các thuốc trị ung thư
| Cơ quan | Biểu hiện độc tính | Loại thuốc |
| Máu | Suy tủy: giảm bạch cầu, tiểu cầu, hồng cầu | Hầu hết các thuốc, trừ asparaginase, bleomycin, vincristin |
| Đường tiêu hóa | Buồn nôn, nôn
Viêm loét niêm mạc, nhiễm khuẩn, khô miệng, tiêu chảy |
Hầu hết các thuốc ung thư |
| Tóc, móng | Rụng tóc có hồi phục | Hầu hết các thuốc, đặc biệt paclitaxel, daunorubicin, cyclophosphamid, doxorubicin |
| Da, mạch | Viêm mạch, hoại tử mô | Antracyclin, alcaloid vinca, meclorethamin, dactinomycin, streptozotocin, mitomycin |
| Gan | Rối loạn chức năng gan, tăng men gan | Methotrexat, mecaptopurin, asparaginase |
| Tim | Suy tim xung huyết không hồi phục, chảy máu màng trong tim | Antracyclin, doxorubixin, daunorubicin, cyclophosphamid |
| Phổi | Khó thở, ho khan, xơ phổi | Bleomycin, busulfan, carmustin |
| Thận | Tổn thương ống thận Viêm bàng quang | Cisplatin, streptozotocin, methotrexat liều cao Cyclophosphamid, ifosfamid |
| Thần kinh | Thần kinh ngoại biên
Bệnh cảm giác Độc tiểu não Viêm màng nhện |
Vincristin, cisplatin
Paclitaxel Cytarabin Cytarabin, methotrexat |
| Gây ung thư thứ phát do thuốc | Đột biến sinh ung thư Bệnh bạch cầu tủy cấp | Antracyclin, procarbazin Tất cả nhóm alkyl hóa, xạ trị |
Độc tính của các thuốc điều trị ung thư được phân loại theo năm mức độ từ 1 đến 5 tương ứng với các mức tối thiểu, trung bình, nghiêm trọng, đe doạ tính mạng và tử vong được trình bày trong Bảng 2.PL4.10.
Bảng 2.PL4.10. Phân loại mức độ nghiêm trọng độc tính của hóa điều trị
| Độc tính | Độ 1 | Độ 2 | Độ 3 | Độ 4 | Độ 5 |
| Tối thiểu | Trung bình | Nghiêm trọng | Đe dọa tính mạng | Tử vong | |
| Giảm bạch cầu | < 1,5 x 109 /L | 1-1,5 x 109 /L | 0,5-1 x 109 /L | < 0,5 x 109 /L | Tử vong |
| Giảm tiểu cầu | <75 x 109 /L | 50-75 x 109 /L | 25-50 x 109 /L | < 25 x 109 /L | Tử vong |
| Tiêu chảy | Tăng < 4 lần mỗi ngày | Tăng 4-6 lần mỗi ngày, cần truyền dịch đường tĩnh mạch < 24 giờ; không ảnh hưởng đến hoạt động hằng ngày | Tăng ≥ 7 lần mỗi ngày, không kiểm soát được, cần truyền dịch đường tĩnh mạch ≥ 24 giờ; phải nhập viện; ảnh hưởng đến hoạt động hằng ngày | Đe dọa tính mạng (ví dụ như giảm thể tích huyết tương,..) | Tử vong |
| Viêm thực quản | Không có triệu chứng bệnh lý; chỉ phát hiện được bằng X quang hoặc nội soi | Có triệu chứng và ảnh hưởng ít đến ăn hoặc nuốt; chỉ định nuôi dưỡng tĩnh mạch < 24 giờ | Có triệu chứng và ảnh hưởng nghiêm trọng đến ăn hoặc nuốt; chỉ định nuôi dưỡng tĩnh mạch ≥ 24 giờ | Đe dọa tính mạng | Tử vong |
| Buồn nôn | Mất cảm giác thèm ăn nhưng không làm thay đổi thói quen ăn uống | Ăn uống giảm nhưng không giảm cân đáng kể, mất nước, suy dinh dưỡng; chỉ định truyền dịch đường tĩnh mạch < 24 giờ | Ăn uống không cung cấp đủ năng lượng, chỉ định truyền dịch, ăn qua sonde hoặc dinh dưỡng tĩnh mạch ≥ 24 giờ | Đe dọa tính mạng | Tử vong |
| Nôn | 1 lần trong 24 giờ | 2-5 lần trong 24 giờ; chỉ định truyền dịch tĩnh mạch < 24 giờ | ≥ 6 lần trong 24 giờ; chỉ định truyền dịch hoặc nuôi dưỡng đường tĩnh mạch ≥ 24 giờ | Đe dọa tính mạng | Tử vong |
Phụ lục 4.11. Bảng kiểm giám sát tác dụng không mong muốn, độc tính của hóa trị
| I. Thông tin chung | ||
| 1 | Mã bệnh án:……………………………………………………………………………………………. | |
| 2 | Khoa/Phòng:……………………………………………………………………………………………. | |
| 3 | Dược sĩ kiểm tra:……………………………………………………………………………………………. | |
| 4 | Ngày kiểm tra:……………………………………………………………………………………………. | |
| 5 | Chẩn đoán ung thư:……………………………………………………………………………………………. | |
| 6 | Chiều cao:…………………. Cân nặng……………………… BSA…………………………………….. | |
| II. Thông tin phác đồ hóa trị | ||
| 1 | Phác đồ hóa chất:……………………………………………………………………………………. Chu……………………………………………………………………………… kỳ thứ mấy:………………………. | |
| 2 | Ngày bắt đầu truyền hóa chất trong chu kỳ:……………………………………………………………………………………………. | |
| 3 | Ngày kết thúc truyền hóa chất trong chu kỳ:……………………………………………………………………………………………. | |
| III. Tác dụng không mong muốn | ||
| TT | Tác dụng không mong muốn | Triệu chứng lâm sàng/Phân độ/Xét nghiệm |
| 1 | Giảm bạch cầu | □ Độ 1 (< 1,5 x 109 /L)
□ Độ 2 (1-1,5 x 109 /L) □ Độ 3 (0,5-1 x 109 /L) □ Độ 4 (< 0,5 x 109 /l) |
| 2 | Giảm tiểu cầu | □ Độ 1 (<75 x 109 /L)
□ Độ 2 (50-75 x 109 /L) □ Độ 3 (25-50 x 109 /L) □ Độ 4 (< 25 x 109 /L) |
| 3 | Thiếu máu | Giảm hemoglobin (Hb)
□ Độ 1 (> 10g/dL □ Độ 2 (8-10 g/dL) □ Độ 3 (<8g/dL) □ Độ (Nguy kịch, cần can thiệp ngay) |
| 4 | Tiêu chảy | □ Độ 1 (Đại tiện < 4 lần mỗi ngày)
□ Độ (Đại tiện 4-6 lần mỗi ngày) □ Độ 3 (Đại tiện ≥ 7 lần mỗi ngày) □ Độ (Đe dọa tính mạng) |
| 5 | Buồn nôn | □ Độ 1 (Chán ăn nhưng chưa thay đổi thói quen ăn uống)
□ Độ (Ăn ít đi tuy nhiên chưa giảm cân) □ Độ 3 (Ăn rất ít, cần sự hỗ trợ y tế như truyền dịch) |
| 6 | Nôn | □ Độ 1 (1 lần trong 24 giờ)
□ Độ 2 (2-5 lần trong 24 giờ) □ Độ 3 (≥ 6 lần trong 24 giờ) |
| 7 | Viêm niêm mạc miệng | □ Độ 1 (Nhẹ, không cần can thiệp y tế)
□ Độ 2 (Đau vừa, không ảnh hưởng tới ăn uống, khuyến cáo thay đổi khẩu phần ăn, không cần can thiệp y tế) □ Độ 3 (Đau nặng, ảnh hưởng tới ăn uống) □ Độ 4 (Nguy kịch, cần can thiệp ngay) |
| 8 | Thoát mạch | □Có □ Không |
| 9 | Ban đỏ, nốt sần trên da | □ Độ 1 (Vết ban hoặc mụn mủ bao phủ <10% diện tích da, không có triệu chứng khác)
□ Độ 2 (Vết ban hoặc mụn mủ bao phủ 10% đến 30% diện tích da, gặp khó khăn trong sinh hoạt) □ Độ 3 (Vết ban hoặc mụn mủ bao phủ >30 % diện tích da, gặp khó khăn trong vệ sinh cá nhân |
| 10 | Hội chứng bàn chân bàn tay | □ Độ 1 (Tình trạng tê, rối loạn cảm giác/dị cảm, đau nhói dây thần kinh, sưng phồng không đau hoặc ban đỏ ở bàn tay hoặc bàn chân và/hoặc không cảm thấy thoải mái nhưng không ảnh hưởng đến hoạt động bình thường)
□ Độ 2 (Ban đỏ và sưng tay và hoặc chân gây đau và hoặc không thoải mái ảnh hưởng đến cuộc sống bình thường hằng ngày của bệnh nhân) □ Độ 3 (Sự tróc vảy da chảy mủ, loét, mụn nước hoặc đau nhiều ở bàn tay hoặc bàn chân và/hoặc rất khó chịu bệnh nhân không thể làm việc được hoặc thực hiện các hoạt động bình thường hằng ngày. |
| 11 | Rụng tóc | □ Có □ Không |
| 12 | Khó nuốt – Nuốt đau | □ Độ 1 (Triệu chứng điển hình nhưng vẫn có khả năng ăn khẩu phần thông thường)
□ Độ 2 (Các triệu chứng gây thay đổi lượng, khẩu phần ăn mà không cần chỉ định can thiệp y khoa) □ Độ 3 (Giảm lượng khẩu phần ăn nghiêm trọng gây đe doạ tính mạng) |
| 13 | Táo bón | □ Độ 1 (Xảy ra không thường xuyên, ít dùng thuốc nhuận tràng)
□ Độ (Thường xuyên xảy ra khiến bệnh nhân hay phải dùng thuốc nhuận tràng, gặp khó khăn trong sinh hoạt cá nhân) □ Độ 3 (Khuyến cáo dùng các phương pháp thụt tháo, gặp khó khăn trong vệ sinh cá nhân) |
| 14 | Mệt mỏi | □ Độ 1 (Hết mệt khi nghỉ ngơi)
□ Độ 2 (Không hết mệt khi nghỉ ngơi, gặp khó khăn trong sinh hoạt) □ Độ 3 (Không hết mệt khi nghỉ ngơi, gặp khó khăn trong tự vệ sinh cá nhân) |
| Bệnh lý thần kinh ngoại vi | □ Độ 1 (Không có triệu chứng; mất phản xạ gân sâu hoặc dị cảm)
□ Độ 2 (Triệu chứng vừa, gặp khó khăn trong sinh hoạt) □ Độ 3 (Triệu chứng nặng, gặp khó khăn trong tự vệ sinh cá nhân) |
|
| 15 | Kéo dài khoảng QT
(Đối với thuốc có tác dụng phụ trên tim mạch) |
□ Độ 1 (0,45 đến < 0,47 giây)
□ Độ 2 (≥ 0,47 đến < 0,50 giây) □ Độ 3 (> 0,50 giây) □ Độ 4 (Các hậu quả đe doạ tính mạng) (ví dụ cơn xoắn đỉnh hoặc loạn nhịp thất nặng) |
| 16 | Tăng ALT, AST | □ Độ 1 ( 1,25 đến < 2,5 x ULN)
□ Độ ( 2,5 đến < 5,0 x ULN) □ Độ 3 (5,0 đến < 10,0 x ULN) □ Độ 4 (≥ 10,0 x ULN) |
| 17 | Tăng bilirubin TP | □ Độ 1 (1,1 đến < 1,6 x ULN)
□ Độ ( 1,6 đến < 2,6 x ULN) □ Độ 3 ( 2,6 đến < 5,0 x ULN) □ Độ 4 (≥ 5,0 x ULN) |
| 18 | Tăng creatinin máu | □ Độ 1 ( 1,1 đến 1,3 x ULN)
□ Độ (> 1,3 đến 1,8 x ULN) □ Độ 3 (> 1,8 đến < 3,5 x ULN) □ Độ 4 (3,5 x ULN) |
ULN: Giới hạn bình thường trên
Phụ lục 4.12. Tác dụng phụ gây nôn, phân loại và phác đồ kiểm soát nôn trong hoá trị
- Nôn và buồn nôn
Cơ chế chính xác gây nôn và buồn nôn của hóa trị chưa được biết rõ. Một trong những cơ chế gây nôn và buồn nôn là kích hoạt thụ thể tiếp nhận hóa chất, các chất dẫn truyền thần kinh như: dopamin, serotonin, histamin,…Hệ thống tiền đình hay thay đổi vị giác do hóa trị cũng gây nôn và buồn nôn. Cơ chế cuối cùng gây nôn và buồn nôn của hóa trị là do ảnh hưởng trực tiếp hoặc gián tiếp lên vỏ não. Nguy cơ nôn và buồn nôn tăng lên khi người bệnh cùng phòng điều trị bị nôn hoặc giảm chất lượng giấc ngủ vào đêm trước điều trị.
- Phân loại nôn do hóa trị
– Nôn cảm ứng: Xảy ra trên những người bệnh trước đó đã trải qua hóa trị và đã từng bị nôn do hóa trị. Nôn xuất hiện trước khi thuốc được đưa vào cơ thể người bệnh.
– Nôn cấp: Xảy ra trong vòng vài giờ đầu ngay sau khi hóa trị (thường trong vòng 1-2 giờ) và có thể kéo dài từ 4 đến 6 giờ.
– Nôn muộn: Xảy ra sau hóa trị từ 16 đến 24 giờ và có thể kéo dài tới 48 giờ. Nôn muộn thường hay gặp khi hóa trị với cisplatin, carboplatin, cyclophosphamid và doxorubicin. Mặc dù nôn muộn có thể không gây nghiêm trọng nhưng chính nó lại ảnh hưởng nhiều đến vấn đề dinh dưỡng và làm kéo dài thời gian nằm viện cho người bệnh.
- Phân loại mức độ gây nôn của các thuốc điều trị ung thư
Theo Hướng dẫn của Hiệp hội Ung thư Hoa Kỳ (NCCN), mức độ gây nôn của các thuốc điều trị ung thư được phân loại như Bảng 1.PL4.12.
Bảng 1.PL4.12. Mức độ gây nôn của các thuốc điều trị ung thư
| Mức độ | Đường tiêm | Đường uống | |
| Nguy cơ cao (>90%) | Phác đồ AC (kết hợp bất kỳ thuốc hoá điều trị nào với anthracyclin)
Carboplatin AUC ≥ 4# Cisplatin Cyclophosphamid > 1.500 mg/m2 |
Dacarbazin
Doxorubicin ≥ 60 mg/m2# Epirubicin > 90 mg/m2# Ifosfamid ≥ 2 g/m2/liều# |
Temozolomid > 75mg/m2/ngày |
| Nguy cơ trung bình (>30-90%) | Bendamustin
Carboplatin AUC < 4 Cyclophosphamid ≤ 1.500 mg/m2 Cytarabin > 200 mg/m2 Dactinomycin Doxorubicin < 60 mg/m2 |
Epirubicin ≤ 90 mg/m2
Irinotecan Methotrexat ≥ 250 mg/m2 Oxaliplatin Temozolomid |
|
| Nguy cơ thấp (10-30%) | Atezolizumab
Cytarabin 100-200 mg/m2 Docetaxel Doxorubicin liposome Etoposid 5-FU |
Gemcitabin Methotrexat >50 – <250 mg/m2 Paclitaxel Pemetrexed Topotecan | Capecitabin Erlotinib Everolimus Gefitinib Imatinib# Osimertinib Regorafenib Sorafenib |
| Nguy cơ rất thấp (<10%) | Bevacizumab
Bleomycin Cetuximab$ Cytarabin <100 mg/m2$ Fludarabin Methotrexat < 5 mg m2$ Panitumumab$ |
Pembrolizumab Rituximab Trastuzumab Vinblastin Vincristin Vinorelbin | |
(#: ESMO và ASCO xếp nguy cơ trung bình; $: ESMO và ASCO xếp nguy cơ thấp)
Khi sử dụng thuốc điều trị ung thư có nguy cơ gây nôn có thể sử dụng các phác đồ kiểm soát nôn như trong bảng sau:
Bảng 2.PL4.12. Phác đồ kiểm soát nôn trong hóa trị
| Mức độ | Ngày 1 | Ngày 2, 3, 4 |
|
Thuốc ung thư đường tiêm |
||
| Nguy cơ cao (>90%) | Thuốc kháng NK-1* + Kháng 5-HT3 + Dexamethason | Dexamethason |
| Olanzapin + Palonosetron + Dexamethason | Olanzapin | |
| Thuốc kháng NK-1 + Kháng 5-HT3 + Dexamethason + Olanzapin | Olanzapin + Dexamethason | |
| Nguy cơ trung bình (>30-90%) | Thuốc kháng 5-HT3 + Dexamethason | Dexamethason HOẶC Kháng 5-HT3# |
| Olanzapin + Palonosetron + Dexamethason | Olanzapin | |
| Thuốc kháng NK-1 + Kháng 5-HT3 + Dexamethason + Olanzapin | Olanzapin + Dexamethason | |
| Nguy cơ thấp (10-
30%) |
Dexamethason | |
| HOẶC Metoclopramid | ||
| HOẶC Thuốc kháng 5-HT3$ | ||
| Nguy cơ rất thấp (<10%) | Không cần dự phòng | |
| Thuốc ung thư đường uống | ||
| Trung bình và cao | Thuốc kháng 5-HT3$ | |
| Thấp và rất thấp | Không cần dự phòng | |
| Chú thích:
*: Nếu thuốc kháng NK-1 sử dụng là aprepitant thì ngày 2, 3 dùng thêm aprepitant #: ondansetron hoặc granisetron hoặc dolasetron. Không cần thiết nếu ngày 1 dùng Palonosetron. $: ondansetron hoặc granisetron hoặc dolasetron |
||
Bảng 3.PL4.12. Chế độ liều của thuốc chống nôn trong kiểm soát tác dụng phụ gây nôn, buồn của thuốc điều trị ung thư
| Phân loại thuốc chống nôn | Thuốc | Liều | Một số lưu ý khi sử dụng |
| Kháng 5-HT3 | Dolasetron | Một lần 100 mg tĩnh mạch hoặc 200 mg uống | + Hiệu quả của đường uống và đường tiêm như nhau
+ Hiệu quả của liều đơn và đa liều như nhau trong kiểm soát nôn cấp + Không thực sự hiệu quả trong kiểm soát nôn muộn + Độc tính trên tim: Kéo dài khoảng QT hoặc PR + Liều đơn tĩnh mạch tối đa của ondansetron là 16 mg |
| Granisetron | HEC: một lần 1-3 mg tĩnh mạch hoặc 2 mg uống MEC: một lần 1 mg tĩnh mạch hoặc 2 mg uống | ||
| Ondansetron | HEC: 1-4 liều 8 mg tĩnh mạch hoặc 2-3 liều 8 mg uống
MEC: một liều 8 mg tĩnh mạch hoặc 2 liều 8 mg uống |
||
| Palonosetron | Một liều 0,25 mg tĩnh mạch | + Hiệu quả hơn các thuốc kháng 5-HT3 thế hệ I.
+ Lựa chọn trong phác đồ 3 thuốc không chứa thuốc kháng NK1 để dự phòng nguy cơ nôn cao và trung bình + Sau khi dùng palonosetron, các thuốc kháng 5-HT3 thế hệ 1 có ít vai trò trong việc kiểm soát nôn muộn |
|
| Kháng NK-1 | Aprepitant | HEC: Ngày 1 (125 mg uống), ngày 2 và 3 (80 mg uống)
MEC: như HEC, từ chu kỳ 1 cho AC hoặc khi nhiều yếu tố nguy cơ tồn tại |
|
| Fosaprepitant | Ngày 1 : 115 mg tĩnh mạch, ngày 2 và ngày 3: 80 mg uống | ||
| Glucocorticoid | Dexamethason | Khi phối hợp kháng NK1: HEC: Ngày 1 (12 mg tĩnh mạch hoặc uống), ngày 2-4 (8 mg tĩnh mạch hoặc uống) MEC: Ngày 1 ( 12 mg tĩnh mạch hoặc uống), ngày 2-3 (8 mg tĩnh mạch hoặc uống) đối với phác đồ nôn muộn
Khi không phối hợp kháng NK1: HEC: Ngày 1 ( 20 mg tĩnh mạch hoặc uống), ngày 2-4 (8 mg tĩnh mạch hoặc uống, 2 lần mỗi ngày) MEC: Ngày 1 ( 8 mg tĩnh mạch hoặc uống), ngày 2-3 (8 mg tĩnh mạch hoặc uống 2 lần mỗi ngày) đối với phác đồ nôn muộn |
+ Hiệu quả rõ ràng trong kiểm soát nôn cấp và nôn muộn
+ Có thể giảm liều hoặc không dùng nếu phác đồ đã chứa steroid + Bệnh nhân không dung nạp dexamethason, có thể thay thế bằng olanzapin + Thận trọng với nguy cơ tăng đường huyết ở bệnh nhân tiểu đường |
| Olanzapin | 10mg/ngày (5mg/ngày với bệnh nhân có gặp nhiều tác dụng phụ) | + Phác đồ phối hợp 3 thuốc hoặc 4 thuốc cho nguy cơ nôn cao và trung bình
+ Hiệu quả hơn metoclopramid trong kiểm soát nôn bộc phát + Tác dụng phụ: ức chế thần kinh trung ương, kéo dài khoảng QT + Thận trọng ở người cao tuổi, người suy nhược + Thận trọng khi kê cùng haloperidol hay metoclopramid + Chống chỉ định phối hợp với benzodiazepin |
|
| Metoclopramid | 10 – 20 mg mỗi 6 giờ | + Tác dụng phụ: gây rối loạn vận động, kéo dài khoảng QT, tăng nhu động ruột
+ Tránh dùng đồng thời với olanzapin, phenothiazin, haloperidol + Thận trọng: bệnh nhân cao tuổi, cơ thể suy nhược |
|
| Chú thích:
HEC: hóa trị gây buồn nôn/nôn tỷ lệ cao; MEC: hóa trị gây buồn nôn/nôn tỷ lệ trung bình AC: anthracyclin và cyclophosphamid |
|||
Phụ lục 4.13. Tác dụng không mong muốn gây tiêu chảy của một số thuốc hoá trị và xử trí
Tiêu chảy là tác dụng không mong muốn thường gặp của nhiều tác nhân hóa điều trị. Hầu hết các trường hợp gặp tiêu chảy thường không nghiêm trọng; nhưng một số trường hợp cần phải giảm liều, thậm chí đe dọa tính mạng.
❖ Một số tác nhân hóa trị gây tiêu chảy
5-Fluouracil (5-FU)
Thuốc 5-FU làm hạn chế phân bào của các tế bào tiết dịch, dẫn đến tăng tỷ lệ các tế bào tiết dịch chưa trưởng thành so với tế bào ruột non trưởng thành có nhung mao. Thể tích dịch tại ruột non tăng vượt quá khả năng hấp thụ của đại tràng, dẫn đến tiêu chảy. 5-FU dùng tiêm bolus gây tiêu chảy nhiều hơn truyền tĩnh mạch kéo dài. Chế độ liều theo tuần gây tiêu chảy nhiều hơn chế độ liều theo tháng. Tiêu chảy thường gặp nhiều nhất khi dùng kết hợp 5-FU với leucovorin. Hay gặp ở nữ nhiều hơn nam, nguyên nhân có thể do thiếu hụt men dihydropyrimidin dehydrogenase (DPYD), men đầu tiên trong chuỗi ba men tham gia vào quá trình chuyển hóa 5-FU.
Irinotecan
Thuốc irinotecan thường gây ra tiêu chảy cấp tính (ngay sau khi dùng thuốc) hoặc tiêu chảy muộn. Tác dụng phụ này là do irinotecan có cấu trúc tương tự acetylcholin. Tuy nhiên, tiêu chảy muộn lại không phải do giải phóng acetylcholin mà do sự kết hợp của nhiều yếu tố gây mất nhu động ruột và các yếu tố kích thích bài tiết gây độc tính trực tiếp cho niêm mạc ruột. Tiêu chảy muộn thường xảy ra ít nhất 24 giờ sau khi dùng thuốc, có thể đe dọa tính mạng; đặc biệt trong phác đồ phối hợp với 5-FU và leucovorin. Liều mỗi 3 tuần gây tiêu chảy nhiều hơn liều hàng tuần.
Capecitabin
Thuốc capecitabin là tiền chất của 5-FU, khi dùng liều thông thường 2.000mg/m2/ngày trong 14 ngày chu kỳ 21 ngày có nguy cơ tiêu chảy trên 30-40% bệnh nhân (mức độ nghiêm trọng 10-20% bệnh nhân).
Một số tác nhân khác
Taxan: Tỷ lệ tiêu chảy của docetaxel 19-47%; Tiêu chảy độ 3 từ 0-27%, đặc biệt bệnh nhân trên 65 tuổi. Paclitaxel liều 175-225 mg/m2 tỷ lệ xảy ra tiêu chảy khoảng 39% (3% ở mức độ 3 và 4); còn liều hàng tuần khoảng 3-7% tiêu chảy ở mức độ 3.
Anthracyclin: Với dạng anthracyclin thông thường, tiêu chảy xảy ra không phổ biến (khoảng 15%) nhưng ở dạng doxorubicin liposome, tiêu chảy lên đến 45%, trong đó 3% ở mức độ 3-4, đặc biệt chủ yếu ở người cao tuổi.
Tần suất và mức độ tiêu chảy và hướng dẫn kiểm soát tác dụng không mong muốn này của một số tác nhân hóa trị được trình bày trong bảng 1.PL4.13, 2.PL4.13 và hình 1.PL4.13.
Bảng 1.PL4.13. Tần suất gặp tiêu chảy ở mức độ 3 và 4 của một số thuốc hóa trị
| STT | Tác nhân hóa điều trị | Tỷ lệ gặp mức độ 3 Và 4 (%) |
| 1 | CapeIRI (capecitabin/irinotecan) | 47 |
| 2 | FOLFOXIRI (fluorouracil/leucovorin/oxaliplatin/irinotecan) | 20 |
| 3 | mIFL (irinotecan/fluorouracil) | 19 |
| 4 | Bolus fluorouracil và acid folinic | 16 |
| 5 | Irinotecan và fluorouracil và acid folinic | 15 |
| 6 | Docetaxel và capecitabin | 14 |
| 7 | FOLFIRI (fluorouracil/leucovorin/irinotecan) | 14 |
| 8 | FLOX (fluorouracil/leucovorin/oxaliplatin) | 10 |
Tần suất và mức độ tiêu chảy của một số tác nhân nhắm trúng đích được trình bày trong bảng 2.PL4.13.
Bảng 2.PL4.13. Tần suất và mức độ tiêu chảy của một số tác nhân nhắm trúng đích
| STT | Phân nhóm | Hoạt chất | Tỷ lệ tiêu chảy (%) | Tỷ lệ tiêu chảy mức độ 3 và 4 (%) |
| 1 | Kháng EGFR | Gefinitib | 26-52 | 1-5 |
| Erlotinib | 18-57 | 3-6 | ||
| Afatinib | 18-57 | 3-6 | ||
| Cetuximab | 13-28 | 4-28 | ||
| Panitumumab | 21 | 8-20 | ||
| 2 | Kháng HER2 | Lapatinib | 47-75 | 3-14 |
| Trastuzumab | 2-63 | 2-6 | ||
| Pertuzumab | 67 | 5-8 | ||
| 3 | Kháng VEGF | Bevacizumab | 20 | 2-7 |
| Aflibercept | 58-69 | 13-19 | ||
| 4 | Ức chế tyrosin kinase nhiều đích | Imatinib | 20-26 | 1 |
| Pazopanib | 52 | 4 | ||
| Sunitinib | 44-55 | 5-8 | ||
| Sorafenib | 43-55 | 2-8 | ||
| Regorafenib | 34-40 | 5-8 | ||
| Cabozantinib | 64 | 12 | ||
| 5 | Kháng mTOR | Everolimus | 30 | 1-3 |
| Temsirolimus | 27 | 1 |
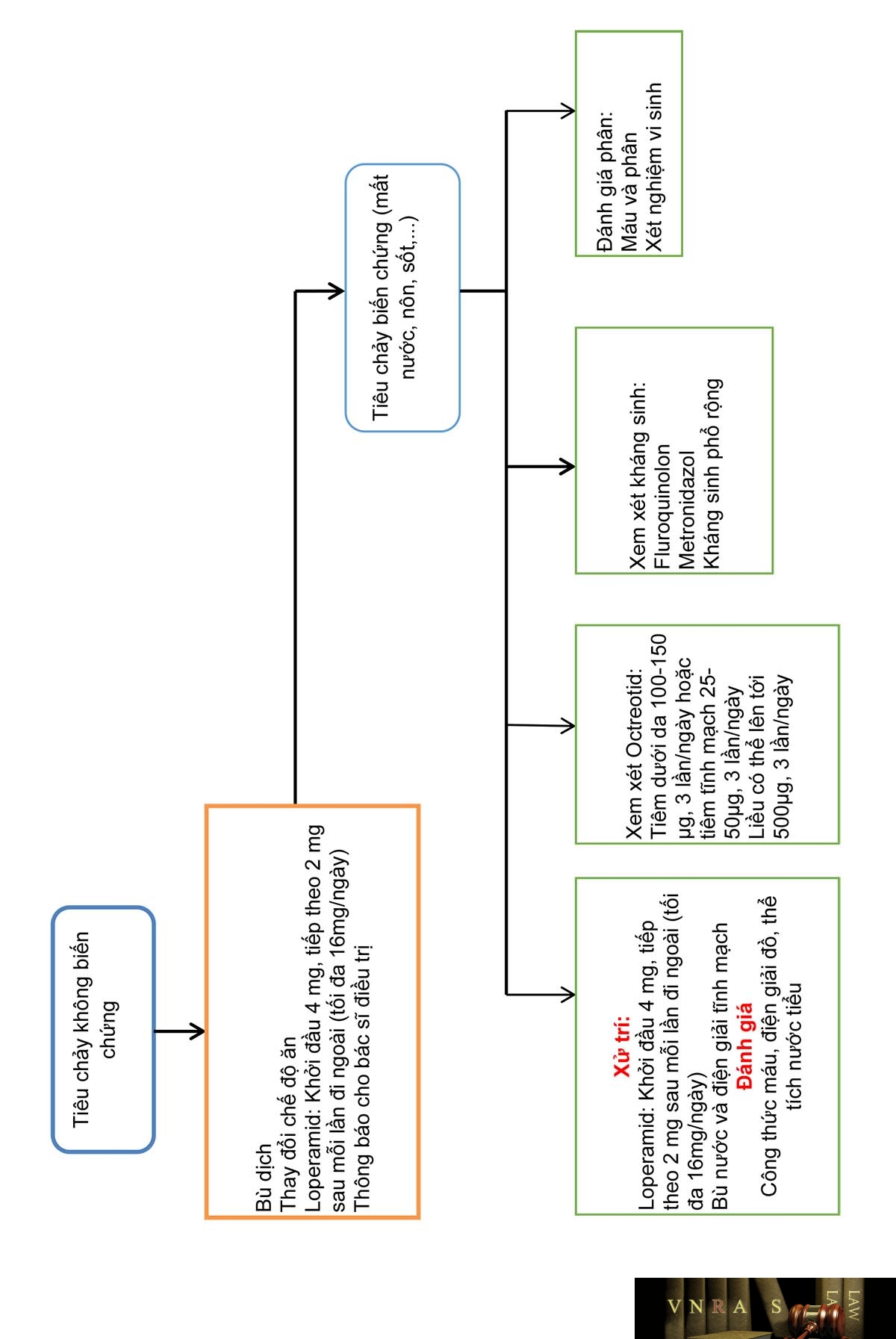
Phụ lục 4.14. Tác dụng không mong muốn gây thoát mạch và quy trình xử trí thoát mạch của các thuốc điều trị ung thư
- Thoát mạch
Triệu chứng lâm sàng
– Xuất hiện ngay sau khi thuốc bị thoát mạch, nhưng có thể xuất hiện muộn từ một ngày đến vài tuần.
– Ban đầu, thường biểu hiện tại chỗ là nóng rát hoặc tê bì, ban đỏ nhẹ, ngứa và sưng phồng.
– Trong vòng 2-3 ngày, ban đỏ và đau tăng lên, da đổi màu và chai cứng lại, bong vảy khô hoặc rộp lên cũng có thể xuất hiện.
– Nếu khối lượng dịch bị thoát mạch ít, các triệu chứng có thể biến mất trong vài tuần tiếp theo. Nếu thuốc thoát ra lan rộng, sâu thì đỏ da, đau, hoại tử, bong vảy và loét sẽ tăng lên; hoại tử vàng có thể xuất hiện sau vài tuần.
- Phân loại các tác nhân gây thoát mạch
Có thể phân loại các thuốc hóa trị thành ba nhóm dựa theo mức độ gây hoại tử mô khi thoát mạch:
- Nhóm chất không gây phỏng (non-vesicant): không gây loét; nếu có thoát mạch thì hiếm khi xảy ra các phản ứng cấp tính hoặc tiến triển thành hoạt tử.
- Nhóm chất gây kích thích (irritant): gây viêm hoặc đau tại vị trí thoát mạch. Một số chất kích thích cũng có thể gây loét, nhưng chỉ trong trường hợp một lượng thuốc rất lớn bị thoát vào mô.
- Nhóm gây phỏng (vesicant): khi bị thoát mạch có thể gây phồng rộp hoặc loét, thậm chí gây hoại tử mô hoặc lột da.
Bảng 1.PL4.14. Phân loại các tác nhân gây thoát mạch
| Nhóm chất gây phỏng | Nhóm chất gây kích thích | Nhóm chất không gây phỏng |
| – Các thuốc liên kết ADN
+ Doxorubicin + Epirubicin + Dactinomycin – Các thuốc không liên kết ADN + Vincristin + Vinorelbin |
– Cyclophosphamid
– Dacarbazin – Etoposid – Fluorouracil – Ifosfamid – Carboplatin – Cisplatin – Docetaxel – Irinotecan – Oxaliplatin – Paclitaxel – Topotecan |
– Bleomycin
– Etoposid – Gemcitabin – Methotrexat – Kháng thể đơn dòng |
* Các yếu tố nguy cơ gây thoát mạch
- Yếu tố liên quan tới bệnh nhân
+ Mạch máu nhỏ (trẻ em, trẻ sơ sinh,…)
+ Tĩnh mạch yếu (người cao tuổi, bệnh nhân ung thư’,…)
+ Tĩnh mạch cứng, xơ hóa
+ Vị trí tiêm tĩnh mạch bị di chuyển
+ Suy giảm tuần hoàn (vị trí đặt cannula bị u, phù hạch bạch huyết,.)
+ Bệnh mắc kèm (ĐTĐ, hội chứng Raynaud, tổn thương do xạ trị,.)
- Khó khăn khi báo cáo triệu chứng sớm
+ Không có khả năng báo cáo các cảm giác khó chịu (như bệnh nhân bị an thần, hôn mê,.)
+ Giảm/mất cảm giác (do kết quả từ bệnh thần kinh, ĐTĐ, bệnh mạch máu ngoại biên,…)
- Đặt đường truyền và quy trình tiêm truyền
+ Nhân viên chưa được đào tạo hoặc thiếu kinh nghiệm
+ Vị trí đặt đường truyền không phù hợp (ví dụ: mặt sau bàn tay, gần xương,…)
+ Chọc dò tĩnh mạch nhiều lần để đặt đường truyền
+ Tiêm bolus
+ Tốc độ truyền nhanh
- Trang thiết bị
+ Loại và kích thước catheter
+ Kim bướm
- Tác nhân điều trị
+ Khả năng liên kết với ADN
+ Khả năng diệt tế bào nhân lên
+ Khả năng gây giãn mô hoặc mạch máu
+ pH, áp suất thẩm thấu, dung môi pha loãng
* Các chất giải độc đặc hiệu đối với một số nhóm hóa điều trị
Trong trường hợp bị thoát mạch, có thể sử dụng một số chất giải độc đặc hiệu như trong Bảng 2.PL4.14.
Bảng 2.PL4.14. Các chất giải độc đặc hiệu đối với một số nhóm hóa điều trị
| Thuốc thoát mạch | Chất giải độc đặc hiệu | Cách sử dụng chất giải độc đặc hiệu |
| Các anthracyclin (doxorubicin, epirubicin)
|
Savene™ (dexrazoxan) | Hoàn nguyên Savene™ bằng 25 mL nước cất vô khuẩn, trước khi pha loãng với dịch truyền.
Truyền tĩnh mạch liên tục Savene™ (dexrazoxan) phong bế vị trí thoát mạch trong 3 ngày: + Ngày 1: 1.000mg/m2 càng sớm càng tốt, không muộn hơn giờ sau khi xảy ra thoát mạch. + Ngày 2: 1.000mg/m2. + Ngày 3: 500mg/m2. |
| DMSO tại chỗ (99%) | Thoa 1 lớp mỏng DMSO (dimethyl sulfoxid) (99%) vào vị trí thoát mạch càng sớm càng tốt, trong vòng 10-25 phút sau thoát mạch. Lặp lại mỗi 8 giờ x 7 ngày. | |
| Các alkaloid vinca | Hyaluronidase | Tiêm hyaluronidase trong vòng 1 giờ sau khi thoát mạch.
Pha loãng 150 – 1.500 IU hyaluronidase trong 1mL nước cất vô trùng. Tiêm dưới da (quanh vùng thoát mạch) 1mL hyaluronidase chia thành 5 lần tiêm (mỗi lần 0,2mL) xung quanh vị trí thoát mạch. |
| Các taxan | Hyaluronidase | Tiêm hyaluronidase trong vòng 1 giờ sau khi thoát mạch
Pha loãng 150 – 1.500 IU hyaluronidase trong 1mL nước cất vô trùng. Tiêm dưới da (quanh vùng thoát mạch) 1mL hyaluronidase chia thành 5 lần tiêm (mỗi lần 0,2mL) xung quanh vị trí thoát mạch. |
❖ Dự phòng biến chứng thoát mạch
Một số biện pháp phòng ngừa đơn giản có thể giảm thiểu khả năng thoát mạch là:
– Đối với đường truyền ngoại vi: nên chọn những đường truyền mới được đặt, lựa chọn các tĩnh mạch lớn, còn nguyên vẹn và máu phải trở lại kim tiêm truyền tốt trước khi bắt đầu truyền.
– Vị trí đặt đường truyền nên lựa chọn theo thứ tự ưu tiên sau: Cẳng tay (tĩnh mạch nền, tĩnh mạch đầu và tĩnh mạch giữa), mu bàn tay, cổ tay, hố trước khu u.
– Các kim bướm hoặc kim nhựa cần được cố định chặt bằng băng dính.
– Xác định sự thông của đường truyền bằng cách bơm 5-10mL natriclorid 0,9% hoặc glucose 5%.
– Nên sử dụng catheter tĩnh mạch trung tâm.
– Cần pha loãng các thuốc hóa chất, nên truyền vào tĩnh mạch ở cẳng tay. Sau khi truyền hóa chất nên truyền tiếp dung dịch natri clorid 0,9% hoặc glucose 5%. Trong quá trình truyền, nên theo dõi chặt dấu hiệu đau (thường được mô tả như cảm giác nóng rát chạy dọc theo tĩnh mạch) và kiểm tra biểu hiện ban đỏ và sưng.
❖ Quy trình xử trí thoát mạch hóa trị trên bệnh nhân ung thư
Quy trình xử trí thoát mạch hóa trị trên bệnh nhân ung thư được trình bày trong sơ đồ dưới đây:
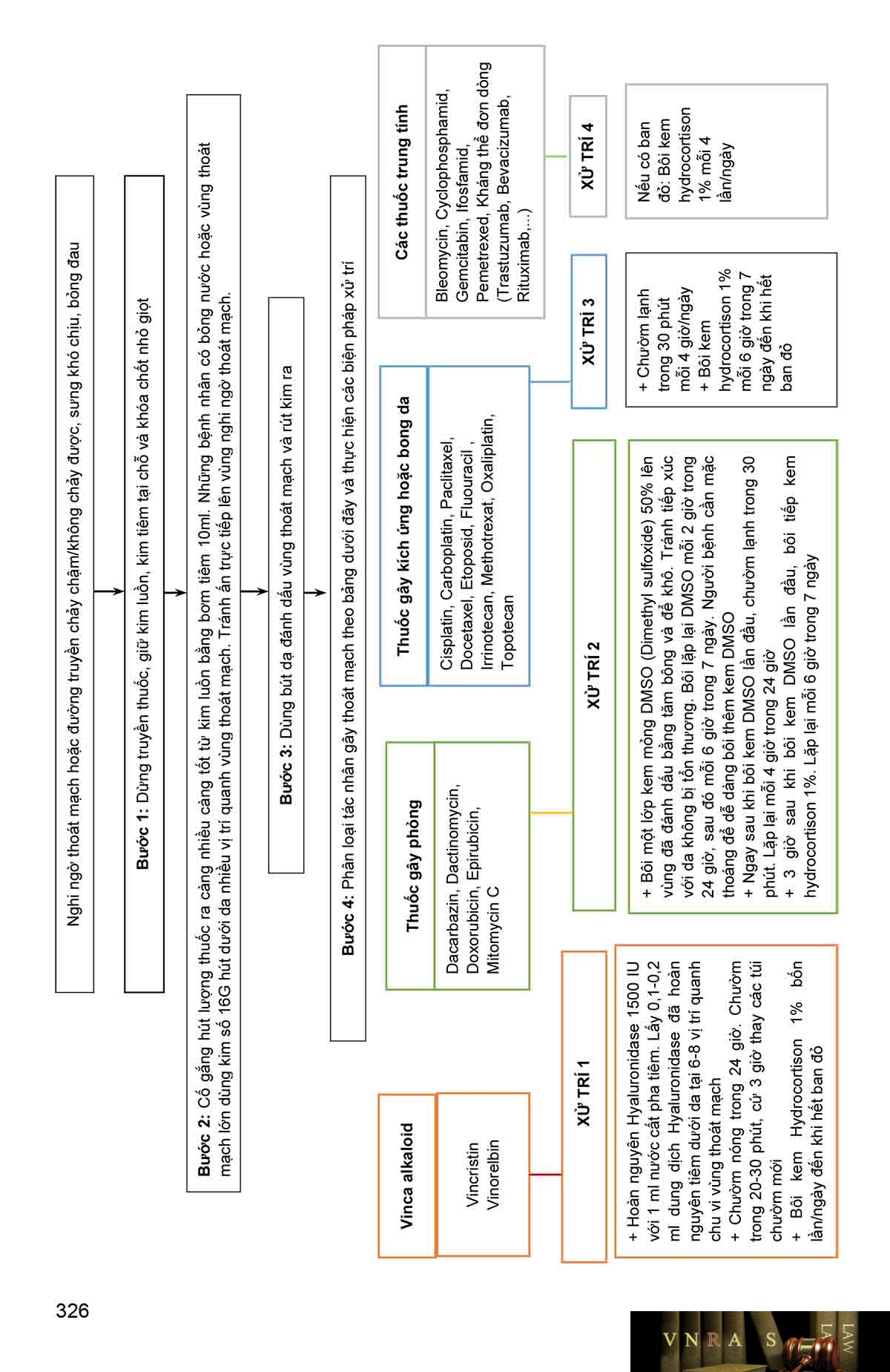
Phụ lục 4.15. Sốt và giảm bạch cầu trung tính trên bệnh nhân sử dụng hóa trị
❖ Nguy cơ sốt do giảm bạch cầu theo phác đồ hóa trị
Bảng 1.PL4.15. Nguy cơ sốt do giảm bạch cầu theo phác đồ hóa trị
| Loại ung thư | Nguy cơ >20% | Nguy cơ (10-20%) |
| Ung thư vú | ❖ Doxorubicin + cyclophosphamid + paclitaxel
❖ TAC (Docetaxel, doxorubicin, cyclophosphamid ❖ TC (Docetaxel, cyclophosphamid) ❖ TCH (Docetaxel, carboplatin, trastuzumab) |
Docetaxel mỗi 3 tuần
Paclitaxel mỗi 3 tuần CMF (Cyclophosphamid, methotrexat, fluoroceracil) AC ->T (Doxorubicin, cyclophosphamid, docetaxel) FEC + T (fluoroceracil, epirubicin, cyclophosphamid, docetaxel) |
| Ung thư phổi tế bào nhỏ | Topotecan | Etoposid/carboplatin |
| Ung thư phổi không tế bào nhỏ | Cisplatin/Paclitaxel Cisplatin/Vinorelbin Cisplatin/Etoposid Cisplatin/Docetaxel Carboplatin/Paclitaxel Docetaxel | |
| Ung thư đại trực tràng | FOLFOX (fluoroceracil, leucovorin, oxaliplatin) | |
| Ung thư bàng quang | MVAC (Methotrexat, vinblastin, doxorubicin, cisplatin) | |
| Ung thư lympho Hodgkin | BEACOPP (Bleomycin, etoposid, doxorubicin, cyclophosphamid, vincristin, procarbazin, prednison) | |
| Ung thư thận | Doxorubicin/gemcitabin | |
| Ung thư lympho không Hodgkin | EPOCH (Etoposid, prednison, vincristin, cyclophosphamid, doxorubicin)
ICE (Ifosfamid, carboplatin, etoposid) CHOP-14 (Cyclophosphamid, doxorubicin, vincristin, prednison) MINE (Mesna, ifosfamid, mitoxantron, etoposide) DHAP (Dexamethason, cisplatin, cytarabin) ESHAP (Etoposid, methylprednisolon, cisplatin, cytarabin) CVAD liều cao (Cyclophosphamid, vincristin, doxorubicin, dexamethason) |
GDP (Gemcitabin, dexamethason, cisplatin/carboplatin)
CHOP (Cyclophosphamid, doxorubicin, vincristin, prednison), bao gồm cả phác đồ với doxorubicin dạng liposome |
| U hắc tố ác tính | Dacarbazin, cisplatin, vinblastin, interleukin-2, interferon alpha | |
| Ung thư buồng trứng | Topotecan
Docetaxel |
Carboplatin/Docetaxel |
| Sarcoma phần mềm | MAID (mesna, doxorubicin, ifosfamid, dacarbazin)
Doxorubicin Ifosfamid/doxorubicin |
|
| Ung thư tinh hoàn | VelP (vinblastin, ifosfamid, cisplatin)
VIP (etoposid, ifosfamid, cisplatin) BEP (bleomycin, etoposid, cisplatin) TIP (paclitaxel, ifosfamid, cisplatin) |
Etoposid/cisplatin |
| Ung thư cổ tử cung | Cisplatin/topotecan
Paclitaxel/cisplatin Topotecan Irinotecan |
|
| Ung thư thực quản và dạ dày | Irinotecan/cisplatin
Epirubicin/cisplatin/fluouracil Epirubicin/cisplatin/capecitabin |
❖ Dự phòng yếu tố kích thích tăng sinh dòng bạch cầu hạt (Granulocyte colony simulating factor_G-CSF) trên bệnh nhân có giảm bạch cầu do hóa trị
Đánh giá bệnh nhân cho việc sử dụng dự phòng G-CSF
Đánh giá bệnh nhân cho việc sử dụng dự phòng G-CSF theo sơ đồ dưới đây:
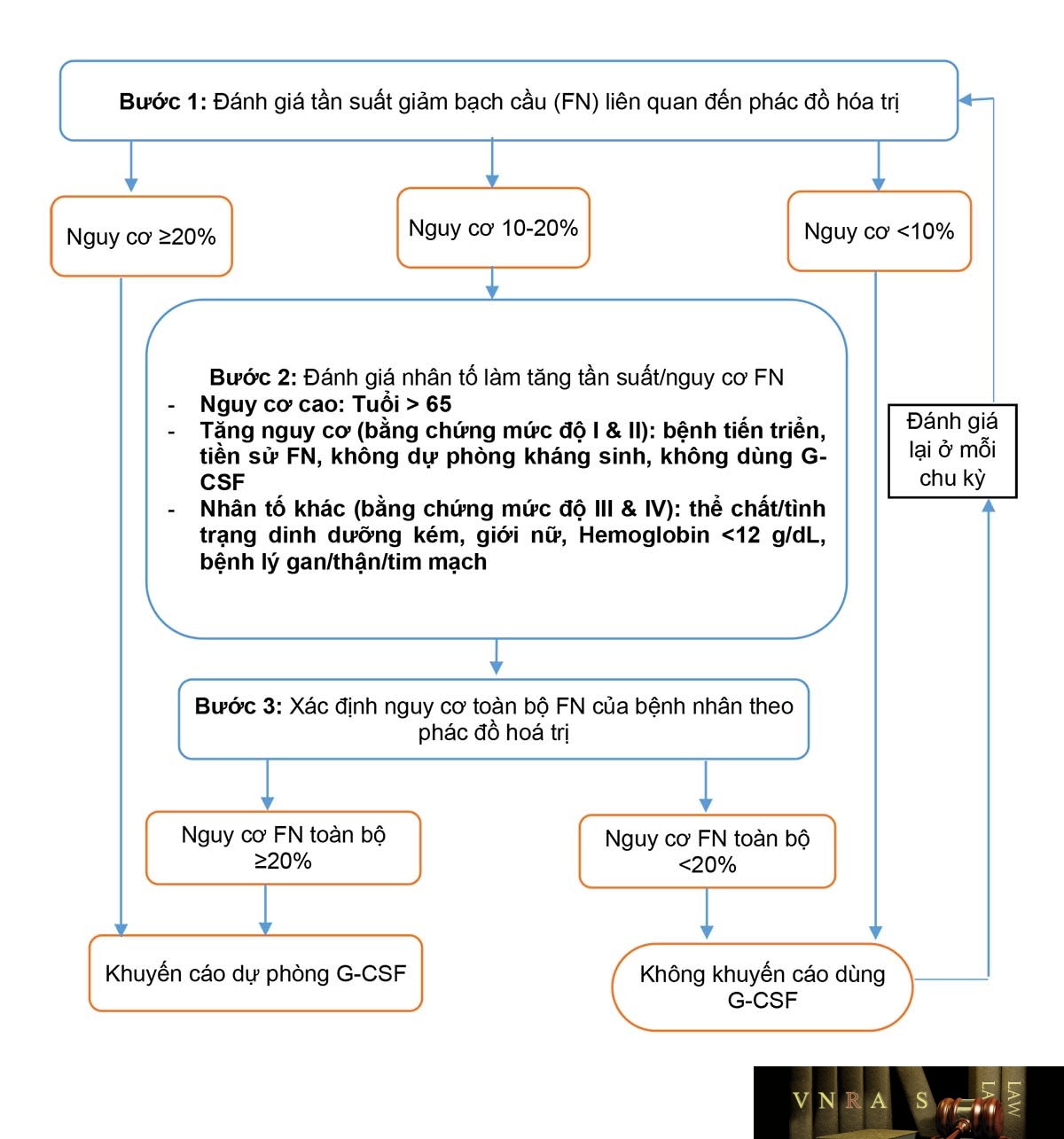
Các thuốc tăng sinh bạch cầu
Filgrastim
– Filgrastim là một yếu tố kích thích tăng sinh dòng bạch cầu hạt (G-CSF: Granulocyte colony stimulating factor).
– Nhược điểm: phải dùng hàng ngày, kéo dài cho đến khi số lượng bạch cầu hạt về giá trị bình thường.
– Dự phòng nguyên phát: Dùng G-CSF trong chu kỳ hóa trị đầu tiên ở bệnh nhân được đánh giá là có nguy cơ cao xảy ra FN.
– Dự phòng thứ phát: Dùng G-CSF trong tất cả chu kỳ hóa trị tiếp theo khi bệnh nhân đã có tiền sử biến cố FN hoặc phải giảm/hoãn liều do giảm bạch cầu.
– Điều trị: Dùng CSFs cho FN như liệu pháp hỗ trợ kháng sinh ở bệnh nhân hóa điều trị có phát triển biến chứng liên quan nhiễm trùng (biến chứng sốt do hạ bạch cầu).
– Liều dùng và cách dùng: Liều hàng ngày 5 mcg/kg tiêm dưới da (thường dùng) hoặc truyền tĩnh mạch đến khi bạch cầu phục hồi về mức bình thường hay gần bình thường theo tiêu chuẩn.
Pegfilgrastim
– Gắn thêm 1 phân tử PEG để kéo dài thời gian bán hủy. Chỉ dùng một liều dưới da 24 giờ sau hóa trị.
– Chỉ dùng trong dự phòng.
– Liều dùng và cách dùng: Một lần duy nhất mỗi chu kỳ, liều 6 mg tiêm dưới da (thường dùng) vào ngày kết thúc hóa trị.
❖ Nhiễm khuẩn trên bệnh nhân ung thư có giảm bạch cầu trung tính
Chẩn đoán nhiễm khuẩn trên ung thư có giảm bạch cầu
❖ Lâm sàng
Sốt là dấu hiệu nhiễm khuẩn thường gặp và xuất hiện sớm trên bệnh nhân giảm bạch cầu trung tính. Sốt do giảm bạch cầu được định nghĩa là sốt ở những bệnh nhân giảm bạch cầu khi đo nhiệt độ 3 lần ở miệng trong 24 giờ là > 38,0 0C (100,4 0F) hoặc một lần đo có nhiệt độ ≥38,5 0C (101,3 0F).
Kiểm tra thường xuyên tất cả vị trí nhiễm khuẩn phổ biến trên bệnh nhân ung thư có giảm bạch cầu trung tính bao gồm: miệng, họng-xoang, mũi, đường hô hấp, đường tiêu hóa, đường tiết niệu, da, mô mềm, vùng đáy chậu và vị trí đặt catheter.
Cần lưu ý dấu hiệu nhiễm khuẩn trên bệnh nhân giảm bạch cầu trung tính có thể bị che lấp do số lượng bạch cầu thấp dẫn đến khả năng đáp ứng viêm kém. Trong một số trường hợp như sốc nhiễm khuẩn hoặc điều trị bằng corticoid, bệnh nhân có nhiễm khuẩn nhưng không sốt, thậm chí thân nhiệt lại giảm.
❖ Cận lâm sàng
Giảm bạch cầu được định nghĩa là lượng bạch cầu trung tính tuyệt đối < 1.000/mcL (tương đương với < 1,0×109/L), giảm bạch cầu nặng khi lượng bạch cầu trung tính tuyệt đối < 500/mcL (tương đương với < 0,5×109/L) và giảm bạch cầu rất nặng khi < 100/^L (tương đương với < 0,1×109/L). Giảm bạch cầu > 7 ngày được gọi là giảm bạch cầu kéo dài.
Cấy máu ít nhất 2 lần (bao gồm cả vị trí đặt catheter).
Cấy các bệnh phẩm khác tại vị trí khác nếu có dấu hiệu nhiễm khuẩn.
Xét nghiệm huyết học và hóa sinh: hồng cầu, tiểu cầu, ure, điện giải, hóa sinh gan, thận.
Xét nghiệm chẩn đoán khác: chụp X-quang, chọc hút và sinh thiết tổn thương da, đo phân áp oxy khi có dấu hiệu bệnh hô hấp hoặc thở nhanh…
Phân tầng nguy cơ nhiễm khuẩn trên bệnh nhân sốt có giảm bạch cầu trung tính
Bảng 2.PL4.15. Phân tầng nguy cơ nhiễm khuẩn ở bệnh nhân sốt có giảm bạch cầu trung tính
| Nguy cơ cao | Nguy cơ thấp |
| ❖ MASCC < 21
❖ Giảm bạch cầu trung tính: thời gian giảm bạch cầu > 7 ngày hoặc ANC <100/mcL ❖ Lâm sàng không ổn định ❖ Bệnh phối hợp ❖ Suy giảm chức năng thận ❖ Suy giảm chức năng gan ❖ Các bệnh lý khác kèm theo ❖ Cường độ phác đồ ức chế miễn dịch ❖ Tuổi cao |
❖ MASCC ≥ 21
❖ Thời gian giảm bạch cầu ≤ 7 ngày ❖ Lâm sàng ổn định ❖ Không có bệnh phối hợp |
Bảng 3.PL4.15. Thang điểm MASCC (Multinational Association for Supportive Care in Cancer)
| Đặc điểm | Điểm |
| Mức độ triệu chứng
• Không có triệu chứng hoặc triệu chứng nhẹ • Triệu chứng trung bình |
5 3 |
| Không có tăng HA | 5 |
| Không có bệnh phổi tắc nghẽn mạn tính | 4 |
| U đặc hoặc không có nhiễm nấm trước đó | 4 |
| Không mất nước | 3 |
| Bệnh nhân ngoại trú | 3 |
| Tuổi < 60 | 2 |
❖ Phác đồ kháng sinh kinh nghiệm trên bệnh nhân giảm bạch cầu trung tính
Dự phòng nhiễm khuẩn
Trước khi xem xét dự phòng kháng sinh, bệnh nhân được phân tầng nguy cơ nhiễm khuẩn ở 3 mức là thấp, trung bình và cao dựa trên bệnh lý nền, tình trạng bệnh, thời gian giảm bạch cầu trung tính, phác đồ hóa trị và cường độ phác đồ ức chế miễn dịch.
Bệnh nhân có nguy cơ nhiễm khuẩn trung bình và cao được khuyến cáo dự phòng đơn độc bằng phác đồ fluoroquinolon (levofloxacin hoặc ciprofloxacin). Ưu tiên levofloxacin trong trường hợp có nguy cơ nhiễm khuẩn niêm mạc liên quan đến vi khuẩn nhóm Streptococcal viridans xâm lấn. Nếu bệnh nhân không dung nạp với fluoroceracil, có thể sử dụng cotrimoxazol.
Điều trị nhiễm khuẩn
Sau khi phân tầng nguy cơ các biến chứng nhiễm khuẩn dựa trên thời điểm sốt, thời gian và mức độ giảm bạch cầu trung tính, điểm ECOG (định nghĩa như bảng 4.PL4.15), điểm MASCC (định nghĩa như bảng 2.PL4.15), chức năng gan, thận, bệnh lý cấp tính mắc kèm, phác đồ điều trị và tình trạng bệnh lý nền, bệnh nhân được điều trị như sau:
Đối với bệnh nhân nguy cơ thấp:
Bệnh nhân ngoại trú: sử dụng kháng sinh đường uống với phác đồ phối hợp ciprofloxacin/amoxicillin-acid clavulanic hoặc ciprofloxacin/clindamycin nếu bệnh nhân dị ứng penicillin hoặc phác đồ đơn độc moxifloxacin hoặc levofloxacin. Có thể sử dụng phác đồ kháng sinh đường tĩnh mạch.
Bệnh nhân nội trú: sử dụng kháng sinh đường uống với phác đồ phối hợp ciprofloxacin/amoxicillin-acid clavulanic hoặc ciprofloxacin/clindamycin nếu bệnh nhân dị ứng penicillin hoặc phác đồ đơn độc moxifloxacin.
Bệnh nhân cũng có thể sử dụng phác đồ kháng sinh đường tĩnh mạch như bệnh nhân nguy cơ cao.
Chỉ sử dụng phác đồ đường uống cho bệnh nhân không buồn nôn/nôn, dung nạp tốt và không được dự phòng bằng fluoroquinolon trước đó. Moxifloxacin không có tác dụng trên Pseudomonas aeruginosa nên không sử dung moxifloxacin trong trường hợp nghi ngờ nhiễm Pseudomonas aeruginosa.
Đối với bệnh nhân nguy cơ cao:
Sử dụng kháng sinh đường tĩnh mạch: Sử dụng phác đồ đơn độc piperacillin- tazobactan, carbapenem; ceftazidim hoặc cefepim.
Phối hợp thêm kháng sinh vào phác đồ khuyến cáo trong các trường hợp sau:
– Trường hợp nghi ngờ nhiễm Pseudomonas aeruginosa (ví dụ tiền sử nhiễm Pseudomonas aeruginosa): phối hợp các kháng sinh nhạy cảm trên Pseudomonas aeruginosa
– Bệnh nhân có lâm sàng không ổn định: Phối hợp P-lactam phổ rộng (meropenem, piperacillin-tazobactan, imipenem-cilastatin) với aminoglycosid và vancomycin.
– Thêm vancomycin vào phác đồ điều trị kinh nghiệm trong các trường hợp: có biểu hiện lâm sàng rõ ràng của nhiễm khuẩn nghiêm trọng liên quan đến đặt catheter tĩnh mạch; cấy máu dương tính với vi khuẩn gram dương trước khi làm kháng sinh đồ; đã biết có Pneumococci kháng penicillin/cephalosporin hoặc MRSA (Methicillin- resistant Staphylococcus aureus); bệnh nhân có lâm sàng không ổn định (hạ HA hoặc sốc) và đang chờ kết quả cấy máu; nhiễm khuẩn da/mô mềm (đặc biệt các nơi nhiễm khuẩn do MRSA là phổ biến). Trong trường hợp nhiễm vi khuẩn kháng vancomycin hoặc bệnh nhân không dùng được vancomycin: dùng linezolid hoặc daptomycin.
Điều chỉnh phác đồ kháng sinh theo vị trí nhiễm khuẩn, hình ảnh X quang và/hoặc kháng sinh đồ (nếu có):
Thâm nhiễm phổi: thêm azithromycin hoặc fluoroquinolon để bao phủ vi khuẩn không điển hình. Cân nhắc thêm vancomycin hoặc linezolid nếu nghi ngờ nhiễm MRSA.
Nếu có biến chứng như hạ HA và viêm phổi hoặc nghi ngờ vi khuẩn kháng thuốc: thêm aminoglycosid hoặc fluoroquinolon và/hoặc vancomycin.
Nếu có viêm phổi hoặc nhiễm khuẩn huyết do vi khuẩn gram âm: thêm vancomycin hoặc chuyển sang carbapenem nếu trước đó chưa dùng carbapenem..
Nhiễm khuẩn xoang/mũi: thêm kháng sinh tác dụng trên vi khuẩn gram dương nếu viêm mô tế bào quanh mắt do nhiễm khuẩn xoang/mũi mở rộng.
Nhiễm khuẩn tại miệng/niêm mạc miệng: nếu có loét/hoại tử, cần đảm bảo phác đồ điều trị có phổ trên vi khuẩn kị khí.
Nhiễm khuẩn tại da/mô mềm: thêm kháng sinh tác dụng trên vi khuẩn gram dương.
Đau vùng bụng: Nếu nghi ngờ nhiễm Clostridium difficile, thêm vancomycin (ưu tiên) hoặc fidaxomicin hoặc metronidazol. Đảm bảo phác đồ điều trị có phổ trên vi khuẩn kị khí.
Tiêu chảy: thêm vancomycin (ưu tiên) hoặc fidaxomicin hoặc metronidazol nếu nghi ngờ hoặc xác định nhiễm Clostridium difficile.
Đau quanh trực tràng: đảm bảo phác đồ điều trị có phổ trên vi khuẩn kị khí. Cân nhắc sử dụng kháng sinh tác dụng trên Enterococci.
Đặt các thiết bị can thiệp mạch: thêm kháng sinh tác dụng trên vi khuẩn gram dương ngay khi bắt đầu hoặc sau 48 giờ khi không đáp ứng.
Mụn sẩn/các dạng tổn thương khác: thêm kháng sinh tác dụng trên vi khuẩn gram dương.
Các triệu chứng trên thần kinh trung ương: phác đồ kháng sinh ban đầu dựa trên kết quả hội chẩn. Nếu nghi ngờ viêm màng não, sử dụng phác đồ phối hợp kháng sinh P- lactam có tác dụng trên Pseudomonas aeruginosa (cefepim, ceftazidim, meropenem) với vancomycin và ampicillin (để bao phủ Listeriosis). Nếu dùng meropenem thì không cần phối hợp ampicillin.
Nếu bệnh nhân có nguy cơ nhiễm vi khuẩn kháng thuốc như huyết động không ổn định hoặc cấy máu dương tính hoặc có nguy cơ tiếp xúc với vùng lưu hành vi khuẩn kháng thuốc:
- Nếu nghi ngờ nhiễm tụ cầu vàng kháng methicillin (MRSA): thêm vancomycin, linezolid hoặc daptomycin.
- Nếu nghi ngờ nhiễm cầu khuẩn ruột kháng Vancomycin (VRE): thêm linezolid hoặc daptomycin.
- Nếu nghi ngờ nhiễm chủng tiết men beta-lactamase phổ rộng (ESBL): dùng phác đồ carbapenem (meropenem hoặc imipenem-cislastatin).
- Nếu nghi ngờ nhiễm Klebsiella sinh carbapenemases (KPCs): dùng colistin hoặc tigecyclin.
Bệnh nhân dị ứng penicillin có dung nạp cephalosporin nhưng có tiền sử phản ứng quá mẫn mức trung bình như phát ban, co thắt phế quản thì tránh dùng P-lactam. Có thể thay thế bằng phác đồ phối hợp ciprofloxacin/clindamycin hoặc aztreonam/vancomycin.
❖ Thời gian điều trị kháng sinh
- Nếu xác định được ổ nhiễm trùng gây triệu chứng sốt, kháng sinh cần được dùng theo thời gian tương ứng với tác nhân gây bệnh cụ thể và vị trí nhiễm trùng (có thể kéo dài 7-10 ngày, thậm chí 14 ngày).
- Trong trường hợp không rõ nguồn gốc nhiễm trùng, thời điểm ngừng thuốc kháng sinh thường phụ thuộc vào tình trạng giảm sốt và giảm bạch cầu. Nên ngừng thuốc kháng sinh nếu số lượng bạch cầu đa nhân trung tính tăng đến > 500/^1 và bệnh nhân hết sốt.
- Đối với bệnh nhân không rõ ổ nhiễm trùng, đã hạ sốt nhưng vẫn trong tình trạng giảm bạch cầu, kéo dài điều trị tới 14 ngày đồng thời theo dõi sát sao khi ngừng kháng sinh.
– Đối với bệnh nhân xác định được ổ nhiễm trùng và lâm sàng đáp ứng với điều trị kháng sinh, nên chuyển đổi đường dùng từ đường tiêm sang uống thích hợp để hoàn thành quá trình điều trị.
Bảng 4.PL4.15. Chỉ số tình trạng chức năng toàn thân
| Điểm | EOCG |
| 0 | Hoàn toàn không có triệu chứng gì |
| 1 | Có triệu chứng nhưng vẫn đi lại được dễ dàng |
| 2 | Có triệu chứng và nằm giường < 50% thời gian trong ngày |
| 3 | Có triệu chứng và nằm giường > 50% thời gian nhưng không liệt giường |
| 4 | Liệt giường |
| 5 | Tử vong |
Phụ lục 4.16. Thiếu máu và điều trị thiếu máu do hóa trị
Thiếu máu và thiếu sắt là biến chứng thường gặp trên bệnh nhân có khối u rắn hoặc bệnh ác tính huyết học, đặc biệt trên bệnh nhân sử dụng hóa trị. Thiếu máu liên quan đến các triệu chứng mệt mỏi, suy giảm thể chất, chất lượng cuộc sống và thời gian sống còn toàn bộ.
❖ Nguy cơ gây thiếu máu của tác nhân/phác đồ hóa trị
Nguy cơ gây thiếu máu của tác nhân/phác đồ hóa trị được trình bày trong bảng sau:
Bảng 1.PL4.16. Tỷ lệ thiếu máu liên quan đến tác nhân phác đồ hóa trị
| Tỷ lệ gặp mức độ 1 Và 2 (%) | Tỷ lệ gặp mức độ 3 Và 4 (%) | Loại ung thư | |
| Tác nhân | |||
| Cisplatin | Không nhận được báo cáo | 11 | Ung thư đầu, cổ |
| Docetaxel | 73-85 | 2-10 | Ung thư phổi không phải tế bào nhỏ |
| 58-60 | 27-42 | Ung thư buồng trứng | |
| 5-FU | Không báo cáo | 11 | Ung thư đầu, cổ |
| 50-54 | 5-8 | Ung thư đại trực tràng | |
| Paclitaxel | 93 | 7 | Ung thư vú |
| Topotecan | Không báo cáo | 32 | Ung thư phổi tế bào nhỏ |
| 67 | 32 | Ung thư buồng trứng | |
| Vinorelbin | 67-71 | 5-14 | Ung thư vú |
| Phác đồ | |||
| Cisplatin-
Cyclophosphamid |
43 | 9 | Ung thư buồng trứng |
| Cisplatin-etoposid | 59 | 16-55 | Ung thư phổi tế bào nhỏ |
| Etoposid-ifosfamid- cisplatin | Không báo cáo | 52 | Ung thư phổi tế bào nhỏ |
| 5-FU-carboplatin | 42 | 14 | Ung thư đầu, cổ |
| CHOP (Cyclophosphamid- doxorubicin-vincristin- prednison) | 49 | 17 | Ung thư lympho không Hogdkin |
| Paclitaxel- doxorubicin | 78-84 | 8-11 | Ung thư vú |
| Paclitaxel- carboplatin | 10-59 | 5-34 | Ung thư phổi không phải tế bào nhỏ |
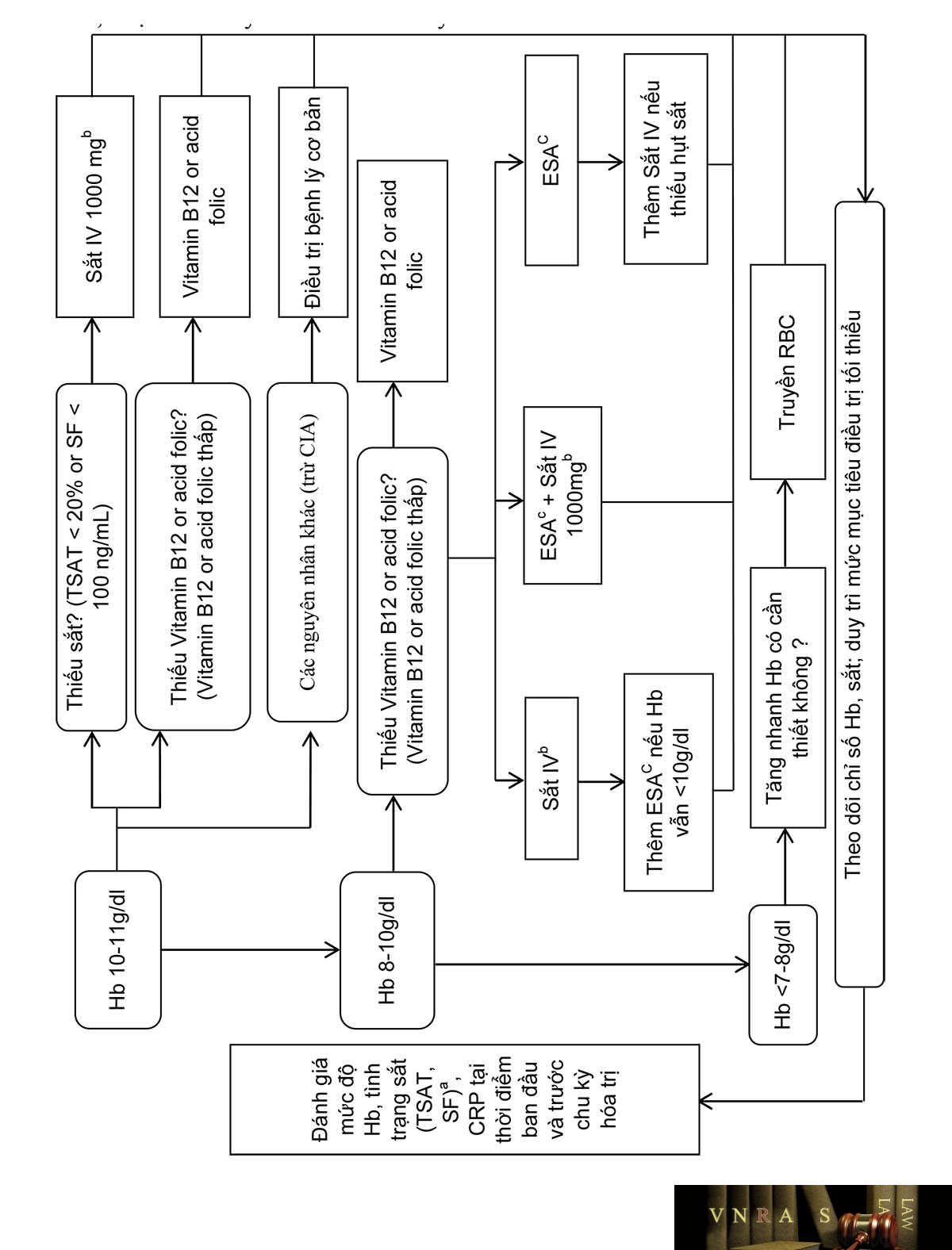
Chú thích:
a: Các thông số khác đánh giá tình trạng thiếu sắt: %HPYO > 5% và hàm lượng Hb của hồng cầu lưới < 28pg
b: Liều duy nhất 1.000 mg sắt hoặc tổng liều tương đương trong nhiều lần truyền. Sắt đường uống được xem xét khi ferritin < 30ng/mL và CRP < 5mg/l
c: Liều dùng ESA cần tuân thủ hướng dẫn sử dụng của thuốc (ví dụ như 450IU/tuần/kg cân nặng đối với epoetin alpha, beta, zeta hoặc 6,75mg/kg cân nặng mỗi 3 tuần hoặc 2,25mg/kg cân nặng hàng tuần đối với darbepoetin alpha; 20.000 IU mỗi lần một tuần đối với epoetin theta, có thể tăng gấp đôi sau 4 tuần khi không đáp ứng. Không được khuyến cáo tăng liều ESA hoặc đổi sang một ESA khác trong vòng 4-8 tuần ở bệnh nhân không đáp ứng.
Ký hiệu: CRP: protein C phản ứng; ESA: tác nhân kích thích hồng cầu, Hb: haemoglobin, ID: thiếu hụt sắt; IV: tĩnh mạch; RBC: hồng cầu; SF: ferritin huyết thanh; TSAT: độ bão hòa transferrin.
Tuy nhiên, khi dự phòng và điều trị thiếu máu, thiếu sắt do hóa trị sẽ có một số nguy cơ như sau:
Bảng 2.PL4.16. Nguy cơ và lợi ích của điều trị thiếu máu và thiếu sắt ở bệnh nhân ung thư
| Tác nhân | Lợi ích | Nguy cơ |
| ESA | Giảm nhu cầu truyền hồng cầu
Cải thiện triệu chứng liên quan đến thiếu máu |
Tăng nguy cơ huyết khối
Chứng bất sản nguyên hồng cầu (Pure Red Cell Aplasia PRCA) (hiếm gặp) Tăng tỷ lệ tử vong trên những bệnh nhân không điều trị ung thư hoặc chỉ điều trị bằng xạ trị Chỉ hiệu quả trên 60% bệnh nhân Giảm đáp ứng theo thời gian |
| Sắt tĩnh mạch | Phục hồi thiếu máu do thiếu sắt
Giảm nhu cầu truyền hồng cầu Tăng đáp ứng của ESA |
Tính an toàn lâu dài trên bệnh nhân ung thư chưa được thiết lập |
| Truyền RBC | Tăng nồng độ Hb và Hematocrit ngay lập tức trên 100% trường hợp
Cải thiện nhanh các triệu chứng liên quan đến thiếu máu |
Tăng nguy cơ huyết khối
Phản ứng truyền máu và quá tải tuần hoàn Truyền tác nhân gây bệnh đã biết chưa biết Có thể giảm sự sống còn trong một số loại ung thư được điều trị bằng phẫu thuật Tăng nguy cơ nhiễm trùng do ức chế miễn dịch. |
Liều thường dùng ESA và sắt trong điều trị thiếu máu và thiếu sắt do hoá trị như sau:
Bảng 3.PL4.16. Liều dùng và cách dùng một số tác nhân kích thích hồng cầu và sắt
| Tác nhân | Liều dùng, cách dùng |
| ESA | |
| Epoetin alpha | 450 lU/kg cân nặng, tiêm dưới da 1 lần/tuần hoặc 150 lU/kg cân nặng tiêm, dưới da 3 lần mỗi tuần. |
| Epoetin beta | 30.000 IU tiêm dưới da (tương đương 450IU/kg cân nặng trên bệnh nhân 70kg), sử dụng 1 lần/tuần hoặc chia 3-7 lần/tuần. |
| Epoetin theta | 20.000 IU tiêm dưới da, không phụ thuộc trọng lượng cơ thể, sử dụng 1 lần/tuần, liều có thể tăng gấp đôi sau 4 tuần nếu Hb không tăng ít nhất 1 g/dL. |
| Epoetin zeta | 450 lU/kg cân nặng, tiêm dưới da 1 lần/tuần hoặc 150 lU/kg cân nặng tiêm dưới da 3 lần mỗi tuần. |
| Darbepoetin alpha | 500mcg (6,75mcg/kg cân nặng), tiêm dưới da 3 tuần/lần hoặc 2,25mcg/kg cân nặng tiêm dưới da 1 lần/tuần. |
| Sắt tĩnh mạch | |
| Sắt gluconat | Liều truyền tối đa: 125 mg sắt
Thời gian truyền tối thiểu: 60 phút |
| Sắt sucrose | Liều truyền tối đa: 200-500 mg sắt
Thời gian truyền tối thiểu: 30-210 phút |
| Sắt dextran | Liều truyền tối đa: phụ thuộc loại sắt dextran, tham khảo tờ hướng dẫn sử dụng của thuốc
Thời gian truyền tối thiểu: 240-360 phút |
| Sắt isomaltoside | Liều truyền tối đa: 20 mg/kg cân nặng (có thể lên tới 1.000 mg)
Thời gian truyền tối thiểu: 15 phút (nếu liều vượt quá 1.000 mg, thời gian truyền tối thiểu lên tới 30 phút) |
| Sắt carboxymaltose | Liều truyền tối đa: 20 mg/kg cân nặng (có thể lên tới 1.000 mg) Thời gian truyền tối thiểu: 15 phút (nếu liều vượt quá 1.000 mg, thời gian truyền tối thiểu lên tới 30 phút) |
Phụ lục 4.17. Tiêu chuẩn thực hành trong giai đoạn chuẩn bị thuốc điều trị ung thư
Giai đoạn này nên được thực hiện trong buồng pha chế thuốc độc tế bào chuẩn có áp lực âm.
- Rửa tay với xà phòng và nước, đeo găng theo hướng dẫn.
- Lau bề mặt bên trong tủ pha chế.
- Lau lọ thuốc bằng cồn 70% để loại bỏ nhiễm bẩn với thuốc độc hại.
- Lau vật tư sử dụng cho chuẩn bị thuốc bằng cồn 70% trước khi đặt bên trong tủ pha chế.
- Sử dụng kim tiêm có thể tích phù hợp, tránh hút đầy hơn 75% chiều dài bơm tiêm.
+ Ống tiêm 3 mL hút dịch không vượt quá 2,3 mL.
+ Ống tiêm 5 mL hút dịch không vượt quá 3,8 mL.
+ Ống tiêm 10 mL hút dịch không vượt quá 7,5 mL.
+ Ống tiêm 20 mL hút dịch không vượt quá 15 mL.
+ Ống tiêm 30 mL hút dịch không vượt quá 22,5 mL.
+ Ống tiêm 60 mL hút dịch không vượt quá 50 mL.
- Mỗi kim tiêm không dùng để chọc quá 3 lần.
- Kiểm tra dung dịch sau khi hoàn nguyên để đảm bảo thuốc được hòa tan hoàn toàn trước khi rút dung dịch thuốc ra khỏi lọ/ống thuốc.
- Điều chỉnh thể tích dung dịch thuốc và/hoặc loại bọt khí trong kim tiêm trước khi rút kim tiêm ra khỏi lọ.
- Không dùng cả hai tay để đậy nắp bơm tiêm chứa thuốc, pít tông nên được kéo xuống để loại thuốc ở lõi kim tiêm và gắn một kim tiêm mới trước khi bơm thuốc vào túi truyền hoặc trước khi đưa sang khu vực sử dụng.
- Không cắm bộ dây truyền vào túi truyền chứa thuốc độc hại hoặc xả dây truyền bằng dung dịch thuốc độc hại vào môi trường mà không được kiểm soát. Nên cắm bộ dây truyền vào túi truyền ngay trước khi thêm thuốc vào dung dịch truyền.
- Chuẩn bị thuốc điều trị cho một bệnh nhân tại một thời điểm. Hạn chế chuẩn bị cùng lúc nhiều thuốc trong không gian làm việc của tủ pha chế tại một thời điểm.
- Hoàn nguyên thuốc trong lọ:
+ Sát khuẩn nắp cao su với gạc tẩm cồn tiệt trùng, để khô hoàn toàn ít nhất 10 giây để tiệt khuẩn. Bề mặt lọ phải khô để tránh đưa cồn vào lọ.
+ Sử dụng kỹ thuật rút thuốc áp lực âm để hạn chế việc thuốc phun ra khỏi lọ do áp lực trong lọ quá cao.
+ Nên sử dụng gạc tiệt trùng tẩm cồn bọc quanh kim tiêm và nắp lọ trong khi rút thuốc ra khỏi lọ.
- Sau khi rút dung dịch thuốc ra khỏi lọ, lau nắp lọ bằng gạc tẩm cồn để loại các giọt nhỏ thuốc phun ra khỏi lọ.
- Thao tác với ống thuốc:
+ Gõ vào ống để loại bỏ thuốc ở phần trên cổ ống thuốc.
+ Lau cổ ống thuốc bằng gạc tẩm cồn.
+ Sử dụng thiết bị bẻ ống hoặc bọc gạc xung quanh cổ ống để bẻ ống thuốc, không sử dụng kẹp Kocher để bẻ ống.
+ Loại bỏ đầu ống thuốc vào hộp chứa đồ sắc nhọn.
+ Để ống khô, thêm từ từ chất pha loãng theo thành ống, nghiêng và xoay ống để đảm bảo độ ẩm của bột và lắc chậm để hòa tan.
+ Rút dung dịch thuốc ra khỏi ống bằng kim lọc hoặc ống hút có bộ lọc hạt 5- micron. Điều chỉnh thể tích sau khi bỏ bộ lọc.
+ Loại bọt khí trong ống hoặc điều chỉnh thể tích bằng cách đóng nắp kim tiêm, đẩy pít tông tăng dần tới khi dung dịch xuất hiện ở trung tâm kim tiêm. Điều chỉnh thể tích bằng cách loại phần dư dung dịch trong ống thuốc.
+ Nếu thuốc độc hại ổn định trên 24 giờ và sẽ tiếp tục được sử dụng, chuyển thuốc vào lọ vô trùng có dán nhãn và ghi ngày rõ ràng.
- Kiểm tra và ghi nhãn cho sản phẩm đúng quy định.
- Rửa tay ngay sau khi tháo bỏ găng.
Phụ lục 4.18. Tiêu chuẩn thực hành trong giai đoạn thực hiện thuốc điều trị ung thư
❖ Thực hiện thuốc đường tiêm truyền tĩnh mạch:
- Chuẩn bị trang bị bảo hộ: găng tay, áo bảo hộ, khẩu trang và các thiết bị như bơm tiêm, kim tiêm, dây truyền, thiết bị tiêm truyền tự động.
- Chuẩn bị sẵn bộ kít dùng cho sự cố tràn và thùng đựng rác thải y tế.
- Mặc trang phục bảo hộ: rửa tay, đeo đôi găng thứ nhất, mặc áo choàng rồi đeo khẩu trang, sau đó đeo đôi găng thứ hai.
- Luôn thực hiện các động tác ở vị trí thấp hơn vị trí của mắt.
- Kiểm tra trực quan thuốc trước khi truyền.
- Đặt một miếng thấm hút có mặt sau làm bằng plastic dưới vị trí tiêm truyền để thấm thuốc rò rỉ ra và ngăn ngừa thuốc tiếp xúc với da bệnh nhân.
- Chỉ được xả các thuốc không độc hại hoặc tráng dây truyền bằng các dung dịch không chứa thuốc độc hại ở khu vực thực hiện thuốc.
- Khi loại bọt khí khỏi bơm tiêm hoặc dây truyền, nên chặn đầu kim tiêm, bơm tiêm hoặc dây truyền bằng bông vô trùng tẩm cồn để thu hồi bất kỳ lượng thuốc điều trị ung thư nào ngẫu nhiên thoát ra.
- Luôn tráng dây truyền trước và sau mỗi lần thực hiện thuốc, giữa hai thuốc, bằng dung môi tiêm truyền thích hợp như natri clorid 0,9% hoặc glucose 5%.
- Truyền thuốc theo y lệnh (kiểm soát tốc độ truyền,…)
- Làm sạch bề mặt tiếp xúc với thuốc độc hại bằng chất tẩy rửa thích hợp.
- Loại bỏ bơm tiêm, chai truyền (vẫn gắn với bộ dây truyền) đã sử dụng vào túi/hộp chứa rác thải độc hại theo quy định xử lý rác thải y tế.
- Tháo và loại bỏ găng cẩn thận, rửa tay ngay sau khi tháo găng.
❖ Thực hiện thuốc đường tiêm bắp hoặc tiêm dưới da:
- Chuẩn bị trang phục bảo hộ (2 lớp găng tay, áo bảo hộ, kính bảo hộ, khẩu trang) và thiết bị cần thiết (bơm tiêm, kim an toàn, kim rút thuốc ra).
- Chuẩn bị sẵn bộ kít dùng cho sự cố tràn và thùng đựng rác thải y tế.
- Mặc trang phục bảo hộ: rửa tay, đeo đôi găng thứ nhất, mặc áo bảo hộ rồi đeo khẩu trang, sau đó đeo đôi găng thứ hai.
- Luôn thực hiện các động tác ở vị trí thấp hơn vị trí của mắt.
- Kiểm tra trực quan thuốc trước khi tiêm.
- Tiêm thuốc theo y lệnh.
- Tháo nắp bơm tiêm và nối với hệ thống kim an toàn.
- Không loại bọt khí từ bơm tiêm hoặc tráng kim an toàn.
- Loại bỏ ống tiêm (vẫn gắn với hệ thống kim an toàn) đã sử dụng vào túi/hộp chứa rác thải độc hại theo quy định xử lý rác thải y tế.
- Tháo và loại bỏ găng cẩn thận, rửa tay ngay sau khi tháo găng.
Phụ lục 4.19. Một số nội dung tư vấn cho người bệnh mắc bệnh ung thư
1. Thông tin về hóa trị
Hóa trị là gì?
Hóa trị là thuốc được sử dụng để ngăn chặn các tế bào phát triển nhanh, trong đó có các tế bào ung thư và cả các tế bào khỏe mạnh phát triển. Vì vậy, có thể gây ra một số tác dụng phụ như rụng tóc, buồn nôn và giảm bạch cầu. Các tác dụng bất lợi thường đỡ hơn hoặc biến mất sau khi dừng điều trị.
Hóa trị được thực hiện như thế nào?
Hóa trị được đưa vào cơ thể theo nhiều đường khác nhau nhưng phổ biến nhất là đường tiêm truyền tĩnh mạch hoặc đường uống.
- Thuốc dùng đường tĩnh mạch được tiêm truyền trực tiếp vào máu thông qua một ống đặt vào cánh tay hoặc ngực. Những loại thuốc này cần được thực hiện tại chuyên khoa ung thư của bệnh viện.
- Thuốc hóa trị đường uống là viên nén hoặc viên nang.
- Hóa trị có thể được sử dụng theo chu kỳ. Một chu kỳ là thời gian giữa các lần điều trị và được tính bao gồm cả ngày hóa trị. Vì hóa trị tấn công các tế bào phát triển nhanh, cơ thể Ông/Bà sẽ cần thời gian để phục hồi lại các tế bào khỏe mạnh sau mỗi lần điều trị.
- Hóa trị có thể bao gồm một loại thuốc hoặc là phối hợp của hai hoặc nhiều loại thuốc.
- Các loại thuốc phối hợp trong hóa trị đều có tác dụng ngăn chặn các tế bào ung thư phát triển nhanh, nhưng mỗi loại tấn công tế bào ung thư theo các cách khác nhau.
Một số điều khác Ông/Bà nên biết về điều trị?
- Một số loại thuốc có thể ảnh hưởng đến tác dụng của thuốc hóa trị nếu dùng cùng nhau. Hãy thông tin bác sĩ những loại thuốc bản thân Ông/Bà đang dùng như:
+ Thuốc điều trị theo chuyên khoa khác
+ Các loại thảo mộc
+ Vitamin
+ Thuốc không kê đơn
- Trước khi hóa trị có thể cần lấy máu để xét nghiệm.
- Điều trị có thể làm cho cơ thể Ông/Bà dễ bị nhiễm trùng. Nên rửa tay thường xuyên và tránh tiếp xúc với những người bị bệnh trong thời gian điều trị.
- Nên uống đủ nước mỗi ngày trong thời gian hóa trị trừ khi Ông/Bà được yêu cầu hạn chế lượng nước sử dụng, nên hỏi kỹ bác sĩ về lượng nước được phép sử dụng.
- Thuốc hóa trị có thể gây buồn nôn. Ông/Bà có thể cần sử dụng một số thuốc trước khi hóa trị để giúp ngăn ngừa buồn nôn hoặc nôn. Ăn một số bữa nhỏ trong ngày có thể giúp giảm buồn nôn.
- Phụ nữ không nên mang thai và nên sử dụng biện pháp tránh thai trong khi hóa trị.
- Đàn ông được điều trị hóa trị nên sử dụng phương pháp tránh thai (bao cao su) khi quan hệ tình dục.
- Hóa trị có thể ảnh hưởng đến khả năng có con của Ông/Bà. Cần trao đổi với bác sĩ trước khi hóa trị nếu Ông/Bà dự định có con trong tương lai.
2. Tác dụng phụ giảm bạch cầu
Bạch cầu đóng vai trò quan trọng trong chống nhiễm trùng. Khi số lượng bạch cầu giảm xuống dưới mức bình thường, Ông/Bà có nhiều nguy cơ bị nhiễm trùng hơn. Một trong các nguyên nhân khiến bạch cầu xuống dưới mức bình thường là xạ trị hoặc hóa trị.
Các biện pháp phòng ngừa nhiễm trùng khi số lượng bạch cầu giảm
- Rửa tay thường xuyên, đặc biệt là trước và sau khi ăn và sau khi đi vệ sinh.
- Người khác nên rửa tay trước khi tiếp xúc với Ông/Bà.
- Không dùng chung khăn với người khác.
- Vệ sinh cá nhân sạch sẽ. Thoa kem dưỡng da cho da khô. Kiểm tra da xem có bị vết cắt, phát ban, đỏ, sưng, đau, ngứa, thoát nước hoặc mùi. Nếu bị vết cắt trên da và không lành trong ba ngày, xin ý kiến bác sĩ điều trị.
- Đánh răng sau khi ăn và trước khi đi ngủ bằng bàn chải đánh răng mềm. Súc miệng bằng dung dịch súc miệng không có cồn.
- Thông tin đến bác sĩ về bất kỳ vết đỏ, mảng trắng, vết cắt hoặc vết sưng ở bên trong miệng, nướu hoặc môi, đau họng, ho.
- Giữ móng tay và móng chân cắt ngắn và sạch sẽ.
- Khi đi tiểu hoặc đi tiêu, dùng khăn giấy mềm lau từ trước ra sau và rửa tay kỹ. Liên hệ nhân viên y tế nếu nước tiểu thay đổi về màu sắc, có mùi hoặc tiểu són.
- Trao đổi với nhân viên y tế nếu bị tiêu chảy.
- Tránh sử dụng lưỡi dao hoặc các vật sắc nhọn.
- Đeo găng tay khi làm vườn.
- Kiểm tra nhiệt độ cơ thể hai lần một ngày, vào buổi sáng và trước khi đi ngủ. Liên hệ nhân viên y tế nếu bị sốt 38OC, lạnh, đổ mồ hôi nhiều hoặc cảm thấy mệt mỏi hơn bình thường.
- Cố gắng nghỉ ngơi, giữ thái độ lạc quan vui vẻ.
- Tìm một việc thú vị để làm (một sở thích, một công việc).
- Nghỉ ngơi và tập thể dục. Cố gắng ngủ 6 đến 8 giờ mỗi đêm.
- Thực hiện ăn chín uống sôi.
Tránh những điều này khi số lượng bạch cầu thấp
Tránh tiếp xúc với các nguồn lây nhiễm có thể:
- Người mắc bệnh truyền nhiễm như: viêm họng, cảm lạnh, lở loét, tiêu chảy, cúm, đau mắt đỏ, bệnh thủy đậu, sởi hoặc quai bị.
- Nơi đông người.
- Nơi ao tù nước đọng như nước trong lọ hoa, cốc giả.
- Tránh tiếp xúc với vật nuôi hoặc chất thải của con người.
- Rất thận trọng khi sử dụng lưỡi dao cạo hoặc các vật sắc nhọn khác.
- Không vệ sinh móng tay bằng dụng cụ sắc nhọn.
- Tham khảo ý kiến bác sĩ trước khi tiêm chủng.
Bản thân Ông/Bà đóng vai trò quan trọng trong việc bảo vệ chính bản thân mình tránh bị nhiễm trùng khi bị giảm bạch cầu.
3. Tác dụng phụ mệt mỏi liên quan đến ung thư
Mệt mỏi liên quan đến ung thư là một trong những tác dụng phụ phổ biến nhất của ung thư và phương pháp điều trị ung thư. Loại mệt mỏi này rất khác so với cảm giác mệt mỏi trong cuộc sống hàng ngày. Mệt mỏi có thể bao gồm thể chất, tinh thần và cảm xúc.
Điều gì gây ra mệt mỏi liên quan đến ung thư?
Mệt mỏi liên quan đến ung thư có thể được gây ra bởi bất kỳ nguyên nhân sau đây:
- Điều trị ung thư
- Một số loại thuốc khác
- Thiếu máu (số lượng hồng cầu thấp)
- Thay đổi giấc ngủ
- Căng thẳng
- Ăn không ngon
- Đau
- Các vấn đề khác về sức khỏe
Một số cách giúp Ông/Bà giảm mệt mỏi
- Luôn hoạt động mỗi ngày. Biến các hoạt động nhỏ như tập thể dục thành thói quen hàng ngày: đi bộ ngắn, thực hiện các bài tập nhẹ nhàng hoặc công việc nhẹ trong hoặc xung quanh nhà.
- Lập kế hoạch hoạt động trong một ngày.
- Uống nhiều nước. Uống tám cốc (mỗi cốc 250 mL) nước/ngày, trừ khi bác sĩ có hướng dẫn khác với Ông/Bà.
- Cố gắng ăn nhiều bữa nhỏ hoặc đồ ăn nhẹ. Ăn thực phẩm giàu protein như thịt, cá, phô mai, sữa chua và sữa lắc để cung cấp thêm vitamin, khoáng chất, calo và protein cho Ông/Bà giúp chống mệt mỏi.
- Dùng các sản phẩm bổ sung dinh dưỡng như các loại sữa bổ sung dinh dưỡng.
- Tinh thần ổn định đóng vai trò rất quan trọng trong quá trình điều trị và hồi phục.
4. Thông tin tác dụng phụ – Buồn nôn và ói mửa
Tại sao người bệnh ung thư bị buồn nôn và nôn?
Nôn hoặc buồn nôn có thể do bất kỳ nguyên nhân nào sau đây:
- Một số loại thuốc hóa trị
- Một số loại thuốc điều trị sinh học
- Xạ trị vào ngực, dạ dày hoặc lưng
- Đau
- Lo lắng
- Táo bón
- Vị trí ung thư
- Một số loại thuốc (như thuốc giảm đau opioid)
- Gây mê trong phẫu thuật hoặc thủ thuật
- Mức độ bất thường của chất điện giải (khoáng chất) trong máu
- Lượng đường trong máu cao
- Nhiễm trùng hoặc các bệnh khác
Tại sao buồn nôn và nôn xảy ra?
- Hóa trị hoặc liệu pháp sinh học có thể gây kích ứng dạ dày hoặc kích hoạt trung tâm nôn trong não. Buồn nôn và nôn có thể xảy ra một vài giờ ngay sau khi điều trị hoặc muộn hơn một vài ngày sau khi điều trị.
- Không phải tất cả các loại thuốc hóa trị và sinh học đều gây buồn nôn và nôn.
- Tần suất và thời gian nôn hoặc buồn nôn xảy ra phụ thuộc vào loại thuốc, liều dùng và cách dùng thuốc.
Các biện pháp để giúp giảm buồn nôn và nôn?
Thuốc chống nôn
- Thuốc chống nôn được sử dụng để giúp ngăn ngừa và kiểm soát buồn nôn và nôn.
- Ông/Bà có thể cần phải uống thuốc chống nôn thường xuyên trước và sau điều trị.
- Nếu thuốc chống nôn đang sử dụng không hiệu quả, hãy báo bác sĩ để kê thuốc chống nôn khác có hiệu quả.
- Một số loại thuốc làm hạ axit dạ dày có thể giúp giảm buồn nôn. Hãy cho bác sĩ biết nếu Ông/Bà đang có ợ nóng hoặc trào ngược axit gây buồn nôn.
Điều chỉnh trong chế độ ăn uống
- Có thể cần hạn chế ăn một số thức ăn trong ngày điều trị. Hãy hỏi nhân viên y tế nếu có thắc mắc về việc ăn uống ngay trước hoặc sau khi điều trị.
- Ăn mỗi lần một lượng nhỏ thức ăn trong suốt cả ngày. Ăn chậm và giành nhiều thời gian để ăn.
- Giữ một lượng nhỏ thức ăn trong dạ dày sẽ giúp kiểm soát cảm giác buồn nôn.
- Hạn chế uống nước trong bữa ăn nhưng uống nhiều nước giữa các bữa ăn.
- Ngay cả khi không thể ăn được, hãy cố gắng uống ít nhất 8 đến 10 ly nước không chứa cafein mỗi ngày để tránh mất nước.
- Ăn thức ăn nhạt như bánh mì nướng khô, bánh quy mặn, bỏng ngô khô, khoai tây luộc hoặc nướng, gạo trắng hoặc chuối. Ăn những thực phẩm dễ tiêu hóa như ngũ cốc, bánh mì trắng, bánh quy giòn, trái cây hoặc rau củ.
- Tránh các món ăn cay nóng như ớt cay hay thịt nướng nước sốt.
- Không ăn thức ăn béo, chiên hoặc dầu mỡ như: khoai tây chiên, pho mát, bơ, dầu, kem, bơ thực vật hoặc thịt đỏ.
- Nếu có vị khó chịu trong miệng, có thể súc miệng, làm sạch răng giả, đánh răng, hoặc mút kẹo cứng như bạc hà.
- Thở chậm, thở sâu bằng miệng hoặc nuốt đôi khi giúp cảm giác buồn nôn qua đi.
- Nghỉ ngơi trước và sau bữa ăn. Không nên nằm xuống ngay sau khi ăn mà ngồi hoặc dựa đầu lên cao.
- Tránh những nơi có đồ ăn có mùi mạnh gây khó chịu.
- Tránh những cảnh tượng, âm thanh và mùi khó chịu có thể kích hoạt buồn nôn.
- Mở cửa sổ hoặc đi ra ngoài để hưởng không khí trong lành.
- Đánh lạc hướng bản thân bằng cách thực hiện một số hoạt động như: đọc, nghe nhạc, chơi game, xem ti vi hoặc làm việc theo sở thích.
- Tìm cách để bản thân được thư giãn.
- Cố gắng nghỉ ngơi hoặc ngủ trưa khi bị buồn nôn.
- Trao đổi với bác sĩ về việc uống vitamin và dinh dưỡng bổ sung.
- Táo bón có thể gây ra hoặc tăng thêm cảm giác buồn nôn. Trao đổi với bác sĩ về những gì có thể làm hoặc làm để giúp đỡ táo bón.
- Uống thuốc để kiểm soát cơn đau.
- Ngồi dậy khi nôn để tránh chất nôn xuống phổi.
Khi nào nên gọi bác sĩ?
Gọi cho bác sĩ nếu có bất kỳ triệu chứng sau đây:
- Đau bụng
- Có máu trong chất nôn
- Chất nôn giống như bã cà phê
- Chóng mặt, đặc biệt khi đứng lên
- Ít đi tiểu
- Nước tiểu sẫm màu
- Giảm > 2 kg trong một tuần hoặc 4,5 kg trong một tháng.
- Nếu không thể uống hoặc giữ đủ nước hoặc nôn hơn 1-2 lần/ngày
5. Tác dụng phụ do số lượng tiểu cầu thấp
Khi có số lượng tiểu cầu thấp, Ông/Bà có nhiều nguy cơ bị chảy máu.
Dưới đây là một số cách giúp bảo vệ bản thân khi có số lượng tiểu cầu thấp:
- Cần thông tin cho bác sĩ nếu đang sử dụng các thuốc điều trị liên quan đến đông máu như: coumarin, lovenox, xarelto hoặc pradaxa.
- Cần thông tin cho bác sĩ nếu có đặt stent và dùng aspirin, các sản phẩm có aspirin hoặc thuốc làm loãng máu khác. Bác sĩ có thể yêu cầu ngừng dùng các loại thuốc này.
- Hỏi dược sĩ nếu không chắc chắn một loại thuốc hoặc sản phẩm có aspirin trong đó.
- Không dùng bất kỳ loại thuốc hoặc thảo dược bổ sung chế độ ăn uống nào mà không hỏi ý kiến bác sĩ hoặc dược sĩ. Một số thuốc và thảo dược có thể thay đổi cách thức hoạt động của tiểu cầu.
- Yêu cầu hỗ trợ khi đi bộ nếu không đi vững.
Bảo vệ da
- Bảo vệ làn da tránh tổn thương.
- Sử dụng dao cạo điện để cạo râu.
- Kiểm tra làn da mỗi ngày để xem có bị vết cắt, vết bầm tím hoặc các vết thương khác hay không.
- Theo dõi đám xuất huyết trên da.
- Không sử dụng các dụng cụ sắc nhọn như kéo, dao hoặc kim.
- Không mặc quần áo bó sát hoặc vải thô.
- Không đi chân trần.
- Không tham gia hoạt động mà có thể ngã hoặc bị va đập.
- Tạo áp lực vững chắc cho bất kỳ vết cắt trong ít nhất 5 phút. Gọi cho bác sĩ nếu vết bầm tím lớn hơn hoặc chảy máu không ngừng.
Bảo vệ niêm mạc trong miệng
- Ăn thức ăn mềm.
- Không ăn thức ăn thô như: các loại hạt, bánh quy giòn, khoai tây chiên hoặc bánh quy có thể gây tổn thương bên trong miệng.
- Giữ môi ẩm. Sử dụng kem dưỡng ẩm môi để tránh khô hoặc nứt.
- Đánh răng nhẹ nhàng bằng bàn chải đánh răng mềm. Nếu không thể sử dụng bàn chải đánh răng, có thể sử dụng tăm bông (tăm) để làm sạch răng và nướu. Không sử dụng chỉ nha khoa, bàn chải đánh răng điện hoặc tăm xỉa răng.
- Kiểm tra miệng mỗi ngày xem có bị chảy máu nướu răng.
- Cần thông tin đến bác sĩ và nha sĩ nếu có can thiệp nha khoa.
Gọi bác sĩ ngay nếu có các dấu hiệu sau đây:
- Nếu chảy máu không dừng sau khi tạo áp lực lên vết thương 5 phút
- Nốt xuất huyết
- Chảy máu, sưng, hoặc vết bầm bất thường
- Máu trong dịch nôn, dịch nôn trông như bã cà phê
- Ho ra máu
- Chảy máu bất thường hoặc chảy máu nướu nặng
- Phân đỏ hoặc đen như hắc ín
- Máu trong nước tiểu (nước tiểu đỏ hoặc hồng)
- Chảy máu kinh nặng hoặc kéo dài hơn bình thường
- Chảy máu âm đạo
- Đau dạ dày nặng
- Mờ mắt
- Đau đầu nặng, lú lẫn, yếu người hoặc tê liệt
TÀI LIỆU THAM KHẢO
Tiếng Việt
- Bộ Y tế (2013), Danh mục hướng dẫn quy trình kỹ thuật khám bệnh, chữa bệnh chuyên ngành ung bướu, Ban hành kèm theo Quyết định số: 3338/QĐ- BYT ngày 09 tháng 9 năm 2013 của Bộ trưởng BYT. 2013, Hà Nội.
- Bộ Y tế (2015), “Chương 11: Sử dụng kháng sinh cho người bệnh suy giảm miễn dịch”, Hướng dẫn sử dụng kháng sinh, Nhà xuất bản Y học, Hà Nội.
- Bộ Y tế (2017), Dược thư quốc gia Việt Nam, Nhà Xuất Bản Y Học, Hà Nội.
- Bộ Y tế (2006), Hướng dẫn chăm sóc giảm nhẹ đối với bệnh ung thư và bệnh AIDS, Nhà xuất bản Y Học.
- Bộ Y tế (2018), Hướng dẫn quản lý thuốc gây độc tế bào dùng trong điều trị ung thư và kiểm soát chất thải liên quan.
- Bộ Y tế (2018), Quyết định 4825/QĐ-BYT 2018 “Hướng dẫn chẩn đoán và điều trị ung thư phổi không tế bào nhỏ”.
- Bộ Y tế (2006), Tương tác thuốc và chú ý khi chỉ định, NXB Y học, Hà Nội
- Bộ Y tế, Bệnh viện Bạch Mai (2014), Hoá chất trong điều trị một số bệnh ung thư.
- Hoàng Kim Huyền, Brouwers J.R.B.J (2014), Những nguyên lý cơ bản và sử dụng thuốc trong điều trị, Tập 2, Nhà Xuất bản Y học, Hà Nội.
- Nguyễn Bá Đức, Trần Văn Thuấn, Nguyễn Tuyết Mai (2010), Điều trị nội khoa ung thư, Nhà xuất bản Y học, Hà Nội.
- Cục Quản lý Dược (2019), Tờ Hướng dẫn sử dụng của các biệt dược gốc.
- Nguyễn Bá Đức, Trần Văn Thuấn, Nguyễn Tuyết Mai (2010), Điều trị nội khoa bệnh ung thư, Nhà xuất bản Y học, 202-212.
- Nguyễn Chấn Hùng (2004), Ung bướu học nội khoa, Nhà xuất bản Y học, 301-302.
- Mai Trọng Khoa (2013), Điều trị u não và một số bệnh lý sọ não bằng dao gamma quay. Nhà xuất bản Y học.
- Mai Trọng Khoa, Nguyễn Xuân Kử (2012), Một số tiến bộ về kỹ thuật xạ trị ung thư và ứng dụng trong lâm sàng. Nhà xuất bản Y học.
- Mai Trọng Khoa và cộng sự (2012), Y học hạt nhân (Sách dùng cho sau đại học). Nhà xuất bản Y học.
- Mai Trọng Khoa (2016), Kháng thể đơn dòng và phân tử nhỏ trong điều trị bệnh ung thư. Nhà xuất bản Y học.
- Mai Hồng Bàng (2016), Ung thư biểu mô tế bào gan, các phương pháp điều trị can thiệp nội mạch. Nhà xuất bản Y học.
- Mai Hồng Bàng (2016), Ung thư biểu mô tế bào gan, các phương pháp điều trị can thiệp qua da. Nhà xuất bản Y học.
Tiếng Anh
- Devita, Hellman et al. (2015), Cancer principle and practice of oncology (10th edition)
- Rudek, M.A., Chau et al (2014), Handbook of Anticancer Pharmacokinetics and Pharmacodynamics, second edition, Humana Press
- Fallon M., GiustiF R., et al. (2018), “Management of cancer pain in adult patients: ESMO ClinicalPractice Guidelines”, 29 (4)pp. iv166-iv191.
- National Comprehensive Cancer Network (2016), Adult cancer pain.
- Twycross et al (2007), Palliative Care Formulary (PCF3)
- CMO document on Opioid Potency Ratios (2005).
- The Palliative Care Handbook (2007), 6th Edition, Wessex SPCT
- Ardalan B, Luis R, Jaime M, Franceschi D (1998). Biomodulation of fluorouracil in colorectal cancer. Cancer Invest. 1998; 16:237-251.
- Balis F (1986), Pharmacokinetic drug interactions of commonly used anticancer drugs. Clin Pharmacokinet 1986; 11: 223-35.
- Beijnen J.H, Lingeman H, Van Munster H.A, Underberg W.J.M (1986), Mitomycin antitumour agents: a review of their physico-chemical and analytical properties and stability. J Pharm Biomed Anal 1986; 4: 275-95.
- Beijnen J.H and Schellens J.H (2004), Drug interactions in oncology. Lancet Oncol. 2004; 5:489-496.
- Gelderblom H, Loos WJ, Verweij J, et al (2002), Modulation of cisplatin pharmacodynamics by Cremophor EL: experimental and clinical studies. Eur J Cancer. 2002; 38:205-213.
- Bergstrom et al (1997), Effects of cisplatin and amphotericin B on DNA adduct formation and toxicity in malignant glioma and normal tisues in rat. Eur.J. Cancer 1997; 33: 153-159.
- Charity D. Scripture and William D. Figg (2006), Drug interations in cancer therapy, Reviews, 2006 July, vol 6, 546- 559, www.nature/reviews/cancer truy cập ngày 25/11/2018.
- Coezy E et al (1992), Tamoxifen and metabolites in MCF7 cells: correlation between binding to estrogen receptor and inhibition of cell growth. Cancer res 1982. 42, 317- 323.
- Frenia M.L and Long K.S. (1992), Methotrexat and nonsteroidal anti-inflammatory drug interactions, Ann. Pharmacother 1992; 26, 234- 247.
- Genentech, Inc. Rituxan product information. Genentech (online), http://www.gene.com/gene/products/information/pdf/rituxan-prescribing.pdf truy cập ngày 07/12/2018.
- Haidar C, Jeha S (2011), Drugs in childhood cancer. Lancet Oncol 2011 Jan;12: 92-9.
- Allen J (2015), Systemic Anticancer Therapy Drug Interactions Table, Version 1 June 2015 (Copyright Northumbria Healthcare NHS Trust & North of England Cancer Network)
- Jonsson E, Fridborg H, Nygren P, Larsson R (1998), Synergistic interactions of combinations of topotecan with standard drugs in primary cultures of human tumor cells from patients. Eur J Clin Pharmacol. 1998;54:509-514.
- Romanelli S, Perego P, Pratesi G, et al (1998), In vitro and in vivo interaction between cisplatin and topotecan in ovarian carcinoma systems. Cancer Chemother Pharmacol. 1998;41:385-390.
- Jos H.B and Jan H.M.S (2004), Drug interations in oncology, The Lancet oncology, 2004, vol 5: 489- 496.
- Kanzawa F, Saijo N (1997), In vitro interaction between gemcitabin and other anticancer drugs using a novel three-dimensional model. Semin Oncol. 1997; 24(2 suppl 7):S7-8-S7-16.
- Kiran Panesar (2011), Typical Drug Interactions in Oncology. 2011; 36, https://www.uspharmacist.com/article/typical-drug-interactions-in-oncology truy cập ngày 25/11/2018.
- Loadman PM, Bibby MC (2004), Pharmacokinetic drug interactions with anticancer drugs. Clin Pharmacokinet 1994; 26: 486-500.
- T et al (2004), The organic anion transporter (OATP) family. Drug metab. Phamacokinet 2004; 19, 171-179.
- Roelof van Leeuwen (2015), Drug-drug interactions in patients treated for cancer: a prospective study on clinical interventions, Ann Oncol. 2015 May;26(5):992-7.
- Roelof van Leeuwen (2014), Drug-drug interactions with tyrosine kinase inhibitors: a clinical perspective. Lancet Oncol. 2014 Jul;15(8):e315-26 Drug- drug interactions in patients treated with anti-cancer agents,
- Roelof van Leeuwen (2011), Potential drug interactions in cancer therapy: a prevalence study using an advanced screening method, Ann Oncol. 2011 Oct;22(10):2334-41
- Roelof van Leeuwen (2013), Potential drug-drug interactions in cancer patients treated with oral anti-cancer drugs, Br J Cancer. 2013 Mar 19;108(5):1071-8.
- A, et al (2002), Cardiac dysfuntion in the trastuzumab clinical trials experience. J. Clin. Oncol 2002; 20: 1215-1221.
- Smith, N.F et al (2005), Identification of OATP1B3 as high-affinity hepatocellular transporter of paclitaxel. Cancer.Biol.Ther 2005; 4, e5-e8.
- Van Meerten E, Verweij J, Schellens JHM (1995), Antineoplastic agents: drug interactions of clinical significance. Drug Safety 1995; 12: 168-82.
- Venonese M.L, et. al (2005), A phase II trial of gerfitinib with 5- fourouracil, leucovorin and irinotecan in patients with colorectal cancer. Br.J.Cancer 2005; 92, 1846-1849.
- Aapro MS, et al (2011), “2010 update of EORTC guidelines for the use of granulocyte-colony stimulating factor to reduce the incidence of chemotherapy- induced febrile neutropenia in adult patients with lympho proliferative disorders and solid tumours”, 47 (1), pp. 8-32.
- American Society of Health-System Pharmacists (2011), AHFS drugs information
- Bossi P., Antonuzzo., et al (2018), “Diarrhoea in adult cancer patients: ESMO Clinical Practice Guidelines”, 29 (4) pp. iv126-iv142.
- Botrel TE., Clark OA., et al (2011), Efficacy of palonosetron (PAL) compared to other serotonin inhibitors (5-HT3R) in preventing chemotherapy-induced nausea and vomiting (CINV) in patients receiving moderately or highly emetogenic (MoHE) treatment: systematic review and meta-analysis, 19 (6), pp.823-32.
- David R., Gandara Fausto Roila., et al (1998), Consensus proposal for 5HT3 antagonists in the prevention of acute emesis related to highly emetogenic chemotherapy dose, schedule, and route of administration, 6(3), pp 237-243.
- European Oncology Nursing Society (2007), Extravasation guidelines.
- European Journal of Oncology Nursing (2008), European Oncology Nursing Society extravasation guidelines, 12, pp. 357-361.
- Freifeld, A.G., J. Bow. E., et al (2011), “Clinical Practice Guideline for the Use of Antimicrobial Agents in Neutropenic Patients with Cancer: 2010 Update by the Infectious Diseases Society of America”, Clinical Infectious Diseases 2011;52(4):e56-e93.
- Golightly L. K, Teitelbaum I, et al (2013), Renal Pharmacotherapy_ Dosage Adjustment of Medications Eliminated by the Kidneys.
- Hesketh Paul J., Kris Mark G., et al (2017), “Antiemetics: American Society of Clinical Oncology Clinical Practice Guideline Update”, 35 (28), pp. 3240-3261.
- Huang J.Q., Zheng G.F., (2010), Do 5-hydroxytryptamine 3 receptor antagonists (5-HT3) improve the antiemetic effect of dexamethasone for preventing delayed chemotherapy-induced nausea and vomiting (CINV)? A meta-analysis of randomized controlled trials.
- A. Pérez Fidalgo, et al (2012), Management of chemotherapy extravasation: ESMOEONS Clinical Practice Guidelines. Annals of Oncology, 23 (7), pp. vii 167- 173.
- Klastersky J, de Naurois J, et al (2016), “Management of febrile neutropaenia: ESMO ClinicalPractice Guidelines”, 27(5), pp. v111-v118.
- MASCC/ESMO (2016), Antiemetic guideline.
- Twycross R, Wilcock A (2007), Palliative Care Formulary, Third Edition
- Jordan K ., Hink A ., et al (2007), A meta-analysis comparing the efficacy of four 5- HT3-receptor antagonists for acute chemotherapy-induced emesis, 15(9), pp. 1023- 33.
- Joseph T.D, Joseph D., et al. (2008), Pharmacotherapy-A Pathophysiologic Approach, 10th
- National Comprehensive Cancer Network (2018), Antiemesis.
- National Comprehensive Cancer Network (2018), Prevention and treatmen of cancer-related infections.
- National Comprehensive Cancer Network (2017), Myeloid growth factors.
- National Cancer Institute, National Institutes of Health (2010), Common Terminology Criteria for Adverse Events (CTCAE), Version 4.0.
- Saito M., Aogi K., et al (2009), Palonosetron plus dexamethasone versus granisetron plus dexamethasone for prevention of nausea and vomiting during chemotherapy:a double-blind, double-dummy, randomised, comparative phase III trial, 10(2), pp. 115-24.
- Sarah Rowland (2016), Extravasation Procedure, NHS Wales.
- Sean c. Sweetman (2009), Martindale – The Complete Drug Reference, 36th Edition.
- The Sydney children’s Hospital Network (2018), IV extravasation management practice guideline.
- Canadian Association of Pharmacy in Oncology (2009), Standards of Practice for Oncology Pharmacy in Canada (version 2).
- American Society of Health-System Pharmacists (2006), ASHP Guidelines on Handling Hazardous Drugs, Am J Health-Syst Pharm. 63, tr. 1172-93.
- Thông tin sản phẩm trên cơ sở dữ liệu tờ hướng dẫn sử dụng của Anh https://www.medicines.org.uk/emc/
- NCCN Clinical Practice Guidelines in Oncology, Small Cell Lung Cancer, Version 1.2019.
- NCCN Clinical Practice Guidelines in Oncology, Non Small Cell Lung Cancer, Version 1.2019.
- NCCN Clinical Practice Guidelines in Oncology, Gastric Cancer, Version 1.2019.
- NCCN Clinical Practice Guidelines in Oncology, Breast Cancer, Version 1.2019.
- NCCN Clinical Practice Guidelines in Oncology, Colon Cancer, Version 1.2019.
- NCCN Clinical Practice Guidelines in Oncology, Rectal Cancer, Version 1.2019.
- NCCN Clinical Practice Guidelines in Oncology, Hepatobiliary Cancers, Version 1.2019.
- Pharmaceutical Press, Stockley’s interaction alert [online], http://www.medicinescomplete.com.
- Truven Health Analytics, Micromedex 2.0, http://micromedex.com.
- Horn J.R, Hansten P.D (2013), Drug Interactions Analysis and Management, Wolters Kluwer Health.
- Vincent de vita et al. (2014), Principle and practice of oncology. Lippincott Ravell publishers. Philadelphia.
- Benjamin Movsas (2014), Cancer Management: A Multidisciplinary Approach, Medical, Surgical, and Radiation Oncology 13th Edition, UBM Medica.
- Nils H. Nicolay, Johanna Rademacher, Jan Oelmann-Avendano (2016), High dose- rate endoluminal brachytherapy for primary and recurrent esophageal cancer., Strahlentherapie und Onkologie.
- National Cancer Institute (2018), CAR T-cell therapy, National Institutes of Health.
- Roxanne Nelson (2018), T-Cell Biomarker Predicts Response to CAR T-Cell Therapy in Patients With CLL. Medscape Medical News, Oncology News.
- UF Health proton therapy institute (2018), What is Proton Therapy.
- The International Agency for Research on Cancer (2018), Viet Nam Source Globocan 2018, World Health Organization.
- British Oncology Pharmacy Association (2018), Standards for Pharmacy Verification of Prescriptions for Cancer Medicines, Third edition, October 2018.
- Clinical Oncological Soieity of Australia (2008), Guidelines for the Safe Prescribing, Supply and Administration of Cancer Chemotherapy.