Báo cáo việc sử dụng nguyên liệu Valsartan do Công ty Zhejiang Huahai Pharmaceutical – Trung Quốc sản xuất
| BỘ Y TẾ
CỤC QUẢN LÝ DƯỢC |
CỘNG HÒA XÃ HỘI CHỦ NGHĨA VIỆT NAM
Độc lập – Tự do – Hạnh phúc |
| Số: 13124/QLD-CL
V/v báo cáo sử dụng nguyên liệu Valsartan do Công ty Zhejiang Huahai Pharmaceutical – Trung Quốc sản xuất |
Hà Nội, ngày 10 tháng 7 năm 2018 |
Kính gửi:
– Cơ sở đăng ký thuốc;
– Cơ sở sản xuất thuốc;
– Cơ sở nhập khẩu thuốc, nguyên liệu làm thuốc.
Cơ quan quản lý dược phẩm Châu Âu (EMA), Cơ quan quản lý dược Canada và một số cơ quan quản lý dược khác đã có thông báo thu hồi các thuốc chứa Valsartan được sản xuất từ nguyên liệu Valsartan do Công ty Zhejiang Huahai Pharmaceutical – Trung Quốc sản xuất. Nguyên liệu này được phát hiện chứa tạp chất N-nitrosodimethylamine (NDMA) có nguy cơ gây ung thư.
Căn cứ vào các quy chế dược hiện hành hiện của Việt Nam, để đảm bảo an toàn cho người sử dụng, Cục Quản lý Dược yêu cầu:
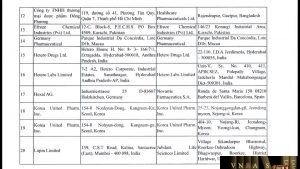
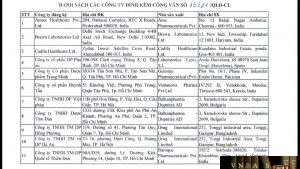
1. Các cơ sở đăng ký thuốc phối hợp với cơ sở sản xuất (có tên trong danh mục kèm theo Công văn này) báo cáo khẩn về nguồn gốc của nguyên liệu Valsartan sử dụng trong sản xuất các thuốc có chứa Valsartan lưu hành tại Việt Nam, cụ thể: tên nhà sản xuất nguyên liệu, địa chỉ, tiêu chuẩn chất lượng.
2. Cơ sở nhập khẩu thuốc, nguyên liệu làm thuốc:
a) Báo cáo tình hình nhập khẩu, phân phối nguyên liệu Valsartan do công ty Zhejiang Huahai Pharmaceutical – Trung Quốc sản xuất (danh sách các cơ sở sản xuất đã mua, số lượng, thời gian)
b) Dừng việc nhập khẩu, cung cấp thuốc đã được sản xuất từ nguyên liệu Valsartan của công ty Zhejiang Huahai Pharmaceutical lưu hành trên thị trường.
3. Bản scan báo cáo gửi về Cục Quản lý Dược theo hòm thư điện tử quanlychatluongthuoc.qld@moh.gov.vn, hoặc bằng văn bản theo địa chỉ 138A Giảng Võ, Ba Đình, Hà Nội trước 16h ngày 11/7/2018 để làm căn cứ xem xét, xử lý tiếp theo.
Sau thời hạn nêu trên, nếu cơ sở không có báo cáo xác định rõ nguồn gốc nguyên liệu valsartan sử dụng, Cục Quản lý Dược sẽ xem xét, xử lý các thuốc chứa Valsartan của cơ sở như thuốc có chứa nguyên liệu Valsartan do công ty Zhejiang Huahai Pharmaceutical – Trung Quốc sản xuất.
4. Cơ sở sản xuất ngừng ngay việc sử dụng nguyên liệu Valsartan của Công ty Zhejiang Huahai Pharmaceutical – Trung Quốc sản xuất để sản xuất thuốc thành phẩm và ngừng cung cấp thuốc đã được sản xuất từ nguyên liệu Valsartan của Công ty Zhejiang Huahai Pharmaceutical lưu hành trên thị trường.
Cục Quản lý Dược thông báo để các đơn vị biết và thực hiện.
| Nơi nhận:
– Như trên; – Cục trưởng Vũ Tuấn Cường (để b/c); – Các phòng ĐKT, website Cục QLD; – Lưu: VT, CL (XH). |
KT. CỤC TRƯỞNG
PHÓ CỤC TRƯỞNG Nguyễn Tất Đạt |
| STT | Công ty đăng ký | Địa chỉ ĐK | Nhà sản xuất | Địa chỉ SX |
| 1 | Amtec Healthcare Pvt., Ltd. | 204, Dattasai Complex, RTC X Roads, Hyderabad 500020, India | Atoz Pharmaceuticals Pvt. | No.12 Balaji Nagar Ambattur, Chennai – 600 053, India |
| 2 | Brawn Laboratories Ltd | Delhi Stock Exchange Building 4/4B Asaf Ali Road, New Delhi 110002, India | Brawn Laboratoties Ltd | 13, New Indi, Township, Farridabad 12 1001, Haryana, India |
| 3 | Cadila Healthcare Ltd. | Zydus Tower, Satellite Cross Road, Ahmedabad 380 015, India | Cadila Healthcare Ltd. | Kundaim Industrial Estate, ponda, Goa-403 401, India |
| 4 | Công ty cổ phần DP Phano | 396-398 Cách mạng tháng 8, Q. Tân Bình, TP. Hồ Chí Minh | Laboratories Lesvi, S.L. | Avda, Barcelona, 69 08970 Sant Joan Despi (Barcelona), Spain |
| 5 | Công ty cổ phần Dược phẩm Trang Minh | 303/16 Tân Sơn Nhi, P. Tân Sơn Nhi, Q. Tân Phú, TP. Hồ Chí Minh | Genome Pharmaceutical (Pvt) | Plot No. 16/1, Phase IV, Industrial Estate Hatta, Pakistan |
| 6 | Công ty cổ phần Huỳnh Tấn | 51 Khuông Việt, Phường Phú Trung, Quận Tân Phú, Tp. Hồ Chí Minh | Vintanova Pharma Pvt Ltd | IV/292 B, Velakkode, Mundur, Thrissur-680 541, Kerala, India |
| 7 | Công ty TNHH DP Việt Pháp | 11B, Phố Hoa Bằng, P. Yên Hòa, Q. Cầu Giấy, TP. Hà Nội | Balkanpharma Dupnitsa AD | 3, Samokovsko shosse Str., Dupnitsa 2600, Bulgaria |
| 8 | Công ty TNHH Dươc Tâm Đan | 1333 đường 31B, Khu phố An Phú An Khánh, Phường An Phú, Quận 2, TP. Hồ Chí Minh | Balkanpharma Dupnitsa AD | 3, Samokovsko shosse Str., Dupnitsa 2600, Bulgaria |
| 9 | Công ty TNHH TM DP Đông Phương | 119, Đường số 41, Phường Tân Quy, Quận 7, TP. Hồ Chí Minh | Drug International Limited | 252, Tonggi industrial area, Tonggi, Gazipur, Bangladesh |
| 10 | Công ty TNHH TM và DP Hà An | Tổ 16, Phường Định Công, Q. Hoàng Mai, TP. Hà Nội | Drug International Limited | 252, Tonggi industrial area, Tonggi, Gazipur, Bangladesh |
| 11 | Công ty TNHH TM-DP Quốc tế Thiên Đan | 90A/D19, Đường Lý Thường Kiệt, Phường 14, Quận 10, TP. Hồ Chí Minh | Baroque Pharmaceuticals Pvt, Ltd | 192/2 Sokhada-388620, Taluka-Khambhat, Dist: Anand (Gujarat), India |
| 12 | Công ty TNHH thương mại dược phẩm Đông Phương | 119, đường số 41, phường Tân Quy, Quận 7, thành phố Hồ Chí Minh | Healthcare Pharmaceuticals Ltd. | Rajendrapur, Gazipur, Bangladesh |
| 13 | Efroze Chemical Industries (Pvt) Ltd. | 12-C, Block-6, P.E.C.H.S PO Bõ 4509, Karachi, Pakistan | Efroze Chemical Industries (Pvt) Ltd. | 146/23 Korangi Industrial Area, Karachi, Pakistan |
| 14 | Germany Pharmaceutical | Parque Industrial Da Concordia, Lote D1b, Macau | Germany Pharmaceutical | Parque Industrial Da Concordia, Lote D1b, Macau |
| 15 | Hetero Drugs Ltd. | Hetero House H. No: 8- 3- 166/7/1, Erragadda, Hyderabad-500018, Andhra Pradesh, India | Hetero Drugs Ltd. | 22-110, 1.D.A Jeedimetla, Hyderabad – 500055, India |
| 16 | Hetero Labs Limited | 7-2 A2, Hetero Corparate, Industrial Estates, Sanathnagar Hyderabad Andhra Pradesh-AP, India | Hetero Labs Limited | Unit-V, Sy. No. 410, 411, APIISCEZ, Polepally Village, Jadeherla Mandal Mahaboognagar Dict-509301, India |
| 17 | Hexal AG. | Industriestrasse 25 D-83607 Holxkirchen, Germany | Novartis Farmaceutica S.A | Ronda de Santa Maria 158 08210 Barbera del Valles, Barcelona, Spain |
| 18 | Korea United Pharm. Inc. | 154-8 Nonhyun-Dong, Kangnam-Ku, Seoul, Korea | Korea United Pharm. Inc. | 25-23, Nojanggongdan-gil, Jeondongmyeon, Sejong-si, Korea |
| 19 | Korea United Pharm. Inc. | 154-8 Nonhyun-Dong, Kangnam-Ku, Seoul, Korea | Korea United Pharm. Inc. | 404-10, Nojang-Ri, Jeondongmyeon, Yeongi-kun, Chungnam, Korea |
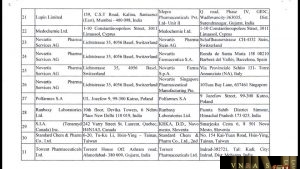
| 20 | Lupin Limited | 159, C.S.T Road, Kalina, Santacruz (East), Mumbai – 400 098, India | Jubilant Life Sciences Limited | Village Sikanndapur Bhainswal, Roorkee-Dehradoon Highway, Bhagwanpur, Roorkee, District Haridwar, Uttarakhand 247661, Indiaa |
| 21 | Lupin Limited | 159, C.S.T Road, Kalina, Santacruz (East), Mumbai – 400 098, India | Mepro Pharmaceuticals Pvt, Ltd- Unit II | Q Road, Phase IV, GIDC, Wadhwancity-360335, Dist. Surendranagar, Gujarat, India |
| 22 | Medochemie Ltd. | 1-10 Constantinoupoleos Street, 3011 Limassol, Cyprus | Medochemie Ltd. | 1-10 Constantinoupoleos Street, 3011 Limassol, Cyprus |
| 23 | Novartis Pharma Services AG | Lichtstrasse 35, 4056 Basel, Switzerland | Novartis Pharma Stein AG | Schaffhauserstrase CH-4332 Stein, Switzerland |
| 24 | Novartis Pharma Services AG | Lichtstrasse 35, 4056 Basel, Switzerland | Novartis Farmaceutica S.A | Ronda de Santa Maria 158 08210 Barbera del Valles, Barcelona, Spain |
| 25 | Novartis Pharma Services AG | Lichtstrasse 35, 4056 Basel, Switzerland | Novartis Farma S.p.A. | Via Provinciale Schito 131- Torre Annunziata (NA), Italy |
| 26 | Novartis Pharma Services AG | Lichtstrasse 35, 4056 Basel, Switzerland | Novartis Singapore Pharmaceutical Manufacturing Pte. | 10Tuas Bay Lane, 637461 Singapore |
| 27 | Polfarmex S.A | UL. Jozefow 9, 99-300 Kutno, Poland | Polfarmex S.A | 9 Jozefow, 99-300 Kutno, Poland |
| 28 | Ranbaxy Laboratories Ltd. | 10th floor, Devika Towers, 6 Nehru Place New Delhi 110 019, India | Ranbaxy Laboratories Ltd. | Paonta Sahib District Sirmour, Himachal Pradesh 173 025, India |
| 29 | S.I.A. (Tenamyd Canada) Inc. | 242 Varry Street St. Laurent, Quebec, H4N1A3, Canada | KRKA, D.D, Novo mesto, Slovenia | Smarjeska Cesta 6, 8 501 Novo Mesto, Slovenia |
| 30 | Standard Chem & Pharma Co., Ltd. | 6-20, Tu-ku Li, Hsin-Ying – Tainan, Taiwan | Standard Chem & Pharma Co., Ltd., 2nd | No. 154 Kai-Yuan Road, Hsin-Ying, Tainan, Taiwan |
| 31 | Torrent Pharmaceuticals Ltd. | Torrent House Off, Ashram road, Ahmedabad-380 009, Gujarat, India | Torrent Pharmaceuticals Ltd. | Indrad-382721, Tal: Kadi, City: Indrad, Dist: Mehsana, India |
Công văn 13124/QLD-CL năm 2018 Báo cáo việc sử dụng nguyên liệu Valsartan do Công ty Zhejiang Huahai Pharmaceutical – Trung Quốc sản xuất
DOWNLOAD VĂN BẢN GỐC DƯỚI ĐÂY