Y tế - Sức Khỏe
Tiêm vaccin trong quá trình mang thai bảo vệ trẻ sơ sinh 2025
Người dịch: NTHN
Xem và tải file PDF tại đây
Bệnh truyền nhiễm gây ra nguy cơ đặc biệt đối với trẻ sơ sinh, và hiện đang có nhu cầu toàn cầu về việc bảo vệ nhóm đối tượng dễ tổn thương này. Do gặp nhiều thách thức trong việc phát triển các loại vaccin hiệu quả ở trẻ sơ sinh, nên chỉ có vaccin viêm gan B và vaccin lao được tiêm trong 28 ngày đầu đời, và ngay cả những loại vaccin này cũng chủ yêu được khuyến nghị cho các nhóm nguy cơ cao. Kháng thể từ mẹ có thể truyền qua nhau thai và mang lại một số bảo vệ cho trẻ sơ sinh, do đó một chiến lược thay thế là tiêm vaccin cho phụ nữ trong thai kỳ. Phương pháp này đã được áp dụng thành công đề bảo vệ trẻ sơ sinh khỏi bệnh uốn ván và ho gà, và những loại vaccin được tiêm chủ yếu đề bảo vệ mẹ trong thai kỳ như vaccin cúm và Covid-19 cũng mang lại một phần miễn dịch cho trẻ sơ sinh. Gần đây, một loại vaccin ngừa RSV đã được phê duyệt để sử dụng trong thai kỳ nhằm bảo vệ trẻ sơ sinh, và một loại vaccin mới có thể được triển khai trong thai kỳ để ngăn ngừa nhiễm trùng do liên cầu khuẩn nhóm B ở trẻ nhỏ cũng đang sắp ra mắt.
TỔNG QUAN
Trẻ sơ sinh đặc biệt dễ bị tổn thương trước các bệnh truyền nhiễm do hệ miễn dịch của các trẻ còn đang trong quá trình phát triển. Đặc biệt, trẻ thiếu trí nhớ miễn dịch bảo vệ vì hầu như chưa từng tiếp xúc với mầm bệnh trước đó. Năm 2015, có khoảng 610.000 trẻ sơ sinh trên toàn thế giới tử vong do bệnh truyền nhiễm, tương đương với tỷ lệ 4.4 ca tử vong trên 100.000 ca sinh sông. Phần lớn các ca tử vong xảy ra tại các quốc gia có thu nhập thấp và trung bình. Ở các nước có thu nhập cao hơn, bệnh truyền nhiễm ít khi gây tử vong nhưng vẫn là nguyên nhân gây nhập viện và tạo gánh nặng lớn cho gia đình và hệ thống y tê, cũng như có thể để lại hậu quả lâu dài cho trẻ nhỏ. Vì vậy, nhu cầu bảo vệ trẻ sơ sinh khỏi các bệnh truyền nhiễm là một vấn đề toàn cầu.
Bài viết này trình bày về cách mà việc tiêm vaccin trong thai kỳ và khi mới sinh có thể giúp bảo vệ trẻ sơ sinh khỏi bệnh truyền nhiễm, bằng cách ngăn ngừa nhiễm bệnh hoặc làm giảm mức độ nặng của bệnh nếu không thể ngăn ngừa hoàn toàn. Bài viết tập trung vào các loại vacxin được phát triển đề bảo vệ trẻ sơ sinh (dưới 28 ngày tuổi). Tuy nhiên, cũng cần lưu ý rằng những biện pháp nhằm bảo vệ trẻ sơ sinh vẫn có thể tiếp tục mang lại hiệu quả bảo vệ trong 3 đến 6 tháng đầu đời
MIỄN DỊCH CỦA VACCIN TRONG MANG THAI
Một phần lý do khiến trẻ sơ sinh dễ bị nhiễm trùng là do hệ miễn dịch ở giai đoạn sơ sinh vẫn còn “chưa trưởng thành” về mặt chức năng. Tuy nhiên, ngày càng có sự đồng thuận rằng thuật ngữ “chưa trưởng thành” có thể không chính xác, và trạng thái này có thể được xem là một cơ chế giúp bảo vệ trẻ sơ sinh khỏi các phản ứng miễn dịch quá mức đối với kháng nguyên môi trường vô hại và các vi sinh vật cộng sinh – những yêu tô mà cơ thể lần đầu tiếp xúc sau khi sinh. Tuy nhiên, điều này lại đặt ra thách thức cho việc tiêm chủng ở trẻ sơ sinh, vì chúng tạo ra đáp ứng miễn dịch kém hiệu quả hơn với một số loại vaccin so với trẻ lớn và người trưởng thành.
Kháng thể từ mẹ có thể đi qua nhau thai và được tiết vào sữa mẹ, mang lại cho trẻ sơ sinh một phần bảo vệ trước các thách thức kháng nguyên mà người mẹ đã từng gặp phải. Do đó, một chiến lược được áp dụng là tiêm vaccin trong thời kỳ mang thai và dựa vào kháng thể từ mẹ đề bảo vệ cho trẻ sơ sinh. Tuy nhiên, tiêm vaccin sống bị chống chỉ định trong thai kỳ do khả năng rằng các mầm bệnh này dù đã được làm suy yếu vẫn có thể gây bệnh qua nhau thai và thai nhi trên lý thuyết. Vì vậy, việc tiêm vaccin cho trẻ sơ sinh được ưu tiên trong trường hợp chỉ có vaccin sống giảm độc lực (chẳng hạn như vaccin BCG phòng bệnh lao). Tiêm chủng cho trẻ sơ sinh cũng được ưu tiên trong trường hợp kháng thể từ mẹ không mang lại sự bảo vệ cho trẻ sơ sinh (ví dụ như vaccin HBV phòng viêm gan B).
Đáp ứng miễn dịch của tiêm chủng trong thai kỳ
Mặc dù thai kỳ không phải là trạng thái bị ức chế miễn dịch, nhưng nó có những thay đổi tình vì trong đáp ứng miễn dịch toàn thân. Do đó, khi mục tiêu của một chương trình tiêm chủng là để bảo vệ trẻ sơ sinh thông qua việc truyền kháng thể qua nhau thai, thì điều quan trọng là phải xác nhận răng loại vaccin sử dụng có khả năng tạo ra phản ứng kháng thể thích hợp.
Vaccin uốn ván, bạch hầu, ho gà vô bào (Tdap) thường được tiêm trong thai kỳ nhằm bảo vệ trẻ sơ sinh khỏi bệnh uốn ván và ho gà. Tuy nhiên, bằng chứng về phản ứng miễn dịch đặc hiệu trong thai kỳ đối với loại vaccin này còn chưa thống nhất. Một số nghiên cứu cho thấy không có sự khác biệt về nồng độ kháng thể giữa phụ nữ mang thai và không mang thai sau khi tiêm Tdap. Tuy nhiên, những nghiên cứu khác lại ghi nhận răng mặc dù tiêm Tdap trong thai kỳ vẫn tạo ra nồng độ kháng thể bảo vệ, nhưng phản ứng miễn dịch này vẫn thấp hơn so với khi tiêm ngoài thai kỳ.
Đối với vaccin cúm và Covid-19, nồng độ kháng thể tạo ra khi tiêm trong thai kỳ nhìn chung tương đương với khi tiêm ngoài thai kỳ. Tuy nhiên, các nghiên cứu sử dụng phương pháp huyết thanh học đã chỉ ra một số khác biệt tỉnh tê giữa nhóm mang thai và không mang thai sau khi tiêm vaccin Covid-19: liều đầu tiên của vaccin mRNA Covid-19 tạo ra kháng thể có khả năng gắn kết với thụ thể Fc, nhưng với tốc độ chậm hơn một chút ở nhóm mang thai so với nhóm không mang thai. Một nghiên cứu khác so sánh ba loại vaccin Covid-19 tiêm trong thai kỳ cũng cho thấy có sự giảm nhẹ về chức năng trung gian qua khảng thế khi tiêm trong tam cá nguyệt thứ hai, so với tam cá nguyệt thứ nhất hoặc thứ ba.
Tóm lại, việc tiêm chủng trong thai kỳ có thể tạo ra phản ứng kháng thể khác biệt trong một số trường hợp. Tuy nhiên, phản ứng kháng thể tạo ra vẫn đủ để bảo vệ. Và vì nồng độ kháng thể có xu hướng giảm dần theo thời gian, việc tiêm vaccin trong thai kỳ vẫn được ưu tiên đề tôi đa hóa khả năng bảo vệ trẻ sơ sinh, hơn là chỉ tiêm chủng trước khi mang thai.
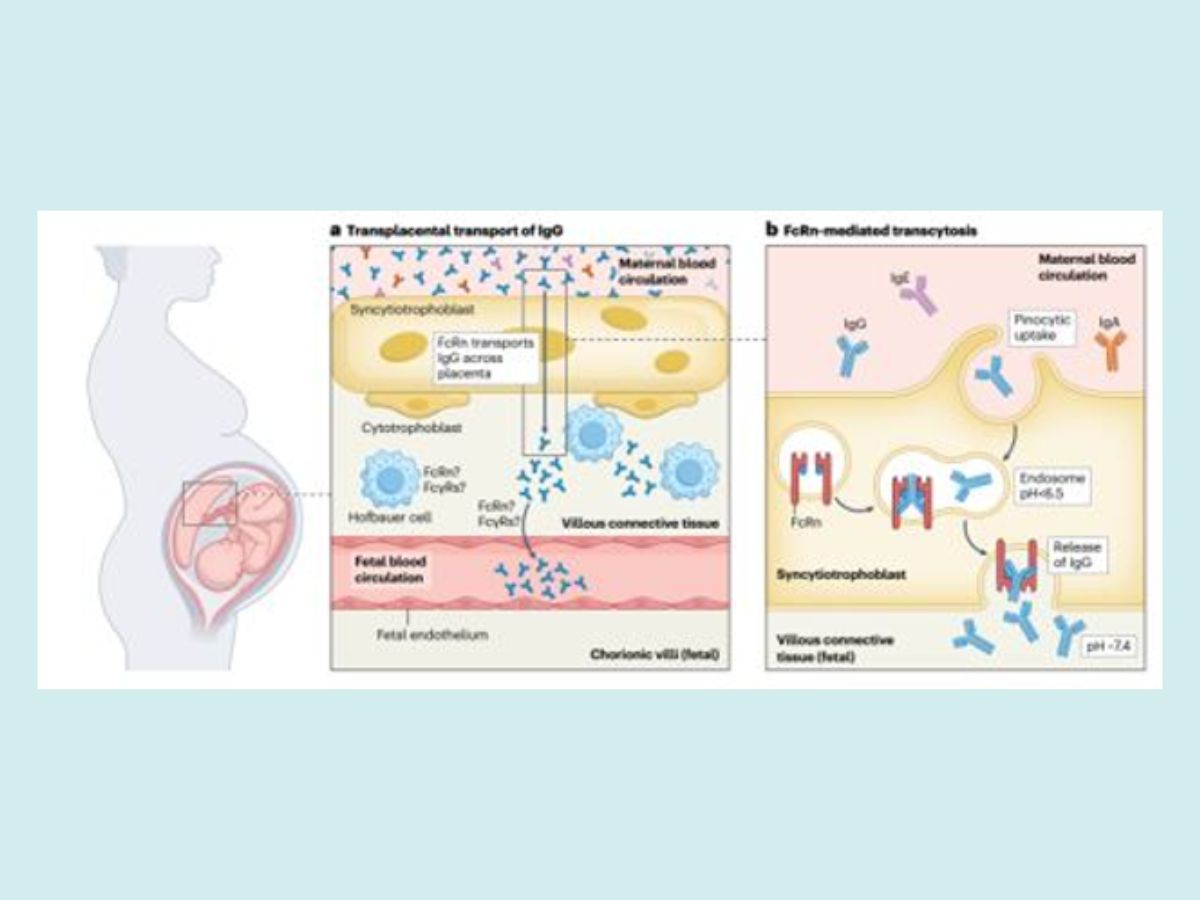
(a) Hệ tuần hoàn của mẹ và thai nhi được ngăn cách bởi các tế bào nuôi dạng nhung mao (villous trophoblast), mô liên kết của thai nhi và các tế bào nội mô của thai nhi. IgG được vận chuyển xuyên qua lớp tế bào hợp bào (syncytiotrophoblast) thông qua cơ chế xuyên màng trung gian thụ thể Fc ở trẻ sơ sinh (neonatal Fc receptor – FcRn), chi tiết được thể hiện ở hình (b). Cách IgG di chuyển qua mô liên kết và lớp nội mô của thai nhi vẫn chưa được hiểu rõ, nhưng FcRn và các thụ thể Fcy khác được biểu hiện trên các đại thực bào nhau thai (tế bào Hofbauer) và tế bào nội mô thai nhi có thể đóng vai trò trong quá trình này. (b) Các tế bào hợp bào (syncytiotrophoblast) hấp thu IgG từ mẹ thông qua cơ chế ẩm bào. Các túi chứa IgG sẽ hòa hợp với endosome chứa FcRn, giúp bảo vệ IgG không bị enzym phân hủy trong môi trường pH thấp. Khi endosome tiên gần về phía thai nhi và hợp nhất với màng tế bào ở phía này, pH tăng dần khiến FcRn giải phóng IgG vào mô liên kết dạng nhung mao.
Sự truyền kháng thể qua nhau thai
Nền tảng cho chiến lược tiêm chủng trong thai kỳ nhằm bảo vệ trẻ sơ sinh chính là quá trình truyền kháng thể từ mẹ qua nhau thai một cách hiệu quả. Trong số 5 lớp kháng thể, IgG là loại duy nhất có thể đi qua nhau thai, và quá trình này được trung gian cụ thể bởi thụ thể Fc ở trẻ sơ sinh. Để di chuyển từ máu mẹ sang tuần hoàn thai nhi, kháng thể phải đi qua các tế bào nuôi (trophoblast) bao phủ nhung mao nhau thai, tiếp theo là mô liên kết dạng nhung mao, và sau cùng là các tế bào nội mô đê vào mao mạch của thai nhi. FcRn được biểu hiện rõ ràng ở các tế bào nuôi dạng nhung mao, và cơ chế mà FcRn vận chuyên IgG qua lớp tế bào này đã được xác định thông qua các tế bào có nguồn gốc từ trophoblast hoặc các dòng tế bào được biển đối để biểu hiện FcRn. Tế bào trophoblast dạng nhung mao hấp thu IgG từ máu mẹ qua cơ chế ẩm bào. Trong endosome, FcRn sẽ gắn với IgG ở điều kiện pH thấp, bảo vệ nó không bị enzym phân hủy trong quá trình vận chuyển sang phía thai nhi. Khi endosome hợp nhất với màng phía thai nhi, pH tăng lên khiên FcRn giải phóng IgG vào mô liên kết dạng nhung mao. Cách IgG tiếp tục di chuyển qua mô liên kết và vào mạch máu của thai nhi vẫn chưa rõ ràng. Các đại thực bào nhau thai (tế bào Hofbauer) có FcRn và các
thụ thể Fcy khác, có thể hỗ trợ cho quá trình này. Trong khi đó, vẫn chưa có sự đồng thuận về việc liệu các tế bào nội mô dạng nhung mao có FcRn hay không, và rất có thể những thụ thể IgG khác sẽ đóng vai trò trung gian trong việc đưa IgG vào các mao mạch của thai nhi. Trong các phân lớp IgG, IgG1 được truyền qua nhau thai hiệu quả nhất, tiếp theo là IgG4, rồi đến IgG2 và IgG3. Do đó, mức độ mà các vaccin kích thích tạo ra từng phân lớp IgG này có thể ảnh hưởng đến hiệu quả bảo vệ trẻ sơ sinh của các loại vaccin khác nhau.
Trong tam cá nguyệt đầu tiên, quá trình truyền IgG qua nhau thai diễn ra rất ít. Việc vận chuyển này được thiết lập dân trong tam cá nguyệt thứ hai: từ tuần thai thứ 12 đến 22, nồng độ IgG trong máu cuống rốn của thai nhi chỉ đạt khoảng 10% so với nồng độ trong máu mẹ, và đến cuối tam cá nguyệt thứ hai, tỷ lệ này tăng lên khoảng 50%. Trong tam cá nguyệt thứ ba, tốc độ truyền tăng mạnh và đến lúc sinh nồng độ IgG ở thai nhi thường vượt qua cả nồng độ ở mẹ. Do đó, thời điểm tiêm chủng lý tưởng nhất để tối ưu hóa lượng IgG đặc hiệu trong máu cuống rốn ở trẻ sinh đủ tháng là từ tuần 26 đến tuần 34 của thai kỳ, mặc dù tỷ lệ trẻ có huyết thanh học dương tính ở bất kỳ mức độ nào vẫn tương tự nêu tiêm chủng diễn ra bất kỳ lúc nào trong khoảng tuần thứ 13 đến 34. Một thử nghiệm ngẫu nhiên cho thấy việc tiêm phòng từ tuần 23 đến 32 cho kết quả nồng độ kháng thể IgG ở trẻ sơ sinh tương đương nhau đối với hai trong ba kháng nguyên của bệnh ho gà được nghiên cứu. Ngược lại, nếu tiêm chủng sau tuần thứ 32-34, mức IgG đặc hiệu ở trẻ sơ sinh sẽ thấp hơn vì không có đủ thời gian để mẹ tạo ra đáp ứng miễn dịch và truyền kháng thể qua nhau thai trước khi sinh. Các nghiên cứu đánh giá hiệu quả của tiêm phòng trong thai kỳ để bảo vệ trẻ sơ sinh phân lớn cho thấy tiêm phòng muộn hơn trong thai kỳ mang lại hiệu quả bảo vệ cao hơn. Tuy nhiên, nêu mục tiêu chính là bảo vệ mẹ khỏi bệnh nặng trong thai kỳ, tiêm phòng có thể được thực hiện sớm hơn, dù có thể làm giảm hiệu quả bảo vệ cho trẻ sau sinh.
Các yếu tố ảnh hưởng đến thời điểm tiêm vaccin trong thai kỳ
Khi mục tiêu chính là bảo vệ em bé sau sinh:
- Vaccin hiệu quả nhất khi được tiêm trong khoảng từ tuần 23 đến tuần 34 của thai kỳ. Trước năm 2016, chương trình tiêm vaccin ho gà tại Anh chủ yêu bao phủ giai đoạn từ tuần 28 đến tuần 38 của thai kỳ.
- Tuy nhiên, việc giới hạn thời gian tiêm chủng vào giai đoạn muộn của thai kỳ có thể khiến trẻ sinh non không được hưởng lợi. Đây là một trong những lý do khiến Vương quốc Anh, vào năm 2016, đã điều chỉnh thời gian khuyến cáo tiêm vaccin ho gà xuống khoảng từ tuần 16 đến 32 của thai kỳ. Những quốc gia chỉ cho phép tiêm vaccin RSV sau tuần 32 của thai kỳ có thể làm giảm khả năng bảo vệ đối với trẻ sinh non.
- Giới hạn tiêm chủng vào giai đoạn đầu thai kỳ cũng có thể khiến một số phụ nữ mang thai bỏ lỡ cơ hội được tiêm vaccin. Vì lý do này, tại Anh những phụ nữ không tiêm vaccin ho gà trong khung thời gian được khuyến cáo vẫn có thể được tiêm sau đó.
Khi mục tiêu chính là bảo vệ mẹ và thai nhi trong thai kỳ:
- Tiêm chủng nhắm vào các virus theo mùa có thể được triển khai dưới dạng các chương trình tiêm chủng theo mùa. Tại Vương Quốc Anh, vaccin cúm được tiêm vào mùa thu trước thời điểm dự đoán có sự lây lan virus cao nhât.
- Đối với các virus đột biến nhanh, mũi tiêm nhắc lại có thể được triển khai ngay khi có vaccin dành cho những biến thể mới. Phương pháp này hiện đang được áp dụng tại Hoa Kỳ cho tiêm chủng covid-19.
Các lưu ý chung:
- Khi xảy ra tình trạng thiếu hụt vaccin, có thể cần phải triển khai tiêm chủng ngay khi vaccin sẵn có.
- Khi ngày càng có nhiều loại vaccin được phát triển để sử dụng trong thai kỳ, việc xem xét tính an toàn và hiệu quả của các loại vaccin khi tiêm cùng lúc sẽ trở nên ngày càng quan trọng.
Ước tính thời gian bán hủy của kháng thể IgG truyền từ mẹ sang trẻ sơ sinh dao động từ 28.7 ngày đên 48.4 ngày, tùy thuộc vào kháng nguyên đặc hiệu. Đối với IgG1 kháng độc tố uốn ván, nồng độ kháng thể giảm xuống còn 10% so với lúc mới sinh sau 4 tháng và 3% sau 6 tháng. Vì lý do này, sự bảo vệ từ kháng thể mẹ truyền dân suy giảm trong 6 tháng đầu đời của trẻ. Điều này cũng ảnh hưởng đến lịch tiêm chủng cho trẻ sơ sinh, bởi vì kháng thể mẹ truyền có thể điều chỉnh đáp ứng miễn dịch của trẻ đối với vaccin. Trong một phân tích tổng hợp trên 7630 trẻ, nồng độ kháng thể mẹ cao gấp đôi có liên quan đến nồng độ kháng thể sau tiêm ở trẻ thấp hơn từ 20% đến 28% đối với vaccin bại liệt bất hoạt, 11% với độc tố ho gà và 13% với độc tố uốn ván. Tác động này ít rõ rệt hơn ở trẻ lớn hơn, khi lượng kháng thể mẹ truyền đã giảm dần. Do đó, mục tiêu của lịch tiêm chủng cho trẻ sơ sinh là tiêm càng sớm càng tốt sau khi nồng độ kháng thể mẹ truyền giảm xuống dưới ngưỡng gây cản trở phản ứng miễn dịch của trẻ.
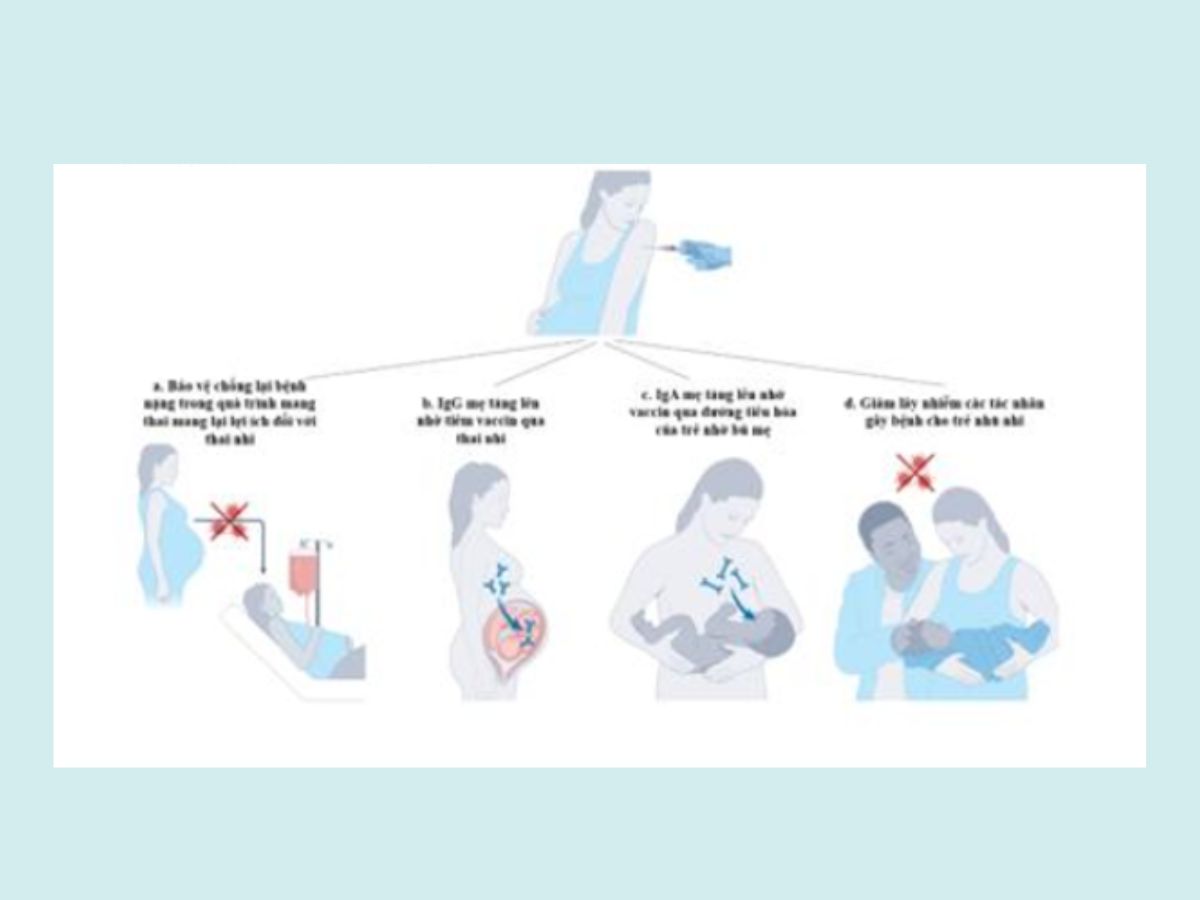
.Việc tiêm vaccin trong thai kỳ bảo vệ trẻ sơ sinh khỏi bệnh truyền nhiễm thông qua 4 cơ chế sau: (a) Bảo vệ mẹ khỏi bệnh nặng trong thai kỳ, từ đó giảm các biến chứng nguy hiểm cho thai nhi. Vaccin cúm và Covid-19 thường được chỉ định vì lý do này. (b) IgG của mẹ được tạo ra nhờ tiêm chủng có thể đi qua nhau thai, giúp bảo vệ trẻ sau sinh. Đây là cơ chế chính đối với các vaccin như ho gà và RSV. (c) IgA của mẹ do tiêm vaccin tạo ra được tiết trong sữa mẹ, đi qua đường tiêu hóa của trẻ. Một số bằng chứng cho thấy vaccin cúm khi tiêm trong thai kỳ có thể tăng cường bảo vệ trẻ sơ sinh qua con đường này. (d) Cha mẹ và người chăm sóc đã tiêm chủng sẽ ít có nguy cơ mắc bệnh hơn, do đó ít có khả năng lây nhiễm cho trẻ sơ sinh (còn gọi là hiệu ứng vỏ bọc).
Kháng thể trong sữa mẹ
Một cách khác mà miễn dịch của mẹ có thể bảo vệ trẻ sơ sinh là thông qua việc truyền kháng thể vào sữa mẹ, cho phép trung hòa mầm bệnh trong đường tiêu hóa của trẻ. Thành phần chủ yêu là IgA, mặc dù cũng có thể phát hiện nồng độ thấp IgG và IgM trong sữa mẹ. Tế bào plasma ở tuyến vú sản xuất IgA và IgM, sau đó các kháng thể này được vận chuyển qua biểu mô tuyến vú vào trong sữa. IgG tuần hoàn trong máu mẹ có thể được vận chuyển vào sữa nhờ thụ thể FcRn, nhưng hiệu quả thấp hơn nhiều so với vận chuyển qua nhau thai. Các tế bào tiết IgA chủ yêu bắt nguồn từ hệ miễn dịch đường ruột, do đó kháng thể ở tuyến vú phản ánh kháng thể ở đường tiêu hóa. Điều này giúp sữa mẹ cung cấp đúng các loại kháng thể thích hợp nhất với môi trường đường ruột của trẻ, tuy nhiên cũng gợi ý rằng các vaccin chủ yếu tạo ra phản ứng IgG tuần hoàn ở mẹ có thể có khả năng hạn chế trong việc truyền kháng thể bảo vệ qua sữa mẹ. Tuy vậy, vẫn có một số bằng chứng cho thấy việc nuôi con bằng sữa mẹ có thể mang lại bảo vệ nhất định. Trong một thử nghiệm ngẫu nhiên có đối chứng về việc tiêm vaccin cúm trong thai kỳ, nuôi con hoàn toàn bằng sữa mẹ sau sinh có liên quan đến việc giảm đáng kê các bệnh hô hấp ở trẻ sơ sinh, nhưng chỉ trong nhóm mẹ đã được tiêm vaccin cúm.
Ngắt chuỗi lây truyền mầm bệnh thông qua tiêm vaccin
Bên cạnh khả năng bảo vệ trực tiếp chống lại mầm bệnh nhờ kháng thể từ mẹ truyền sang, tiêm vaccin cho mẹ còn có thể gián tiếp bảo vệ trẻ bằng cách ngăn chặn quá trình lây truyền mầm bệnh. Chiến lược này đôi khi được mở rộng để tiêm chủng cho các đối tượng tiếp xúc gần với trẻ sơ sinh, và đã chứng minh hiệu quả trong việc bảo vệ trẻ khỏi bệnh cúm. Chiến lược này cũng được áp dụng với bệnh ho gà, nhưng trong thực tế, số người cần tiêm để đạt hiệu quả bảo vệ lại quá lớn, khiến chi phí không hiệu quả ở những nơi có tỷ lệ mắc ho gà thấp. Do đó, hiệu quả của chiến lược tạo vỏ bọc phụ thuộc nhiều vào tỷ lệ mắc bệnh trong cộng đồng – chiến lược này sẽ hợp lý hơn ở các khu vực có nguy cơ dịch cao.
CHƯƠNG TRÌNH TIÊM CHỦNG
Việc tiêm chủng trong thai kỳ để bảo vệ trẻ sơ sinh là một chiến lược đã có lịch sử lâu đời. Ngay từ năm 1877, các báo cáo đã ghi nhận răng trẻ sơ sinh có mẹ được tiêm vaccin đậu mùa trong thai kỳ cũng được bảo vệ khỏi bệnh đậu mùa. Từ giữa thế kỷ XX trở đi, việc tiêm chủng khi mang thai ngày càng trở thành một công cụ quan trọng trong bảo vệ sức khỏe trẻ sơ sinh.
Tiêm vaccin uốn ván trong thai kỳ
Uốn ván là bệnh do bào tử vi khuẩn Clostridium tetani xâm nhập vào các vết thương hở. Trẻ sơ sinh đặc biệt dễ bị nhiễm uốn ván trong các điều kiện y tế hạn chế, nơi dụng cụ cắt dây rốn không được tiệt trùng đúng cách. Uốn ván sơ sinh thường khởi phát từ ngày thứ 3 đến ngày thứ 28 sau sinh, với các biểu hiện như mất phản xạ bú và co thắt cơ. Nếu không được điều trị, uốn ván sơ sinh gần như luôn gây tử vong, và ngay cả khi có chăm sóc y tế, tỷ lệ tử vong vẫn dao động từ 10% đến 60% đối với trẻ bị nhiễm.
Vaccin uốn ván đầu tiên sử dụng độc tố uốn ván hấp phụ trên muối nhôm, được sử dụng rộng rãi trong thế chiến thứ hai. Đến năm 1959, một nghiên cứu quan sát đã cho thấy tiêm vaccin uốn ván cho thai phụ giúp bảo vệ gân 95% trẻ sơ sinh khỏi tử vong do uốn ván sơ sinh. Thử nghiệm lâm sàng ngẫu nhiên đầu tiên cho thấy không có trường hợp tử vong nào do uốn ván sơ sinh ở trẻ có mẹ được tiêm 2-3 liều vaccin, so với tỷ lệ tử vong 7.8% ở nhóm đối chứng. Các nghiên cứu sau đó cũng xác nhận rằng 2-3 liều vaccin uốn ván trong thai kỳ có hiệu quả bảo vệ lên đến 98% và không làm tăng nguy cơ biến chứng nghiêm trọng cho mẹ hoặc trẻ sơ sinh. Năm 1988, khoảng 787.000 trẻ sơ sinh tử vong do uốn ván mỗi năm. Do đó, năm 1989 Hội đồng Y tê Thế giới đã đặt mục tiêu giảm tỷ lệ uốn ván sơ sinh xuống dưới 1 ca trên 1.000 trẻ sinh sống ở mỗi quận/huyện. Đến năm 2018, số ca tử vong đã giảm còn khoảng 25.000 ca, tức giảm 97% so với năm 1988, nhờ mở rộng quy mô tiêm chủng.
Tiêm vaccin ho gà trong thai kỳ
Ho gà là một bệnh lý đường hô hấp dễ lây nhiễm, do vi khuẩn Bordetella pertussis gây ra, đặc trưng bởi các cơn ho kịch phát kèm theo tiếng rít đặc trưng thì hít vào. Tại Mỹ, giai đoạn 1940-1948 số ca tử vong do ho gà ở trẻ sơ sinh cao gấp gần ba lần tổng số ca tử vong do sởi, quai bị, rubella, scarlet fever, bạch hầu, bại liệt và viêm màng não cộng lại. Ho gà hiện vẫn gây 85.900 ca tử vong mỗi năm ở trẻ sơ sinh trên toàn cầu, khiên đây trở thành một trong những nguyên nhân hàng đầu gây tử vong có thể phòng ngừa bằng vaccin.
Vaccin ho gà toàn bào đã được phát triển từ năm 1914, và một nghiên cứu năm 1943 cho thấy kháng thể có thể truyền qua nhau thai, mang lại một phần miễn dịch cho trẻ sơ sinh khi mẹ được tiêm vaccin trong thai kỳ. Tuy nhiên, chương trình tiêm vaccin ho gà cho phụ nữ mang thai không được triển khai ngay, một phần là do lo ngại về tác dụng phụ của vaccin toàn bào, và một phần vì chương trình tiêm chủng cho trẻ sơ sinh khi đó đã đạt hiệu quả cao. Đến thập niên 1970-1980, vaccin ho gà vô bào ra đời với độ an toàn cao hơn. Cùng với sự bùng phát trở lại của bệnh ho gà vào đầu thế kỷ XXI, điều này thúc đây Mỹ và Anh chính thức khuyến nghị tiêm vaccin ho gà trong thai kỳ vào các năm 2010.
Tại Anh, sau khi triển khai tiêm vaccin ho gà trong thai kỳ, số ca mắc ở trẻ dưới 3 tháng tuổi giảm tới 78%. Nhiều nghiên cứu cũng ghi nhận hiệu quả bảo vệ khỏi nhập viện ở trẻ dưới 3 tháng tuổi dao động từ 66% đến 94% mà không làm tăng nguy cơ tai biến sản khoa hoặc sơ sinh.
Khuyến nghị về thời điểm và loại vaccin được sử dụng trong thai kỳ đã thay đổi kể từ khi chương trình tiêm phòng ho gà được triển khai. Tại Vương quốc Anh, vaccin ho gà ban đầu được khuyến cáo tiêm trong khoảng từ 28 đến 38 tuần của thai kỳ. Tuy nhiên, từ năm 2016, khoảng thời gian khuyến nghị đã được mở rộng ra từ 16 đến 32 tuần. Sự thay đổi này nhằm tăng khả năng các thai phụ được tiêm phòng đúng thời điểm, đồng thời đảm bảo rằng những trẻ sinh non cũng có thể nhận được lợi ích từ kháng thể mẹ truyền sang. Một nghiên cứu vào năm 2016 cho thấy việc tiêm vaccin sớm hơn trong thai kỳ giúp tối ưu hóa tỷ lệ huyết thanh dương tính với kháng nguyên ho gà ở trẻ sơ sinh, và đây là một yếu tố góp phần vào sự thay đổi chính sách. Ngoài ra, một thử nghiệm ngẫu nhiên có đối chứng sau đó cũng cho thấy rằng việc tiêm phòng vào bất kỳ thời điểm nào trong khoảng từ 23 đến 32 tuần đều tạo ra nồng độ kháng thể tương đương nhau ở trẻ sơ sinh, càng cùng cô thêm cơ sở cho chính sách tiêm phòng sớm hơn trong thai kỳ.
Đáp lại các phát hiện rằng việc sử dụng vaccin phối hợp nhiều thành phần bao gồm bạch hầu, uốn ván và ho gà (DTaP), có chứa thêm thành phần vaccin bại liệt bất hoạt (IPV) – gọi chung là DTaP/IPV-trong thai kỳ có thể làm giảm khả năng chuyển đổi huyết thanh sau khi trẻ được chủng ngừa bại liệt, kể từ tháng 7 năm 2024, tại Vương quốc Anh, các thai phụ đã được khuyến cáo tiêm loại vaccin Tdap không chứa thành phần IPV. Việc tiêm vaccin ho gà trong thai kỳ có thể làm cùn mòn (blunting) đáp ứng miễn dịch của trẻ sau khi tiêm mũi vaccin ho gà đầu tiên, và hiệu ứng này đặc biệt rõ rệt ở trẻ được tiêm vaccin ho gà dạng toàn bào thay vì vaccin ho gà vô bào trong phác đồ tiêm chủng. Tuy nhiên, các bằng chứng dịch tễ học hiện tại không cho thấy có sự suy giảm miễn dịch này ảnh hưởng rõ rệt đến hiệu quả bảo vệ trên lâm sàng, và lợi ích của việc tiêm vaccin cho mẹ trong thai kỳ đối với trẻ sơ sinh vượt trội hơn nguy cơ tiềm tàng làm gia tăng bệnh ở trẻ nhỏ.
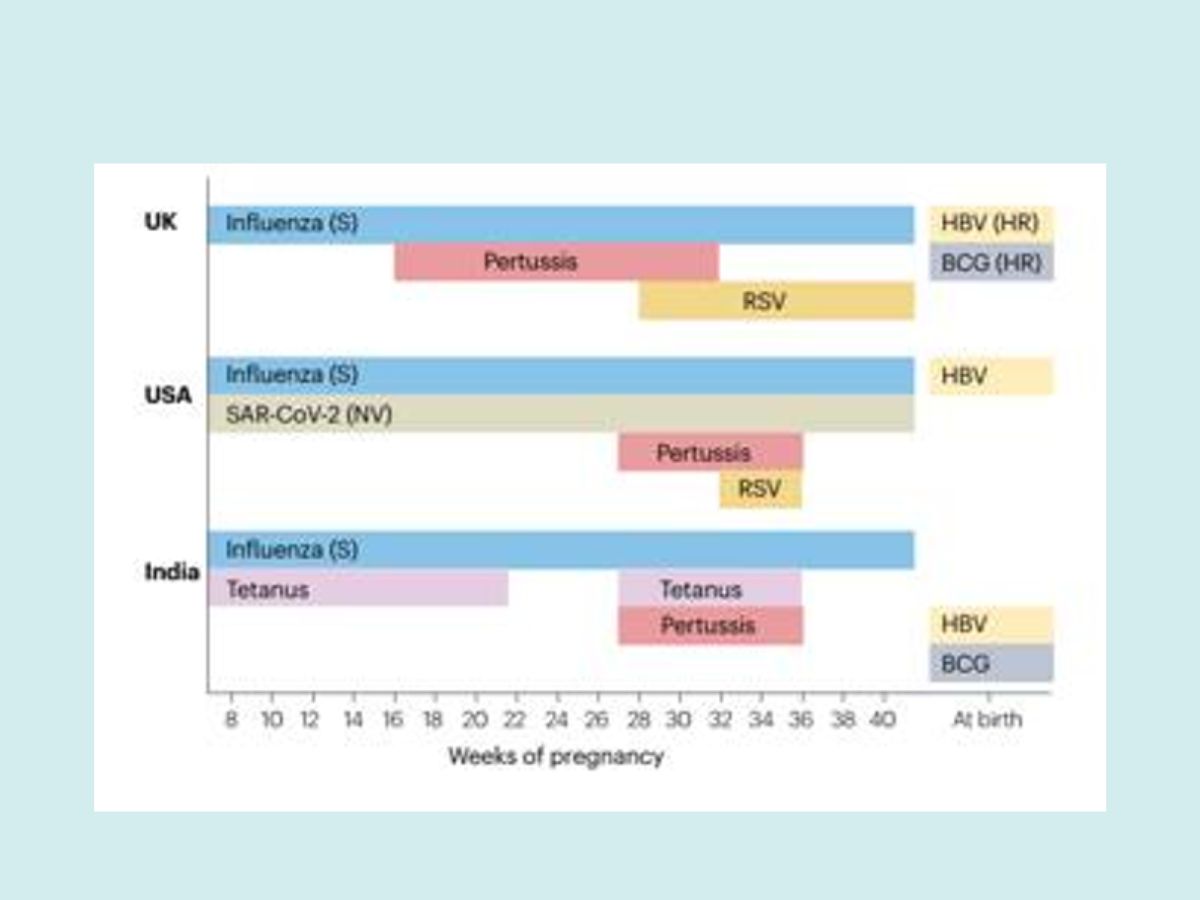
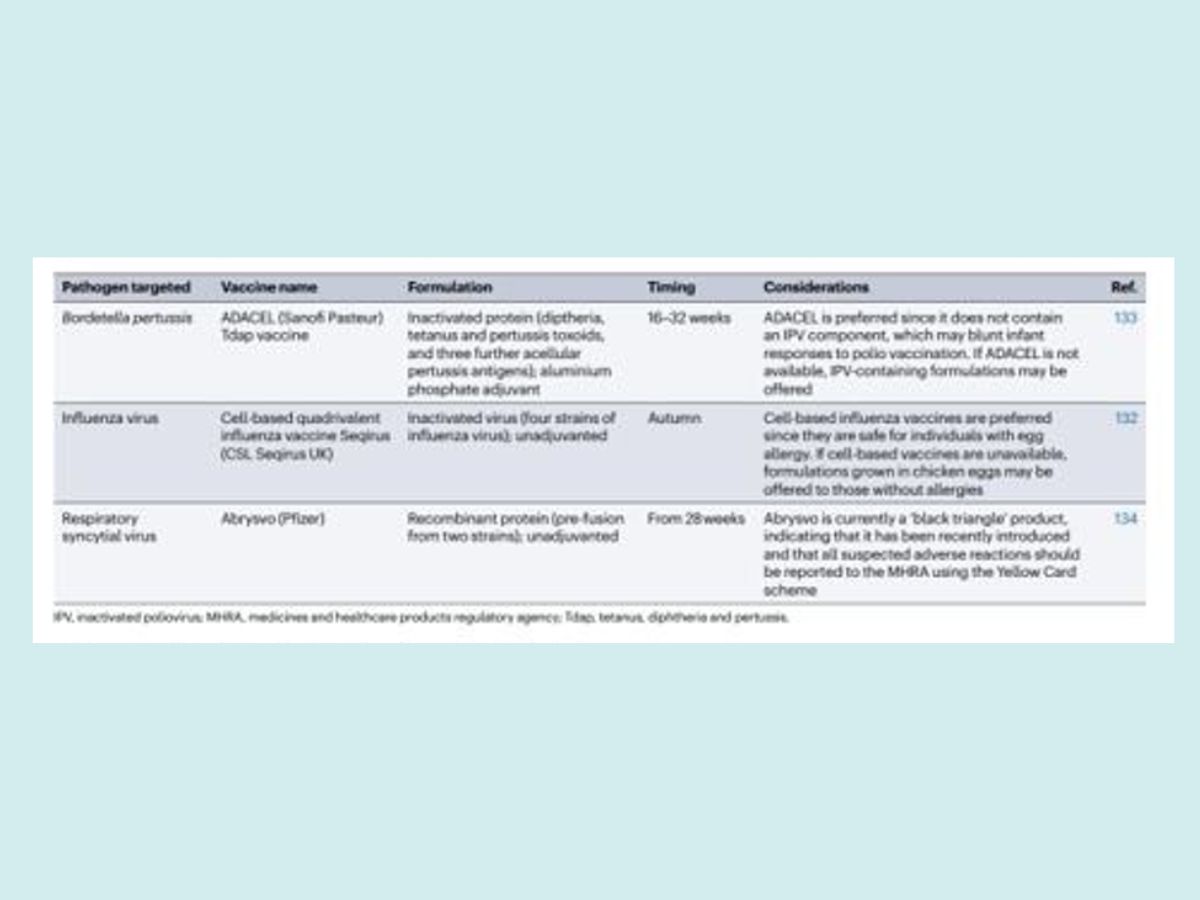
Các loại vaccin được cung cấp theo mùa được ký hiệu bằng (S), những loại vaccin được cung cấp khi có công thức mới nhằm vào biến thể mới được ký hiệu (NV), và các vaccin chỉ được cung cấp cho những trẻ sơ sinh có nguy cơ cao được ký hiệu bằng (HR). Tại Anh, vaccin Covid-19 từng được triển khai theo chiến dịch tiêm chủng mùa vụ cho đến mùa Xuân năm 2025, nhưng các phân tích chi phí – lợi ích hiện không còn ủng hộ việc tiếp tục điều này. Ở Hoa Kỳ, vaccin cúm thường được tiêm vào mùa thu, nhưng nếu tam cá nguyệt thứ ba rơi vào mùa hè, có thể xem xét tiêm vào mùa hè để bảo vệ trẻ sơ sinh. Tại Ấn Độ, mũi tiêm phòng uốn ván thứ hai có thể được kết hợp với mũi nhắc lại Tdap.
Tiêm vaccin cúm và Covid-19 trong thai kỳ
Mang thai làm tăng nguy cơ mắc bệnh nặng viêm phổi do virus gây ra. Do đó, vaccin cúm và vaccin Covid-19 được khuyến cáo sử dụng để bảo vệ cả mẹ và thai nhi trong thời kỳ mang thai. Tiêm phòng trong thai kỳ có hiệu quả 49% trong việc ngăn ngừa nhiễm virus cúm và 94% hiệu quả trong việc ngăn ngừa nhập viện do Covid-19. Cả hai loại vaccin này đều không liên quan đến nguy cơ tăng các biến chứng chu sinh, một số nghiên cứu thậm chí còn ghi nhận tỷ lệ sinh non và thai lưu giảm ở các trường hợp đã tiêm phòng, có thể là nhờ việc ngăn ngừa các biến chứng do nhiễm virus gây ra. Mặc dù mục tiêu chính của việc tiêm phòng là để bảo vệ thai phụ khỏi bệnh nặng trong thai kỳ, nhưng ngày càng có nhiều nhận thức rằng việc bảo vệ trẻ sơ sinh cũng là một lợi ích quan trọng.
Các thử nghiệm ngẫu nhiên có đối chứng được thực hiện tại các quốc gia thu nhập thấp đã nhất quán cho thấy rằng tiêm vaccin cúm trong thai kỳ có hiệu quả 56% trong việc ngăn ngừa nhiễm virus cúm đã được xét nghiệm xác nhận ở trẻ dưới 2 tháng tuổi và hiệu quả 35% ở trẻ dưới 6 tháng tuổi. Tại các quốc gia thu nhập cao, các nghiên cứu quan sát cho thấy việc tiêm vaccin cúm mùa trong thai kỳ có hiệu quả từ 41% đến 71% trong việc ngăn ngừa nhiễm cúm được xét nghiệm xác nhận ở trẻ sơ sinh, và hiệu quả từ 39% đến 92% trong việc ngăn ngừa nhập viện do cúm. Đối với vaccin Covid-19, hiệu quả tiêm trong thai kỳ dao động từ 21% đến 84% trong việc ngăn ngừa nhiễm covid ở trẻ sơ sinh, và từ 32% đến 95% ngăn ngừa nhập viện do Covid-19 ở trẻ. Các loại vaccin được điều chỉnh phù hợp với biến thể virus đang lưu hành và được tiêm sau tuần 20 của thai kỳ cho thấy hiệu quả bảo vệ cao nhất.
Hiệu quả bảo vệ rõ rệt này, cùng với bằng chứng cho thấy trẻ sơ sinh đặc biệt dễ bị tổn thương bởi cúm và covid-19, đã làm dấy lên lời kêu gọi điều chỉnh lịch tiêm chủng nhằm tối đa hóa khả năng bảo vệ cho trẻ sơ sinh, thay vì chỉ tập trung vào mẹ và thai nhi trong thời kỳ mang thai. Việc tiêm vaccin cúm trong thai kỳ hiện được triển khai rộng rãi dưới hình thức chiến dịch tiêm phòng theo mùa, trước các đợt dịch virus cúm được dự đoán xảy ra vào mùa đông. Vaccin covid-19 cũng từng được triển khai tại Anh dưới dạng chiến dịch theo mùa (trước mùa xuân năm 2025) hoặc tại Mỹ khi có vaccin phù hợp với biên thê mới. Để tối ưu hóa khả năng bảo vệ cho trẻ sơ sinh, các mũi tiêm nhắc lại có thể được lên lịch trong khung thời gian tương tự như tiêm phòng ho gà trong thai kỳ. Theo hiểu biết hiện tại, vẫn chưa có kế hoạch chính thức để thực hiện thay đổi này, tuy nhiên tại Mỹ đã có khuyên cáo cập nhật rằng việc tiêm vào mùa hè trong tam cá nguyệt thứ ba có thể được cân nhắc nhằm tăng cường bảo vệ cho trẻ sơ sinh. Cùng với việc cơ quan quản lý dược phẩm tại Úc gần đây đã cấp phép cho vaccin cúm sử dụng trong thai kỳ với mục đích bảo vệ trẻ sơ sinh, những động thái này cho thấy một số quốc gia có thể sẽ cân nhắc thay đổi chiến lược tiêm chủng trong tương lai gần.
Tiêm vaccin viêm gan B ngay sau sinh
Virus viêm gan B có thể gây nhiễm trùng cấp tính hoặc mãn tính, và có tới 85-90% trẻ sơ sinh được sinh ra từ các bà mẹ dương tính với kháng nguyên HBV sẽ phát triển tình trạng nhiễm trùng mạn tính, khiến các em có nguy cơ bị xơ gan, suy gan và ung thư gan. Do lây truyền trong thời kỳ chu sinh là một trong những con đường chính lây lan HBV trên toàn cầu, việc phòng ngừa con đường này là điều thiết yêu nêu WHO muốn đạt được mục tiêu loại trừ HBV vào năm 2030.
Hiện có rất ít bằng chứng cho thấy việc truyên kháng thể thụ động chống HBV qua nhau thai có thể bảo vệ trẻ sơ sinh khỏi nhiễm virus. Ngược lại, việc tiêm vaccin HBV cho trẻ ngay sau sinh giúp giảm 73% nguy cơ nhiễm HBV ở trẻ sơ sinh. Khi kết hợp giữa tiêm vaccin HBV và miễn dịch thụ động với globulin miễn dịch chống lại HBV, hiệu quả bảo vệ tăng lên đến 92%. Không có mối lo ngại nào về tính an toàn của việc tiêm vaccin HBV ngay sau sinh, cả trong thử nghiệm lâm sàng lẫn trong dữ liệu theo dõi hậu tiêm chủng.
Do đó, WHO khuyến nghị tiêm vaccin HBV cho tất cả trẻ sơ sinh ngay sau sinh. Gần như tất cả các quốc gia ở châu Mỹ và châu Á đã áp dụng khuyến nghị này, trong khi nhiêu quốc gia châu Âu – bao gồm cả Vương quốc Anh – lại thực hiện sàng lọc HBV trong thai kỳ và chỉ tiêm chủng cho các trẻ sơ sinh có nguy cơ, còn phần lớn trẻ khác sẽ được tiêm vaccin có thành phần HBV trong lịch tiêm chủng định kỳ sau sinh. Tuy nhiên, sự thành công của chiến lược sàng lọc và chọn lọc này phụ thuộc rất lớn vào khả năng phát hiện phần lớn các ca nhiễm HBV ở phụ nữ mang thai điều mà ngay cả ở các quốc gia có thu nhập cao cũng không phải lúc nào cũng thực hiện được.
Tiêm phòng lao và bại liệt ở các khu vực lưu hành dịch
Bệnh lao và bệnh bại liệt là những nguyên nhân chính gây tử vong ở trẻ sơ sinh và trẻ nhỏ tại các quốc gia nơi các bệnh này vẫn đang lưu hành. Do đó, WHO khuyến nghị chủng ngừa bại liệt càng sớm càng tốt sau sinh ở Afghanistan và Pakistan, và tiêm phòng lao ở hầu hết các quốc gia thuộc khu vực cận Sahara, châu Phi, Nam Á và Đông Nam Á. Hiện tại, vaccin duy nhất phòng lao là vaccin BCG. Vì là vaccin sống giảm độc lực, BCG bị chống chỉ định trong thai kỳ, do đó chiến lược tiêm phòng lao trong thai kỳ hiện chưa thể áp dụng.
Mỗi liều vaccin BCG tiêm cho trẻ sơ sinh có hiệu quả khoảng 80% trong việc bảo vệ trẻ dưới 5 tuổi khỏi tử vong do bệnh lao. Một liều bổ sung vaccin bại liệt uống ngay sau sinh cũng được khuyến nghị, vì nó giúp tăng tỷ lệ chuyển đổi huyết thanh sau khi hoàn thành ba liêu trong lịch tiêm chủng cho trẻ nhỏ – vốn không đủ để bảo vệ trẻ trước bệnh bại liệt tại các khu vực lưu hành virus. Vì cả vaccin BCG và vaccin bại liệt uống đều là vaccin sống giảm độc lực, chúng có khả năng gây bệnh, đặc biệt ở những trẻ bị suy giảm miễn dịch. Tại Anh, vaccin BCG chỉ được khuyến cáo tiêm cho trẻ sơ sinh có nguy cơ, và ở các khu vực có chương trình tầm soát suy giảm miễn dịch kết hợp (SCID), việc tiêm BCG sẽ được trì hoãn cho đến khi có kết quả xét nghiệm.
Nguy cơ gây hại tiêm ân từ vaccin BCG, cùng với hiệu quả bảo vệ tương đối thấp của nó, khiến cho việc phát triển một loại vaccin lao mới trở thành ưu tiên hàng đầu. Đối với vaccin bại liệt uống, chủng ngừa ngay sau sinh được cho là giúp nguy cơ mắc bệnh liên quan đến vaccin, vì trẻ sơ sinh vẫn còn được bảo vệ phần nào nhờ kháng thể từ mẹ.
Các chương trình mới nổi nhằm bảo vệ chống lại RSV
Virus hợp bào hô hấp (RSV) là nguyên nhân hàng đầu gây nhiễm trùng đường hô hấp dưới cấp tính ở trẻ nhỏ. Trên toàn cầu vào năm 2019, ước tính có khoảng 33 triệu ca LRTI liên quan đến RSV ở trẻ dưới 5 tuổi, trong đó 95% ca bệnh và 97% trong số 100.000 ca tử vong xảy ra tại các quốc gia có thu nhập thấp và trung bình. Ở các quốc gia có thu nhập cao, RSV là nguyên nhân chính gây nhập viện và là một vấn đề lớn trong việc sử dụng nguồn lực y tê. Trẻ sơ sinh nhỏ tuổi bị ảnh hưởng nặng nề do bệnh nặng, với tỷ lệ nhập viện cao nhất rơi vào nhóm trẻ từ 28 ngày đến 3 tháng tuổi. Trẻ sinh non chiếm khoảng 25% số ca nhập viện do nhiễm trùng đường hô hấp dưới liên quan đến RSV.
Vì vậy, việc phát triển các chiến lược phòng ngừa an toàn, hiệu quả và hợp túi tiền để giảm tỷ lệ bệnh tật và tỷ lệ tử vong liên quan đến RSV – bao gồm cả ở trẻ đẻ non – là một vấn đề ưu tiên toàn cầu. Gần đây, các chiến lược như tiêm vaccin trong thai kỳ và tiêm phòng phổ cập cho trẻ sơ sinh bằng kháng thể đơn dòng của RSV đã được triển khai. Cả hai chiến lược này đều nhằm bảo vệ trẻ sơ sinh và trẻ nhỏ trong mùa RSV đầu tiên trong đời bằng cách trì hoãn lân nhiễm RSV đầu tiên cho đến khi trẻ lớn hơn – khi mà thời điểm nguy cơ mắc bệnh nặng thấp hơn.
Tiêm vaccin RSV trong thai kỳ
Một loại vaccin sử dụng protein RSV prefusion F (RSV pre-F) vừa mới được phát triển đề tiêm phòng trong thai kỳ và hiện đã được cấp phép sử dụng tại nhiều quốc gia dưới tên thương mại Abrysvo. Trong một thử nghiệm lâm sàng pha III, loại vaccin này cho thấy hiệu quả 81.8% trong ngăn ngừa LRTI nặng liên quan đến RSV ở trẻ sơ sinh dưới 90 ngày tuổi và 69.4% ở trẻ dưới 180 ngày tuổi. Việc tiêm vaccin Abrysvo trong thai kỳ đã được triển khai như một chương trình theo mùa tại Argentina và Hoa Kỳ từ năm 2023 và như một chương trình quanh năm tại Anh từ năm 2024. Đáng lưu ý, trong thử nghiệm pha III của Abrysvo có ghi nhận sự chênh lệch không có ý nghĩa thống kê về tỷ lệ sinh non – nhưng không làm gia tăng tỷ lệ tử vong liên quan – tại Nam Phi và Brazil, trong khi hiện tượng này không xảy ra ở các quốc gia thu nhập cao. Dấu hiệu này đã được đánh giá cân trọng trong quá trình cấp phép, đặc biệt là trong bối cảnh thử nghiệm pha III khác về vaccin RSV pre-F đã bị dùng vào tháng 2 năm 2022 do ghi nhận sự khác biệt đáng kể về tỷ lệ sinh non giữa nhóm tiêm vaccin và nhóm dùng giả dược. Hiện tượng này chủ yếu xuất hiện trong một giai đoạn cụ thể tại các quốc gia có thu nhập thấp và trung bình. Dấu hiệu này có thể phản ánh các đặc điểm dịch tễ học đặc trưng của các khu vực thu nhập thấp, nhưng sự khác biệt về tiêu chuẩn chăm sóc trước sinh giữa các địa điểm nghiên cứu cũng có thể là một yếu tố góp phần. Khoảng thời gian giữa tiêm vaccin và sinh nở là tương tự giữa các nhóm, và không ghi nhận sự chênh lệch về tỷ lệ sinh non trong nhóm thai kỳ nguy cơ cao trong thử nghiệm pha III.
Việc không ghi nhận tín hiệu bất thường nào ở các quốc gia thu nhập cao cho thấy lợi ích của việc tiêm vaccin RSV trong thai kỳ vượt trội hơn rủi ro ở những quốc gia này. Tuy nhiên, để đảm bảo niêm tin vào chương trình tiêm chủng, tỷ lệ sinh non đang được theo dõi chặt chẽ. Dữ liệu mới từ Hoa Kỳ cho thấy tỷ lệ sinh non sau khi tiêm vaccin RSV phù hợp với tỷ lệ sinh non trước đó. Để giảm thiểu nguy cơ tiềm ẩn của việc đẻ non, Hoa Kỳ đã chọn chỉ tiêm vaccin RSV sau tuần thai thứ 32. Argentina cũng tiêm từ 32 tuần và ở Anh là từ 28 tuần. Điều này có nghĩa là những trẻ sinh cực non – tức là sinh trước thời điểm vaccin có thể được tiêm – sẽ không nhận được kháng thể IgG đặc hiệu RSV từ mẹ truyền qua nhau thai, nhưng vẫn có thể được hưởng lợi từ việc gián đoạn lây truyền RSV và kháng thể đặc hiệu RSV truyền qua sữa mẹ.
Việc triển khai tiêm chủng theo mùa ở Hoa Kỳ và Argentina còn giới hạn thêm khả năng hưởng lợi, vì những thai phụ có thai ngoài khoảng thời gian được chỉ định trong mùa sẽ không được đề nghị tiêm vaccin RSV. Hiện tại một loại vaccin mRNA (mRNA-1345, do Moderna phát triển) mã hóa protein pre-F đã được ổn định đang trong giai đoạn thử nghiệm lâm sàng pha III ở thai phụ trên toàn cầu và vừa được cấp phép cho các chỉ định khác.
Miễn dịch thụ động chống lại RSV ngay sau sinh
Từ những năm 1990, việc tiêm hàng tháng palivizumab – một kháng thể đơn dòng kháng protein F của RSV – trong mùa RSV đã được khuyến nghị cho những trẻ sơ sinh có nguy cơ cao nhất mắc RSV bệnh nặng tại các quốc gia thu nhập cao. Sự ra đời gần đây của nirsevimab, một kháng thể đơn dòng chống lại RSV có tác dụng kéo dài (với thời gian bán hủy lên đến 79 ngày và chỉ cần một liều tiêm bắp duy nhất), đã tạo nên bước đột phá và cho phép triển khai rộng rãi miễn dịch thụ động để bảo vệ trẻ sơ sinh tại châu Âu và Bắc Mỹ. Trong nghiên cứu pha III, nirsevimab (hiện được cấp phép với tên thương mại là Beyfortus) cho thấy hiệu quả phòng LRTI liên quan đến RSV cần chăm sóc y tê lên đến 150 ngày, 74.5% hiệu quả ở trẻ đủ tháng và trẻ non muộn (> 35 tuần thai), 70.1% hiệu quả ở trẻ sinh non từ 29 tuần đến dưới 35 tuần.
Kể từ khi được cấp phép và triển khai, nirsevimab đã cho thấy hiệu quả vượt trội với độ bao phủ ấn tượng ở nhiều quốc gia. Tại Tây Ban Nha, sau khi chương trình tiêm chủng phố biên cho trẻ sơ sinh được áp dụng từ tháng 9/2023, tỷ lệ bao phủ đạt từ 78.7% đên 98.6% tại ba khu vực, với hiệu quả 70.2% trong việc ngăn ngừa nhập viện do RSV-LRTI. Các nghiên cứu tiếp theo tại khu vực Galicia (Tây Ban Nha) và Pháp cho thấy rằng cân 25 đến 39 trẻ sơ sinh được miễn dịch thụ động để ngăn ngừa một ca nhập viện vì RSV, thể hiện tính hiệu quả về mặt chi phí và tác động y tế. Tại Luxembourg, năm 2023 – nơi tỷ lệ bao phủ đạt 84% – độ tuổi trung bình khi nhập viện vì RSV tăng từ 7.8 lên 14.4 tháng, trong khi thời gian nằm viện ở trẻ dưới 6 tháng giảm từ 5.6 xuống còn 3.4 ngày, cho thấy bệnh nhẹ hơn. Tại Pháp, dữ liệu thực tế tiếp tục xác nhận kết quả thử nghiệm lâm sàng pha III, với hiệu quả 75.9% trong việc giảm ca nặng cân hồi sức. Trong khi đó, tại Mỹ, tỷ lệ bao phủ trong mạng lưới giám sát vaccin chỉ đạt 4-12% nhưng trong số trẻ đã tiêm, hiệu quả ngăn ngừa nhập viện do RSV vẫn rất cao, đạt 90%. Điều này cho thấy tiềm năng lớn của nirsevimab nêu được triển khai rộng rãi hơn tại các quốc gia có tỷ lệ bao phủ còn thấp.
Việc sử dụng kháng thể đơn dòng chống lại RSV cho trẻ sơ sinh là một chiến lược rất hấp dẫn nhằm bảo vệ trẻ trong 6 tháng đầu đời, đặc biệt là ở những nhóm dân cư còn do dự với tiêm chủng khi mang thai. Tuy nhiên, tại hầu hết các quốc gia, lựa chọn không thuộc về gia đình mà được quyết định ở cấp quốc gia, tùy theo chiến lược y tế công cộng. Thêm vào đó, chi phí cao của kháng thể đơn dòng hiện tại là rào cản lớn khiên chiến lược này chưa thể triển khai rộng rãi trên toàn cầu. Tuy nhiên, việc cấp phép thêm các kháng thể đơn dòng RSV có tác dụng kéo dài sẽ giúp cải thiện nguồn cung, tăng tính bền vững và có thể giảm chi phí trong tương lai. Trong số này, clesrovimab, một kháng thể nhằm vào vị trí khác trên protein F của RSV, hiện đang gần hoàn thành thử nghiệm lâm sàng pha III, mở ra triển vọng tăng cường khả năng tiếp cận miễn dịch thụ động cho trẻ sơ sinh trên toàn thế giới.
TÀI LIỆU THAM KHẢO
- Male V, Jones CE. Tiêm chủng trong thai kỳ để bảo vệ trẻ sơ sinh. Nat Rev Immunol. 23 tháng 4 năm 2025. doi: 10.1038/s41577-025-01162-5. Bản điện tử trước khi in. PMID: 40269273.