Tổng số phụ: 240,000₫
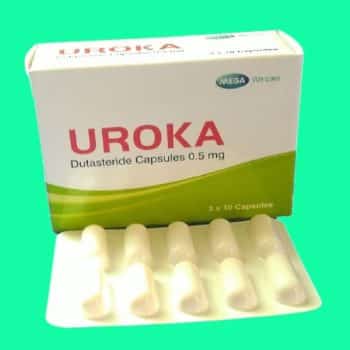
UROKA 0.5mg
Thuốc kê đơn
Thuốc UROKA 0.5mg là thuốc chứa hoạt chất dutasteride hàml ượng 0.5mg, được dùng để cải thiện triệu chứng và hạn chế tiến triển của bệnh tăng sản lành tính tuyến tiền liệt.
Hàm lượng 0,5mg
Dạng bào chế Viên nang mềm
Số đăng ký 885110169700
Số quyết định 06/QĐ-QLD
Năm cấp 07/12/2024
Đợt cấp 122 bổ sung
Xuất xứ Thái Lan
Quy cách đóng gói Hộp 3 vỉ x 10 viên
Hạn sử dụng 48 tháng
Trong bài viết này, dược sĩ Lưu Văn Hoàng giới thiệu đến các bạn thuốc UROKA 0.5mg được sản xuất bởi Mega Lifesciences Public Company Limited có số đăng ký lưu hành tại Việt Nam là 885110169700
UROKA 0.5mg là thuốc gì?
Thành phần
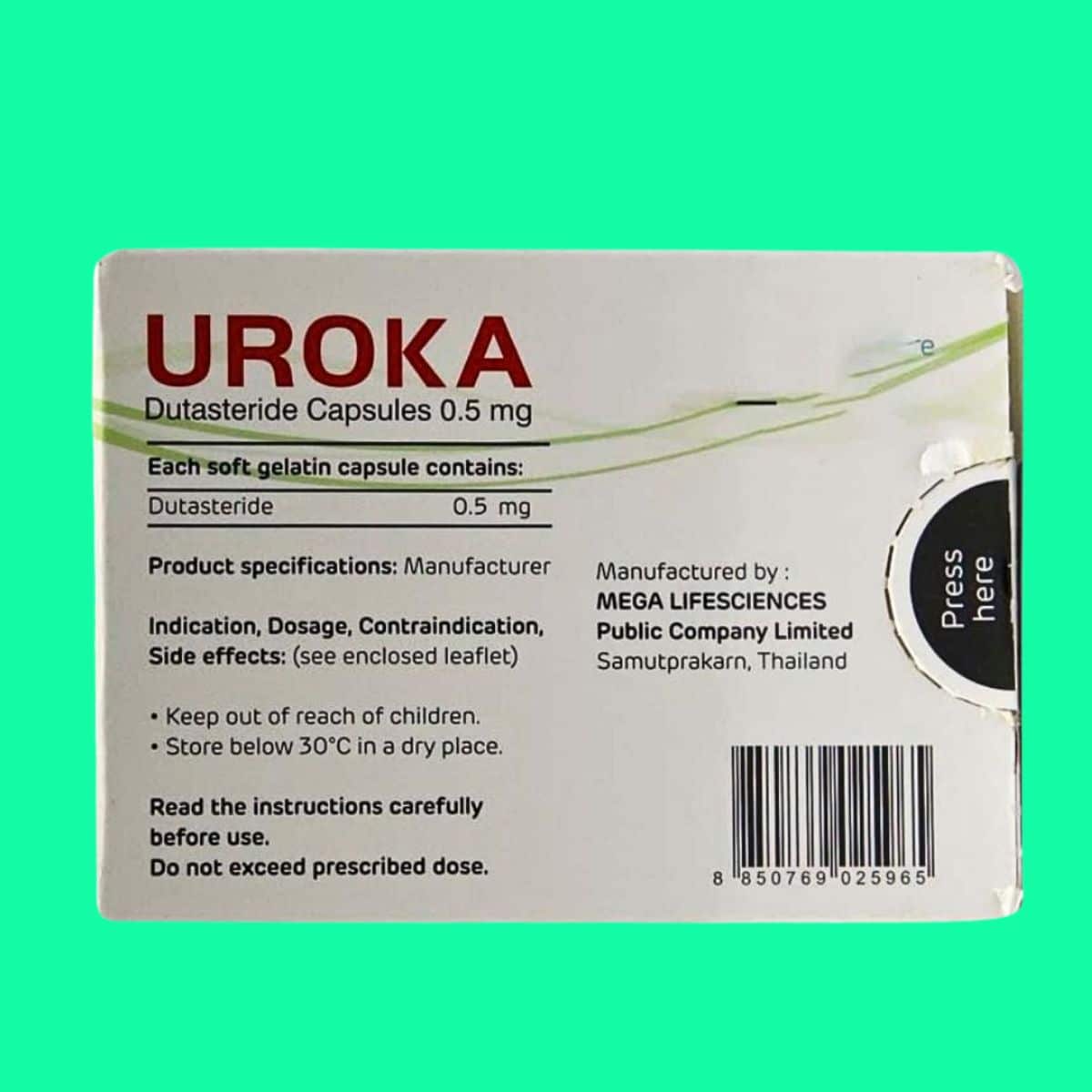
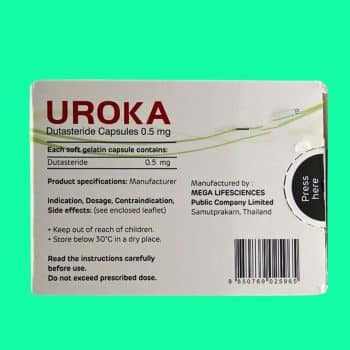
Trong mỗi viên uống UROKA 0.5mg có chứa:
- Dược chất: Dutasteride………………0.5mg
- Tá dược: Capmul MCM NF, butylated hydroxytoluene, gelatin, glycerin, nước tinh khiết, titanium dioxide, oxide sắt vàng.
Dạng bào chế: Viên nang mềm
Trình bày
SĐK: 885110169700
Quy cách đóng gói: Hộp 3 vỉ x 10 viên
Xuất xứ: Thái Lan
Hạn sử dụng: 48 tháng
Tác dụng của thuốc UROKA 0.5mg
Cơ chế tác dụng
Dutasteride ức chế đồng thời hai isoenzym 5-alpha-reductase loại 1 và loại 2, là các enzym biến đổi testosterone thành dihydrotestosterone (DHT). Vì DHT là androgen chủ yếu thúc đẩy sự phát triển mô tuyến tiền liệt, việc ức chế tổng hợp DHT dẫn đến giảm kích thước tuyến và cải thiện các triệu chứng liên quan.
Đặc điểm dược động học
Hấp thu: Sau liều uống 0,5 mg, dutasteride đạt nồng độ đỉnh trong huyết thanh trong khoảng 1–3 giờ; sinh khả dụng xấp xỉ 60% so với đường tĩnh mạch và không bị ảnh hưởng bởi thức ăn.
Phân bố: Thuốc phân bố rộng (thể tích phân bố ~300–500 lít) và gắn mạnh vào protein huyết tương (>99,5%). Khi dùng hàng ngày, nồng độ huyết thanh đạt khoảng 65% mức cân bằng sau 1 tháng và gần 90% sau 3 tháng; mức ổn định hoàn chỉnh đạt sau khoảng 6 tháng. Nồng độ trong dịch tuyến cũng đạt trạng thái ổn định tương tự; sau 52 tuần trung bình đo được khoảng 3,4 ng/ml.
Chuyển hóa: Dutasteride chủ yếu được chuyển hóa bởi CYP3A4 thành một số chất chuyển hóa hydroxyl và dihydro; nhiều chất chuyển hóa chính và phụ đã được phát hiện trong huyết thanh.
Thải trừ: Thuốc UROKA 0.5mg được thải chủ yếu qua phân dưới dạng chất chuyển hóa; lượng thuốc dạng không đổi bài tiết qua phân chiếm phần trăm nhỏ. Lượng rất nhỏ (<0,1% liều) xuất hiện trong nước tiểu. Thời gian bán thải cuối cùng kéo dài khoảng 3–5 tuần, và nồng độ có thể vẫn phát hiện được trong huyết thanh trong 4–6 tháng sau khi ngừng dùng.
Thuốc UROKA 0.5mg được chỉ định trong bệnh gì?
UROKA (dutasteride 0,5 mg) được sử dụng để điều trị và ngăn chặn tiến triển của phì đại lành tính tuyến tiền liệt (BPH) bằng cách giảm triệu chứng, thu nhỏ thể tích tuyến, cải thiện dòng tiểu, giảm nguy cơ bí tiểu cấp và làm giảm nhu cầu can thiệp phẫu thuật.
Dutasteride cũng có thể được dùng phối hợp với tamsulosin (thuốc chẹn alpha) để đạt hiệu quả trong việc giảm kích thước tuyến và cải thiện triệu chứng.
Liều dùng và cách sử dụng
Liều dùng
Người lớn, bao gồm người cao tuổi: 1 viên UROKA 0,5 mg mỗi ngày.
Có thể cần dùng UROKA liên tục tối thiểu 6 tháng để đánh giá đáp ứng điều trị
Dùng đơn trị hoặc phối hợp tamsulosin 0,4 mg trong điều trị BPH.
Không cần chỉnh liều dùng UROKA với bệnh nhân suy thận, nhưng cần thận trọng với người suy gan do chưa có minh chứng về an toàn hiệu quả
Cách sử dụng
Viên UROKA 0.5mg được dùng bằng đường uống, không cắn, nhai hoặc mở nang để tránh kích ứng niêm mạc miệng – hầu họng
Dùng được bất cứ lúc nào trong ngày tuỳ thuộc lịch trình phù hợp của người bệnh
Không sử dụng thuốc UROKA 0.5mg trong trường hợp nào?
Người dị ứng với dutasteride, các thuốc ức chế 5-alpha-reductase khác hoặc bất kỳ thành phần nào có trong UROKA 0.5mg
Phụ nữ
Trẻ em

Lưu ý đặc biệt khi sử dụng thuốc
Thận trọng
Cần theo dõi nguy cơ ung thư tuyến tiền liệt trước và trong quá trình điều trị.
Cần thiết lập giá trị PSA nền mới sau 6 tháng điều trị và theo dõi định kỳ; bất kỳ tăng PSA nào so với mức thấp nhất khi đang điều trị cần được đánh giá kỹ lưỡng.
Mặc dù chưa xác định mối quan hệ nhân quả rõ ràng giữa dutasteride (đơn trị hay phối hợp) và suy tim, cần theo dõi các biểu hiện tim mạch.
Bệnh nhân nên báo cáo kịp thời mọi thay đổi ở mô vú như khối u hoặc tiết dịch ở núm khi dùng thuốc
Vì dutasteride có thể hấp thu qua da, phụ nữ và trẻ em cần tránh tiếp xúc với viên nang bị hỏng; nếu tiếp xúc xảy ra, rửa sạch da bằng xà phòng và nước ngay lập tức.
Do thuốc chuyển hóa rộng và có thời gian bán thải dài, cần thận trọng khi sử dụng ở bệnh nhân có rối loạn chức năng gan.
Tác dụng phụ
Các khảo sát lâm sàng cho thấy một số rối loạn liên quan đến chức năng sinh dục gặp nhiều hơn ở người dùng dutasteride, chẳng hạn như giảm khả năng cương, giảm nhu cầu tình dục, thay đổi xuất tinh, cùng với hiện tượng đau hoặc tăng kích thước mô vú ở nam. Những biểu hiện này đôi khi vẫn tồn tại sau khi ngừng thuốc, nhưng mức độ ảnh hưởng thực sự của dutasteride đối với tình trạng kéo dài này vẫn chưa được xác định.
Dữ liệu hậu mãi ghi nhận thêm vài phản ứng ít gặp: dị ứng (phát ban, mề đay, phù mạch), thay đổi khí sắc hướng trầm cảm, rụng lông hoặc tăng lông ở một số vùng, cùng với đau hay sưng tinh hoàn. Khi xuất hiện bất kỳ dấu hiệu bất thường nào, người dùng cần liên hệ cơ sở y tế.
Tương tác
Dutasteride được chuyển hóa chủ yếu qua CYP3A4, vì vậy thuốc có thể tăng nồng độ trong huyết tương nếu dùng đồng thời với các thuốc ức chế enzym này. Một số dữ liệu cho thấy khả năng thải trừ giảm khi phối hợp với verapamil hoặc diltiazem, nhưng sự thay đổi này hiếm khi gây hệ quả lâm sàng nhờ phạm vi an toàn của thuốc khá rộng.
Nhiều thử nghiệm in vitro cho thấy dutasteride không phụ thuộc vào các isoenzym CYP khác và cũng không tranh chấp đáng kể với các thuốc liên kết mạnh với protein huyết tương. Các nghiên cứu trên người với tamsulosin, terazosin, warfarin, digoxin hay cholestyramine đều không ghi nhận biến đổi quan trọng về dược lực hoặc dược động học.
Trong các nghiên cứu lớn, đa số người bệnh dùng đồng thời nhiều loại thuốc nhưng không xuất hiện tương tác đáng kể với các thuốc hạ lipid máu, ACEI, thuốc chẹn beta, chẹn kênh canxi, thuốc lợi tiểu, corticosteroid, NSAID, PDE5i hay fluoroquinolon. Do chưa có dữ liệu về tương kỵ, thuốc không được pha trộn chung với chế phẩm khác.
Lưu ý cho phụ nữ có thai và cho con bú
Thuốc UROKA 0.5mg không dùng cho phụ nữ. Các dữ liệu tiền lâm sàng cho thấy việc làm giảm nồng độ DHT do dutasteride có thể gây ảnh hưởng đến sự hình thành cơ quan sinh dục ngoài của thai nam nếu mẹ phơi nhiễm. Chưa rõ thuốc có tiết vào sữa mẹ hay không.
Lưu ý khi sử dụng cho người lái xe và vận hành máy móc
Dutasteride không làm suy giảm hay thay đổi khả năng làm việc với máy móc hoặc điều khiển phương tiện.
Quá liều và xử trí
Trong thử nghiệm trên người tình nguyện, việc dùng liều rất cao trong thời gian ngắn không tạo ra mối lo ngại đặc biệt về an toàn. Ở các nghiên cứu lâm sàng, dùng liều cao hơn liều thường quy trong nhiều tháng cũng không làm phát sinh thêm các phản ứng ngoài những tác dụng đã biết ở liều điều trị. Không có thuốc giải độc UROKA đặc hiệu; khi nghi ngờ quá liều, cần xử trí hỗ trợ và điều trị triệu chứng.
Bảo quản
Giữ UROKA 0.5mg ở nơi khô ráo, thoáng mát (<30℃), tránh ánh nắng quá mạnh từ mặt trời
Không để UROKA 0.5mg trong tầm với trẻ em
Không sử dụng UROKA 0.5mg khi quá hạn cho phép
Sản phẩm tương tự
Quý khách có thể tham khảo các sản phẩm khác của nhà thuốc có cùng hoạt chất và tác dụng với UROKA 0.5mg như:
Dutasvitae 0.5mg có thành phần chính là Dutasvitae 0.5mg, được sản xuất bởi CYNDEA PHARMA, S.L-Tây Ban Nha, điều tị bệnh lý tuyến tiền liệt
Avodart có thành phần chính là Dutasvitae 0.5mg, được sản xuất bởi GlaxoSmithKline Pharmaceuticals SA – BA LAN, S.L-Tây Ban Nha, điều tị bệnh lý tuyến tiền liệt
Tài liệu tham khảo
- Tờ Hướng dẫn sử dụng thuốc UROKA 0.5mg được Bộ Y tế phê duyệt. Xem và tải về bản PDF đầy đủ tại đây. Truy cập ngày 19 tháng 11 năm 2025
- Eun HC, Kwon OS, Yeon JH, Shin HS, Kim BY, Ro BI, Cho HK, Sim WY, Lew BL, Lee WS, Park HY, Hong SP, Ji JH (2010). Efficacy, safety, and tolerability of dutasteride 0.5 mg once daily in male patients with male pattern hair loss: a randomized, double-blind, placebo-controlled, phase III study. J Am Acad Dermatol. Truy cập ngày 19 tháng 11 năm 2025 từ: https://pubmed.ncbi.nlm.nih.gov/20605255/

 Acid Trichloracetic 80
Acid Trichloracetic 80 












Cường Nguyễn –
bài viết chi tiết, đọc dễ hiều