Y tế - Sức Khỏe
TỰ DỊ ỨNG (AUTOALLERGY) VÀ NHỮNG ĐIỀU BÁC SĨ DỊ ỨNG CẦN BIẾT
Lượt dịch: NT ΗΝ
TỔNG QUAN
Hen suyễn, viêm da cơ địa (AD), mày đay mạn tính (CU) và dị ứng thức ăn là những rối loạn miễn dịch thường gặp nhất được các bác sĩ chuyên khoa dị ứng điều trị. Hen suyễn là bệnh đường hô hấp dưới, đặc trưng với các triệu chứng như ho, khò khè, khó thở và tăng phản ứng phế quản. Nhiều kiểu hình nội tại (endotype) của hen suyễn đã được mô tả, bao gồm hen suyễn Th2-cao, đặc trưng nồng độ cao các cytokine type 2 và tình trạng viêm đường thở do bạch cầu ái toan, và hen suyễn Th2-thấp liên quan đến viêm do bạch cầu trung tính hoặc tình trạng viêm ít bạch cầu hạt. Viêm da cơ địa (AD) là một bênh viêm da mạn tính thường gặp, đặc trưng với ngứa, đỏ và khô da. Nguyên nhân của AD mang tính đa yếu tố, bao gồm các yếu tố kích thích từ môi trường, khuynh hướng di truyền, hàng rào bảo vệ da bị suy yếu và sự rối loạn điều hòa của hệ miễn dịch. Tương tự như hen suyễn, AD cũng có các cơ chế sinh lý bệnh khác nhau; tuy nhiên, việc xác định các endotype có tính tái lập ổn định vẫn còn nhiều thách thức. Mày đay mạn tính, một rối loạn viêm da do tế bào mast chi phối, đặc trưng với sẩn ngứa, phù mạch hoặc cả hai, tái phát kéo dài hơn 6 tuần. CSU có thể được phân loại thành mày đay mạn tính tự phát và mày đay mạn tính có yếu tố thúc đẩy (ClndU), trong đó CSU xảy ra khi không xác định được các kích thích vật lý hoặc môi trường cụ thể. Trong những năm gần đây, các tiến bộ trong nghiên cứu miễn dịch học đã cho thấy tự miễn đóng vai trò trung tâm trong cơ chế bệnh sinh của CSU. Dị ứng thức ăn là các phản ứng miễn dịch bất thường được kích hoạt khi tiếp xúc với những loại thực phẩm nhất định và theo định nghĩa cổ điển là các phản ứng quá mẫn qua trung gian IgE. Tuy nhiên, những tiến bộ gần đây, vídụ như trong các công cụ chẩn đoán, đã đưa ra các đề xuất về endotype dị ứng thực phẩm khác nhau.
Ảnh hưởng đến khoảng 30-40% dân số toàn cầu, các bệnh lý này đang ngày càng trở nên phổ biến và phức tạp hơn, thường liên quan đến nhiều yếu tố khởi phát và các kiểu hình bệnh chồng lấp. Trong khi trước đây chúng thường được xem là các rối loạn quá mẫn với kháng nguyên ngoại sinh (dị ứng), các nghiên cứu gần đây cho thấy một số bệnh cũng có thể liên quan đến đáp ứng miễn dịch chống lại chính kháng nguyên của cơ thể, hiện tượng được gọi là tự dị ứng (autoallergy). Khái niệm này nằm ở giao điểm giữa dị ứng và tự miễn, nhưng vẫn chưa được nhận biết đầy đủ trong thực hành lâm sàng hàng ngày. Trong bài viết này, chúng tôi cung cấp cho bác sĩ dị ứng một góc nhìn tổng quan ngắn gọn và có giá trị lâm sàng về tự dị ứng thông qua việc trả lời 5 câu hỏi chính trong bảng 1: (1) Tự dị ứng là gì và khác gì so với dị ứng cổ điển? (2) Tự dị ứng phổ biến đến mức nào? (3) Tự dị ứng có ý nghĩa lâm sàng hay không? (4) Làm thế nào để chẩn đoán tự dị ứng? (5) Tự dị ứng được điều trị như thế nào? Trong bài viết này chúng tôi tập trung vào hen, viêm da cơ địa, mày đay mạn tính và dị ứng thức ăn.
TỰ DỊ ỨNG LÀ GÌ VÀ KHÁC GÌ SO VỚI DỊ ỨNG CỔ ĐIỂN?
IgE được biết là một yếu tố quan trọng trong phản ứng quá mẫn type 1. Dị ứng cổ điển qua trung gian IgE liên quan đến phản ứng quá mẫn với các kháng nguyên môi trường (ngoại sinh) (ví dụ: phấn hoa và protein thực phẩm), trong đó các tế bào trình diện kháng nguyên trình diện dị nguyên cho tế bào T chưa biệt hóa. Các tế bào Th2 đã biệt hóa sau đó hoạt hóa tế bào B, khởi phát quá trình chuyển lớp kháng thể và sản xuất IgE. IgE có thể gắn lên các tế bào hiệu ứng như basophil và mast cell thông qua thụ thể ái lực cao FcERI. Khi cơ thể tiếp xúc lại với dị nguyên, dị nguyên sẽ liên kết chéo các phân tử IgE trên bề mặt mast cell và basophil, gây giải phóng các hạt và histamine, leukotriene và các cytokine.
Các bằng chứng ngày càng cho thấy IgE ngoài việc nhận diện kháng nguyên ngoại sinh, còn có thể nhắm vào các kháng nguyên của chính cơ thể, gây phản ứng tự miễn được gọi là tự dị ứng hoặc tự miễn type 1. Trong tự dị ứng, hệ miễn dịch tạo ra tự kháng thể IgE chống lại kháng nguyên nội sinh (còn gọi là tự kháng nguyên hay autoantigen) hoặc tự dị nguyên (autoallergens), bao gồm thyroid peroxidase (TPO), interleukin-24 (IL-24), MnSOD, cùng với nhiều kháng nguyên khác. Tương tự như trong dị ứng cổ điển, dạng tự miễn này dẫn đến sự hoạt hóa của tế bào mast cell và basophils thông qua sự liên kết chéo của IgE gắn với thụ thể FcERI, từ đó gây phản ứng viêm và các biểu hiện lâm sàng như mày đay.
Bảng 1: Tóm tắt câu hỏi và câu trả lời
| Câu hỏi | Câu trả lời |
| Tự dị ứng là gì và khác gì so với dị ứng cổ điển? | Trong tự dị ứng, các kháng thể IgE được tạo ra chống lại các protein nội sinh của cơ thể (tự kháng nguyên – autoantigens). Các kháng thể này gắn lên thụ thể trên bề mặt tế bào mast và basophils, hoạt hóa chúng và gây ra các triệu chứng bệnh. Ngược lại, dị ứng cổ điển liên quan đến đáp ứng IgE đối với các dị nguyên ngoại sinh, như phấn hoa hoặc protein thực phẩm, mặc dù kiểu biểu hiện triệu chứng có thể như nhau. |
| Tự dị ứng phổ biến đến mức nào? | Tự dị ứng được cho là khá thường gặp, tuy nhiên tỷ lệ mắc có thể khác nhau đáng kể giữa các bệnh lý, các nhóm nghiên cứu và phương pháp phát hiện. |
| Tự dị ứng có ý nghĩa lâm sàng không? | Trong một số bệnh như viêm da cơ địa (AD) và mày đay mạn tính tự phát (CSU), sự hiện diện của tự kháng thể IgE có liên quan đến mức độ hoạt động bệnh cao hơn và nhiều bệnh đi kèm hơn. Tuy nhiên, các bằng chứng hiện nay chưa hoàn toàn nhất quán, và cần thêm nhiều nghiên cứu để làm rõ vấn đề này. |
| Làm thế nào để chẩn đoán tự dị ứng? | Tự dị ứng có thể được đánh giá bằng nhiều phương pháp nhằm phát hiện tự kháng thể IgE và/hoặc tự kháng nguyên, ví dụ: các xét nghiệm miễn dịch, protein microarrays, xét nghiệm chức năng (vídụ: test hoạt hóa basophil), test da. Tuy nhiên chưa có phương pháp nào hiện được thiết lập trong thực hành lâm sàng thường quy để phát hiện tự dị ứng. Vì vậy, việc phát triển các công cụ chẩn đoán tiêu chuẩn và được xác nhận lâm sàng vẫn là một nhu cầu cấp thiết. |
| Tự dị ứng được điều trị như thế nào? | Omalizumab, một kháng thể đơn dòng kháng IgE đã được phê duyệt để điều trị hen, mày đay tự phát mạn tính và dị ứng thức ăn. Các lựa chọn điều trị khác tập trung vào ức chế các cytokine quan trọng trong quá trình sản xuất IgE và hoạt hóa mast cell, bao gồm thuốc chẹn IL-4/IL-13 (dupilumab), thuốc ức chế BTK (remibrutinib), kháng thể kháng KIT làm giảm số lượng tế bào mast (barzolvolimab). |
Đáp ứng IgE chống lại các kháng nguyên nội sinh có thể phát sinh thông qua nhiều cơ chế miễn dịch khác nhau, ngày càng được ghi nhận trong các bệnh viêm mạn tính và bệnh tự miễn. Một trong những cơ chế này là molecular mimicry, trong đó các kháng nguyên ngoại sinh (như protein của vi sinh vật hoặc ký sinh trùng) có sự tương đồng về cấu trúc hoặc trình tự với các protein đặc hiệu của mô người hoặc các dị nguyên bên ngoài, từ đó gây đáp ứng IgE phản ứng chéo. Sanchez và cộng sự đề xuất rằng thyroid peroxidase (TPO) có thể tương đồng với các protein nội sinh của bạch cầu ái toan, như eosinophil peroxidase, từ đó có khả năng kích hoạt đáp ứng IgE tự phản ứng. Ngoài ra, phản ứng IgE với profilin của người, vốn là tự kháng nguyên IgE đầu tiên được xác định, đã được phát hiện ở những người dị ứng phấn hoa, gợi ý về hiện tượng molecular mimicry.
Một cơ chế góp phần khác là sự lan rộng epitope, trong đó phản ứng miễn dịch ban đầu chống lại một epitope dần dần mở rộng sang các epitope khác trên cùng một hoặc các tự kháng nguyên liên quan, từ đó làm tăng cường quá trình tự miễn và tự dị ứng. Ngoài ra, tái tổ hợp chuyển lớp kháng thể sang IgE tại chỗ có thể xảy ra trong các cấu trúc lympho bậc ba hình thành trong các mô bị viêm mạn tính như da. Những cấu trúc lympho này tạo ra vi môi trường chuyên biệt hỗ trợ sự hoạt hóa liên tục của tế bào B và quá trình chuyển lớp kháng thể ngay tại mô, cho phép sản xuất IgE chống lại các kháng nguyên của mô tại chỗ mà không phụ thuộc vào cơ quan miễn dịch trung ương. Sự sản xuất IgE tại chỗ như vậy cũng đã được đề xuất xảy ra ở các cơ quan hàng rào như biểu mô đường hô hấp và niêm mạc mũi, đặc biệt trong bệnh hen và viêm mũi dị ứng. Một mô hình được đề xuất của tự dị ứng (Hình 1) phản ánh chuỗi phản ứng quá mẫn typ 1 cổ điển, gồm giai đoạn mẫn cảm tiếp theo là giai đoạn hiệu ứng, nhưng có những khác biệt quan trọng về nguồn gốc của kháng nguyên.
Các xét nghiệm chức năng như test hoạt hóa basophil (BAT – Basophil activation test), cùng với các thử nghiệm như test lấy da (skin prick test) và passive transfer đã làm nổi bật vai trò của IgE tự phản ứng trong cơ chế bệnh sinh của hen suyễn, viêm da cơ địa, mày đay tự phát mạn tính và dị ứng thức ăn. Đáng chú ý, thí nghiệm chuyển thụ động IgE kháng TPO từ bệnh nhân CSU đã được chứng minh có thể gây phản ứng sân phủ ban đỏ trên da người khỏe mạnh. Kết quả này được minh họa trong nghiên cứu của Sanchez và cộng sự, qua đó càng cùng cố vai trò gây bệnh của IgE tự phản ứng trong CSU. Ví dụ, basophil từ các bệnh nhân hen dương tính với IgE kháng eosinophil cationic protein (ECP) và IgE kháng eosinophil peroxidase (EXP) cho thấy mức độ hoạt hóa phụ thuộc liều lượng khi được kích thích bằng tự kháng nguyên tương ứng. Tương tự, các xét nghiệm sử dụng tế bào leukemia bạch cầu ái kiềm của chuột cho thấy a-lactalbumin của người có thể kích thích giải phóng các chất trung gian gây dị ứng ở người bị dị ứng sữa đã được mẫn cảm trước đó.
TỰ DỊ ỨNG PHỔ BIẾN ĐẾN MỨC NÀO?
Hiện tượng tự dị ứng đã được phát hiện trong nhiều rối loạn qua trung gian miễn dịch khác nhau. Tuy nhiên, tỷ lệ hiện diện của IgE tự phản ứng thay đổi đáng kể tùy thuộc vào bệnh lý nền, tự dị nguyên cụ thể, đặc điểm của quần thể nghiên cứu, cũng như các phương pháp phát hiện được sửdụng. Bảng 2 cung cấp tổng quan về tính tự phản ứng của IgE trong các bệnh đã được báo cáo, bao gồm thông tin về các tự kháng nguyên đã được xác định, tỷ lệ hiện mắc và các kỹ thuật phát hiện.
Các nghiên cứu về hen suyễn đã xác định sự hiện diện của tự kháng thể IgE nhắm vào nhiều tự kháng nguyên khác nhau, bao gồm DFS70, periplakin, yếu tố thấp, kháng nguyên tiểu cầu, EXP và ECP, với tỷ lệ mắc được báo cáo dao động từ 8.7% đến 70%. Trong bối cảnh dị ứng thức ăn, các báo cáo hiện có về tự kháng thể IgE còn khá hạn chế và chủ yếu tập trung vào dị ứng sữa bò, trong đó IgE tự phản ứng đã được phát hiện chống lại các protein tương đồng ở người của a-lactalbumin, ẞ-casein và x-casein (xem Bảng 2). Đáng chú ý, tỷ lệ IgE tự phản ứng trong dị ứng sữa dường như khá cao, dao động từ 35% đến 100%.
Trong mày đay tự phát mạn tính (CSU), nhiều đích của tự kháng thể IgE đã được xác định, bao gồm IL-24, TPO, TG, DNA sợi kép, ECP, EXP, thụ thể FcERI, tissue factor và tissue-transglutaminase 2. Tỷ lệ IgE tự phản ứng được báo cáo trong CSU dao động rất lớn, từ 0-100%. Tuy nhiên, phần lớn các nghiên cứu ghi nhận tỷ lệ khoảng 30-60%. Một nghiên cứu gần đây trên 111 bệnh nhân CSU cho thấy hơn một nửa số bệnh nhân (58%) biểu hiện kiểu hình tự dị ứng, cho thấy tự dị ứng là một đặc điểm khá phổ biến của CSU.
IgE tự phản ứng cũng có thể được phát hiện ở một số người khỏe mạnh, với tỷ lệ được báo cáo dao động từ 0 đến khoảng 30%. Tuy nhiên, trong những trường hợp này, các kháng thể như vậy thường được xem là không có tính gây bệnh. Sanchez và cộng sự đã chứng minh rằng những người khỏe mạnh có IgE chống lại ECP và EXP vẫn cho thấy rất ít hoặc hầu như không có sự hoạt hóa bạch cầu ái kiểm khi được kích thích bằng các tự kháng nguyên này.
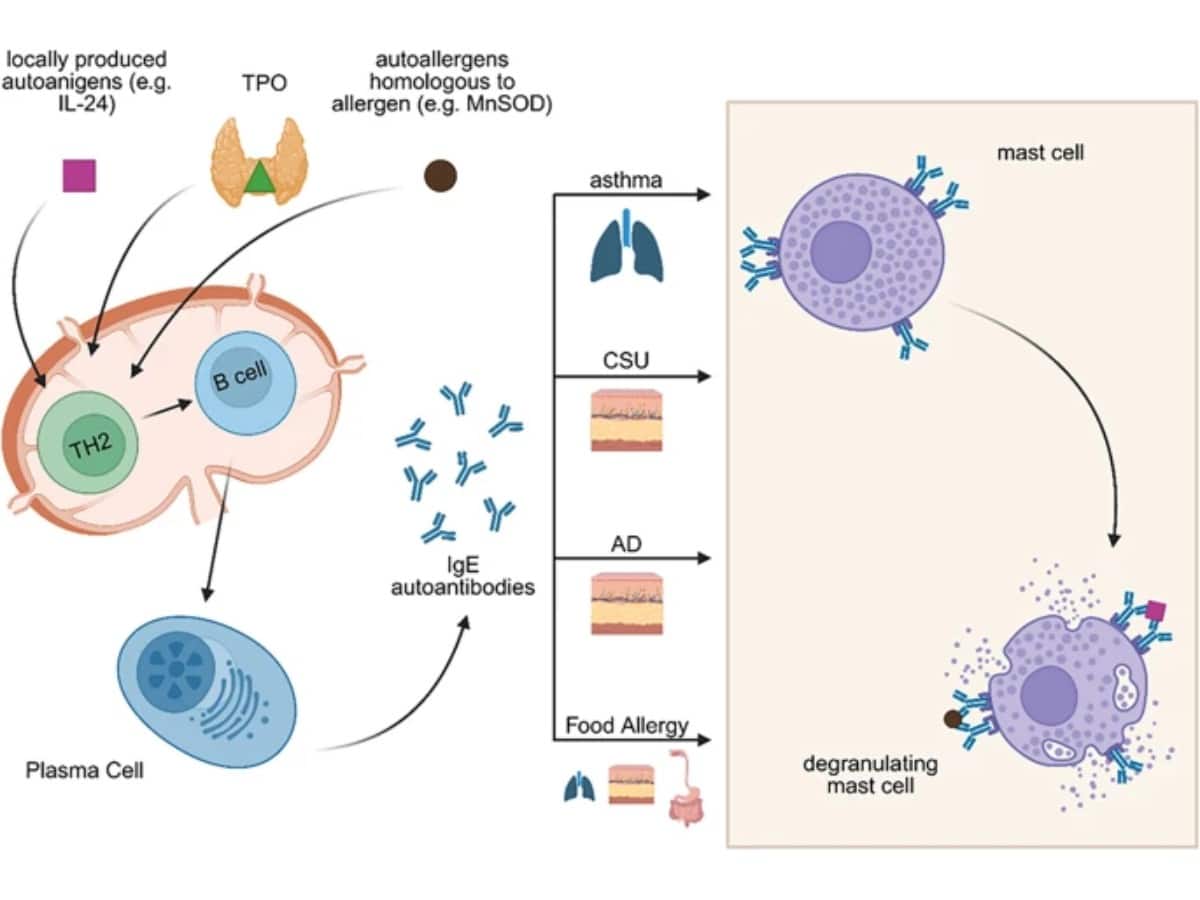
Hình 1. Cơ chế bệnh sinh của tự dị ứng trong hen, mày đay mạn tính tự phát, viêm da cơ địa và dị ứng thức ăn. Tương tự như phản ứng quá mẫn type 1, tự dị ứng cũng đặc trưng bởi hai giai đoạn, gồm giai đoạn mẫn cảm và giai đoạn hiệu ứng. Tuy nhiên, các cơ chế chính xác dẫn đến quá trình mẫn cảm trong tự dị ứng vẫn chưa được hiểu rõ. Một số giả thuyết đã được đề xuất để giải thích sự hình thành IgE tự phản ứng. Một giả thuyết cho rằng khi có sự hiện diện của các tín hiệu cảnh báo từ mô tổn thương, tự kháng nguyên có thể được tế bào trình diện kháng nguyên thu nhận, từ đó gây hoạt hóa tế bào Th2. Các tế bào Th2 này sau đó thúc đẩy tế bào plasma sản xuất kháng thể IgE tự phản ứng. Một cơ chế khác được đề xuất là molecular mimicry, trong đó sự tương đồng cấu trúc giữa các kháng nguyên môi trường hoặc vi sinh vật với protein của cơ thể dẫn đến sự hình thành các tự kháng thể IgE. Các tự kháng thể IgE có thể gắn lên các tế bào mast cư trú trong mô, như ở phổi trong hen, ở da trong viêm da cơ địa, ở phối, ruột và da trong dị ứng thức ăn. Sự hoạt hóa tế bào mast và quá trình phóng hạt sau đó có thể được kích hoạt bởi tự dị nguyên có phản ứng chéo với dị nguyên ngoại sinh (ví dụ: MnSOD), sự tái tiếp xúc với tự dị nguyên được tạo ra tại chỗ (ví dụ: IL-24), hoặc dị nguyên tại chỗ có phản ứng chéo với các protein khác của người (vídụ: TPO và EXP).
TỰ DỊ ỨNG CÓ Ý NGHĨA LÂM SÀNG HAY KHÔNG?
Ý nghĩa lâm sàng của tự dị ứng dựa trên các bằng chứng cho thấy IgE tự phản ứng có liên quan đến mức độ nặng của bệnh và các đặc điểm lâm sàng khác. Trong viêm da cơ địa, tự kháng thể IgE cũng liên quan với da khô, chàm tổ địa, nhiễm trùng và ngứa. Trong hen, những bệnh nhân có IgE kháng periplakin có tần suất xuất hiện polyp mũi cao hơn so với các bệnh nhân không có tự kháng thể này. Trong mày đay mạn tính tự phát, IgE kháng TPO có liên quan đến tần suất cao hơn của cơ địa dị ứng và hen suyễn. Ngoài ra, nồng độ IgE kháng TPO còn tương quan với nồng độ IgG kháng TPO, cùng cố giả thuyết rằng bệnh nhân CSU có nguy cơ mắc các bệnh lý tuyến giáp tự miễn và rối loạn chức năng tuyến giáp. Phản ứng chéo giữa protein của bò và của người đặc biệt có ý nghĩa lâm sàng trong trường hợp trẻ sơ sinh bị dị ứng sữa bò vẫn còn triệu chứng, mặc dù người mẹ đã tránh hoàn toàn các sản phẩm từ sữa.
Trong mày đay mạn tính tự phát, mức độ tự kháng thể IgE được ghi nhận có liên quan đến mức độ hoạt động của bệnh trong một số nghiên cứu, nhưng không được ghi nhận trong các nghiên cứu khác. Ví dụ, nồng độ IgE kháng IL-24 có tương quan với điểm hoạt động mày đay trong 7 ngày (UAS7). Ngoài ra, cũng đã được chứng minh rằng mức độ tự kháng thể tăng lên trong các giai đoạn bùng phát của bệnh. Tương tự, trong viêm da cơ địa, IgE tự phản ứng cũng có tương quan với mức độ nặng của bệnh trong một số nghiên cứu, mặc dù một số nghiên cứu khác không tìm thấy mối liên hệ này. Ví dụ, bệnh nhân AD có IgE tự phản ứng chống lại các protein của biểu bì có điểm IGA và EASI cao hơn so với những bệnh nhân AD không có tự phản ứng. Ngoài ra, đa số bệnh nhân hen suyễn có tự kháng thể chống EXP và/hoặc ECP đều mắc hen suyễn nặng.
LÀM SAO ĐỂ CHẨN ĐOÁN TỰ DỊ ỨNG?
Trong dị ứng cổ điển, có nhiều xét nghiệm đã được chứng nhận và phê duyệt để phát hiện IgE đặc hiệu với dị nguyên. Ngược lại, hiện nay chưa có xét nghiệm nào được phê duyệt để xác định tự kháng thể IgE trong thực hành lâm sàng thường quy. Cho đến nay, tất cả xét nghiệm dùng để đánh giá nồng độ tự kháng thể IgE trong huyết thanh, như ELISA hoặc Western Blot chỉ được sử dụng cho mục đích nghiên cứu. Tỷ lệ mắc được báo cáo dao động rất lớn, ví dụ 0-100% đối với IgE kháng TPO trong CSU, do thiếu sự chuẩn hóa, sai lệch trong lựa chọn mẫu, cỡ mẫu nhỏ, và những hạn chế về phương pháp nghiên cứu. Trong một số trường hợp hiếm, test lấy da cũng đã được sửdụng để phát hiện sự hiện diện của IgE tự phản ứng. Đáng chú ý, gần đây việc sử dụng microarray IgE đặc hiệu dị nguyên đã được đề xuất cho viêm da cơ địa và các bệnh tự dị ứng khác. Đặc biệt, việc đo IgE chống lại các dị nguyên phân tử ngoại sinh có tương đồng với protein của người có thể trở thành một dấu ấn sinh học tiềm năng cho tự dị ứng.
Test hoạt hóa bạch cầu ái kiềm (BAT) và xét nghiệm giải phóng histamine từ bạch cầu ái kiềm (BHRA) được sử dụng để chứng minh ý nghĩa chứng minh của các tự kháng nguyên và/hoặc làm công cụ chẩn đoán, ví dụ trong dị ứng thức ăn. Có nhiều quy trình BAT khác nhau, nhưng nhìn chung được chia thành hai phương pháp chính: trực tiếp và gián tiếp. Phương pháp trực tiếp sửdụng máu toàn phần của bệnh nhân. Phương pháp gián tiếp: bạch cầu ái kiềm của người cho được mẫn cảm với huyết thah của bệnh nhân, từ đó chuyển các kháng thể IgE liên quan sang các tế bào này. Sau khi kích thích bằng kháng nguyên, các dấu ấn hoạt hóa như CD203c và CD63 thường được đo bằng kỹ thuật flow cytometry để định lượng mức độ hoạt hóa của bạch cầu ái kiểm. BHRA là một kỹ thuật tương tự, nhưng thay vì đo các dấu ấn hoạt hóa trên bề mặt tế bào, phương pháp này đo lượng histamine được giải phóng.
Cần có thêm nhiều nỗ lực để phát triển các công cụ đã được thẩm định và có khả năng tái lập, nhằm phát hiện và định lượng IgE tự phản ứng một cách đáng tin cậy. Việc thiết lập các ngưỡng lâm sàng và xác định mối liên hệ giữa IgE tự phản ứng với mức độ hoạt động của bệnh cũng như đáp ứng điều trị sẽ là những bước quan trọng để tích hợp chẩn đoán tự dị ứng trong thực hành lâm sàng. Ngoài ra, việc tích hợp các nền tảng công nghệ cao như proteomics đa mồi cũng có thể mang lại những hiểu biết mới và hỗ trợ phát triển các dấu ấn sinh học cho liệu pháp chính xác trong lĩnh vực tự dị ứng.
TỰ DỊ ỨNG ĐƯỢC ĐIỀU TRỊ NHƯ THẾ NÀO?
Chiến lược điều trị chính trong tự dị ứng là trung hòa IgE lưu hành trong máu, từ đó làm gián đoạn chuỗi hoạt hóa phía sau của các tế bào hiệu ứng, như tế bào mast. Omalizumab hiện vẫn là kháng thể đơn dòng kháng IgE duy nhất đã được phê duyệt để điều trị hen dị ứng, mày đay mạn tính tự phát và dị ứng thực phẩm. Ngoài ra, một số thuốc biosimilar của omalizumab cũng đã được cấp phép hoặc sẽ sớm được cấp phép cho các chỉ định này.
Về mặt cơ chế, omalizumab gắn vào một epitope cấu trúc nằm trong miền C€3 của IgE, đây là vùng rất quan trọng cho sự tương tác với cả FcCRI và thụ thể IgE ái lực thấp (CD23). Bằng cách nhắm vào miền này, omalizumab bắt giữ IgE tự do và ngăn cản IgE gắn vào các thụ thể trên tế bào mast, bạch cầu ái kiềm, tế bào B và các tế bào trình diện kháng nguyên. Điều quan trọng là omalizumab không gắn với IgE đã gắn sẵn trên FcERI, do đó tránh gây hoạt hóa tế bào ngay lập tức. Sự giảm nồng độ IgE tự do trong tuần hoàn dẫn đến nhiều tác dụng điều hòa miễn dịch, bao gồm giảm biểu hiện FcERI trên tế bào mast, bạch cầu ái kiểm và tế bào dendritic, từ đó làm giảm độ nhạy với kháng nguyên và giảm sự hoạt hóa tế bào. Ngoài ra, omalizumab còn làm giảm quá trình trình diện kháng nguyên được hỗ trợ bởi IgE của các tế bào dendritic cell.
Sự đáp ứng nhanh và thuận lợi với omalizumab cho thấy vai trò lâm sàng của autoreactive IgE trong mày đay mạn tính tự phát. Omalizumab giúp đạt đáp ứng hoàn toàn ở 70% bệnh nhân CSU có IgE kháng TPO. Mặc dù thử nghiệm này không đánh giá liệu những bệnh nhân có tự kháng thể IgE có đáp ứng với omalizumab tốt hơn so với những người không có hay không, nhưng một nghiên cứu gần đây trên bệnh da có liên quan đến tự kháng thể IgE đã ủng hộ giả thuyết này. Cụ thể 75% bệnh nhân pemphigoid bọng nước có nồng độ IgE kháng BP180-NC16A huyết thanh tăng ở thời điểm ban đầu đạt đáp ứng hoàn toàn với omalizumab, so với 41% ở những bệnh nhân không có các tự kháng thể này (p = 0.01). Các bằng chứng ban đầu cũng cho thấy điều trị bằng omalizumab có thể làm giảm đáng kể nồng độ tự kháng thể IgE trong huyết thanh, chẳng hạn IgE kháng TF và IgE kháng TG, ở bệnh nhân CSU chỉ sau một tuần điều trị.
Ngoài việc tác động trực tiếp vào IgE, bệnh nhân mắc các bệnh tự dị ứng (autoallergic diseases) cũng có thể hưởng lợi từ việc nhắm vào các yếu tố bệnh sinh quan trọng khác, bao gồm các cytokine IL-4 và IL-13, BTK và thụ thể KIT. Dupilumab, một chất ức chế IL-4Ra có khả năng chặn tín hiệu của cả IL-4 và IL-13, hiện đã được phê duyệt điều trị hen phế quản, viêm da cơ địa và mày đay mạn tính tự phát tại Hoa Kỳ, Nhật Bản, Brazil và các Tiểu vương quốc Ả Rập và hiện đang được xem xét phê duyệt tại Liên minh châu Âu. Dupilumab đã được chứng minh làm giảm đáng kể nồng độ IgE toàn phần ở bệnh nhân viêm da cơ địa, đồng thời giảm tới 86% nồng độ IgE đặc hiệu với các dị nguyên thức ăn sau 3 năm điều trị. BTK đóng vai trò quan trọng trong cả tín hiệu thụ thể tế bào B (BCR) và sự hoạt hóa tế bào mast. Hiện nay, một số thuốc ức chế BTK như remibrutinib, rilzabrutinib, atuzabrutinib, branebrutinib và fenebrutinib đang được đánh giá lâm sàng để sử dụng tiềm năng trong dị ứng thức ăn, CSU, hen và viêm da cơ địa. Ví dụ, remibrutinib đã cho thấy hiệu quả điều trị và hồ sơ an toàn thuận lợi trong điều trị CSU, vì thuốc ức chế hiệu quả sự hoạt hóa của tế bào mast và bạch cầu ái kiềm do hiện tượng bắt chéo IgE hoặc các yếu tố hoạt hóa có nguồn gốc từ huyết thanh gây ra.
Do có khả năng ngăn chặn sự phóng hạt của tế bào qua trung gian IgE, remibrutinib cũng có thể mang lại lợi ích trong các bệnh lý tự dị ứng. Ngoài ra, ức chế BTK có thể hạn chế sự phát triển của các tế bào autoreactive B cells và thúc đẩy self-tolerance bằng cách ngăn chặn sự vượt qua các điểm kiểm soát dung nạp miễn dịch ngoại vi. Thụ thể KIT, một yếu tố điều hòa quan trọng đối với sự sống còn, tăng sinh và hoạt hóa của tế bào mast, có thể bị ức chế bởi các kháng thể đơn dòng như barzolvolimab. Trong một thử nghiệm lâm sàng giai đoạn 1b, 43% bệnh nhân CSU được điều trị bằng barzolvolimab đạt đáp ứng hoàn toàn (UCT = 16) vào tuần thứ 12, cho thấy tiềm năng lâm sàng của các liệu pháp làm giảm số lượng tế bào mast trong điều trị bệnh tự dị ứng. Hiện nay, các thử nghiệm lâm sàng giai đoạn 2 và 3 của barzolvolimab trong điều trị CSU vẫn đang được tiến hành.
TÀI LIỆU THAM KHẢO
Steinert C, Pashuk M, Kolkhir P, Kocatürk E, Xiang YK. Tự dị ứng và những điều mà bác sĩ chuyên khoa dị ứng cần biết. Curr Allergy Asthma Rep. 2025 ngày 9 tháng 8;25(1):34. doi: 10.1007/s11882-025-01215-8. PMID: 40782271; PMCID: PMC12335397.