Y tế - Sức Khỏe
Tổng quan: Nguồn gốc của hoạt chất Alkaloid
Nhà thuốc Lưu Văn Hoàng – Chủ đề: Tìm hiểu chung về:Tìm hiểu chung về: Alkaloid theo dòng lịch sử
Nguồn: Bộ môn dược liệu – Đại học Y Dược TP HCM
Nguồn gốc ra đời của Alkaloid

Trong vương quốc hóa học các hợp chất tự nhiên, alkaloid là một thế tộc quan trọng, vừa đa dạng về cấu trúc lại thể hiện độc tính do đó mang đến hy vọng chữa lành những căn bệnh nan y trong đó bao gồm ung thư, đúng như câu thành ngữ “thuốc đắng dã tật”. May mắn thay, lịch sử nói rằng alkaloid đã làm được. Hãy ôn lại những câu chuyện xưa bắt đầu từ một loài cây có tên rất đẹp: Hỉ thụ. Liệu Hỉ thụ có mang đến Hỉ cho chúng ta hay không?
Về chi Hỉ thụ (Camptotheca sp.) và Camptothecin – alkaloid kháng ung thư
Theo tiếng Hoa thì Hỉ thụ (喜树) có nghĩa là cây hạnh phúc. Chi Camptotheca có 2 loài: Camptotheca acuminata Decne. và Camptotheca lowreyana S.Y.Li, thuộc về họ Lam quả (Nyssaceae), nhưng đôi khi được đặt trong họ lớn hơn là Sơn thù du (Cornaceae) đều có thể bắt gặp ở Trung Quốc. Phương Tây cũng gọi Hỉ thụ bằng những cái tên rất mỹ miều: happy tree, cancer tree, tree of life. “Campto” theo tiếng Hy Lạp có nghĩa là cong và theca là một trường hợp (đặc biệt). Điều này liên quan đến bao phấn được uốn cong vào trong một cách đặc biệt, được đặt bởi Joseph Decaisne vào năm 1873. Tên loài, acuminata, đề cập đến đầu nhọn của lá. Các mô tả về loài dựa trên mẫu vật thu thập tại Lộc Sơn, tỉnh Giang Tây trong chuyến đi thăm dò thực vật năm 1868-1870 của Cha Armand David.
Trong y học cổ truyền Trung Hoa, Hỉ thụ (Camptotheca acuminata) từng được sử dụng để chữa vẩy nến, buồn nôn do bệnh gan, cảm cúm và đôi khi ung thư. Cũng có nhận định cho rằng trước đây, Hỉ thụ chủ yếu làm cảnh và…củi. Tên Hỉ thụ được giả định do sử dụng dân gian để trị đờm khó chữa, liên quan đến hen suyễn tái phát, tạo nên niềm vui cho người bệnh khi khỏi. Tên gọi địa phương của Hỉ thụ rất đa dạng: hồi dại hay chuối dại ở Quý Châu, hoặc đặt theo môi trường sinh sống: hạn liên tử (Giang Tô, Giang Tây, Tứ Xuyên), thủy lật tử (hạt dẻ sống ở nước, Hồ Nam), bọt nước (Vân Nam), cọ nước (Quảng Đông), thủy đông qua (bầu trắng nước, Tứ Xuyên), thủy đĩnh mộc (cây mọc theo sông, Tứ Xuyên),…
Đi nửa vòng Trái đất qua Hoa Kỳ, vào thập niên 50 thế kỉ trước, những bệnh do nhiễm trùng đã được chặn đứng bởi việc phát minh ra kháng sinh. Chính quyền cũng như các nhà khoa học chuyển qua tập trung giải những bài toán khác: các bệnh liên quan đến tim mạch và ung thư.
NCI (National Cancer Institute: Viện Ung thư Quốc gia) thành lập Trung Tâm Hóa Trị Liệu Ung Thư Quốc Gia (Cancer Chemotherapy National Service Center: CCNSC) vào năm 1955 để sàng lọc các chất có khả năng kháng ung thư, ban đầu là các chất đã biết, chất tổng hợp được, sau đó chuyển sang chiết xuất từ dược liệu bao gồm cả động thực vật.
Trong cùng thời gian đó, Monroe Wall làm Trưởng một dự án của Cục Nông nghiệp Hoa Kỳ (USDA) về việc tìm phytosterol làm nguyên liệu khả dĩ để tổng hợp cortison. Trong quá trình đó, hàng ngàn mẫu chiết xuất được gửi đến NCI để thử khả năng kháng ung thư. Trong số này, dịch chiết từ cây Hỉ thụ thể hiện tiềm năng. Nhưng USDA không hứng thú trong đề tài này.
Mãi đến khi Viện Nghiên Cứu Tam Điểm (RTI: Research Triangle Institute) ở Bắc Carolina thành lập, Wall lại nhen nhóm ý định phân lập hoạt chất từ Hỉ thụ và đến đây vào tháng 7 năm 1960. RTI là Viện đầu tiên được thành lập trong Khu nghiên cứu tam điểm vào năm 1958, lấy tên tam điểm từ sự hợp tác giữa ba trường đại học: Đại học Bắc Carolina, Chapel Hill; Đại học Duke và Đại học Bang Bắc Carolina. Năm 1962, Wall thu hút thêm Masukh Wani về RTI, sự hợp tác này thành công trong suốt 4 thập kỷ.
Theo mô tả của Wani, RTI lúc đầu không có gì ngoài 4 bức tường, nhưng sự có mặt của bức tường thứ 5: ngài Wall đã khởi động Labo Hóa hợp chất tự nhiên. Nói một cách rất “nghề” thì cách làm việc của nhóm Wall-Wani là phân lập hướng tác dụng (‘bioactivity-directed fractionation’). Từ 20 kg dược liệu bao gồm thân và vỏ thân Hỉ thụ, cao chiết được tách thành nhiều phân đoạn khác nhau, thử hoạt tính, sau đó tập trung vào phân đoạn có hoạt tính, lại tách thành phân đoạn nhỏ, thử hoạt tính, rồi lại phân lập,… Tất cả phân đoạn sau khi phân tách được thử hoạt tính in vitro trên dòng tế bào KB và in vivo trên tế bào L1210 của chuột bị leukemia.
Hợp chất tinh khiết có hoạt tính rất cao kháng lại L1210 được đặt tên camptothecin (CPT-1). Cấu trúc được xác định bằng cách kết tinh và sử dụng kỹ thuật nhiễu xạ tinh thể tia X. Wall, Wani và cộng sự công bố trên Journal of the American Chemical Society vào năm 1966.
NCI tiếp tục thử nghiệm trên lâm sàng nhưng có hai vấn đề xảy ra là tính tan trong nước kém của camptothecin cũng như tác dụng phụ trên bệnh nhân. Diễn trình bị kéo dài thêm mười lăm năm cho đến khi các nhà khoa học hiểu được cơ chế.
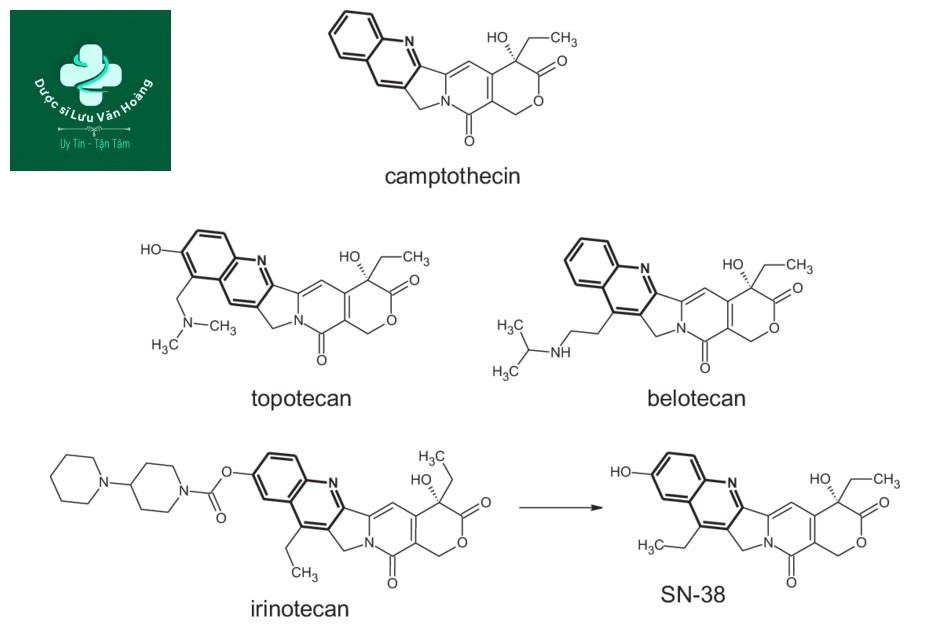
Camptothecin tham gia vào liên kết giữa topoisomerase I và ADN, điều này dẫn đến tổn thương ADN và gây ra apoptosis – “chết theo lập trình”. Cơ chế đặc biệt trên thu hút sự chú ý vào camptothecin một lần nữa. Các nhà khoa học đã sử dụng SAR (liên quan giữa cấu trúc và tác dụng) để tạo nên các phân tử tiềm năng mới dựa vào camptothecin.
Vào giữa thập niên 90, FDA đã chấp thuận 2 hợp chất dựa trên camptothecin là topotecan và irinotecan (CPT-11) trong điều trị ung thư buồng trứng, vú, phổi và trực tràng.
Như vậy, đi một quãng đường đăng đẳng 4 thập kỉ, Hỉ thụ – “cây hạnh phúc” cuối cùng đã đơm hoa hạnh phúc.
Con đường đi tìm thuốc hạ sốt
Trôi dạt qua Nam Mỹ cùng người Quechua bản địa vùng Peru, Bolivia và Ecuador. Họ thường dùng vỏ cây cinchona (người Việt gọi là Canh-ki-na) trộn với nước có vị ngọt, dùng để giãn cơ (khi bị chuột rút chẳng hạn) hoặc chống run rẩy khi trời lạnh.
Sở dĩ phải trộn với nước có vị ngọt vì loài cây này có vị rất đắng. Cách uống của người Quechua khá giống với việc sau này người ta pha nước giải khát Tonic bằng cách cho một ít quinin (mình hay gọi là kí ninh) – thành phần chính của cinchona vào nước soda, rồi pha nước Tonic vào rượu gin hay vodka tùy ý. “Đắng như quinin” là một câu thành ngữ đấy ạ.
Các nhà truyền giáo dòng Tên người Tây Ban Nha đã mang những cây cinchona đầu tiên đến với Châu u. Sớm nhất vào đầu thế kỷ 17, người u đã dùng cinchona dạng nguyên bản vào việc chữa trị, thông qua những quan sát của các nhà truyền giáo về cách dùng của người Quechua.
Cinchona là cái tên được Carl Linnaeus đặt cho cây này, tưởng nhớ tên nữ Bá tước Chinchon, vợ của Bá tước thứ 4 của Chinchón (Tây Ban Nha), phó vương Peru Luis Jerónimo de Cabrera, câu chuyện về họ cùng mối liên hệ giữa cinchona và bệnh sốt rét được thầy thuốc Ý Sebastiano Bado thuật lại vào năm 1663. Theo đó, một nhà cầm quyền Tây Ban Nha đã khuyên họ sử dụng cinchona sau khi người vợ bị sốt và kết quả khỏi bệnh. Người vợ của Bá tước đã yêu cầu một lượng lớn dược liệu để mang về Châu u.
Năm 1820, bộ đôi nghiên cứu người Pháp Pierre Joseph Pelletier và Joseph Bienaimé Caventou lần đầu tiên phân lập quinin từ vỏ cây Cinchona, cái tên quinin xuất phát từ ngôn ngữ bản địa quina hoặc quina-quina: vỏ cây hoặc vỏ cây thánh.
Trước khi phân lập quinin thì người u sấy hoặc phơi khô vỏ cây cinchona, nghiền mịn rồi trộn với rượu vang cho dễ uống. Người Việt chúng ta đọc Canh-ki-na có lẽ bắt nguồn từ “quinqina”trong tài liệu của ngài Paul Briquet người Pháp. Một sự thật đáng buồn là quinin và cây cinchona đã góp phần vào công cuộc thực dân hóa Châu Phi của người u. Trước đó, khi bước vào vùng đất này, người ta vẫn hay gọi là “ngôi mộ của người da trắng” do mắc phải bệnh sốt rét.
Thị trường buôn bán quinin trở nên căng thẳng, Peru và những nước xung quanh nghiêm cấm xuất khẩu cây giống và hạt giống cinchona vào đầu thế kỷ 19. Bất chấp vậy, Hà Lan vẫn buôn lậu loại cây này. Họ thành lập Cục Kina, đem trồng cinchona tại Indonesia và biến nơi đây thành nguồn cung cấp 97% sản lượng quinin trên thế giới.
Chúng ta nên biết rằng trong thời điểm ấy, sốt rét là một nỗi ám ảnh đối với nhân loại, nhất là với các đội quân đi chinh phục khắp thế giới. Vào Thế chiến thứ II, quân Đồng minh đã bị cắt nguồn cung quinin khi mà Đức chiếm Hà Lan và Nhật thì kiểm soát Indonesia. Hoa Kỳ đã thu được 4 triệu hạt giống từ Philippines và vận hành một số đồn điền ở Costa Rica. Nhưng cũng không kịp để cho hàng ngàn lính Hoa Kỳ phải bỏ mạng ở Châu Phi và Nam Thái Bình Dương.
Quinin vẫn là thuốc chống sốt rét hàng đầu cho hậu Thế chiến thứ II. Bromo Quinine là một viên nén “brand name” của hãng Grove được đưa ra thị trường từ 1889 cho đến khoảng những năm 1960. Theo đúng quy ước alkaloid, phải viết là “quinine” mới đúng. Quinine là một alkaloid, chất này gây độc đối với ký sinh trùng sốt rét Plasmodium falciparum. Cơ chế tác động của quinine cùng nhóm thuốc quinolin cho đến ngày nay vẫn chưa thực sự rõ ràng, nó có liên quan đến việc can thiệp vào khả năng hòa tan và chuyển hóa haemoglobin của loài ký sinh trùng này. Quinin còn được chỉ định off-label trên Hội chứng bồn chồn chân vào ban đêm.
Quinin cùng với đồng phân của mình là quinidin được sử dụng như một tác nhân có định hướng cho hóa học tổng hợp bất đối xứng (tạo ra đồng phân quang học mong muốn). Phản ứng mang tên “dihyroxy hóa bất đối Sharpless”. Nhà khoa học Karl Barry Sharpless đã được trao giải Nobel Hóa học 2001 cho những công trình tổng hợp hóa hữu cơ có định hướng.
À, cây canh-ki-na họ Cà phê (Rubiaceae) nhé (nhìn là thấy cà phê luôn rồi á).
Trong đại dịch COVID-19, thuốc sốt rét tổng hợp có cấu trúc dựa trên quinin là hydroxycloroquin được đề xuất sử dụng do đặc tính kháng virus. Tuy nhiên, thử nghiệm lâm sàng sau đó cho thấy thuốc này không đạt hiệu quả mà còn có thể mang lại tác dụng phụ. Việc tận dụng các thuốc kháng ký sinh trùng như hydroxycloroquin, ivermectin hay artesunat trong bối cảnh khẩn cấp do đặc tính độc tế bào của các thuốc này là điều dễ hiểu. Tuy nhiên, chỉ định dùng thuốc chỉ được đưa ra sau khi đã có bằng chứng hiệu quả trên lâm sàng rõ rệt. Do đó, cần hết sức thận trọng trong việc tư vấn và sử dụng thuốc.
Xem thêm:
Câu chuyện thần thoại

Theo quyển sử thi Odyssey của Homer, nhân vật chính cùng tên trên đường chiến thắng trở về quê nhà đã được thần bảo hộ Hermes trao cho một loại thảo dược ‘moly’ với mô tả “rễ đen, hoa trắng như sữa”, còn không quên bồi thêm câu “khó khăn thế nhân mới nhổ nổi, song với thần linh thật dễ dàng”. Thảo dược này giúp anh chàng Odyssey miễn nhiễm với bát canh Mạnh Bà, à xin lỗi có một chút nhầm lẫn, chúng ta đang ở phương Tây, chén thuốc độc của “yêu phụ” Circe. Người uống phải sẽ bị mất trí nhớ.
Nhận diện thuốc giải
Dựa trên những mô tả đó, các nhà thực vật học đã xác định loài thảo dược ‘moly’ kia chính là cây ‘snowdrop’ Galanthus nivalis. ‘Gala’ theo tiếng Hy Lạp là sữa, ‘anthos’ là hoa. Nhìn cây thì chúng ta cũng hiểu sao gọi là snowdrop. Sự đam mê sưu tập, phân loại các giống ‘snowdrop’ khác nhau thậm chí còn phát sinh ra thuật ngữ galanthophile, tương tự như việc sưu tập các giống Huệ của người đam mê.
Phân lập thuốc giải
Mãi về sau, đến thập niên 50 của thế kỷ 20, khoảng độ 1956, tại Liên Xô, nhà hóa học người Bulgaria Dimitar Paskov đã phân lập được galantamin từ loài Galanthus nivalis. Galantamin là một alkaloid mang hoạt tính kháng cholinesterase và được sử dụng để chữa triệu chứng của bệnh Alzheimer’s. Hợp chất này còn được tìm thấy ở nhiều loài khác trong họ Thủy tiên.
Nhận diện thuốc độc
Thuốc độc mà yêu phụ Circe sử dụng được dự đoán chiết xuất từ nhóm cây thuộc chi Cà độc dược Datura (như cà độc dược lùn Datura stramonium chẳng hạn). Nhắc đến chi Datura thì người ta toàn gọi bằng những cái tên hãi hùng: hơi thở của quỷ, bóng đêm chết chóc, cà độc dược, loa kèn của quỷ… hay có tên thân thiện hơn như hoa mặt trăng, loa kèn của thiên thần, táo gai. Tên chi Datura có nguồn gốc từ tiếng Phạn dhattūra chỉ cây cà độc dược Datura metel, loài cây được dâng lên cho thần Shiva theo Ấn Độ Giáo.
Có thật sự độc không?
Gọi là Cà độc dược mà ^ ^. Các alkaloid của chi Datura thuộc về khung tropan: atropin, scopolamin,… Có một dạo xôn xao chuyện lừa đảo thôi miên bằng scopolamin, dấy lên nghi ngại về việc trồng các loài Cà độc dược làm cây cảnh ven đường. Nhưng scopolamin vẫn dùng trong y dược, điển hình là miếng dán chống say tàu xe. Hay atropin dùng trong các trường hợp: loét dạ dày – hành tá tràng, hội chứng kích thích ruột, triệu chứng ngoại tháp, bệnh Parkinson giai đoạn đầu,…nói chung là kháng muscarin, ức chế phó giao cảm.
Theo truyền miệng vui tính, atropin làm giãn đồng tử, biến đôi mắt phái đẹp long lanh hơn, nhưng mơ huyền mờ là có thật ạ, thế nên các cô nàng cứ chớp chớp lúc đi dạ hội, làm nhiều đấng anh hùng phải khuynh đảo nơi bàn tiệc.
Không có ‘moly’ có giải độc được không?
Dĩ nhiên là còn nhiều loại thuốc giải độc khác và một trong số đó là physostigmin (eserin) chiết xuất từ loài đậu Calabar (Physostigma venenosum). Vùng Calabar ngày nay thuộc Nigeria. Như vậy, khi một chất thể hiện sự đối kháng với alkaloid nhà Cà, nó gợi ý cho người ta về việc chữa chứng mất trí nhớ (tất nhiên là khoa học phức tạp hơn). Một đàn em bán tổng hợp của physostigmin là rivastigmin đã được FDA chấp thuận trở thành thuốc dùng cho Alzheimer’s. Physostigmin thuộc vào dạng có tuổi trong làng Hóa thực vật. Tính đối kháng với chất kháng cholinergic nghiễm nhiên biến physostigmin thành kẻ thù của alkaloid nhà Cà (như atropin, scopolamin).
Nếm thử thuốc độc là có thật
Câu chuyện lưu truyền tiếp theo, là việc tự…nếm độc để thử của các chuyên gia độc học. Đầu tiên là ngài Robert Christison, đã đích thân nếm thử mùi vị của đậu Calabar, rất may là ông còn sống để ghi chép lại sự kiện này. Một vài nhà khoa học Edinburgh tiếp tục nghiên cứu về loài đậu Calabar, trong có có việc chiết được hoạt chất chính mà sau đó được gọi là physostigmin. Họ nghiên cứu về tác dụng đối kháng giữa atropin và physostigmin. Mà vì đối kháng atropin (cộng với việc thử trên mắt) nên physostigmin ban đầu dùng trong y học để chữa glaucom, được đề xuất bởi Lugwid Laqueur. Laqueur cũng là một người đã tự nếm trải tác dụng của physostigmin khi mắt ông bị glaucom, dù người ta cho rằng ông có phương pháp khoa học hơn để thực hiện thử nghiệm so với Christison (chắc do có bệnh mới thử).
Vị đắng của alkaloid
Khả năng chịu được vị đắng khác nhau tùy cá nhân, nhưng có thể tăng giảm thông qua việc tăng hay giảm tiếp xúc thường xuyên với các thực phẩm/thuốc có vị đắng. Các dược liệu chứa alkaloid thường được liên tưởng đến vị đắng như: cinchona, cà belladon, ô đầu,… 2 alkaloid thường được quy gán rộng rãi cho vị đắng là cafein và quinin. Mặc dù vị đắng được cho liên quan đến cơ chế phòng vệ của cơ thể, một số món ăn, thức uống lại cần đến vị đặc trưng này như trà, khổ qua, bia, socola, cà phê,…Nước tonic là một thực thể thú vị: thời xưa, soda và đường đóng vai trò điều vị cho quinin; ngày nay, quinin lại trở thành chất tạo đắng cho nước soda đường.
Nhìn chung, cafein có vị đắng ở mức trung bình, nếu có thể so sánh thì khoảng 1/100 – 1/30 so với quinin. Hai người anh em theophyllin và theobromin cũng có vị đắng tương đương, cùng nhau tồn tại trong trà, cà phê và ca cao. Vị đắng của ca cao còn do các dẫn xuất của 2,5-diketopiperazin và flavanol trong khi vị đắng của trà do catechin và tanin. Quá trình rang cà phê chỉ làm giảm đi chút đỉnh cafein nên giải pháp tốt nhất cho việc loại đi vị đắng là dùng cà phê tách cafein hoặc các giống arabica rang nhạt. Quinin có ngưỡng đắng ở độ pha loãng 1:184175. Solanin và những người anh em của mình bên cạnh vị đắng còn mang lại cảm giác bỏng rát. Khá bất ngờ khi alkaloid nổi tiếng về vị cay là capsaicin cũng gây ra cảm giác đắng, điều đồng thời tìm thấy ở menthol, bằng một cách trung gian nào đó.
Trong tiểu thuyết đầu tay Vụ án bí ẩn ở Styles của nhà văn Agatha Christie, nạn nhân trong câu chuyện bị đầu độc bởi strychnin. Tác giả đã có hiểu biết khá rõ về hóa học thông qua lời nói của thám tử Poirot rằng strychnin không thể được cho vào ca cao do ngưỡng đắng 1:70000 của nó, nhưng với cà phê thì có thể. Vụ án kết thúc với lời giải thích rằng hung thủ sử dụng kali bromid để tủa strychnin khỏi hỗn dịch tonic của nạn nhân và lắng xuống đáy chai. Khi nạn nhân uống liều cuối vào nửa đêm đã bị ngộ độc strychnin.
Cơ chế cảm thụ
Các protein TAS2R đóng vai trò trong việc thụ cảm vị đắng. Các phối tử đã được biết và làm chuẩn để nghiên cứu vị đắng bao gồm cycloheximid, denatonium, PROP (6-n-propyl-2-thiouracil), PTC (phenylthiocarbamid). Cơ chế tác động phân tử vẫn còn được nghiên cứu, trong đó gợi ý sự khác biệt giữa các vị đắng là có thật, do sự đa hình của một số protein thụ thể. Mặc dù tất cả TAS2R đều nằm trong tế bào chứa gustducin, việc loại bỏ gustducin không làm giảm hoàn toàn cảm nhận vị đắng. Điều này chứng minh phản ứng với vị đắng chính là cơ chế phòng vệ của cơ thể người và động vật.
Không ngạc nhiên khi TAS2R được chứng minh có vai trò miễn dịch tại các tế bào biểu mô có lông chuyển ở đường thở như mũi, xoang. Một ví dụ đặc biệt là TAS2R38, thụ thể có khả năng liên kết phối trí với cả 2 hợp chất đắng PROP và PTC, cũng nhạy cảm với sản phẩm của Pseudomonas aeruginosa như các quinolon hay acyl-homoserin lacton. Các chất độc tiết ra của vi khuẩn chính là chất chủ vận của TAS2R, làm tiết ra nitric oxid hoặc các defensin. Ở người, TAS2R còn có trong bạch cầu, vú, đường ruột hay lớp sừng. Một giải thích được đề xuất rằng ở những loài thực vật, chúng “bắt chước” các chất độc của vi khuẩn làm tác nhân chống xâm hại, và đến lượt con người cảm nhận thì trở thành vị đắng. Vi khuẩn, thực vật và động vật luôn có những tác động qua lại lẫn nhau trong hành trình lịch sử.
Vai trò của vị đắng đối với sức khỏe con người
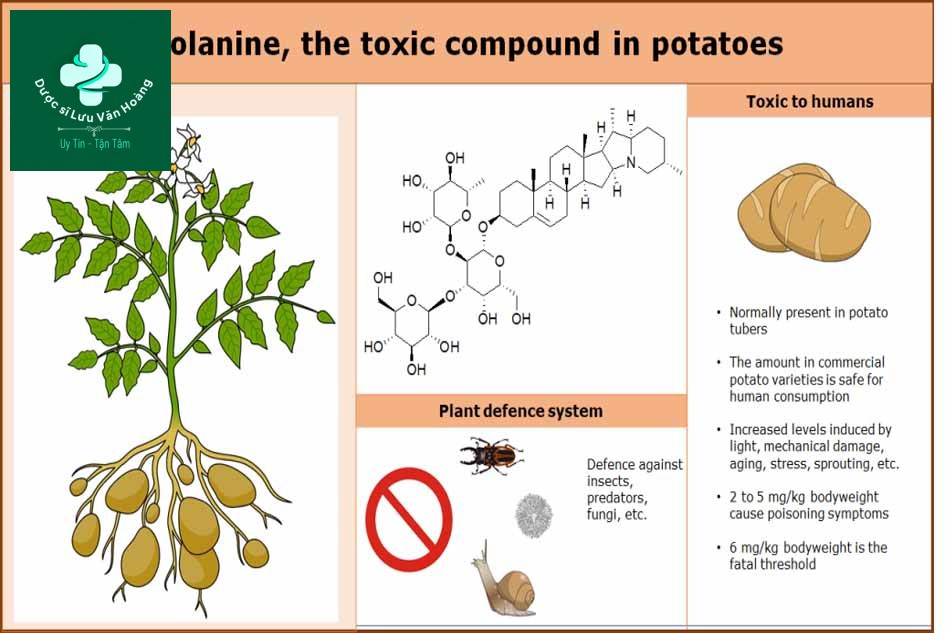
Quá trình chọn lọc tự nhiên và nhân tạo trong việc tìm kiếm nguồn lương thực của con người đã dẫn đến nhu cầu thuần hóa, tạo các giống có năng suất cao kết hợp với độc tính thấp. Các loài lúa gạo, lúa mì, bắp có nguồn gốc tổ tiên từ cỏ hầu như khá ít độc tính nhưng mất thời gian và công sức thu hái, chế biến. Các loài lương thực có độc bao gồm khoai tây chứa solanin, quả bí dại chứa cucurbitacin và đậu chứa phytohemagglutinin được con người thuần hóa, lai giống để tạo nên các loài ít độc như ngày nay. Điều này thực tế khá dễ hiểu: các loài không chứa độc sẽ bị sâu bệnh gây hại tấn công nên cần sự chăm sóc của con người nhiều hơn. Tuy nhiên, không loại trừ khả năng vẫn còn tồn tại chất độc trong khẩu phần ăn của chúng ta hàng ngày. Vị đắng góp phần vào việc nhận dạng chúng.
Ví dụ điển hình về tầm quan trọng của vị đắng đối với an toàn thực phẩm và dịch bệnh chính là sắn (Manihot esculenta). Đứng ở góc độ nuôi trồng, sắn là loài được canh tác mà không cần thuốc trừ sâu hoặc quá nhiều lao động thủ công. Điều này giải thích do cơ chế phòng vệ của sắn đối với sâu bệnh, đồng thời cũng có khả năng gây độc cho con người. Khi nhai sắn, cặp enzym-cơ chất linamarase-linamarin phản ứng với nhau làm giải phóng acid hydrocyanid. Ngộ độc phổ biến ở một số vùng của châu Phi đến nỗi hội chứng này được đặt tên là konzo (chân bị trói, trong ngôn ngữ Yaka). Để xử lý vấn đề này, người ta thường dùng phương pháp ướt: trộn bột sắn với nước theo một tỷ lệ nhất định, dàn trải phơi ngoài nắng hoặc trong bóng râm để giải phóng HCN. Bột ẩm sau đó được nấu với nước tạo thành cháo không đắng, do linamarin có vị đắng đã bị mất đi.
Các chất chống xâm hại thực vật có thể chia làm 3 nhóm lớn: chứa Nitơ (alkaloid hoặc chứa cyanid), terpen và phenol. Đa số các chất này đồng thời có vị đắng.
Nhưng vị đắng trong hạt thì sao?
Khi tìm tư liệu cho bài viết này, tác giả thấy một câu hỏi trên trang Quora “tại sao ngay cả loại quả ngọt nhất cũng chứa hạt đắng?” Hạt của các loài thực vật trong chi Prunus, họ Rosaceae như đào, mận, táo, mơ, hạnh đắng, cherry,…chứa hợp chất amygdalin – glycosid cyanogenic (amygdalē trong tiếng Hy Lạp chỉ hạnh nhân, amygdal của người được đặt tên dựa trên hình dáng giống hạnh nhân). Ion cyanid có thể bị giải phóng khỏi amygdalin bởi β-glucosidase gây ngộ độc. Một sản phẩm phân hủy khác là benzaldehyd tạo nên vị đắng. Sự khác nhau ngọt/đắng giữa các giống hạnh nhân có liên quan đến hàm lượng amygdalin chứa trong đó.
Vị đắng của tim sen liên quan đến nhóm hợp chất alkaloid khung isoquinolin trong khi ở bạch quả là các glycosid cyanogenic. Glycosid cyanogenic có thể loại đi bằng nhiệt nhưng 4′-O-methylpyridoxin (MPN), một chất độc thần kinh và dẫn xuất của Vitamin B6 thì không. Người ta nhận thấy hàm lượng MPN ít hơn nhiều trong lá Bạch quả, và ngay trong hạt thì hàm lượng này cũng thay đổi theo mùa, cao nhất ở tháng 8. Có lẽ ở một góc cạnh nào đó, bên cạnh giá trị dinh dưỡng nuôi mầm sống, các loài thực vật cũng bảo vệ hạt giống của mình bằng các chất độc, tránh sâu bệnh hay các loài động vật ăn mất. Sự đáp ứng khác nhau giữa các loài động vật với các hợp chất dường như tùy thuộc vào tập tính sinh học của mỗi loài (ví dụ con gì thường ăn cây gì). Sẽ hiếm có loài vật nào cố gắng tiêu hóa những đối tượng như hạt đào, nhưng với vi khuẩn thì chưa hẳn, nên mặc dù có lớp vỏ cứng cáp vẫn cần thêm các hợp chất phòng vệ.
Mặt khác, không hẳn hợp chất đắng nào cũng độc, và không phải chất độc nào cũng có vị đắng.
Hệ cơ sở dữ liệu về các hợp chất đắng BitterDB: https://bitterdb.agri.huji.ac.il/dbbitter.php
Sự gian truân của khoa học

Lấy mẫu
Vào một ngày nắng nóng tháng Tám năm 1962, nhà thực vật học Arthur Barclay đang đứng ở Rừng quốc gia Gifford Pinchot thuộc bang Washington, tại cao độ 450 mét, nhìn chăm chú một cây lá kim cao 25 foot – khoảng 7,6 mét. Sau khi tốt nghiệp Đại học Harvard, Barclay về làm việc tại Bộ nông nghiệp Hoa Kỳ, USDA. Nhiệm vụ của ông là thu thập mẫu thực vật cho Viện Ung Thư Hoa Kỳ, NCI. Vào thời điểm đó, NCI nhận khoảng 1000 mẫu mỗi năm cho công việc nghiên cứu của mình. Barclay xác định loài lá kim kia chính là thanh tùng Thái Bình Dương, Taxus brevifolia, tức thông đỏ Mỹ theo cách gọi của chúng ta.
T. brevifolia, Taxaceae là một cây thường xanh với chiều cao trung bình, vỏ thân màu đỏ, phẳng, lá kim dài 1 inch hơi cong, gỗ cứng. Loài này ít có sâu bệnh do độc tính của chúng. Điều đáng nói là chúng rất chậm lớn. Loại gỗ đàn hồi ít bị mục nát có màu nâu đỏ này được cư dân châu Mỹ sử dụng để làm công cụ, cung tên, mũi tên và mái chèo. Các công dụng khác bao gồm chế tạo lao, lưỡi câu, nêm, gậy, thìa, trống, giày trượt tuyết và đầu mũi tên. (Taxša (tiếng Ba Tư cổ): mũi tên. Brevis: nhỏ; folium: lá)
Gửi mẫu
Mẫu thu thập của Barclay sau đó được gửi đến Quỹ nghiên cứu Cựu sinh viên Wisconsin (chính là tổ chức đã cáng đáng chi phí cho warfarin) để bắt đầu chiết xuất. Vỏ thân cây này cho thấy hoạt tính kháng tế bào KB và nhanh chóng thu hút sự chú ý của NCI. Vào tháng 8 năm 1964, Barclay quay về chỗ cũ thu thập thêm 30 pound tức hơn 13 kg mẫu gửi cho Viện Nghiên cứu Tam điểm RTI, nơi của Wall và Wani.
Thất bại ban đầu
30 pound Taxus brevifolia sau khi gửi đến RTI tiếp tục được phân lập hướng tác dụng – theo cách mà Wall và Wani vẫn đang làm. Tuy nhiên, những nỗ lực ban đầu thất bại, thêm vào đó camptothecin phân lập từ Hỉ thụ cũng đang chiếm nhiều công sức của nhóm. Chưa kể còn nhiều loài cây khả quan khác. Một lúc nào đó, Wall đã sẵn sàng…bỏ cuộc với T. brevifolia.
Kết quả phân lập
Vào tháng 9 năm 1966, nhóm nghiên cứu phân lập được một chất kết tinh từ trong số các phân đoạn. Wall gọi nó là “taxol”. Tax- của tên chi và -ol, tức là gì chúng ta biết rồi đấy, alcol. Thực ra, lúc đầu chưa biết cấu trúc của taxol, nhưng họ chắc chắn rằng nó mang nhiều nhóm hydroxyl. Mặt khác, Wall và Wani nói rằng taxol mang lại thanh âm đẹp khi đọc. Taxol® ra đời.
Phần tiếp theo là xác định cấu trúc. Họ đã sử dụng các kỹ thuật nhiễu xạ tinh thể tia X, phổ khối và cộng hưởng từ hạt nhân với phiên bản của thập niên 60 để tìm ra công thức phân tử là C47H51NO14!!!. Bộ đôi nhận ra Taxol® mang trong mình hai thành phần: khung cấu trúc chính gắn với một chuỗi bên, theo cách gọi hài hước là có một cái đuôi.
Vào 1971, tận 5 năm sau, Wall, Wani và cộng sự công bố cấu trúc hoàn chỉnh của Taxol® trong bài báo sáu trang, nói về một hợp chất nguồn gốc tự nhiên với tiềm năng kháng ung thư. Cấu trúc của Taxol® phức tạp đến nỗi họ có vẻ như đã công bố cấu trúc với vị trí chuỗi bên bị gắn sai. (Taxol® có đến 12 C bất đối trong cấu trúc).
Nhiều vấn đề tồn đọng
Nhưng phải thêm 20 năm để Taxol® trở thành một thuốc hóa trị liệu ung thư. Lý do ban đầu là gian truân phân lập. Đến giờ, chúng ta sẽ hiểu vì sao khi mới phân lập, Taxol® lại ẩn nấp mãi mới chịu lộ diện – bởi vì hàm lượng quá nhỏ của nó trong loài thông đỏ chậm lớn T. brevifolia. Hơn nữa, vỏ thân là một tài nguyên cực kỳ hữu hạn, cây này không có vỏ thân thì khắc chết.
Bất chấp những cản trở trên, nghiên cứu về Taxol® vẫn được tiếp tục. Nó cho thấy hoạt tính kháng tế bào ung thư hắc tố B16. Cùng với đó là khả năng làm thu nhỏ ung thư vú trên chuột. Một bước đột phá là khi Susan Horwitz, nhà dược lý học phân tử thuộc Trường Y Albert Einstein – Đại học New York’s Yeshiva khám phá ra cơ chế tác động độc đáo của Taxol®.
Cơ chế tác động
Những khám phá trước đó trên các tác nhân kháng ung thư thường thấy rằng chúng ức chế phân chia tế bào bằng cách ngăn cản tạo thành các vi ống (microtubule) – một thành phần quan trọng trong quá trình phân bào. Trái lại, Horwitz nhận thấy Taxol® lại kích thích sự tạo thành các vi ống và làm bền vững chúng. Điều này khiến cho các tế bào cứ nhân đôi ADN trong khi chúng không có khả năng phân chia, và thế là chết theo lập trình – apoptosis. Qua lời kể và những gì chứng kiến thực tế, người ta thấy rằng nữ khoa học gia Susan Horwitz đã góp phần đáng kể vào quá trình phát triển thuốc kháng ung thư Taxol® bằng cách miệt mài nghiên cứu như một đam mê, khi bà nhận ra có những điều thú vị trong cấu trúc và tác dụng của Taxol®.
Cửa đóng hay mở
Khi thử nghiệm lâm sàng trên các thể ác tính ung thư buồng trứng, Taxol® mang đến tỉ lệ đáp ứng chưa từng có: 30%. Nhưng để có thuốc cho toàn bộ bệnh nhân ung thư buồng trứng, NCI (Viện Ung Thư Quốc Gia Hoa Kỳ) sẽ phải cung cấp 240 pound – tức 109 kg Taxol®. Điều này đồng nghĩa với việc đốn hạ 360.000 cây thông đỏ T. brevifolia. Không cần phải là nhà toán học để giải được phương trình này: vô nghiệm!
Ánh sáng cuối đường hầm
Nhưng cơ hội lại đến, khi các nhà khoa học phân lập được 10-deacetyl-baccatin III, gọi tắt là 10-DAB, từ loài thanh tùng Châu u, Taxus baccata. 10-DAB có khung cấu trúc chính của Taxol®, mà thiếu đi chuỗi bên. Không sao, họ sẽ bán tổng hợp được thôi. Pierre Potier đến từ Pháp đã đề xuất quy trình bán tổng hợp nhưng hiệu suất khá thấp và sau đó nhóm của Robert A. Holton từ Đại học Bang Florida đưa ra một quy trình khác với hiệu suất gấp đôi. Điều quan trọng là 10-DAB đến từ một nguồn nguyên liệu tái tạo: lá kim của cây. (bacca: berry)
Các nhà khoa học đã nỗ lực không ngưng nghỉ để đi tìm những con đường khả thi tạo ra Taxol® như công trình tổng hợp hóa học của Robert A. Holton với…45 bước (hầu như là quy trình ngắn nhất), hay sử dụng vi sinh vật. Thông qua những nghiên cứu về 10-DAB và Taxol®, một phân tử khác có tiềm năng kháng ung thư đã được bán tổng hợp nên: docetaxel, tức Taxotere®, bởi nhóm nghiên cứu của Pierre Potier. Potier đã mất đi người vợ của mình do căn bệnh ung thư vú, điều khiến ông chú tâm vào lĩnh vực nghiên cứu này.
Những vấn đề khác
Những chuyện ấy đâu đã là tất cả. Anh chàng Taxol® còn mang đến bài toán về sinh khả dụng: mặc dù tan tốt trong PEG 75% nhưng khi thử nghiệm trên mô hình khối u B16 và P388 tác dụng đã giảm đi so với ban đầu. Lần hồi mãi, hệ phân phối thuốc được chọn là ethanol, cremophor và saline (5:5:90) với nồng độ hoạt chất 0,3 – 0,6 mg/mL.
Tùng đã nở hoa (áo hạt nha, hạt trần mà)
Các thử nghiệm lâm sàng tốt đẹp làm tiền đề để NCI lựa chọn nhà sản xuất nhằm đưa ra thị trường. Tháng 12 năm 1992, Taxol® được FDA chấp thuận để chữa trị ung thư buồng trứng kháng Platinum. Sau đó, Taxol® còn được chấp thuận điều trị ung thư vú và u Kaposi liên quan đến AIDS.
Như vậy, đó là quá trình dài gian truân, kết hợp liên ngành giữa các nhà khoa học từ khắp nơi trên địa cầu để một thuốc điều trị ung thư như Taxol® có thể đến tay người bệnh. Có những lúc các nhà khoa học gần như muốn từ bỏ, nhưng mỗi tín hiệu mới lại ánh lên trong họ những niềm tin lạc quan.
Taxol® là tên thương mại, nó còn có tên dùng chung là paclitaxel. Ở Việt Nam cũng có loài Taxus wallichiana, nhưng chính xác tại đâu thì là một câu chuyện dài, vì loài đang bị đe dọa khai thác.
Tài liệu tham khảo:
Tuzim K., Korolczuk A. (2021), “An update on extra-oral bitter taste receptors”, J Transl Med, 19, 440 .
Wooding, S. P., Ramirez, V. A., & Behrens, M. (2021), “Bitter taste receptors: Genes, evolution and health”, Evolution, medicine, and public health, 9(1), 431–447.
Ntie-Kang, F. (2019), “Mechanistic role of plant-based bitter principles and bitterness prediction for natural product studies II: prediction tools and case studies”, Physical Sciences Reviews, 4(, 20190007.Bassoli, A., Borgonovo, G. and Busnelli, G. (2007), “Alkaloids and the Bitter Taste”, Modern Alkaloids: Structure, Isolation, Synthesis and Biology, 53-72.
Achan, J., Talisuna, A. O., Erhart, A., Yeka, A., Tibenderana, J. K., Baliraine, F. N., Rosenthal, P. J., & D’Alessandro, U. (2011). Quinine, an old anti-malarial drug in a modern world: role in the treatment of malaria. Malaria journal, 10, 144.
Flückiger, Friedrick A.; Daniel, Hanbury (1874), “Cortex Cinchonæ”, Pharmacographia: A History of the Principal Drugs of Vegetable Origin, Met with in Great Britain and British India. London: Macmillan and Co. pp. 302–331.
Meyer, Christian G.; Marks, Florian; May, Jürgen (1 December 2004). “Editorial: Gin tonic revisited”. Tropical Medicine & International Health. 9 (12): 1239–1240.
Homer, Sử thi Odyssey
– Lee M. R. (1999), “The snowdrop (Galanthus nivalis): from Odysseus to Alzheimer”, Proceedings of the Royal College of Physicians of Edinburgh, 29(4), 349–352.
-Cinelli, M. A., & Jones, A. D. (2021), “Alkaloids of the Genus Datura: Review of a Rich Resource for Natural Product Discovery”, Molecules (Basel, Switzerland), 26(9), 2629.
-McHugh, J. (2021), An Unholy Brew: Alcohol in Indian History and Religions, Oxford University Press.
-Proudfoot, A.(2006), “The Early Toxicology of Physostigmine”, Toxicol Rev 25, 99–138 .
American Chemical Society. National Historic Chemical Landmarks. Discovery of Camptothecin and Taxol®. http://www.acs.org/…/landmarks/camptothecintaxol.htmlExit Disclaimer. Published 2003. Accessed March 31, 2022.
Żwawiak, Justyna & Zaprutko, Lucjusz. (2014), “A brief history of taxol”, Journal of Medical Sciences, 1, 47.
Printz C. (2011), “Scientist honored for work with paclitaxel: interest in a unique chemical structure leads to drug that helps millions”, Cancer, 117(3), 2827-2828.

Pingback: So Sánh Rượu Bạch Tật Lê Với Các Loại Rượu Thuốc Phổ Biến - Rừng Núi Tây Bắc
Pingback: Những Công Dụng Tuyệt Vời Của Hạt Dổi Đối Với Sức Khỏe - Nông sản Anh Tùng
Pingback: Cà Gai Leo - Thảo Dược Tăng Cường Miễn Dịch và Chống Viêm Tự Nhiên - Thảo dược Bá An